Пластический компонент в алгоритме хирургического лечения больных с флегмоной верхней конечности
Автор: Красенков Ю.В., Татьяненко В.К., Давыденко А.В., Зайцев П.П., Гаербеков А.Ш., Богданов В.Л.
Журнал: Московский хирургический журнал @mossj
Рубрика: Общая хирургия
Статья в выпуске: 4 (86), 2023 года.
Бесплатный доступ
Введение. Заживление ран после гнойных процессов мягких тканей на фоне развившегося компартмент-синдрома представляет научный и практический интерес, ведь в большинстве случаев раны после вскрытия флегмоны являются широкими, и сведение краев технически невозможно.Цель исследования. Улучшить результаты лечения больных с флегмоной верхней конечности и компартмент-синдромом, путем использования разработанного способа пластической операции на завершающем этапе.Материалы и методы исследования. В исследование вошло 134 пациента, проходивших лечение по поводу флегмоны верхней конечности (локализация: плечо, предплечье) на фоне компартмент-синдрома, по разработанному алгоритму, защищенному патентом РФ, в условиях отделения гнойной хирургии ГБУ «ГБСМП» в г. Ростове-на-Дону, ГБУ РО «Центральная городская больница» в г. Батайске в период с 2016 по 2023 год. В контрольную группу входило 62 пациента. Пациенты были сопоставимы по полу, возрасту, степени патологического процесса. Комплекс лабораторно-диагностических мероприятий осуществляли в соответствии с общепринятыми стандартами лечения гнойной патологии. При установлении тканевой гипертензии (ТД выше 10 мм рт. ст.) выполняли Z-образную фасциотомию (Патент РФ № 2755169). У 10 больных II серии (основная группа) для закрытия раневого дефекта был использован оригинальный способ пластики (патент РФ № 2709726).Заключение. Комплексный подход к лечению ран и компартмент-синдрома, использование кожно-подкожно-фасциального лоскута показали положительные результаты. Полученные результаты позволяют рекомендовать разработанный комплекс лечебных мероприятий, включающий пластический компонент, при лечении пациентов с межмышечной флегмоной верхней конечности.
Флегмона, фасциотомия, тканевая гипертензия, компартмент-синдрома, пластическая операция
Короткий адрес: https://sciup.org/142239443
IDR: 142239443 | УДК: 616-089.197.1 | DOI: 10.17238/2072-3180-2023-4-29-37
Plastic component in the algorithm of surgical treatment of patients with phegmon of the upper limb
Introduction. Wound healing after purulent processes of soft tissues against the background of developed compartment syndrome is of scientific and practical interest, because in most cases, wounds after opening the phlegmon are wide, and bringing the edges together is technically impossible.Purpose of the study. To improve the results of treatment of patients with phlegmon of the upper limb and compartment syndrome by using the developed method of plastic surgery at the final stage.Materials and methods of research. The study included 134 patients undergoing treatment for phlegmon of the upper extremity (localization: shoulder, forearm) against the background of compartment syndrome, according to a developed algorithm protected by a patent of the Russian Federation, in the purulent surgery department of the State Budgetary Emergency Hospital in Rostov-on-Don, State Budgetary Institution RO "Central City Hospital" in Bataysk from 2016 to 2023. The control group included 62 patients. The patients were comparable by gender, age, and degree of the pathological process. A set of laboratory and diagnostic measures was carried out in accordance with generally accepted standards for the treatment of purulent pathology. When tissue hypertension was established (TD above 10 mm Hg), a Z-shaped fasciotomy was performed (RF Patent № 2755169). In 10 patients of series II (main group), an original plastic method was used to close the wound defect (RF patent № 2709726).Conclusion. An integrated approach to the treatment of wounds and compartment syndrome and the use of a cutaneous subcutaneous fascial flap showed positive results. The results obtained allow us to recommend the developed complex of treatment measures, including a plastic component, in the treatment of patients with intermuscular phlegmon of the upper limb.
Текст научной статьи Пластический компонент в алгоритме хирургического лечения больных с флегмоной верхней конечности
На протяжении всей истории хирургии процесс заживления ран всегда вызывал особый интерес. Известно, что практически все тканевые структуры имеют способности к регенерации, однако этот процесс довольно сложен и имеет ряд возможных осложнений [1]. Послеоперационные раны кожных покровов конечностей, появившиеся после лечения острых гнойно-воспалительных заболеваниях мягких тканей конечностей, составляют не малую долю контингента пациентов хирургических стационаров [2]. Лечение таких пациентов может представлять особую сложность для хирургов. Продолжительный период времени методом выбора лечения длительно незаживающих ран являлась ранняя свободная аутодермопластика [3, 4]. Альтернативами этому служат методы наложения вторичных швов, лейкопластырное натяжение с использованием omnistrip. К сожалению, данные методы не всегда позволяют достигнуть желаемого результата, в большинстве случаев раны после вскрытия флегмоны являются широкими, и сведение краев технически невозможно [5]. Существенную проблему представляет развитие компартмент-синдрома у пациентов с флегмонами верхней конечности. Данный синдром вызывает нарушение микроциркуляции и нейроишемические нарушения, что напрямую отражается на регенерации пораженных тканей [6, 7]. Лечение этого контингента представляет высокую значимость и существенный интерес. Основываясь на указанных фактах, целесообразным является разработка и внедрение в практику метода пластики раневого дефекта, образовавшегося на заключительном этапе лечения пациентов с флегмоной верхней конечности на фоне компартмент-синдрома.
Цель исследования. Улучшить результаты лечения больных с флегмоной верхней конечности и компартмент-синдромом путем использования разработанного способа пластической операции на заключительном этапе.
Материалы и методы исследования
В исследование вошло 134 пациента, проходивших лечение по поводу флегмоны верхней конечности (локализация: плечо, предплечье) на фоне компартмент-синдрома, по разработанному алгоритму, защищенному патентом РФ, в условиях отделения гнойной хирургии ГБУ «ГБСМП» в г. Ростове-на-Дону, ГБУ РО «Центральная городская больница» в г. Батайске в период с 2016 по 2023 год. В контрольную группу входило 62 пациента. Пациенты были сопоставимы по полу, возрасту, степени патологического процесса.
Критерии исключения из исследования:
☐ наличие сопутствующей гнойной патологии костной системы верхней конечности;
☐ гнойно-некротические формы заболевания;
☐ наличие флегмоны кисти;
☐ наличие специфических заболеваний;
☐ наркотическая зависимость;
☐ иммунодефицитные состояния.
Комплекс лабораторно-диагностических мероприятий осуществляли в соответствии с общепринятыми стандартами лечения гнойной патологии, он был дополнен алгоритмом ведения пациентов. При установлении факта наличия тканевой гипертензии (ТД выше 10 мм рт. ст.) меняли тактику оперативного лечения, которая должна быть направлена на снижение и нормализацию показателей ТД, путем выполнения Z-образной фасциотомии (Патент РФ № 2755169) [8].
Послеоперационное лечение проводили с использованием противовоспалительной и антибактериальной (руководству- ясь чувствительностью возбудителя к препаратам) терапии, лекарственных средств, улучшающих регионарную микро-гемоциркуляцию и дополняли ультразвуковой кавитацией ран, сеансами озонотерапии (с концентрацией O3в воде 4000 мкг/л).
Разработанная нами тактика лечения пациентов с флегмоной верхней конечности и компартмент-синдромом позволила существенно сократить количество осложнений в раннем послеоперационном периоде. Число ранних послеоперационных осложнений у больных основной группы составило 6 случаев (8,3 %), тогда как в контрольной осложнений было в 3,3 раза больше (27,4 %). На наш взгляд это связано с лечением, проводимым в присутствии тканевой гипертензии.
Степень выраженности миофасциального болевого синдрома оценивали по методике, предложенной Ф.А. Хабировым (2019) [9].
Оценку результатов лечения осуществляли в 2 этапа: в раннем (30 дней после выписки) и позднем (через 6 месяцев после выписки) послеоперационном периоде. Результаты лечения оценивали как положительные, удовлетворительные и неудовлетворительные, сравнивая показатели с таковыми для неоперированной конечности.
-
• Положительным считали результат лечения, при котором была восстановлена функциональная активность мышц верхней конечности на стороне операции, отсутствие болевого синдрома, триггерных зон и гипертрофических рубцов; зафиксирована высокая степень качества жизни больного.
-
• Удовлетворительным считали результат при наличии тканевой гипертензии I–II степени, единичных триггерных зон, снижении функции мышц верхней конечности на стороне операции на 30–50 % от физиологической нормы, наличии гипертрофического рубца шириной до 1,0 см, снижении качества жизни больного не более чем на 30 %.
-
• Неудовлетворительным считали результат при наличии тканевой гипертензии III степени, снижении функции мышц верхней конечности на стороне операции более чем на 50 %, наличии постоянных триггерных зон с иррадиацией боли в сустав, гипертрофического рубца шириной более 1 см, снижении качества жизни более чем на 30 %.
Оперативное лечение межмышечной флегмоны плеча (n=64) и предплечья (n=70) исследуемых выполнялось по проекционным схемам Гостищева В.К.
Второй этап хирургического лечения больных с межмышечной флегмоной верхней конечности включал в себя выбор способа закрытия раневого дефекта. Он зависел от сроков очищения раны, фазы раневого процесса и КОЕ (не более 10 4 –10 5 в 1 г ткани).
В послеоперационном периоде, в соответствии с разработанной нами схемой лечебно-реабилитационного алгоритма у всех 134 больных проведен курс восстановительной терапии.
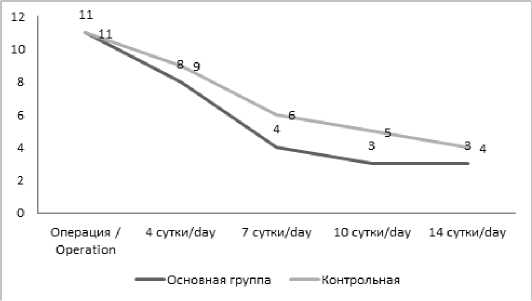
Рис. 1. Сравнительная оценка КОЕ в 1 г ткани пациентов обеих групп
Fig. 1. Comparative assessment of CFU in 1 g of tissue from patients in both groups
Из материала, представленного на рисунке 1, видно, что у больных основной группы КОЕ падал до критического уровня на 7-е сутки после операции.
Показаниями для наложения одного из предложенных швов на раневой дефект были следующие:
☐ Отсутствие свищевых затеков.
☐ Возможность сопоставления краев раны без натяжения после хирургической обработки ее краев.
Первично отсроченные швы были наложены у 18 больных. При наложении вторичных швов (n=34) на дно операционной раны укладывали перфорированный дренаж, конец его выводили через верхний и нижний углы. На расстоянии 1,0–1,5 см от краев раны накладывали режущей иглой лигатуры нитью капрон, которые проводили под дном раны. Такие же лигатуры делали на противоположной стороне на том же расстоянии от краев раны. Швы накладывали на расстояние 1,5–2,0 см друг от друга.
У 10 больных II серии (основная группа) для закрытия раневого дефекта был использован разработанный нами оригинальный способ пластики (патент РФ № 2709726).
Показаниями к разработанному нами способу операции являются:
☐ Отсутствие свищевых затеков.
☐ Площадь раневого дефекта более 20 см 2 .
Техника выполнения пластического компонента в лечении больных заключалась в следующем. Выкраивали кожно-подкожно-фасциально-мышечный трансплантат на основе пле-челучевой мышцы, включающий дистальный конец мышцы с расположенной над ним кожно-подкожно-фасциальной пластинкой, по форме идентичной форме раневого дефекта области верхней конечности. Производили выделение проксимального конца мышцы с оставлением интактной сосудисто-нервной ножки. Отсекали мышцу от места прикрепления к латеральному краю плечевой кости. Далее трансплантат разворачивали во фронтальной плоскости в области сосудисто-нервной ножки под углом 30–40° при пластике дефекта задней поверхности области предплечья; под углом 45–60° при пластике дефекта передней поверхности области предплечья; под углом 80–90° при пластике дефекта передней поверхности области плеча; под углом 100–110° при пластике дефекта задней поверхности области плеча. Дистальный конец через подкожный тоннель подводили к дефекту тканей в области верхней конечности. Осуществляли послойную фиксацию.
Разработанный способ иллюстрируется следующими чертежами (рис. 2 и 3).
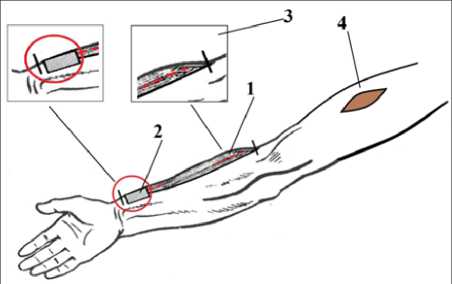
Рис. 2. Вскрытие кожно-подкожно-фасциального трансплантата на основе плечелучевой мышцы Fig. 2. Opening of the skin-subcutaneous-fascial graft based on the brachioradialis muscle
На рисуснке 2 показано вскрытие кожно-подкожно-фасциального трансплантата на основе плечелучевой мышцы, где:
-
1. Плечелучевая мышца выделена на всем протяжении.
-
2. Контуры кожно-подкожно-фасциального трансплантата на основе плечелучевой мышцы.
-
3. Поднадкостничное отсечение проксимального сухожилия плечелучевой мышцы от плечевой кости.
-
4. Послеоперационная рана овальной формы на плече.
-
5. Контуры мышечной части трансплантата на основе пле-челучевой мышцы.
-
6. Узловые швы на предплечье в зоне забора трансплантата.
-
7. Узловые швы, фиксирующие кожно-подкожно-фасциальный мышечный трансплантат овальной формы на основе плечелучевой мышцы к ране овальной формы на плече.
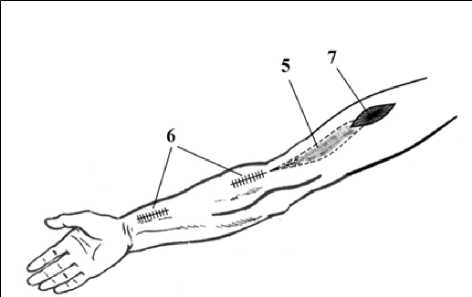
Рис. 3. Проведение кожно-подкожно-фасциального трансплантата на основе плечелучевой мышцы к дефекту на переднем отделе плечевой области Fig. 3. Carrying out a skin-subcutaneous-fascial graft based on the brachioradialis muscle to a defect in the anterior part of the shoulder region
На рисунке 3 показано проведение кожно-подкожно-фасциального трансплантата на основе плечелучевой мышцы к дефекту на переднем отделе плечевой области.
Технический результат – повышение эффективности лечения больных с флегмоной мягких тканей верхней конечности за счет закрытия раневого дефекта любой локализации, купирования воспаления и реваскуляризации зоны пластики.
Данный технический результат достигается за счет использования кожно-подкожно-фасциально-мышечного трансплантата на основе плечелучевой мышцы, выкроенного с учетом формы послеоперационной раны для ликвидации раневого дефекта разной локализации, при хирургическом лечении флегмоны верхней конечности.
Заявляемая методика позволяет формировать трансплантат, который включает все составные части поврежденного сегмента верхней конечности (кожа, подкожная клетчатка, фасция, мышца).
Статистическая обработка количественных результатов проводилась с использованием программы SPSS Statistics 10 IBM (США) с вычислением критериев Манна-Уитни, Вилкок-сона. Статистически значимыми считали различия показателей при р<0,05.
Результаты и обсуждение
Известно, что плечелучевая мышца начинается сухожилием от латерального края плечевой кости, дистальнее ее сухожилие прикрепляется к шиловидному отростку лучевой кости. Основная сосудисто-нервная ножка представлена возвратной артерией и веной от лучевых артерий и вены, поверхностным нервом от лучевого нерва. В среднем и нижнем отделах в кровоснабжении мышцы принимают участие мышечные ветви от лучевой артерии и вены.
Установлено, что контрастная масса, введенная через основной сосудистый пучок, питающий плечелучевую мышцу (возвратная артерия от лучевой артерии), при одновременном переносе мышечных ветвей от лучевой артерии, во все возрастные периоды заполняла сосудистое русло плече-лучевой мышцы от проксимального до дистального сухожилия.
Уровень положения основных сосудисто-нервных ворот представлен в таблице 1, из которой явствует, что он соответствует верхней трети медиального края мышцы. Синтопия элементов сосудисто-нервного пучка у ворот мышцы выглядит следующим образом: наиболее поверхностно лежит нерв, кзади от него – артерия и еще глубже – вена.
Таблица 1
Уровень положения (в см) основных сосудисто-нервных ворот плечелучевой мышцы предплечья (М±m)
Level of position (in cm) of the main neurovascular portal of the brachioradialis muscle of the forearm (M±m)
Table 1
|
Возрастной период / Age period |
Показатель / Index |
||
|
От медиального края мышцы / From the medial edge of the muscle |
От середины передней линии локтевой ямки / From the middle of the anterior line of the cubital fossa |
От наружного надмыщелка плечевой кости / From the external epicondyle of the humerus |
|
|
Юношеский / Youthful |
1,22±0,13 |
1,26±0,15 |
1,96±0,12 |
|
Первый зрелый / First mature |
1,48±0,14 |
1,56±0,13 |
2,20±0,16 |
|
Второй зрелый / Second mature |
1,73±0,15 |
1,8±0,15 |
2,28±0,24 |
|
Пожилой / Elderly |
1,5±0,14 |
1,62±0,14 |
2,53±0,3 |
|
Примечание / Note |
P<0,05при сравнении исследуемых групп P<0,05 when comparing study groups |
||
Результаты рентгеновазографии кожно-подкожного участка, расположенного в области нижней трети плечелучевой мышцы, позволили определить следующие особенности его ангиоархитектоники. Так мышечно-кожные ветки в области плечелучевой мышцы, служат продолжением мышечных ветвей от лучевой артерии, участвующей в кровоснабжении этой мышцы. Было установлено, что в подкожно-жировом слое над плечелучевой мышцей выделено 6 постоянных мышечно-кожных артерий у трупов мезоморфного типа телосложения, 4 при долихоморфном типе телосложения и 7 при брахиморфном типе телосложения. Основные сосудистые ворота над плечелучевой мышцей сконцентрированы в области латерального ее края. Линии внедрения артерий в кожно-подкожный слой имеет косые направления сверху вниз, снутри кнаружи и сзади наперед, т.е. совпадает с линией натяжения кожи, что следует учитывать при формировании кожно-подкожной составляющей частей сложного трансплантата.
По рентгеновазограммам установлено, что тип ветвления кожно-подкожных ветвей от мышечных ветвей лучевой артерии в области кожно-подкожного слоя был рассыпной. В то время как плечелучевая мышца имеет магистральный тип кровоснабжения. Зоны кровоснабжения каждой из указанных ветвей составляли от 1,25х1,65 см до 2,2х2,7 см. Они были более насыщенными при мезо- и брахиморфном типах телосложения по сравнению с долихоморфным типом.
Проведенное цитологическое исследование раневого экссудата при предложенной технологии показало, что воспа- лительная реакция у больных основной группы была менее выражена (в 1,3 раза), а фибропластическая выше в 1,4 раза чем у пациентов контрольной группы. Это носило отражение и в непосредственных результатах лечения (табл. 2).
Из данных, представленных в таблице 2, следует, что из 34 больных оперированных с ушиванием раны вторичными швами над перфорированным дренажом у 1 больного было нагноение раны. Были сняты швы и разведены края раны. Дальнейшее лечение велось открытым методом с использованием антисептиков и мазей на водорастворимой основе. Такая же картина наблюдалась и у 1 больного с некрозом кожных краев ран и 1 больного с кровотечением. У 1 больного с лейкопластырным натяжением рану вели открытым методом. В подгруппе больных (18 пациентов), у которых ушивание раны вели первично-отсроченными швами, у одного больного отмечен некроз кожных краев раны, что по всей видимости связано с тугим завязыванием лигатур. Швы были сняты, края раны иссечены, и она велась открытым методом. У 1 больного было кровотечение, которое было остановлено тугим бинтованием. В подгруппе больных с пластикой раневого дефекта сложным трансплантатом по оригинальной методике осложнений в ближайшем послеоперационном периоде не было.
При изучении состояния кровоснабжения сформированного кожно-подкожно-фасциального трансплантата на основе пле-челучевой мышцы полярографическим методом в сроки перед выпиской из стационара и на 30 и 60 сутки после операции получены следующие результаты, подробно представленные в таблице 3.
Таблица 2
Осложнения раннего послеоперационного периода на втором этапе операции у больных основной группы
Complications of the early postoperative period at the second stage of the operation
Table 2
|
Метод операции / Operation method |
Число оперирован-ных больных / Number of operated patients |
Характер осложнений / The nature of the complications |
Общее количество осложнений / Total number of complications |
|||
|
Гнойно-воспалительный процесс / Purulent-inflammatory process |
Несостоятельность швов/ Suture failure |
Кровотечение / Bleeding |
Некроз одного из компонента трансплантата / Necrosis of one of the graft components |
|||
|
Первично отсроченные швы / Primarily delayed sutures |
18 |
- |
- |
- |
- |
0 |
|
Вторичные швы на рану над перфорированным дренажом / Secondary sutures on the wound over the perforated drain |
34 |
1 |
1 |
1 |
0 |
3 |
|
Лейкопластырное натяжение / Adhesive tension |
10 |
0 |
0 |
1 |
0 |
1 |
|
Пластика кожно-подкожно-фасциальным лоскутом / Plasty with a skin-subcutaneous-fascial flap |
10 |
0 |
0 |
0 |
0 |
0 |
|
Всего / Total |
1 |
1 |
2 |
0 |
4 |
|
Регистрация парциального напряжения кислорода проводилась полярографическим методом, на полярографе «Орион-102» при помощи двух электродов. Один электрод устанавливали в области питающей ножки кожно-подкожно-фасциального трансплантата, на основе плечелучевой мышц, второй электрод – в зоне пластики дефекта сегмента верхней конечности.
Таблица 3
Показатели парциального напряжения кислорода в зоне пластики кожно-подкожно-фасциальным трансплантатом на основе плечелучевой мышцы (рО2, мм рт. ст.)
Table 3
Indicators of oxygen partial tension in the area of plastic surgery with a skin-subcutaneous-fascial graft based on the brachioradialis muscle (рО2, mmHg)
|
Показатели / Indicators |
Сроки послеоперационного периода / Terms of the postoperative period |
|
|
30 дней/day |
60 дней/day |
|
|
Р02 1 (норма более 50) / (norm more than 50) |
40,4±2,12 |
47,62±1,89 |
|
Р02 2 (норма 41-44) / (norm 41-44) |
33,7±0,52 |
39,42±0,21 |
|
t1 |
12,10±0,31 |
11,34±0,42 |
|
t2 |
92,81±1,87 |
92,94±1,76 |
|
t3 |
14,56±0,22 |
14,74±0,34 |
|
t4 |
93,75±2,60 |
92,8±2,53 |
|
Примечание / Note |
P<0,05при сравнении исследуемых групп / P<0.05 when comparing study groups |
|
*Среднее значение Р021 у здоровых лиц – 42,23±0,45 мм рт. ст.
Примечание: Р02 1 – в см вод.ст. на первом электроде (питающая ножка мышц); Р02 2 – на втором электроде (дистальный отдел мышцы);
t1 – латентный период, равный времени с момента подачи кислорода до начала повышения Р02 2 ;
t2 – время достижения максимального уровня Р02 2 ;
t3 – латентный период времени с момента прекращения подачи кислорода до начала падения уровня Р02 2 ;
t4 – время достижения стабильного уровня Р02 после прекращения подачи кислорода.
Данные, представленные в таблице 3, свидетельствуют о том, что показатели напряжения кислорода в области обоих электродов были относительно близки по значению друг к другу, что указывало на сходство кислородного режима в области их введения. Естественно, значения насыщения кислородом сосудистой ножки были выше, чем периферических отделов трансплантата, но эта разница не выходила за физиологические пределы (р<0,05).
Принимая во внимание динамику показателей t1, t2, t3, t4 можно прийти к заключению, что оптимальные условия оксигенации мышечной части трансплантата, от которой зависит его жизнеспособность, определялись к 30 суткам исследования. К 180 суткам констатировали нормализацию показателей полярограмм мягких тканей зоны пластики.
Сроки временной нетрудоспособности пациентов при закрытие раневых дефектов различными способами представлены в таблице 4.
Таблица 4
Средние сроки временной нетрудоспособности исследуемых
Table 4
Average terms of temporary disability of the studied
|
№ |
Метод операции / Operation method |
Средние сроки временной нетрудоспособности (в днях) / Average period of temporary disability (in days) |
||
|
Лечение в стационаре / Treatment in a hospital |
Амбулаторное лечение / Ambulatory treatment |
Общие сроки лечения / General terms of treatment |
||
|
1. |
Отсроченные первичные швы / Delayed primary sutures |
10,4±1,24 |
5,8±1,10 |
16,2±0,95 |
|
2. |
Вторичные швы на рану над сквозным перфорированным дренажом / Secondary sutures on the wound over the through perforated drainage |
10,7±1,28 |
6,9±1,12 |
18,6±1,23 |
|
3. |
Лейкопластырное натяжение / Adhesive tension |
11,4±1,73 |
7,4±1,22 |
20,2±1,17 |
|
4. |
Пластика кожно-подкожно-фасциальным лоскутом / Plastic skin-subcutaneous-fascial flap |
14,1±1,31 |
6,3±1,32 |
21,1±1,53 |
Неудовлетворительный результат/ Unsatisfactory result
Из материала, представленного в таблице 3, явствует, что средние сроки временной нетрудоспособности составили в стационаре 11,6 дня и амбулаторного – 6,7 дня.
При этом самый большой показатель временной нетрудоспособности был в группе больных с закрытием дефекта трансплантатом (стационарное лечение 14,1 день, амбулаторное 6,9 дней).
Для визуализации эффективности разработанной нами тактики лечения пациентов с флегмоной верхней конечности представляем результаты лечения в графическом варианте (рис. 4).
Данные диаграммы наглядно показывают высокую эффективность разработанного алгоритма лечения пациентов, полное исключение неудовлетворительных результатов лечения, высокий уровень положительных результатов.
Удовлетворительный результат/ Satisfactory result
Положительный результат / Positive result

о.о%о,о^,оаз,сю,о5с,сбс.о%о.свс сао.оюо о%
Рис. 4. Результаты лечения пациентов основной и контрольной клинических групп в отдаленные сроки послеоперационного периода Fig. 4. The results of treatment of patients of the main and control clinical groups in the long-term postoperative period
Заключение
Проведенные исследования позволили обосновать целесообразность применения разработанного лечебного алгоритма в клинике на заключительном этапе лечения больных с межмышечной флегмоной верхней конечности.
Операция выполнена по разработанной методике. В ближайшем послеоперационном периоде осложнения (серома, краевое кровотечение из раны) было у 2-х больных, перенесших реконструктивный этап операции. В отдаленные сроки (6–12 мес.) осложнений не было. Функция верхней конечности в полном объеме. О жизнеспособности трансплантата свидетельствуют результаты полярографического исследования.
Комплексный подход к лечению ран и компартмент-син-дрома, использование кожно-подкожно-фасциального лоскута показали положительные результаты. Полученные результаты позволяют нам рекомендовать разработанный комплекс лечебных мероприятий включающий пластический компонент, при лечении пациентов с межмышечной флегмоной верхней конечности.
Список литературы Пластический компонент в алгоритме хирургического лечения больных с флегмоной верхней конечности
- Жариков А. Н., Алиев А. Р. Хирургическое лечение длительно незаживающих ран кожи и мягких тканей с помощью раневого покрытия на основе бактериальной целлюлозы. Бюллетень медицинской науки, 2022. № 3 (27). С. 91-97. DOI: 10.31684/25418475_2022_3_91 EDN: NDUNXU
- Аль-Канани Э. С., Гостищев В. К., Ярош А. Л., Карпачев А. А., Солошенко А. В., Жарко С. В., Линник М. С. Лечение гнойной инфекции мягких тканей: от истории к настоящему (литературный обзор). Актуальные проблемы медицины, 2020. № 43 (1). С. 155-164.
- Tottoli E. M., Dorati R., Genta I., Chiesa E., Pisani S., & Conti B. Skin wound healing process and new emerging technologies for skin wound care and regeneration. Pharmaceutics, 2020, № 12(8), рр. 735.
- Makhmudov S., Babajanov A., Toirov A., Akhmedov A., & Musoev S. The features of autodermoplasty in traumatic wounds of the skin and soft tissues. International Journal of Health Sciences, 2022, № 6(I), рр. 7792-7795. EDN: WDXFLX
- Образцова А. Е., Ноздреватых А. А. Морфофункциональные особенности репаративного процесса при заживлении кожных ран с учетом возможных рубцовых деформаций (обзор литературы). Вестник новых медицинских технологий. Электронное издание, 2021. № 1 (15). DOI: 10.24412/2075-4094-2021-1-3-3 EDN: DNUEYX
- Maniar R., Hussain A., Rehman M. A., & Reissis N. Unusual presentation of acute compartment syndrome of the forearm and hand. BMJ Case Reports CP, 2020, № 13(9), e235980. DOI: 10.1136/bcr2020-235980
- Zhang D., Tarabochia M., Janssen S.J., Ring D., Chen N. Acute compartment syndrome in patients undergoing fasciotomy of the forearm and the leg. International Orthopaedics, 2019, № 43, pp. 1465-1472. EDN: VKCZHW
- Способ лечения острого тканевого гипертензионного синдрома при сочетанной межмышечной флегмоне верхней конечности: пат. 2755169 Рос. Федерация. № 2021107276; заявл. 18.03.2021; опубл. 13.09.2021, Бюлл. № 26. 9 с.
- Хабиров, Ф. А., Хабирова, Ю. Ф. Миофасциальная больсовременные проблемы диагностики и лечения в практике врача первичного звена. Практическая медицина, 2019. № 17(7). С. 8-17. EDN: ZEGCAQ
- Способ закрытия раневого дефекта после хирургического лечения флегмон мягких тканей верхней конечности: пат. 2709726 Рос. Федерация. № 2019101236; заявл. 14.01.2019; опубл. 19.12.2019, Бюлл. № 35. 15 с.


