Почвенные актинобактерии рода Rhodococcus, обладающие высокой амидазной активностью
Автор: Демаков В.А., Павлова Ю.А., Максимов А.Ю., Кузнецова М.В.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 10, 2009 года.
Бесплатный доступ
Исследованы почвенные культуры актинобактерий рода Rhodococcus, обладающие термостабильной амидазной активностью. Проведен ПЦР-анализ и секвенирование генов амидаз. Выявлены последовательности, гомологичные известным генам амидаз из R. erythropolis (GenBank, M88614), R. erythropolis (GenBank, E12517) и R. rhodochrous N774.
Короткий адрес: https://sciup.org/147204471
IDR: 147204471 | УДК: 579.26:579.222.4
Soil aсtinobacteria of genus Rhodococcus having high amidase activity
Soil cultures of Rhodococcus genera actinobacteria having termostable activity were investigated. The PCAanalysis and sequencing of amidase genes was carried out. Sequences, homologous to known amidase genes from R. erythropolis, GenBank, M88614, R. erythropolis, GenBank, E12517 and R. rhodochrous N774 were revealed
Текст научной статьи Почвенные актинобактерии рода Rhodococcus, обладающие высокой амидазной активностью
-
a Пермский государственный университет, 614990, Пермь, ул. Букирева, 15
-
b Институт экологии и генетики микроорганизмов УрО РАН, 614081, Пермь, ул. Голева, 13
Исследованы почвенные культуры актинобактерий рода Rhodococcus , обладающие термостабильной амидазной активностью. Проведен ПЦР-анализ и секвенирование генов амидаз. Выявлены последовательности, гомологичные известным генам амидаз из R. erythropolis (GenBank, M88614), R. erythropolis (GenBank, E12517) и R. rhodochrous N774.
Амидазы (КФ 3.5.1.4) – ферменты, катализирующие реакции гидролиза амидосоединений, участвуют в метаболизме азота и широко распространены в природе: они обнаружены у прокариот и эукариот (Fournand, 2001). У бактерий присутствие амидазной активности нередко ассоциировано с метаболизмом нитрилов. Микроорганизмы, активно использующие амиды и нитрилы в качестве ростового субстрата, обнаружены среди бактерий различных таксономических групп: Agrobacterium, Alcaligenes, Bacillus, Brevibacterium, Pseudomonas , Rhodococcus и др (Забазная, 1998, Кузнецова, 1997; Максимов, 2003; Моисеева, 1991, Banerjee, 2002; Cowan, 2000; Kotlova, 1999, Yanenko, 1995).
Амидазы, выделенные из различных источников, характеризуются различной субстратной специфичностью (Banerjee, 2002). Некоторые из них преимущественно гидролизуют амиды алифатических кислот, другие расщепляют ароматические соединения, в то время как остальные трансформируют амиды α- или ω-аминокислот. Некоторые амидазы обладают стереоселективностью (Four-nand, 2001). Однако распространение ферментных систем разных типов, способных трансформировать различные виды субстратов, не является видоспецифическим признаком (Перцович, 2005).
Данная работа посвящена исследованию почвенных микроорганизмов, обладающих высокой амидазной активностью, и анализу генов амидаз.
Материалы и методы исследования
Объектами исследования являлись полученные в результате селекции на ацетонитриле штаммы Rhodococcus erythropolis, активно трансформирующие амиды и нитрилы карбоновых кислот. Культуры выращивали на минеральной безазотной солевой среде N, содержащей ацетонитрил в концентрации 10 мМ .
Трансформацию амидов и нитрилов с использованием активной биомассы проводили в 1 мл 10 мМ калий-натрий фосфатного буфера, pH 7.2, при начальной концентрации субстрата 2% параллельно при 25 и 50°С в течение 10 мин. Реакцию останавливали добавлением концентрированной HCl до концентрации 2%. Пробы центрифугировали при 12 тыс. об/мин в течение 5 мин. Продукты реакции анализировали методами газовой хроматографии и ВЭЖХ.
Газовую хроматографию продуктов трансформации нитрилов проводили на хроматографе Chrom 5d ( " LP " , Чехословакия), оснащенном плазменно-ионизационным детектором. Хроматографическая колонка длиной 2 м и внутренним диаметром 3 мм была заполнена носителем полисорб-1, фракция 0,25-0,5 мм ( " Реахим " , Россия). В газ-носитель азот подавался с объемным расходом 35 см3/мин. Температура термостата 190 ± 3 ° С, температура испарителя 220 ± 10 ° С. В качестве стандартов использовали растворы чистых нитрилов, амидов и карбоновых кислот.
Удельную активность ферментов – амидазы и нитрилгидратазы – выражали в мкмоль продукта реакции (кислоты или амида), образуемого за 1 мин, в пересчете на 1 мг веса сухих клеток (мкмоль/мг/мин).
Хромосомную ДНК получали фенольным методом, модифицированным для выделения ДНК из актиномицетов (Клонирование ДНК, 1988).
Праймеры для амплификации генов нитрилгидратазы (А) и нитрилазы (Б )
|
Выявляемый тип гена |
Праймер |
Последовательность |
|
Амидаза, гомологичная ферментам из R. erythropolis (E12517) и R. rhodochrous N-774 (X54074) |
AmiRhd-1 AmiRhd-2 |
5’-ATGGCGACAATCCGACCTGACGACA 5’-CTAGGCGGGGCTGAGTTGTGGTGCAGA |
|
Амидаза, гомологичная ферменту из R. erythropolis (M88714) |
AmiReR-1 AmiReR-2 |
5’-ATGCGACACGGTGACATCTCCTCGA 5’-TTACGCTTCGACGGTCTTCTCGAC |
|
Амидаза, гомологичная ферменту из R. erythropolis (AY026386) |
AmiReX-1 AmiReX-2 |
5’-GTGCGACCCAATCGCCCATTCGGCC 5’-CTACCGCAGCACCGGTGCGCTCGG |
|
Амидаза, гомологичная ферментам из R. rhodochrous J1 (S38270) |
AmiJ1-1 AmiJ1-2 |
5’-ATGTCTTCGTTGACTCCCCCCAATT 5’-TTATGTCAGGGTGCCGGCTGCAGC |
|
Rhodococcus sp. (BD061400) |
AmiBD-2 |
5’-TCAGGACGGCACCGAGGGTCGCGG |
|
Амидаза, гомологичная ферменту Rhodococcus sp. (A19131) |
AmiRsp-1 AmiRsp-2 |
5’-ATGGGCTTGCATGAACTGACGCTCG 5’-TCAAAGCGGCGCCAGTCGCGGCCA |
|
α-субъединица Со-нитрилгидратазы ( R. rhodochrous J1) |
F AM3 R АМ9 |
5’-GTGATACATATGAGCGAGCACGTCAAT 5’-ATGCATCATACGATCACTTCCTG |
|
β- субъединица Со-нитрилгидратазы ( R. rhodochrous J1) |
F АМ2 R АМ7 |
5’-GTGATACATATGGATGGTATCCACGAC 5’-ATGCATCACGCAGAGATCAGGTA |
|
α- субъединица Fe-нитрилгидратазы ( R. rhodochrous N-774, X54074) |
F АМ5 R АМ8 |
5’-СATATGTCAGTAACGATCGAC 5’-ATGCATCAGACGGTGGGAACCTG |
|
β- субъединица Fe-нитрилгидратазы ( R. rhodochrous N-774, X54074) |
F АМ4 R АМ6 |
5’-СATATGGATGGAGTACACGAT 5’-ATGCATCAGGCCGCAGGCTCGAG |
Амплификацию ДНК проводили с применением термостабильной Taq -SE ДНК-полимеразы (ООО «СибЭнзим», Новосибирск) на термоциклере Т3 (Biometra, Германия). Олигонуклеотидные праймеры разработаны с использованием базы данных GenBank (таблица).
Режим амплификации включал начальный цикл денатурации – 1 мин при 94°С; денатурацию, 94°С - 40 с; отжиг, 55-63° - 30 с; элонгацию, 72°С -60 с; (35 циклов) и завершающий этап – 60 с при 72°С.
Электрофоретическое разделение продуктов реакции проводили в 1,5 % агарозном геле в трис-боратном буфере при напряженности электрического поля 6 В/см.
Результаты и их обсуждение
Выделено более 400 клонов бактерий, способных к быстрому росту при использовании ацетонитрила или изобутиронитрила в качестве единственного источника углерода и азота. Для дальнейшего исследования отобраны 25 клонов, активно утилизирующих амиды и нитрилы и различающихся по морфологическим характеристикам.
Проведена идентификация бактерий по совокупности культурально-морфологических, биохимических, хемотаксономических свойств. Видовая принадлежность представителей рода Rhodococ-cus была подтверждена методом ПЦР-анализа генов 16S РНК с видоспецифическими праймерами.
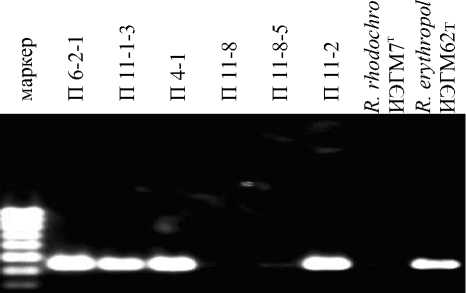
Рис. 1. Идентификация штаммов R. erythropolis по генам 16S РНК
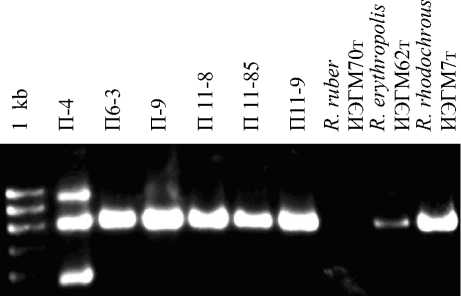
Рис. 2. Идентификация штаммов R. rhodochrous по генам 16S РНК
Основная часть активных изолятов была представлена нокардиоподобными микроорганизмами, в основном относящимися к роду Rhodococcus (рис. 1, 2).
В ходе селекционного процесса при постепенным повышении концентрации субстрата (нитрила) получены культуры R. erythropolis П4-1, П6-21, П11-2, П11-1-3 и R. rhodochrous П-11-8, П-1185, проявляющих амидазную активность более 6 Ед. при 25°С и более 30 Ед. при 50°С, а также активность нитрилгидратазы более 10°С. Установлено, что наилучшими субстратами для ферментов большинства штаммов являются ацетамид и пропионамид. Никотинамид и бензамид гидролизовались с меньшей скоростью.
Молекулярный анализ генов амидаз и нитрил-гидратаз
Для идентификации генов, кодирующих ферменты гидролиза амидов и нитрилов, проведен ПЦР-анализ с применением набора праймеров, специфичных для известных в настоящее время видов амидаз и нитрилгидратаз.
Показано, что геномы изолятов Rhodococcus содержат преимущественно последовательности, родственные ранее известным генам амидаз R. erythropolis , GenBank , E12517, R. rhodochrous N-771, X54074 и R. erythropolis , GenBank, M88614 (рис.3). Гены других видов амидаз встречались со значительно меньшей частотой.
Большинство штаммов также содержали последовательности, родственные генам α- и β- субъединиц Fe-содержащей нитрилгидратазы штаммов R. rhodochrous N-774, Rhodococcus sp. R312.
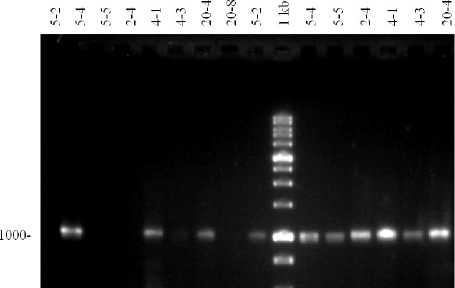
Рис. 3. Амплификация последовательностей, гомологичных генам амидазы R. erythropolis , GenBank, M886142.
Проведено секвенирование полученных ПЦР-фрагментов с помощью ДНК-секвенатирующей системы MegaBase1000.
Установлено, что гомология известной последовательности E12517 составляет от 94 до 99% (рис. 4, 5,А). У некоторых штаммов обнаружен ряд нуклеотидных замен, что, очевидно, обуславливает различия субстратной специфичности ферментов.
Последовательности, полученные в ПЦР-реакции с праймерами AmiReR, на 82-99% гомологичны гену амидазы R. erythropolis , приведенному в базе данных GenBANK под номером M88614 (рис.5,Б), относящемуся к структурному семейству нитрилаз-цианидгидратаз (Перцович, 2005).
----------------------------------------------------------------------------------------------------------------------------Section 1
(1) 1 ,10 go go 40 gO 66
П6-2-1 (1) TCC6AAACC3TCGAACTA6T6GCCCTGACCGSCCACCAC66CATCACCGCCCTCGGCG6CGCGA6C
AmiRhd fr (1) TCCGAAACC6TC*AACTGGTGGCCCTG*CC6GCCACCACGGC*TCACCACCCTCGGCGGCGCGAGC
П11-2 (1) TCCGAAACCGTCAAACTGGTGGCTCTGACCGGCCACCACGGCATCACCACCCTCGGCGGCGCGAGC
E12517 fr (1) TCCGAAACCGTCAAACTGGTGGCTCTGACCGGCCACCACGGCATCACCACCCTCGGCGGCGCGAGC
П4-1 (1) TCCGAAACCGTCAAACTGGTGGCTCTGACCGGCCACCACGGCATCACCACCCTCGGCGGCGCGAGC
П11-8-5 (1) TCCGAAACCGTCAAACTGGTGGCTCTGACCGGCCACCACGGCATCACCACCCTCGGCGGCGCGAG-
K17p (1) TCCGAAACCGTCAAACTGGTGGCTCTGACCGGCCACCACGGCATCACCACCCTCGGCGGCGCGAGC
Consensus (1) TCCGAAACCGTCAAACTGGTGGCTCTGACCGGCCACCACGGCATCACCACCCTCGGCGGCGCGAGC -------------------------------------------------------------------------------------------------------------------Section 2
(67) 67 80 90 J 00 1g 0 120 132
П6-2-1 (67) TACGGCAAAGCCCGGAACCTCGTACCGCTCGCCCGCGCCGCCTACGACAATGCCTTGAGACAATTC
AmiRhd fr (67) tacggcaaagcccggaacctcgtaccgcttgcccgcgccgcctacgacactgccttgagacaattc
П11-2 (67) tacggcaaagcccggaacctcgtaccgctcgcccgcgcagcctacgacactgccttgagacaatt.c
E12517 fr (67) TACGGCAAAGCCCGGAACCTCGTACCGCTCGCCCGCGCCGCCTACGACACTGCCTTGAGACAATTC
П4-1 (67) TACGGCAAAGCCCGGAACCTCGTACCGCTCGCCCGCGCCGCCTACGACACTGCCTTGAGACAATTC
П11-8-5 (66) TACGGCAAAGCCCGGAACCTCGTACCGCTCGCCCGCGCAACCTACGACACTGCCGTGAGACAATTN
K17p (67) TACGGCAAAGCCCGGAACCTCGTACCGCTCGCCCGCGCAGCCTACGACACTGCCTTGAGACAATTC
Consensus (67) TACGGCAAAGCCCGGAACCTCGTACCGCTCGCCCGCGCCGCCTACGACACTGCCTTGAGACAATTC -------------------------------------------------------------------------------------------------------------------Section 3 133) 133 140 150 160 ,170 180 198
П6-2-1 133) GACGTCCTGGTGATGCCCACACTGCCCTACGTCGCATCCGAAGTTCCGGCGAAGGACGTGGATCGT
AmiRhd fr 133) GACGTCCTGGTGATGCCAACGCTGCCCTACGTCGCATCCGAATTGCCGGCGAAGGACGTAGATCGT
П11-2 133) GACGTCCTGGTGATGCCCACACTGCCCTACGTCGCATCCGAACTACCGGCGAAGGACGTGGATCGT
E12517 fr 133) GACGTCCTGGTGATGCCCACACTGCCCTACGTCGCATCCGAACTACCGGCGAAGGACGTGGATCGT
П4-1 133) GACGTCCTGGTGATGCCCACACTGCCCTACGTCGCATCCGAATTGCCGGCGAACGACGTGGATCGT
П11-8-5 132) GACGTCCTGGTGATGCCCACACTGCCCTACGTCGCATCCGAATTGCCGGCGAACGACGTGGATCGT
K17p 133) GACGTCCTGGTGATGCCCACACTGCCCTACGTCGCATCCGAATTGCCGGCGAACGACGTGGATCGT
Consensus 133) gacgtcctggtgatgcccacactgccctacgtcgcatccgaattgccggcgaaggacgtggatcgt -------------------------------------------------------------------------------------------------------------------Section 4
Рис. 4. Нуклеотидные последовательности генов амидаз штаммов почвенных изолятов Rhodococcus , гомологичные генам R. erythropolis (E12517) и R. rhodochrous N744 (X54074).
А ---------------------------П 6-2-1 (0.0198)
---------------------------------------AmiRhd fr (0.0281)
------П11-2 (0.0045)
- E12517fr(0.0015)
П4-1 (0.0007)
--------------П11-8-5 (0.0120)
K17p (0.0000)
Б
111-8-5Г-А (-0.0004)
2-4ff-AR (0.0002)
11-2^(0.0002)
------------4-1 For-A (0.0082)
----------------------------------------------------------------5-2F-A [0.0404]
-------------------4-3F-A (0.0124)
-------------------------------------------------------------------------------------5-4for A (0.0534)
Рис. 5. Филогенетические древа нуклеотидных последовательностей, гомологичных генам амидазы R. rhodochrous N744 (А), R. rhodochrous M88614 (Б)
Заключение
Бактерии, активно трансформирующие амиды карбоновых кислот, широко представлены в почве естественной среды. Среди культур, обладающих высоким уровнем нитрилгидратазной и амидазной активности, преобладают представители рода Rhodococcus .
Среди почвенных изолятов Rhodococcus , обладающих высокой амидазной активностью, наиболее распространены гены амидаз двух типов, гомологичные последовательностям из R. erythropolis , GenBank , E12517 и R. erythropolis , GenBank, M88614.
Филогенетический анализ секвенированных последовательностей позволяет предположить, что структура вновь выявленных генов ближе к гипотетической предковой форме алифатической амидазы, чем последовательности, депонированные в GenBank E12517, M88614 (рис. 5).
Работа поддержана программой Президиума РАН «Молекулярная и клеточная биология», ВЦП «Развитие научного потенциала высшей школы (2009–2010 гг.)» и грантом поддержки молодых ученых УрО РАН.
Список литературы Почвенные актинобактерии рода Rhodococcus, обладающие высокой амидазной активностью
- Забазная Е.В. Отбор штаммов, трансформирующих акрилонитрил и акриламид в акриловую кислоту/Е.В. Забазная, С.В. Козулин, С.П. Воронин//Прикладная биохимия и микробиология. 1998. Т. 34, № 4. С. 377-384.
- Клонирование ДНК. Методы/пер. с англ.; под ред. Д. Гловера. М.: Мир, 1988. 538 с.
- Кузнецова М.В. Распространение нитрилконвертирующих бактерий в почвах Пермского края/М.В. Кузнецова, А.Ю. Максимов, Г.В. Овечкина, В.А. Демаков//Вестник Перм. ун-та. 2007. Т.5(10). С.96-99.
- Максимов, А.Ю. Влияние нитрилов и амидов на рост и нитрилгидратазную активность штамма Rhodococcus sp. gt1/А.Ю. Максимов, М.В. Кузнецова, Г.В. Овечкина и др.//Прикладная биохимия и микробиология. 2003. Т. 39, № 1. С. 63-68.
- Моисеева Т.Н. Скрининг штаммов-деструкторов акриловой кислоты и ее производных/Т.Н. Моисеева, С.В. Козулин, Л.К. Куликова, С.П. Воронин//Биотехнология. 1991. № 6. С. 79-83.
- Перцович С.И. Алифатическая амидаза из Rhodococcus rhodochrous-представитель семейства нитрилаз/цианидгидратаз/С.И. Перцович, Д.Т. Гуранда, Д.А. Подчерняев, А.С. Яненко, В.К. Швядас//Биохимия. 2005. Т.70. С.1556-1565
- Asano Y. Overview of screening for new microbial catalysts and their uses in organic synthesis -selection and optimization of biocatalysts//J. Biotechnol. 2002. Vol. 94. P. 65-72.
- Banerjee A. The nitrile-degrading enzymes: current status and future prospects/A. Banerjee, R. Sharma, U.C. Banerjee//Appl. Microbiol. Biotechnol. 2002. Vol. 60. P. 33-44.
- Cowan D. Biochemistry and biotechnology of mesophilic and thermophilic nitrile metabolizing enzymes/D. Cowan, R. Cramp, R. Pereira et al.//Extremophiles. 1998. Vol. 2, № 3. P. 207-216.
- Fournand D. Aliphatic and enantioselective amidases: from hydrolysis to acyl transfer activity/D. Fournand and A. Arnaud//J.Appl.Microbiol. 2001. Vol.91. P. 381-393.
- Kotlova E. K. Isolation and primary characterization of an amidase from Rhodococcus rhodochrous E.K. Kotlova, G.G. Chestukhina, O.B. Astaurova., T.E Leonova, A.S. Yanenko, V.G. Debabov//Biochemistry. 1999. Vol. 64, N. 4. P. 384-389.
- Yanenko A.S. Regulation of nitrile utilization in Rhodococcus/A.S. Yanenko, O.B. Astaurova, T.V. Gerasimova et al.//Biotechnologia. 1995. №.7-8. P. 139-144.


