Подходы к количественному моделированию структуры щелочных боросиликатных систем
Автор: Трофимов Евгений Алексеевич, Еремяшев Вячеслав Евгеньевич, Аникеев Андрей Николаевич, Габова Алина Юрьевна, Александрович Сергей Николаевич
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Физическая химия
Статья в выпуске: 4 т.5, 2013 года.
Бесплатный доступ
На основе простых исходных представлений получена модель, качественно соответствующая экспериментальным данным и описывающая изменения в структуре продуктов закалки силикатных, боратных и боросиликатных расплавов. Представленный набор уравнений, описывающих взаимодействие между структурными единицами, и значений констант позволяет на качественном уровне адекватно реальности моделировать структуру твёрдых оксидных сплавов Na 2O-SiO 2, Na 2O-B 2O 3 и применим к описанию системы Na 2O-B 2O 3-SiO 2 с любым соотношением [Na 2O]/[B 2O 3].
Боросиликатные стекла, структура, моделирование
Короткий адрес: https://sciup.org/147160273
IDR: 147160273 | УДК: 544.23
Methods of quantitative modeling for the structures of alkaline borosilicate systems
On the basis of simple initial concepts the model for description of changes in the structure of hardening products for silicate, borate and borosilicate melts, qualitatively corresponding to the experimental data, has been arrived at. The presented set of equations describing the interaction between the structural units and the values of the constants adequately permits designing the structure of solid oxide alloys Na 2O-SiO 2, Na 2O-B 2O 3; this method can be applied to Na 2O-B 2O 3-SiO 2 system description for any ratio [Na 2O]/[B 2O 3].
Текст научной статьи Подходы к количественному моделированию структуры щелочных боросиликатных систем
Экспериментальное исследование методами колебательной спектроскопии и спектроскопии ЯМР, обеспечивающее получение детальной информации об особенностях анионной структуры боратных и силикатных стекол, применительно к боросиликатным системам осложнено рядом факторов. Боросиликатные стекла характеризуются неоднородным распределением катионов-модификаторов между боратной и силикатной составляющими и большим набором структурных единиц, что требует большего объема экспериментальных исследований стекол с широким изменением состава. Имеет место и неоднозначность интерпретации спектральных данных вследствие взаимного влияния колебаний структурных единиц различного строения [4–5].
Эта проблема может быть частично разрешена в рамках термодинамического моделирования процессов взаимопревращения анионов в составе боросиликатных расплавов при изменении температуры и состава системы. Данный подход, реализованный с опорой на имеющиеся данные спектральных исследований, обеспечивает возможность согласования представлений о структуре боратных, силикатных и боросиликатных стекол и экстраполяции результатов в области ранее неизученных и промежуточных составов стекол [6].
В рамках обработки полученных экспериментальных результатов с помощью термодинамического моделирования, основанного на различных вариантах модели ассоциированных растворов, нами была сформулирована термодинамическая модель, описывающая соотношение и взаимодействие структурных единиц различного строения, существующих в щелочных боросиликатных системах широкого диапазона составов. Количественные параметры модели были подобраны, опираясь на данные исследований бинарных и тройных систем, проведенных методами спектроскопии КР и ЯМР, а также термодинамических расчетов в рамках других моделей. Сопоставление результатов расчета по этой модели с экспериментальными данными позволило оценить адекватность предлагаемой модели и ее применимость для расчета в других системах.
Методика моделирования
Расчёт концентраций структурных единиц твёрдых фаз, относящихся к системам Na 2 O–SiO 2 , Na 2 O–B 2 O 3 , Na 2 O–B 2 O 3 –SiO 2 , опирается на следующие положения:
-
1. Структурными единицами в продуктах закалки системы Na2O–SiO2 являются SiO4/2, SiO 3/2 O–, SiO 2/2 O 2 2–, SiO 1/2 O 3 3–, SiO 4 4–, O2-, Na+. В системе Na 2 O–B 2 O 3 такими единицами являются BO 3/2 , BO 2/2 O–, BO 1/2 O 2 2–, BO 3 3– , O2-, Na+, а также сложная диборатная единица B 4 O 5 O 4/2 2–, в составе которой два из четырёх атомов бора четырёхкоординированы.
-
2. Составы, относящиеся к тройной системе Na2O–B2O3–SiO2, характеризуются наличием всех перечисленных выше структурных единиц, которые наличествуют в двойных системах, а также дополнительно ещё двух сложных единиц, в которых атом бора находится в четырёхкоординированном состоянии – BSiO4– и BSi3O8–.
-
3. Структурные единицы, слагающие стёкла (за исключением катионов натрия), обратимо реагируют друг с другом. Для каждой реакции можно записать выражение для константы равновесия. При этом активность структурных единиц считается равной их концентрации в составе твёрдой оксидной фазы.
Характеристики отрицательных и нейтральных структурных единиц и их условные обозначения (за исключением катионов натрия и анионов кислорода) представлены в табл. 1. Процесс их взаимопревращения исчерпывающим образом может быть описан набором химических реакций, представленным в табл. 2. Таким образом, в основе модели лежат перечисленные в столбце 3 табл. 2 трансцендентные уравнения равновесия вместе с очевидными уравнениями материального баланса.
Для численного решения систем уравнений относительно валового состава оксидной системы и визуализации результатов расчёта использованы возможности программного пакета MathCAD.
Таблица 1
Структурные единицы силикатных, боратных и боросиликатных стёкол
|
Химическая формула |
Условное обозначение |
Число атомов кислорода на атом неметалла |
Заряд частицы на один атом неметалла |
|
SiO 4/2 |
Q4 |
2 |
0 |
|
SiO 3/2 O– |
Q3 |
2,5 |
–1 |
|
SiO 2/2 O 2 2– |
Q2 |
3 |
–2 |
|
SiO 1/2 O 3 3– |
Q1 |
3,5 |
–3 |
|
SiO 4 4– |
Q0 |
4 |
–4 |
|
BO 3/2 |
B 3 |
1,5 |
0 |
|
BO 2/2 O– |
B 2 |
2 |
–1 |
|
BO 1/2 O 2 2– |
B 1 |
2,5 |
–2 |
|
BO3 3– |
B0 |
3 |
–3 |
|
B 4 O 5 O 4/2 2– (2BO 4/2 – · 2BO 3/2 ) |
B T |
1,75 |
–0,5 |
|
BSiO 4 –(1) (BO 4/2 – · SiO 4/2 ) |
B Q |
2 |
–0,5 |
|
BSiO 4 –(2) (SiO 3/2 O– · BO 3/2 ) |
QB |
2 |
–0,5 |
|
BSi 3 O 8 – (BO 4/2 – · 3SiO 4/2 ) |
B3Q |
2 |
–0,25 |
Таблица 2
Уравнения реакций взаимопревращения структурных единиц
|
№ |
Уравнение реакции |
K |
lgK |
|
1 |
2 SiO 4 4–= 2 SiO 1/2 O 3 3–+ O2– |
[SiO 1/2 O 3 3– ] 2 [O 2– ] K(1) = [SiO 4 4–]2 |
–4,5 |
|
2 Q0 = 2 Q1 + O2– |
|||
|
2 |
2 SiO 1/2 O 3 3–= SiO 4 4–+ SiO 2/2 O 2 2– |
[SiO 4 4– ][SiO 2/2 O 2 2– ] K(2) = [SiO 1/2 O 3 3–]2 |
–2,3 |
|
2 Q1 = Q0 + Q2 |
|||
|
3 |
2 SiO 2/2 O 2 2–= SiO 1/2 O 3 3–+ SiO 3/2 O– |
[SiO 1/2 O 3 3– ][SiO 3/2 O – ] K(3) = [SiO 2/2 O 2 2–]2 |
–2,1 |
|
2 Q2 = Q1 + Q3 |
|||
|
4 |
2 SiO 3/2 O–= SiO 2/2 O 2 2–+ SiO 4/2 |
[SiO 2/2 O 2 2– ][SiO 4/2 ] K(4) = [SiO 3/2 O–]2 |
–1,88 |
|
2 Q3 = Q2 + Q4 |
|||
|
5 |
2 BO 3 3–= 2 BO 1/2 O 2 2– + O2– |
K(5) = [BO 1/2 O 2 2– ] 2 [O 2– ] [BO 3 3–]2 |
–3,5 |
|
2 B0 = 2 B1 + O2– |
|||
|
6 |
2 BO 1/2 O 2 2– = BO 3 3– + BO 2/2 O– |
[BO 3 3– ][BO 2/2 O – ] K(6) = [BO 1/2 O 2 2–]2 |
–3,0 |
|
2 B1 = B0 + B2 |
Физическая химия
Окончание табл. 2
|
№ |
Уравнение реакции |
K |
lgK |
|
7 |
6 BO 2/2 O–= 2 BO 1/2 O 2 2– + B 4 O 5 O 4/2 2– |
[BO 1/2 O 2 2– ] 2 [B 4 O 5 O 4/2 2– ] K(7) = [BO 2/2 O–]6 |
–2,1 |
|
6 B2 = 2 B1 + BT |
|||
|
8 |
B 4 O 5 O 4/2 2–= 2 BO 3/2 + 2 BO 2/2 O– |
[BO 3/2 ]2[BO 2/2 O–]2 K(8) = [B 4 O 5 O 4/2 2–] |
–2,85 |
|
BT = 2 B3 + 2 B2 |
|||
|
9 |
BSiO 4 –(1) = BO 2/2 O– + SiO 4/2 |
[BO 2/2 O – ][SiO 4/2 ] K(9) = [BSiO 4 –(1)] |
–0,7 |
|
BQ = B2 + Q4 |
|||
|
10 |
2 BSiO 4 –(2) = SiO 4/2 + BO 1/2 O 2 2– + BO 3/2 |
[SiO 4/2 ] 2 [BO 1/2 O 2 2– ][BO 3/2 ] K(10) = [BSiO4–(2)]2 |
–3,15 |
|
QB = 2 Q4 + B1 + B3 |
|||
|
11 |
BSi 3 O 8 –= BO 2/2 O– + 3 SiO 4/2 |
[BO 2/2 O–][SiO 4/2 ]3 K(11) = [BSi 3 O 8 –] |
–0,3 |
|
B3Q = B2 + 3 Q4 |
Результаты и их обсуждение
Результаты моделирования количественного состава твёрдых оксидных фаз систем Na2O– SiO 2 , Na 2 O–B 2 O 3 , и NaBO 2 –SiO 2 , соответствующей системе Na 2 O–B 2 O 3 –SiO 2 для случая [Na 2 O]/[B 2 O 3 ]=1, представлены на рис. 1–3. По оси ординат отложены концентрации структурных единиц в мольных долях от общего их количества (за вычетом катионов натрия). Согласно представлениям, лежащим в основе модели, четырёхкоординированный бор присутствует в исследуемых системах только в составе сложных тетраборатных и боросиликатных единиц. Результаты моделирования пересчитаны на содержание исключительно простых единиц Qn и Bn, строение и механизм взаимного превращения которых показан в табл. 2. Это сделано с целью облегчения сопоставления результатов нашего моделирования с экспериментальными результатами, полученными методами спектроскопии ЯМР и КР, а также с результатами моделирования, выполненного другими авторами.
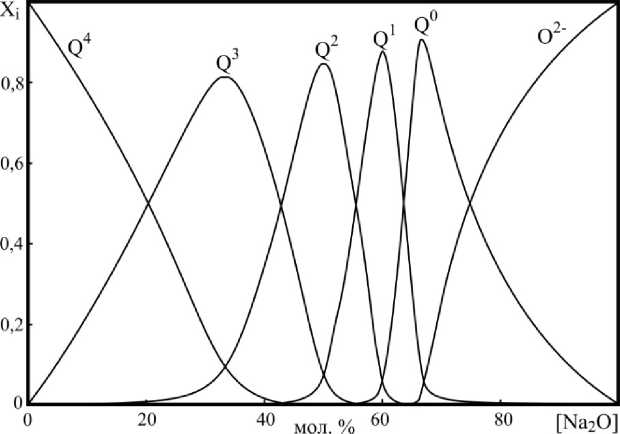
Рис. 1. Результаты моделирования количественного состава продуктов закалки в системе Na 2 O–SiO 2
Для силикатной системы в полном соответствии с экспериментальными данными добавление оксида-модификатора влечет образование и увеличение доли Qn единиц, содержащих большее количество немостиковых атомов кислорода. На диаграмме, построенной для боратной системы, с увеличением доли NaBO2 в составе стекла прослеживается закономерное увеличение доли структурных единиц, образованных трехкоординированным бором, сначала с одним (BO2/2O–), а затем двумя и тремя немостиковыми атомами кислорода (BO1/2O22–, BO33–). Бор в четвертной координации наблюдается только до 60 мол. % NaBO2, достигая максимума своего содержания при 30–40 мол. % NaBO2.
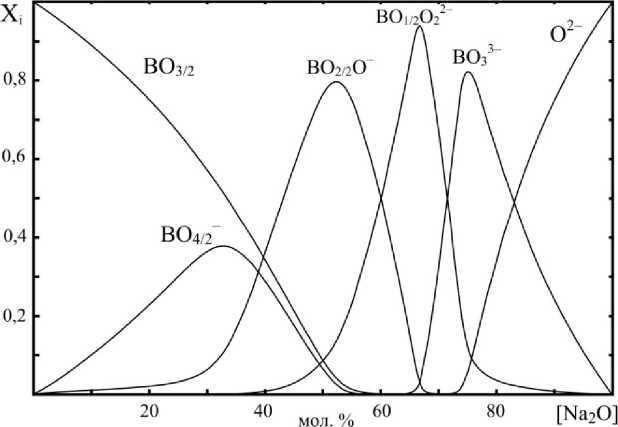
Рис. 2. Результаты моделирования количественного состава продуктов закалки в системе Na 2 O–B 2 O 3
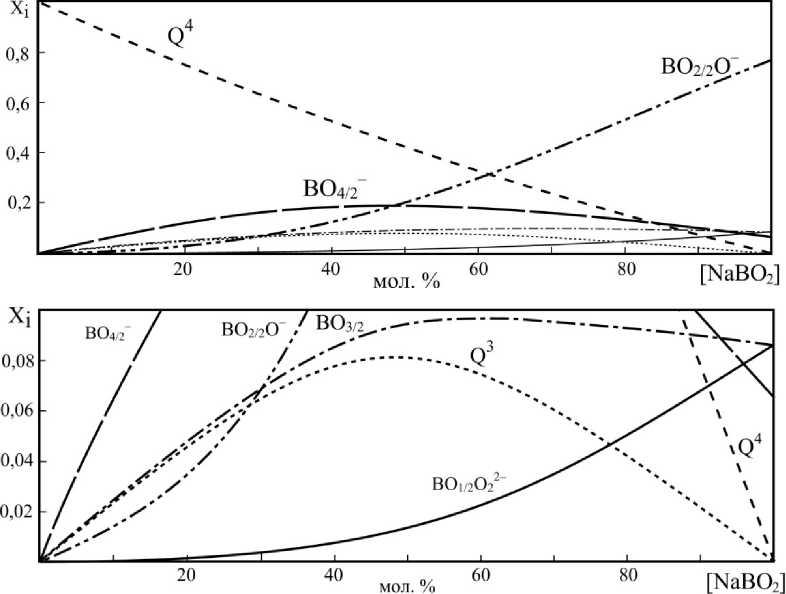
Рис. 3. Результаты моделирования количественного состава продуктов закалки в системе NaBO 2 –SiO 2
Изменения, которые происходят с увеличением содержания NaBO2 в системе NaBO2–SiO2, можно свести к следующим основным тенденциям: уменьшение концентрации Q4, рост доли BO 2/2 O– и увеличение доли четырёхкоординированного бора во всем диапазоне составов, которая до некоторого момента превышает долю трехкоординированного бора. Qn единицы, содержащие
Физическая химия
немостиковые атомы кислорода, во всем диапазоне составов представлены только Q3 единицами, концентрация которых сначала растет, а затем падает.
В целом наблюдаемые закономерности качественно соотносятся с экспериментальными данными во всем диапазоне изученных составов [5–8]. Это указывает на адекватность предлагаемой термодинамической модели, а наблюдаемые количественные отклонения обусловлены рядом объективных причин. Вынужденное упрощение многообразия смешанных боросиликатных единиц обеспечило упрощение математического решения, но негативно сказалось на количественном соответствии расчетных и экспериментальных данных. Помимо соответствия исходных положений модели реалиям структуры исследуемой системы ключевым фактором, влияющим на точность проведённого моделирования, являются значения констант равновесия реакций (см. табл. 2). За исключением значения для реакции 2Q3 = Q2 + Q4, непосредственно заимствованного из работы [7], эти значения подобраны в процессе моделирования с опорой на экспериментальные данные, представленные в литературе. Такие данные зачастую противоречивы и относятся, как правило, не ко всему диапазону составов, а к областям с относительно низким содержанием Na2O. Поэтому точность большинства значений lgK заведомо невысока, и работы по их уточнению на основе экспериментальных данных должны быть продолжены. Для некоторых диапазонов концентраций, по которым существуют надёжные экспериментальные данные [8], соответствие разработанной нами модели реальности носит количественный характер.
Заключение
На основе простых исходных представлений получена модель, качественно соответствующая экспериментальным данным и описывающая изменения в структуре продуктов закалки силикатных, боратных и боросиликатных расплавов, происходящие с изменением их состава. Представленный набор уравнений, описывающих взаимодействие между структурными единицами, и значений констант позволяет на качественном уровне адекватно реальности моделировать структуру твёрдых оксидных сплавов Na2O–SiO2, Na2O–B2O3 и потенциально применим к описанию системы Na 2 O–B 2 O 3 –SiO 2 с любым соотношением [Na 2 O]/[B 2 O 3 ]. Результат, полученный при моделировании, качественно, а в некоторых случаях и количественно, соотносится с экспериментальными данными и обеспечивает возможность экстраполяции наблюдаемых структурных изменений в области, ранее неизученных и промежуточных составов стекол.
Работа выполнена в рамках ФЦП «Научные и научно-педагогические кадры инновационной России» на 2009–2013 годы по проекту № 14.B37.21.0608 и при поддержке РФФИ, грант № 13-08-00545.
Список литературы Подходы к количественному моделированию структуры щелочных боросиликатных систем
- Du, L.-S. Solid-state NMR study of metastable immiscibility in alkali borosilicate glasses/L.-S. Du, J.F. J. Stebbins//Non-Cryst. Solids. -2003. -V. 315. -P. 239-255.
- Manara, D. Advances in understanding the structure of borosilicate glasses: A Raman spectroscopy study/D. Manara, A. Grandjean, D.R. Neuville//American Mineralogist. -2009. -V. 94, № 5-6. -P.777-784.
- Еремяшев, В.Е. Влияние параметров R и K на особенности анионной структуры щелочных боросиликатных стекол/В.Е. Еремяшев, Л.А. Шабунина//Вестник ЮУрГУ. Серия «Химия». -2011. -№ 6 (33). -С. 68-72.
- Еремяшев, В.Е. Изучение влияния замещения катиона натрия катионами щелочноземельных металлов на структуру боросиликатных стекол/В.Е. Еремяшев, А.А. Осипов, Л.М. Осипова//Стекло и керамика. -2011. -№ 7. -С. 3-6.
- Effects of the Iron Content and Redox State on the Structure of Sodium Borosilicate Glasses: A Raman, Mossbauer and Boron K-Edge XANES Spectroscopy Study/B. Cochain, D.R. Neuville, G.S. Henderson et al.//Journal of the American Ceramic Society. -2012. -V. 95, № 3. -P. 962-971.
- The thermodynamic modelling of glass properties: A practical proposition/N.M. Vedishcheva, B.A. Shakhmatkin, M.M. Shultz et al.//J. Non-Crystalline Solids. -1996. -V. 196. -P. 239-243.
- Malfait, W.J. Quantitative Raman spectroscopy: Speciation of Na-silicate glasses and melts/W.J. Malfait, V.P. Zakaznova-Herzog, W.E. Halter//American Mineralogist. -2008. -V. 93. -P.1505-1518.
- Structural investigation of sodium borate glasses and melts by Raman spectroscopy. II. Conversion between BO4 and BO2O-units at high temperature/Y. Tetsuji, K. Noboru, S. Shuichi et al.//J. Non-Crystalline Solids. -2003. -V. 321. -P. 147-156.


