Поиск и изучение генов, кодирующих металло-бета-лактамазы, у госпитальных штаммов Pseudomonas aeruginosa
Автор: Кузнецова Марина Валентиновна, Егорова Дарья Олеговна, Карпунина Тамара Исаковна
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 3-4, 2011 года.
Бесплатный доступ
Изучены карбапенемоустойчивые нозокомиальные штаммы Pseudomonas аeruginosa, изолированные в хирургических стационарах г. Перми и пос. Лобаново. Установлено, что в геноме 34 культур присутствуют фрагменты ДНК, соответствующие по размеру генам blaVIM-2. Принадлежность амплифицированных генов к подгруппе blaVIM-2 была подтверждена результатами рестрикционного анализа с эндонуклеазой HindII. Сравнение нуклеотидных последовательностей blaVIM шести изолятов, принадлежащих к разным геномогруппам, показало высокий уровень сходства (99-100%) участков генов длиной 615-741 п.н. с геном blaVIM-2 референтного штамма P. aeruginosa COL-1 (GenBank GQ853417.1).
Pseudomonas аeruginosa, карбапенемы, металло-бета-лактамазы
Короткий адрес: https://sciup.org/147204561
IDR: 147204561 | УДК: 579.61:579.25:579.841.11
Search study of metallo-betta-lactamase genes from the Pseudomonas aeruginosa clinical isoltes
The Pseudomonas аeruginosa nosocomial cultures resistant to carbapenemes isolated from surgical hospitals in c. Perm and Lobanovo. It is established that genome of 34 cultures are present the fragments of DNA corresponding on the size to the genes blaVIM-2. Results DNA restriction analysis with endonuclease HindII has been confirmed, that DNA fragments from PCR amplification are members of subgroup blaVIM-2. Comparison of the nucleotide sequences blaVIM of the six isolates, belonging to different variant genome type, has shown high level of similarity (99-100 %) fragments of genes in length 615-741 bp. with a gene blaVIM-2 of the P. aeruginosa COL-1 (GenBank GQ853417.1).
Текст научной статьи Поиск и изучение генов, кодирующих металло-бета-лактамазы, у госпитальных штаммов Pseudomonas aeruginosa
Карбапенемы – это один из важнейших классов антибиотиков, сочетающий исключительно широкий спектр антибактериальной активности, низкую токсичность и благоприятные фармакологические параметры (Галкин, 2007). Меропенем и имипенем, наряду с другими «антисинегнойными» средствами, являются препаратами выбора в терапии тяжелых нозокомиальных инфекций, вызванных P. aeruginosa (Руднов, 2005; Иванов и др., 2009).
Наиболее распространенным механизмом резистентности к карбапенемам у P. aeruginosa является их ферментная инактивация. Этот механизм может реализовываться с помощью бета-лактамаз трех классов: некоторыми ферментами классов А и D и металло-бета-лактамазами класса В (Queenan, Bush, 2007). Для P. aeruginosa описано пять основных групп карбапенемаз молекулярного класса В, подкласса В1: VIM, IMP, SPM, GIM и SIM. Все они содержат по два атома цинка и различаются аминокислотными последовательностями. Гены, кодирующие большую часть этих ферментов, в составе генных кассет включены в различные мобильные элементы, в основном интегроны 1-го класса.
VIM-1-карбапенемаза (for “Verona integron-encoded metallo-lactamase”) была впервые выделена из нозокомиального штамма P. aeruginosa в Вероне (Италия) в 1997 г. (Lauretti, Riccio, Mazzariol et al., 1999). Позднее описан VIM-2-фермент из штамма, изолированного еще в 1996 г. во Франции (Poirel, Naas, Nicholas et al., 2000). Госпитальные штаммы P. aeruginosa чаще всего продуцируют именно VIM-ферменты (Lee, Lim, Yum et al., 2002; Черкашин, Федорчук, Иванов и др., 2006; Шевченко, Эйдельштейн, Степанова, 2007). Внутри VIM-карбапенемаз выделяют две большие филогенетические линии: подгруппа VIM1 (VIM-1, 4, 5, 12, 14, 19) и подгруппа VIM2 (VIM-2, 3, 6, 8, 9, 10, 11, 13, 15, 16, 17, 18, 23), в отдельный кластер выделен единственный фермент VIM-7 (Toleman, Rols-ton, Jones, Walsh, 2004). Сегодня описано 25 вариантов этих ферментов, и их список постоянно пополняется #table1). Первый фермент IMP-группы (for “active on imipenem”) был описан у А. baumannii, изолированного в госпитале Италии (Riccio, Franceschini, Boschi et al., 2000). После этого IMP-карбапенемазы найдены во всем мире, включая США и Австралию. GIM-1-фермент (for “German imipenemase”) был изучен в Германии в 2002 г. (Castanheira, Toleman, Jones et al., 2004), SPM-1 (for “Sao Paulo metallo-lactamase”) впервые выделен у штаммов P. aeruginosa из Сан-Паулу в Бразилии (Poirel, Magalhaes, Lopes, Nordmann, 2004). Фермент SIM-1 (for “Seoul imipenemase”) – последний из металло-лактамаз описан в Корее (Lee, Yum, Yong et al., 2005). Если SPM-, GIM- и SIM-ферменты почти не распространись за пределы
страны их происхождения, то VIM и IMP-металло-бета-лактамазы описаны по всему миру и продолжают обнаруживаться не только у P. aeruginosa , но и у других видов бактерий (Queenan, Bush, 2007).
Цель настоящего исследования – поиск и изучение генов металло-бета-лактамаз у нозокомиальных штаммов P. aeruginosa .
Материалы и методы исследования
Исследовано 34 штамма P. aeruginosa , обладающих фенотипическими признаками продукции ме-талло-бета-лактамаз (положительных в ЭДТА-тесте) (Arakawa et al., 2000). Культуры выделены в 2008– 2009 гг. от больных крупных хирургических стационаров г. Перми (краевая клиническая больница – ККБ, городская клиническая больница – ГКБ) и пос. Лобаново Пермского края (центральная районная больница – ЛКБ).
ДНК получали, как описано G.G. Stone, R.D. Oberst, S. Hays et al. (1994). Петлю биомассы бактериальной культуры инокулировали в 100 мкл сверхчистой воды, прогревали при 95°С в твердотельном термостате «Термит» 15 мин, пробы охлаждали, центрифугировали 5 мин при 12 тыс. об./мин. Супернатант использовали в генетических исследованиях.
Генетическое типирование (фингерпринтинг) штаммов осуществляли с использованием методов
RAPD-ПЦР (с праймером М13) и BOX-ПЦР (Versa-lonic et al., 1994). Продукты реакции разделяли посредством электрофореза в 1.2%-ном агарозном геле.
Таблица 1
Праймеры для ПЦР-анализа генов металло-бета-лактамаз
Рестрикционный анализ амплифицированных фрагментов ДНК, с использованием праймеров к bla VIM-2 -гену, проводили с помощью эндонуклеазы Hind II. 5 мкл ПЦР-продукта обрабатывали 1 ед. ре-стриктазы (Fermentas, Литва) с использованием рекомендуемого буфера и при соответствующем температурном режиме.
«Healthcare» (США) использовался согласно рекомендациям производителя. Для секвенирующей ПЦР использовали те же праймеры, что и для наработки ампликонов. Предварительный анализ гена blaVIM-2 и «внутреннего» фрагмента генов blaVIM и поиск гомологичных последовательностей осуществляли, используя программы BLAST и базы данных GenBank/EMBL/DDBJ . Далее их анализировали с использованием программ CLUSTAL X 1.83 (Thompson et al., 1994), TREECON version 1.3b (Van de Peer et al., 1994). Анализ первичной структуры белков осуществляли с помощью программы Vector NTI 10 . Поиск гомологичных последовательностей выполнен с использованием программ BLAST. Выравнивание аминокислотных последовательностей проведено с помощью программы CLUSTAL X 1.83.
Результаты и их обсуждение
Скрининг штаммов на наличие генов, кодирующих металло-бета-лактамазы
Для определения родства выделенных изолятов и отбора штаммов для дальнейших исследований проведено их генетическое типирование. Штаммы P. aeruginosa , выделенные от больных ГКБ, распределились в две геномогруппы. Изоляты 2ПЛ, 31 и 60, полученные из ЛКБ, обладают индивидуальными RAPD-профилями. Все культуры P. aeruginosa ККБ образуют одну геномогруппу (табл. 2). На матрице ДНК исследуемых штаммов была проведена амплификация нуклеотидных последовательностей, гомологичных гену bla VIM-2 и консервативному участку генов группы VIM.
Таблица 2
Распределение исследуемых штаммов P. aeruginosa в геномогруппы
|
ЛПУ |
Изолят |
Геномо-группа |
|
ГКБ |
11р, 9р, 2р, 10к, 11к, 12к, 13к, 1-13, 2-1, 2-4, 2-9, 3-4, 3-6, 3-7, 3-9, 3-14, 3-16, 3-17, 3-22, 3-22а |
I |
|
125, 127, 128, 129 |
II |
|
|
ККБ |
195, 196, 197, 198, 201, 203 |
III |
|
ЛКБ |
2 ПЛ |
IV |
|
31 |
V |
|
|
60, 18 |
VI |
Специфичная амплификация была обнаружена у 34 штаммов, изолированных из 3 стационаров (ГКБ, ККБ, ЛКБ) (рис. 1). Амплифицированные участки ДНК длиной около 260 п.н. соответствуют по размеру консервативной части генов группы VIM, а ДНК-фрагменты размером 800 п.н. – полному bla VIM-2 -гену.
261 п.н.
---►
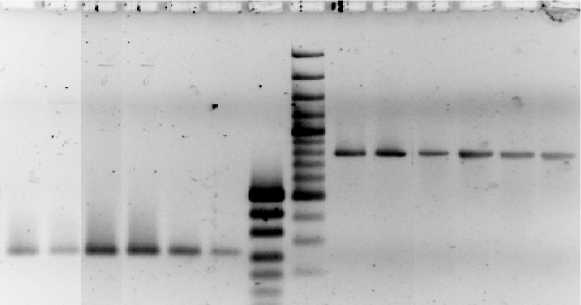
801 п.н. ◄---
1 2 3 4 5 6 7 8 9 10 11 12 13 14
А
В
Рис. 1 . Электрофореграмма продуктов амплификации консервативных последовательностей (А) и полных генов (В), кодирующих металло-бета-лактамазы, изолятов P. aeruginosa :
1, 9 – штамм 129 (ГКБ, геномогруппа II); 2,10 – штамм 3-16 (ГКБ, геномогруппа I); 3, 11 – штамм 198 (ККБ, геномогруппа III); 4, 12 – штамм 2ПЛ (ЛКБ, геномогруппа IV); 5, 13 – штамм 31 (ЛКБ, геномогруппа V); 6, 14 – штамм 60 (ЛКБ, геномогруппа VI); 7 – маркер молекулярных масс pUC19 ДНК/MspI (“Силекс”, Россия); 8 – маркер молекулярных масс O’GeneRulerTM 100bp Plus DNA Ladder (“Fermentas”, Литва)
Амплификация с праймерами к фланкирующим участкам генов других металло-бета-лактамаз не дала положительного результата.
ПДРФ-анализ амплифицированных участков
Для выявления сходства и различий между исследуемыми генами, кодирующими VIM-карба-пенемазы, был проведен анализ полиморфизма длин рестрикционных фрагментов амплифициро-ванных последовательностей. Набор рестрикционных фрагментов, полученный после обработки ампликонов blaVIM-2-гена исследуемых штаммов ре-стриктазой HindII, был представлен фрагментами ДНК длиной 414 и 387 п.н. (рис. 2). Длины полу- ченных рестрикционных фрагментов сопоставимы с длинами фрагментов на рестрикционных картах гена blaVIM-2 известных карбапенеморезистентных штаммов P. aeruginosa (рис. 3).
Анализ нуклеотидной последовательности амплифицированных фрагментов bla VIM-2
Определены нуклеотидные последовательности фрагментов и полных генов металло-бета-лактамаз группы VIM, амплифицированные с ДНК штаммов P. aeruginosa 3-16, 127, 2ПЛ, 31, 60, 198, являющихся представителями разных геномогрупп. Анализ нуклеотидной последовательности фрагментов длиной около 260 п.н. исследуемых штам- мов показал их 100%-ное сходство между собой, а также с известными последовательностями гена blaVIM-2 на участке с 114 по 353 нуклеотид. Исследуемые участки ДНК размером 615-741 п.н. были на 99–100% сходны с последовательностью blaVIM-2-гена известных штаммов (табл. 3, рис. 4). Степень сходства с геном blaVIM-2 референтного штамма P. aeruginosa COL-1 (GenBank AF191564.1) составила 99-100%. Обнаружены точечные нуклеотидные замены в последовательности исследуемых генов у 4 штаммов (табл. 3), в трех из них выявлена замена аминокислотного остатка.
У штаммов P. aeruginosa 2ПЛ, 31 и 3–16 обнаружена точечная мутация bla VIM-2 -гена в позиции 85, несущая замену серина на пролин, которая характерна для генов, кодирующих ферменты подгруппы VIM-1 и VIM-7 (Lauretti et al., 1999; Tole-man et al., 2007). Учитывая, что эта область находится на поверхности белка и удалена от активного центра, данные замены не влияют на связывание фермента с субстратом – антибиотиком. Несмотря на выявленные нуклеотидные замены результаты сравнительного анализа свидетельствуют о наличии bla VIM-2 -генов в штаммах P. aeruginosa , изолированных из крупных стационаров г. Перми и пос. Лобаново.
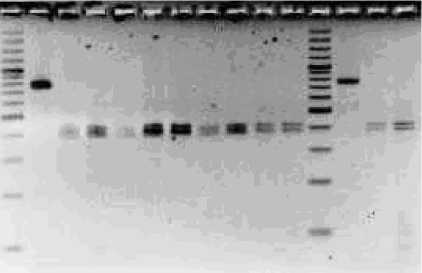
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
Рис. 2 . Электрофореграмма гидролиза ПЦР-продуктов амплификации bla VIM-2 -гена, обработанных Hind II:
1, 12 – маркер молекулярных масс O’GeneRulerTM 100bp Plus DNA Ladder; 2, 13 – ампликоны bla VIM-2 -гена; изоляты из ЛКБ: 3 – штамм 2ПЛ; 4 – штамм 31; 5 – штамм 60; изоляты из ККБ: 6 – штамм 198; 7
– штамм 201; 8 – штамм 203; изоляты из ГКБ: 9 – штамм 3-16; 10 – штамм 128; 11 – штамм 127; 14 – штамм 1-13; 15 – штамм 3-9
0.1
VIM2 (GQ853417.1)
VBI16 (ELT419746)
VBI15 (ELT419745)
VIM18 (АМ778091)
VIM3 (PS-26/00)
там (AY165025)
mill (AY605049)
2 ПЛ
bla VIM-1
109 305 387
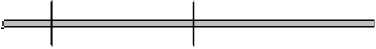
bla VIM-2
414 387
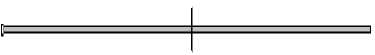
801 п.н.
Рис. 3 . Карты расположения сайтов реестрик-ции эндонуклеазы Hind II на генах bla VIM .
Карты построены с помощью программы Vector NTI для известных последовательностей, кодирующих металло-бета-лактамазы основных ферментов группы VIM (подгруппа VIM-1 – карта на примере bla VIM-1 идентична картам других ферментов данной подгруппы, подгруппа VIM-2 – карта на примере bla VIM-2 соответствует картам остальных ферментов данной подгруппы, за исключением bla VIM-13)
юо
3-16
— VIM8 (AY524987)
¥IM5(PSEK5)
VIM1 (Y180502)
таи 4 (FJ445404)
VIM4 (GU250441)
VIM13(EF577407)
Рис. 4 . Древо сходства нуклеотидных последовательностей полных генов металло-бета-лактамаз (группа VIM) бактерий рода Pseudomonas , построенное методом UPGMA :
“Bootstrap”-анализ проведен на 1000 повторностях. Жирным крупным шрифтом выделены штаммы, исследуемые в данной работе. В скобках указаны номера последовательностей, депонированных в GenBank, или обозначение штамма
Таблица 3
Анализ нуклеотидной последовательности фрагментов полных генов bla VIM-2
|
Штамм |
Размер секвенированного фрагмента, п.н. (расположение на гене bla VIM-2 P. aeruginosa COL-1 ) |
Сходство с bla VIM-2 P. aeruginosa COL-1 , % |
Нуклеотидные замены* |
Аминокислотные замены* |
|
|
2ПЛ |
665 |
с 24 п.н. по 689 п.н. |
99 |
Т85С |
S29P |
|
31 |
637 |
с 68 п.н. по 704 п.н. |
99 |
T85C |
S29P |
|
60 |
615 |
с 51 п.н. по 665 п.н. |
100 |
- |
- |
|
3-16 |
741 |
с 61 п.н. по 801 п.н. |
99 |
T85C |
S29P |
|
127 |
678 |
с 97 п.н. по 774 п.н. |
99 |
G744A |
нет замены |
|
198 |
637 |
с 63 п.н. по 698 п.н. |
100 |
- |
- |
*Номер замены соответствует месту нуклеотида и аминокислотного остатка от начала гена bla VIM-2
Заключение
Таким образом, устойчивость к карбапенемам 34 культур P. aeruginosa , изолированных из двух стационаров г. Перми и пос. Лобаново, обусловлена продукцией ими металло-бета-лактамаз группы VIM, и в частности – фермента VIM-2. Можно предположить, что в Пермском крае циркулируют преимущественно продуценты VIM-2-подобных ферментов. Полученные результаты согласуются с литературными данными о распространенности VIM-2-обусловленной карбапенеморезистентности внутрибольничных штаммов P. aeruginosa в России и странах Европы (Poirel, Naas, Nicholas et al., 2000; Черкашин, Федорчук, Иванов и др., 2006; Шевченко, Эйдельштейн, Степанова, 2007).
Список литературы Поиск и изучение генов, кодирующих металло-бета-лактамазы, у госпитальных штаммов Pseudomonas aeruginosa
- Галкин Д.В. Карбапенемы через 20 лет после открытия: современные микробиологические и клинические аспекты//Клин. микробиол. антимикроб. химиотер. 2007. Т. 9, № 2. С. 133-152.
- Иванов Д.В. и др. Особенности антибиотикочувствительности важнейших грамотрицательных возбудителей нозокомиальных инфекций//Вест. Росс. гос. мед. ун-та. 2009. № 2. С. 26-29.
- Руднов В.А. Антибиотикотерапия госпитальных инфекций, вызванных P. aeruginosae//Рус. мед. журн. 2005. Т. 13. № 7. С. 485-490.
- Черкашин Е.А., Федорчук В.В., Иванов Д.В. и др. Исследование распространенности метало-бе-талактамаз в Российской Федерации//Вестн. Моск. ун-та. Сер. Химия. 2006. №4 7(3). С. 83-86.
- Шевченко О.В., Эйдельштейн М.В., Степанова М.Н. Металло-лактамазы: значение и методы выявления у грамотрицательных неферментирующих бактерий//Клин. микробиол. антимикроб. химиотер. 2007. Т. 9. № 3. С. 211-218.
- Arakawa Y., Shibata N., Shibayama K. [et al] Convenient test for screening metallo-b-lactamaseproducing gram-negative bacteria by using thiol compounds//J. Clin. Microbiol. 2000. Vol. 38. P. 40-43.
- Castanheira M., Toleman M.A., Jones R.N. et al. Molecular characterization of -lactamase gene, bla-GIM-1, encoding a new subclass of metallo-blactamase//Antimicrob. Agents Chemother. 2004. Vol. 48. P.4654-4661.
- Lauretti L., Riccio M.L., Mazzariol A. et al. Cloning and characterization of [bla.sub.VIM], a new integron-borne metallo-[beta]-lactamase gene from a Pseudomonas aeruginosa clinical isolate//Antimicrob. Agents. Chemother. 1999. Vol. 43. P. 1584-1590.
- Lee K., Lim J.B., Yum J.H. et al. [bla.sub.VIM-2] cassette-containing novel integrons in metallo-[beta]-lactamase-producing Pseudomonas aeruginosa and Pseudomonas putida isolates disseminated in a Korean hospital//Antimicrob. Agents. Chemother. 2002. Vol. 46. P. 1053-1058.
- Lee K., Yum J.H., Yong D., et al. Novel acquired metallo-b-lactamase gene, blaSIM-1, in a class 1 integron from Acinetobacter baumannii clinical isolates from Korea. Antimicrob//Agents Chemother. 2005. Vol. 49. P. 4485-4491.
- Poirel L., Naas T., Nicholas D. et al. Characterization of VIM-2, a carbapenem-hydrolyzing metallobeta-lactamase and its plasmid-and integron-borne gene from a Pseudomonas aeruginosa clinical isolate in France//Antimicrob. Agents. Chemother. 2000. Vol. 44. P. 891-897.
- Poirel L., Magalhaes M., Lopes M., Nordmann P. Molecular analysis of metallo-beta-lactamase gene blaSPM-1-surrounding sequences from disseminated Pseudomonas aeruginosa isolates in Recife, Brazil//Antimicrob. Agents Chemother. 2004. Vol. 48. Р. 1406-1409.
- Queenan A.M., Bush K. Carbapenemases: the versatile b-lactamases//Clin. Microbiol. Rev. 2007. Vol. 20. P. 440-458.
- Riccio M.L., Franceschini N., Boschi L. et al. Characterization of the metallo-beta-lactamase determinant of Acinetobacter baumannii AC-54/97 reveals the existence of blaIMP allelic variants carried by gene cassettes of different phylogeny//Antimicrob. Agents Chemother. 2000. Vol. 44. P. 1229-1235.
- Shibata N., Doi Y., Yamane K. et al. PCR typing of genetic determinants for metallo-beta-lactamases and integrases carried by gram-negative bacteriaisolated in Japan, with focus on the class 3 integron//J. Clin. Microbiol. 2003. Vol. 41. P. 5407-5413.
- Stone G.G., Oberst R.D., Hays S. [et al.] Detection of Salmonella serovars from clinical samples by enrichment broth cultivation-PCR procedure//J. Clin. Microbiol. 1994. Vol. 32. P. 1742-1749.
- Thompson J.D., Higgins D.G., Gibson T.J. CLUSTAL W: improving the sensitivity of progressive multiple sequence alignment son//Nucl. Acids. Res. 1994. Vol. 22. P. 4673-4680.
- Toleman M.A., Rolston K., Jones R., Walsh T.R. bla-VIM-7, an evolutionarily distinct metallo-betalactamase gene in a Pseudomonas aeruginosa isolate from the United States//Antimicrob. Agents Chemother. 2004. Vol. 48, N 1. P. 329-332.
- Tsakris A., Pournaras S., Woodford N. et al. Outbreak of infections caused by Pseudomonas aeruginosa producing VIM-1 carbapenemase in Greece//J. Clin. Microbiol. 2000. Vol. 38. P. 1290-1292.
- Van de Peer Y., DeWachter R. TREECON for Windows a software package for the construction and drawing of evolutionary trees for the Microsoft Windows environment//Comput. Appl. Biosci. 1994. Vol. 10. P. 569-570.


