Поиск корректоров метаболических нарушений при сахарном диабете 2-го типа среди 5-замещенных бензимидазолов, содержащих во втором положении циклическую алкиламиногруппу
Автор: Чепляева Н.И., Кузнецова В.А., Спасов А.А., Косолапов В.А., Жуковская О.Н., Анисимова В.А., Соловьева О.А., Сороцкий Д.В., Таран А.С., Воробьев Е.С., Леглер М.В.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Рубрика: Фармакология токсикология
Статья в выпуске: 3 (43), 2014 года.
Бесплатный доступ
В представленной работе было изучено влияние 5-замещенных бензимидазолов, содержащих во втором положении циклическую алкиламиногруппу на активность дипептидилпептидазы 4-го типа, гликогенфосфорилазы и антигликирующее и антиоксидантное действие в тест-системах in vitro. В результате выявлено три соединения, которые эффективно ингибировали дипептидилпептидазу 4-го типа, но уступали препарату сравнения ситаглиптину. Помимо этого два соединения продемонстрировали антиоксидантное действие сопоставимое с дибунолом.
Дипептидилпептидаза 4-го типа, гликогенфосфорилаза, антигликируюшая активность, антиоксидантная активность, сахарный диабет, производные бензимидазола
Короткий адрес: https://sciup.org/142149112
IDR: 142149112 | УДК: 547.785.51+615.015.1
Search of correctors metabolic abnormalities in diabetes mellitus type 2 among 5-substituted benzimidazoles, containing cyclic alkylamino group in second position
We studied the effect of 5-substituted benzimidazoles containing a cyclic alkylamino group in the second position on the activity of dipeptidyl peptidase type 4, glycogen phosphorylase and antiglycation, antioxidant effects in test systems in vitro. As a result, three compounds were found to effectively inhibit dipeptidyl peptidase type 4, but did not measure up to the drug of reference, sitagliptin. In addition, the two compounds showed an antioxidant effect comparable with dibunol.
Текст научной статьи Поиск корректоров метаболических нарушений при сахарном диабете 2-го типа среди 5-замещенных бензимидазолов, содержащих во втором положении циклическую алкиламиногруппу
Производные бензимидазола представляют крайне перспективный класс соединений для поиска и создания лекарственных препаратов вследствие наличия широкого спектра фармакологической активности. У данной группы соединений продемонстрированы антигистаминная, антиоксидантная, противосудорожная, анальгетическая, антиаритмическая, антисеротониновая, антиагрегантная, антитромботическая, гемореологическая, местноанестезирующая [1–3] антибактериальная, противопаразитарная, противогрибковая, противотуберкулезная, противоопухолевая [7] активности.
Так, O. E. Owen с соав. (1985) продемонстрировали, что противогельминтный препарат – Мебендазол, производное 5-бензоилбензимида-зол-2-карбомата оказывает гипогликемическое действие за счет повышения секреции инсулина β-клетками, что послужило началом поиска препаратов для терапии сахарного диабета (СД) и его осложнений среди производных бензимидазола [10]. В связи с этим были проведены исследования по выявлению антидиабетических свойств среди производных бензимидазола [2, 5, 6].
* Исследование выполнено за счет гранта Российского научного фонда (проект №14-25-00139).
* Работа частично финансировалась в рамках проектной части государственного задания в сфере научной деятельности, проект № 4.196.2014/ К и выполнена с использованием оборудования ЦКП «Молекулярная спектроскопия» Южного федерального университета.
Современный уровень научных исследований этиологии и патогенеза СД позволяет находить новые мишени для антидиабетических соединений и создавать новые классы препаратов для пероральной сахароснижающей терапии. Следует отметить разнонаправленность поиска лекарственных препаратов: так, восстановление инсулиносекреторной функции β-клеток поджелудочной железы, посредством ингибирования дипептидилпептидазы 4-го типа (ДПП-4) является одним из перспективных подходов в терапии СД 2-го типа [9, 12]. M. B. Wallace с соав. синтезировали серию не ковалентных ингибиторов ДПП-4 на основе N-метилбензимидазола, среди которых найдено соединение с высоким уровнем ингибирующей активности (IC50 = 8 нМ) [14].
Применение ингибиторов гликогенфосфо-рилазы (ГФ) было предложено в качестве одной из терапевтических стратегий терапии СД 2-го типа. Ингибирование данного фермента будет препятствовать гликогенолизу, обеспечивая снижение производства глюкозы в печени и снижение уровня глюкозы крови, обеспечивая тем самым потенциально новый метод лечения СД 2-го типа [13].
Помимо этого необходимо отметить важность поиска и доклинического исследования ингибиторов не ферментативного гликозилирования белков (ингибиторов реакции Мейларда) и препаратов с антиоксидантной активностью, как средств ранней патогенетической коррекции осложнений СД. На сегодняшний день нет соединений, специфически угнетающих образование конечных продуктов гликирования, применяемых в клинической практике [11]. Интерес к данной проблеме и поиску лекарственных средств, способных тормозить реакцию Мейларда, снижать образование конечных продуктов гликирования и предотвращать развитие осложнений СД, неуклонно растет. Таким образом, мишень-ориентированный поиск новых антидиабетических средств является актуальным направлением в современной диабетологии.
МЕТОДИКА ИССЛЕДОВАНИЯ
В работе были использованы 5-замещен-ные бензимидазолы I–V, содержащие во втором положении циклическую алкиламиногруппу. Данные соединения были синтезированны сотрудниками НИИ ФОХ ЮФУ.
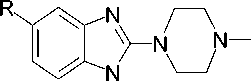
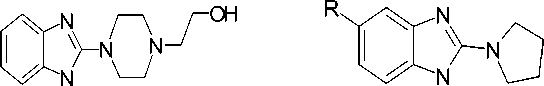
III
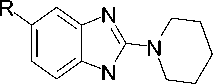
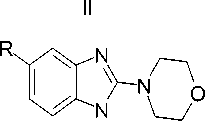
IV V
I R=H (a), Me (б), МеО (в); III R=H (a), Me (б), Cl (г); IV R= Me (б), Сl (г); V R = H (a), Me (б), MeO (в).
Для оценки способности соединений ингибировать дипептидилпептидазу 4-го типа (ДПП-4) по Yogisha S. (2010) с модификацией смешивали 10 мкл раствора исследуемого соединения в концентрации 0,1 мМ с 50 мкл 0,1 М Трис-HCl буфера (pH 8,4) и 40 мкл плазмы человека. Анализируемую смесь преинкубировали при 37 °С в течение 5 мин. После преинкубации добавляли 100 мкл 1 мМ субстрата реакции – Гли-Про-p-нитроанилида (Sigma, США) и полученную смесь инкубировали при 37 ° С в течение 15 мин. Развитие желтого окрашивания из-за высвобождения 4-нитроанилина определяли при 405 нм, используя прибор для считывания планшетов (ELx800, Bio Tec, США) [15]. В качестве препарата сравнения был выбран ситаглиптин (Sigma, США).
Для оценки ГФ ингибиторной активности in vitro 100 мкл 50 мМ HEPES буфера с pH 7,2 содержащего 100 мМ хлорид калия, 2,5 мМ хлорид магния, 0,5 мМ глюкозо-1-фосфата (Sigma, США), 1 мг/мл гликогена, преинкубировали с мышечной гликогенфосфорилазой α кролика (Sigma, США) и исследуемыми соединениями при 30 °С 30 минут. После преинкубации количество высвобожденного неорганического фосфата измеряли через 20 минут после добавления 150 мкл 1 М раствора HCl, содержащего 10 мг/мл молибдата аммония и 0,38 мг/мл малахитового зеленого. Развитие окрашивания определяли при 620 нм, используя прибор для считывания планшетов (ELx800, Bio Tec, США) [16]. В качестве вещества сравнения был выбран CP316819 (Sigma, США). Для определения ингибирующей концентрации (IC50) разведения соединении и CP316819 в 14 % ДМСО в концентрации от 10 мМ добавляли в реакционную смесь, при этом в контрольную смесь без ингибитора вносили ДМСО в аналогичной концентрации.
Реакцию гликирования белков моделировали в реакционной смеси, содержащей глюкозу (500 мМ), бычий сывороточный альбумин (БСА) (1 мг/мл), растворенные в фосфатном буферном растворе (рН 7,4) [8]. В экспериментальные образцы добавляли растворы изучаемых веществ в конечной концентрации 1 мМ, в контрольные образцы – фосфатный буферный раствор в эквивалентном объеме (50 мкл). В качестве препарата сравнения использовали Аминогуанидин. Образцы инкубировали при температуре 60 ° С в течение суток. По истечении срока инкубации на спектрофлуориметре MPF-400 (Hitachi, Япония) при длине волны возбуждения 370 нм и испускания 440 нм проводили определение специфической флуоресценции гликированного БСА. Антигликирующую активность рассчитывали по отношению к показателю флуоресценции контрольных образцов.
Антиоксидантное действие соединений определяли in vitro на модели аскорбат-зависимого перекисного окисления липидов (ПОЛ) печени крыс [4]. О скорости окисления судили по накоплению малонового диальдегида, определяемого с помощью тиобарбитуровой кислоты. Вещества изучали в концентрации 1 мкМ. Для оценки эффективности соединений рассчитывали процент ингибирования реакции. Действие веществ сравнивали с активностью дибу-нола (Merck, Германия).
Статистическую обработку данных проводили с использованием U-критерий Манна–Уитни с использованием пакета программ Graphit 4.0.15 (Erithacus Software, Ltd, UK).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯИ ИХ ОБСУЖДЕНИЕ
В работе представлены результаты ми-шень-ориентированного поиска новых соединений с антидиабетическим действием в группе 5-замещенных бензимидазолов I–V, содержащих во втором положении циклическую алкиламиногруппу. Среди изученных производных бензимидазола у соединений Ia, II, Va ДПП-4 ингибирующая активность была ниже, чем у препарата сравнения ситаглиптина в 1,3 раза (см. табл.).
ДПП-4 ингибирующая, ГФ ингибирующая, антигликирующая и антиоксидантная активность соединений I–V
|
Шифр |
ДПП-4 ингибирующая активность (0,1 мМ), Δ % ингибирования |
ГФ ингибирующая активность(0,1 мМ), Δ % ингибирования |
Антигликирующая активность (1 мМ), Δ % ингибирования флуоресценции БСА |
Антиоксидантная активность (модель аскорбат-зависимого ПОЛ, 1 мкМ), Δ % ингибирования |
|
I a |
67,1 ± 18,5 |
– |
26,9 ± 2,8*◊ |
|
|
I б |
36,1 ± 4,2* |
|||
|
I в |
41,7 ± 20,6 |
18,3 ± 7,8 |
– |
– |
|
II |
65,8 ± 8,8 |
11,68 ± 5,98◊ |
24,5 ± 5,3* |
|
|
III a |
34,8 ± 5,0 |
0,43 ± 0,43◊ |
32,1 ± 3,1* |
|
|
III г |
42,1 ± 2,7 |
14,6 ± 5,5 |
14,53 ± 5,60*◊ |
– |
|
III б |
58,3 ± 11,3 |
19,0 ± 3,7 |
– |
– |
|
IV г |
54,6 ± 18,5 |
20,9 ± 4,7 |
14,81 ± 5,90◊ |
– |
|
IV б |
59,0 ± 4,4 |
16,4 ± 7,3 |
– |
28,2 ± 3,6* |
|
V а |
65,4 ± 5,3 |
– |
24,5 ± 3,2*◊ |
|
|
V б |
52,4 ± 17,4 |
28,3 ± 4,3 |
– |
– |
|
V в |
38,2 ± 19,0 |
23,8 ± 3,1 |
– |
– |
|
Аминогуанидин |
70,68 ± 5,71* |
|||
|
Дибунол |
38,2 ± 1,0* |
|||
|
Ситаглиптин |
88,0 ± 1,6 |
|||
|
CP316819 |
81,2 ± 4,0* |
П р и м еч а н и я:
* данные достоверны по отношению к контролю, U-критерий Манна–Уитни (p < 0,05);
◊ данные достоверны по отношению к показателям препарата сравнения, U-критерий Манна–Уитни (p < 0,05);
… – не исследовалось;
«–» – отсутствие эффекта;
БСА – бычий сывороточный альбумин; ГФ – гликогенфосфорилаза; ДПП-4 – дипептилпептидаза 4-го типа;
ПОЛ – перекисное окисление липидов.
Следует отметить, что данные вещества во втором положении бензимидазола имеют метилпиперазиновый, гидроксиэтилпиперазино-вый и морфолиновый радикалы.
Однако введение в пятое положение базовой структуры метильного радикала или хлора приводит к снижению эффективности ингибирования ДПП-4. Так, соединения IIIб, IVг, Vб, содержащие пирролидиновый, пиперидиновый и мофо-линовый заместитель во втором положении, уступали по активности препарату сравнения в 1,6 раза. Iв, IIIа, IIIг, Vв продемонстрировали низкий уровень активности.
Ингибирование гликогенолиза является одним из перспективных фармакологических подходов в терапии СД 2-го типа. Ингибиторы ГФ снижают распад гликогена и повышенную продукцию глюкозы печенью и воздействуют на один из основных патогенетических факторов, что позволяет корректировать гипергликемию и не приводит к гипогликемии. В данном исследовании все соединения по уровню активности значительно уступали соединению CP 316819, которое является высокоактивным ингибитором индол-карбоксиамидного сайта ГФ.
Помимо этого необходимо отметить важность поиска и доклинического исследования ингибиторов неферментативного гликирования белков (ингибиторов реакции Мейларда) и препаратов с антиоксидантной активностью как средств ранней патогенетической коррекции осложнений СД.
В результате изучения антигликирующей активности установлено, что вещества II, IIIг и IVг снижают специфическую флуоресценцию гликированного БСА на 11,7; 14,5 и 14,8 % соответственно, уступая препарату сравнения Аминогуанидину. Остальные соединения не оказывают влияния на образование КПГ.
При исследовании антиоксидантной активности были выявлены соединения Iв и IIIа, которые по своей способности тормозить процессы ПОЛ в тест-системе in vitro сопоставимы с препаратом сравнения Дибунолом.
ЗАКЛЮЧЕНИЕ
Таким образом, у производных бензимидазола I–V выявлено ДПП-4 ингибирующее и антиоксидантное действия, а представленные базовые структуры могут быть использованы для оптимизации и создания высокоактивных соединений.
Список литературы Поиск корректоров метаболических нарушений при сахарном диабете 2-го типа среди 5-замещенных бензимидазолов, содержащих во втором положении циклическую алкиламиногруппу
- Анисимова В. А., Спасов А. А., Косолапов В. А.//Химико-фармацевтический журнал. -2012. -Т. 46, № 9. -С. 6-10.
- Анисимова В. А., Спасов А. А., Толпыгин И. Е.//Химико-фармацевтический журнал. -2010. -Т. 44, № 7. -С. 7-13.
- Киселев А. В., Галенко-Ярошевский П. А., Сахнов С. Н. и др.//Вестник ВолгГМУ. -2013. -Т. 48, № 4. -С. 108-113.
- Ланкин В. З., Гуревич С. М., Бурлакова Е. Б. Биоантиокислители. -М.: Наука, 1975. -Т. 52. -С. 73-78.
- Спасов А. А., Петров В. И., Чепляева Н. И. и др.//Вестник РАМН. -2013. -№ 4. -С. 43-49.
- Anisimova V. A., Spasov A. A., Kosolapov V. A., et al.//Pharmaceutical chemistry journal. -2013. -Vol. 46, № 11. -P. 647-652.
- Fei F., Zhou Z. M.//Expert Opinion on Therapeutic Patents. -2013. -Vol. 23, № 9. -P. 1157-1179.
- Jedsadayanmata A.//Naresuan University Journal. -2005. -Vol. 13, № 2. -P. 35-41.
- Majumdar S. K., Inzucchi S. E.//Endocrine. -2013. -Vol. 44. -P. 47-58.
- Owen O. E., Smitha R. H., Caprio S., et al.//Metabolism. -1985. -Vol. 34, № 6. -P. 567-570.
- Stirban A., Gawlowski T., Roden M.//Mol. Metab. -2014. -Vol. 3, № 2. -P. 94-108.
- Vella A.//J. Clin. Endocrinol. Metab. -2012. -Vol. 97, № 8. -P. 2626-2628.
- Verspohl E. J.//Pharmacol. Rev. -2012. -Vol. 64, № 2. -P. 188-237.
- Wallace B. M., Feng J., Zhang Z.//Bioorganic & Medicinal Chemistry Letters. -2008. -Vol. 18. -P. 2362-2367.
- Yogisha S., Raveesha K. A.//Journal of Natural Products. -2010. -№ 3. -P. 76-79.
- Yu L. J., Chen Y., Treadway J. L.//J. Pharmacol. Exp. Ther. -2006. -Vol. 317, № 3. -P. 1230-1237.


