Поиск природных пептидаз в микробном мате горячего источника Гарга и их разнообразие
Автор: Лаврентьева Е.В., Раднаев В.С.
Журнал: Вестник Бурятского государственного университета. Химия. Физика @vestnik-bsu-chemistry-physics
Статья в выпуске: 1, 2020 года.
Бесплатный доступ
Цель исследования - определить природные пептидазы в микробном мате горячего источника Гарга и их разнообразие. Статья посвящена комплексному исследованию пептидаз, которые представляют отдельную группу гидролитических ферментов участвующие в разложение органического вещества. Научная новизна работы заключается в анализе препаратов микробных сообществ горячих источников Байкальской рифтовой зоны методом высокопроизводительного секвенирования, которые обеспечивают гидролиз биополимеров на первых этапах деструкции органического вещества. В результате был проведен метагеномный анализ, который позволил выявить распространение пептидаз класса металлопептидаз в изученных микробных сообществах. В метагеномных последовательностях были идентифицированы потенциальные пептидазы, которые могут представлять биотехнологический интерес.
Пептидазы, микробный мат, гидролитические ферменты, металло- пептидазы, метагеномомы, секвенирование, байкальская рифтовая зона
Короткий адрес: https://sciup.org/148316720
IDR: 148316720 | УДК: 579.262(282.256.3) | DOI: 10.18101/2306-2363-2020-1-45-53
Search for natural peptidases in the microbial mat of hot spring Garga and their variety
The aim of the study is to determine the natural peptidases in the microbial mat of the Garga hot spring and their diversity. The article is devoted to a comprehensive study of peptidases, which are a separate group of hydrolytic enzymes involved in the decomposition of organic matter. The scientific novelty of the work lies in the analysis of preparations of microbial communities of hot springs of the Baikal rift zone by high-performance sequencing, whichprovide hydrolysis of biopolymers at the first stages of destruction of organic matter. As a result, a metagenomic analysis was performed, which revealed the spread of metal- peptidases in the studied microbial communities. Potential peptidases that may be of biotechnological interest have been identified in metagenomic sequences.
Текст научной статьи Поиск природных пептидаз в микробном мате горячего источника Гарга и их разнообразие
Гидролитические бактерии являются инициаторами процесса разложения органического вещества в микробных сообществах природных местообитаний. За последнее десятилетие появляется все больше информации о наличии полного комплекса гидролитических ферментов у представителей прокариот [1–3]. Интенсивность их деятельности очень сильно зависит от многих экологических факторов, в том числе температуры, окислительно-восстановительных условий, реакции среды. В составе органического вещества одним из основных компонентов является белок. Процесс протеолиза имеет важное биологическое значение, так как играет регулирующую роль в функционировании как клетки, так и экосистемы в целом.
Пептидазы (EC. 3.4) представляют собой отдельную подгруппу гидролитических ферментов, которые катализируют расщепление пептидных связей в белковых субстратах. В зависимости от способа действия и каталитического механиз- ма пептидазы делятся на шесть основных классов, включая сериновые пептидазы (EC. 3.4.21), цистеиновые пептидазы (EC. 3.4.22), аспарагиновые пептидазы (EC. 3.4.23), металлопептидазы (EC. 3.4.24), треониновые эндопептидазы (3.4.25) и глутаминовые (3.4.23.32) . В дополнение к их ключевой метаболической и физиологической значимости, они имеют различное коммерческое применение во всем мире.
Процесс деструкции белка пептидазами в природных экосистемах слабоизу-чен, известно лишь несколько работ, посвященных изучению гидролиза белка в морских экосистемах [2, 4] и в почве [5] .
Объекты и методы исследования
Высокотемпературный источник Гарга находится в долине р. Гарги, расположен в отрогах Икатского хребта, окаймляющего котловину с восточной стороны (54о19'203'' N и 110о59'646'' E. Участок выхода сложен водноледниковыми верхнечетвертичными отложениями, которые перекрывают палеозойские граниты, и связаны с мощным Гаргинским разломом, протягивающимся в северо-восточном направлении на 30-40 км. Температура воды на изливе достигает 74°С, рН 8,3.
Поиск пептидаз в микробном мате горячего источника Гарга проведен в ООО «Биоспарк», г. Москва.
Результаты и обсуждение
Физико-химические условия горячего источника Гарга
Термальная сульфатно-натриевая вода изливается со скоростью 5 л/с в небольшой грот, расположенный на правом берегу реки Гарга, на высоте около 100 м от уреза воды (674 м над уровнем моря). Температура воды на выходе достигает 74°С. Вода, стекая по ручью, образует травертин высотой 1,5-2 м, длиной до 50 м, шириной до 25 м и является одним из самых крупных в Байкальском регионе.
Химический состав воды (табл. 1). Доминирующий катион — Na+, его содержание составило 312,04 мг/дм3. Концентрации ионов Mg2+, К+ и Са2+ составили 0,08, 11,3 и 23 мг/дм3, соответственно. Содержание карбонатов составило 6 мг/дм3, гидрокарбонатов — 109 мг/дм3. Концентрация сульфатов 390 мг/дм3. Содержание хлоридов и фторидов 51 мг/дм3 и 11 мг/дм3, соответственно. Для источника Гарга характерно высокое содержание радона, до 43 эман.
Таблица 1
|
Na+ |
K+ |
Ca2+ |
Mg2+ |
СО 3 2- |
НСО 3 - |
NO 3 - |
NO2- |
SO 4 2- |
Н 2 SiO 3 |
F |
PO 4 3- |
Cl- |
|
312,04 |
11,3 |
23 |
0,08 |
6 |
109,83 |
7,4 |
0,004 |
390 |
89 |
10,5 |
2,02 |
51,41 |
Химический состав воды горячего источника Гарга, мг/дм3 (в месте отбора микробного мата)
Микроэлементный состав воды показал, что в Гаргинских водах отмечены повышенные концентрации B, Rb, Li, Ba, Sr. Повышенные содержания данных элементов в целом характерны для термальных источников, разгружающихся в 46
пределах Икатского хребта. Высокие содержания Sr и некоторых других элементов в горячем источнике связаны с их высоким содержанием в гранитоидных породах Баргузинского комплекса.
Для поиска природных пептидаз был отобран микробный мат при температуре воды 54,2°С, рН воды составила 8,3 и минерализация 0,74 г/ дм3.
Метагеномный анализ
На первой стадии выполнения работ по метагеномному анализа были получены данные по поглощению света препаратом ДНК (рис. 1, табл. 2)
Таблица 2
Качество и количество ДНК в полученных препаратах (Гарга)
|
A260 A230 A260 A280 Raw A260 A260 A260 Concent- A340 Turbidi (10 (10 (10 /A23 /A28 mm) mm) mm) 0 0 (ng/ul) mm) mm) |
Общее кол-во ДНК, мкг |
|
215,94 3,24 4,32 2,22 0,9 1,33 1,94 2,23 |
21,6 |
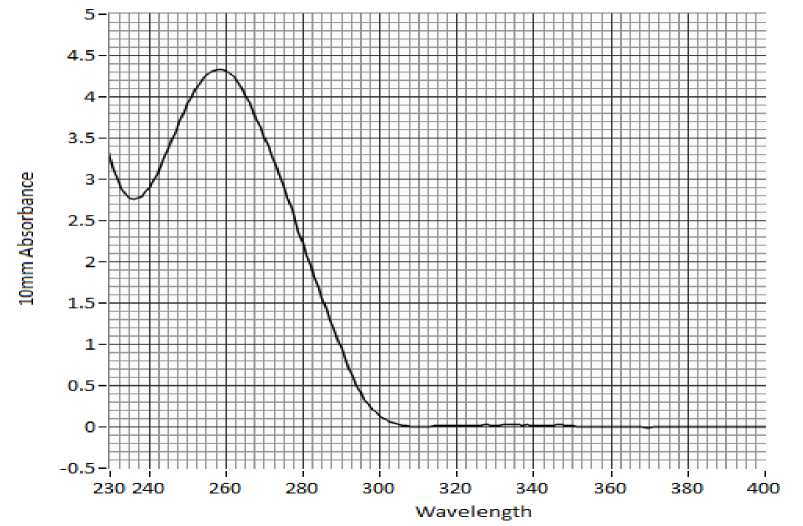
Рис. 1. Кривая поглощения света препаратами ДНК
Секвенирование полученных библиотек на платформе Illumina HiSeq
Качественные и количественные характеристики полученных данных секвенирования (табл. 3) Усредненные показатели качества прочтения (Q) каждого нуклеотида (рис. 2).
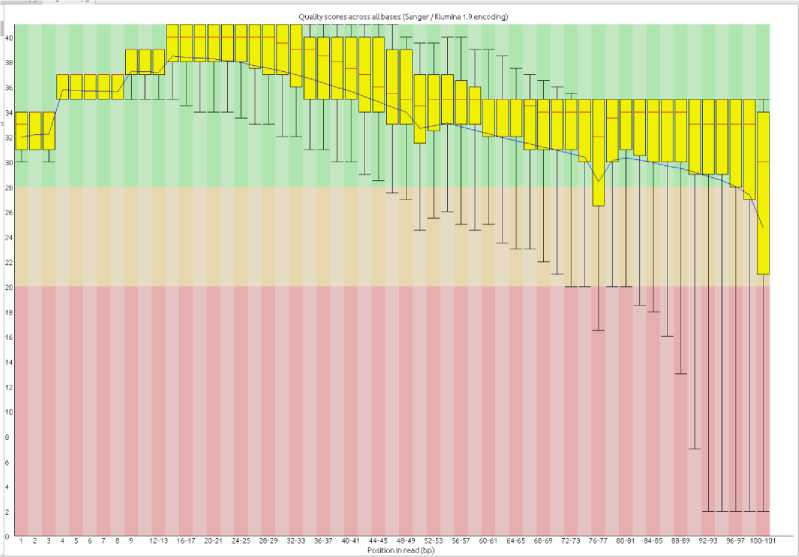
Рис. 2. Усредненные показатели качества прочтения (Q — ось ординат) каждого нуклеотида (позиции обозначены по оси абсцисс)
Качественные и количественные характеристики полученных данных секвенирования
Таблица 3
|
Образец |
Количество прочтений |
Длина прочтений |
Усредненный GC cостав прочтений |
|
Гарга |
94242298 |
101 |
59% |
На основании полученной аннотации в изученном образце был получен перечень всех выявленных типов протеаз (табл. 4)
Ферменты, идентифицированные в метагеномных последовательностях, которые могут представлять интерес для биотехнологии
Таблица 4
Перечень всех выявленных типов протеаз для каждого образца (Гарга)
|
Тип протеазы |
Код фермента по EC |
Номенклатура |
|
ATP-dependent Clp protease |
3.4.21.92 |
Сериновая пептидаза Гидролиз белка на мелкие пептиды в присутствии АТФ и Mg2+ |
|
ATP-dependent zinc metalloprotease |
3.4.24.- |
Металлоэндопептидаза |
|
CAAX amino terminal protease self- immunity |
||
|
Carboxy-terminal processing protease |
3.4.21.102 |
Сериновая пептидаза |
|
Caudovirus prohead protease |
||
|
Cysteine protease StiP |
3.4.22.- |
Цистеиновая эндопептидаза |
|
DNA-binding ATP-dependent protease La |
||
|
Extracellular basic protease |
3.4.21.- |
Сериновая эндопептидаза |
|
Extracellular metalloprotease |
3.4.21.- |
Сериновая эндопептидаза |
|
Extracellular serine protease |
3.4.21.- |
Сериновая эндопептидаза |
|
Germination protease precursor |
3.4.24.78 |
Металлоэндопептидазы Принадлежит семейству пептидаз M63 |
|
Hydrogenase maturation protease |
||
|
Intracellular serine protease |
3.4.21.- |
Сериновая эндопептидаза |
|
intramembrane serine protease GlpG |
||
|
Lon protease |
3.4.21.53 |
Сериновая эндопептидаза La Принадлежит семейству S 16 |
|
Metalloprotease LoiP |
3.4.24.- |
Металлоэндопептидаза |
|
Metalloprotease MmpA |
3.4.24.- |
Металлоэндопептидаза |
|
Minor extracellular protease Epr |
3.4.21.- |
Сериновая эндопептидаза |
|
Minor extracellular protease vpr |
3.4.21.- |
Сериновая эндопептидаза |
|
Multifunctional acyl-CoA thioesterase I and protease I and lysophospholipase L1 |
||
|
Neutral metalloprotease |
3.4.24.- |
Металлоэндопептидааз |
|
Neutral protease B |
3.4.24.- |
Металлоэндопептидаза |
|
Papain family cysteine protease |
||
|
Periplasmic pH-dependent serine endoprotease DegQ |
3.4.21.107 |
Сериновая эндопептидаза Принадлежит семейству S1B |
|
Periplasmic serine endoprotease DegP |
3.4.21.107 |
Сериновая эндопептидаза Принадлежит семейству S1B |
|
Prohead core protein protease |
|
Protease 1 |
3.4.21.50 |
Сериновая эндопептидаза Lysyl endopeptidase |
|
Protease 2 |
3.4.21.83 |
Сериновая эндопептидаза Oligopeptidase B |
|
Protease 3 |
3.4.24.55 |
Металлоэндопептидаза Pitrilysin |
|
Protease 4 |
3.4.21.- |
Сериновая эндопептидаза |
|
Protease HtpX |
3.4.24.- |
Металлоэндопептидаза |
|
Protease LasA |
3.4.24.- |
Металлоэндопептидаза |
|
Protease PrsW |
||
|
Protease TldD |
||
|
Putative CtpA-like serine protease |
3.4.21.- |
Сериновая эндопептидаза |
|
Putative cysteine protease YraA |
||
|
Putative metalloprotease YpwA |
3.4.24.- |
Металлоэндопептидаза |
|
Putative peptide zinc metalloprotease protein YydH |
||
|
Putative protease YdeA |
||
|
Putative protease YhbU |
||
|
Putative serine protease HhoA |
||
|
Putative serine protease HtrA |
||
|
Putative subtilase-type serine protease precursor |
3.4.21.- |
Сериновая эндопептидаза |
|
Putative zinc metalloprotease Rip3 |
||
|
Putative zinc protease AlbF |
3.4.24.- |
Металлоэндопептидаза |
|
Retroviral aspartyl protease |
||
|
Rhomboid protease AarA |
3.4.21.105 |
Сериновая эндопептидаза Rhomboid protease |
|
Rhomboid protease GlpG |
3.4.21.105 |
Сериновая эндопептидаза Rhomboid protease |
|
Rhomboid protease GluP |
3.4.21.105 |
Сериновая эндопептидаза Rhomboid protease |
|
Serine endoprotease DegS |
3.4.21.107 |
Сериновая эндопептидаза Принадлежит семейству S1B |
|
Serine protease AprX |
3.4.21.- |
Сериновая эндопептидаза |
|
Serine protease Do-like HtrA |
3.4.21.107 |
Сериновая эндопептидаза Принадлежит семейству S1B |
|
Serine protease Do-like HtrB |
3.4.21.107 |
Сериновая эндопептидаза Принадлежит семейству S1B |
|
Serine protease HtrA-like protein |
3.4.21.- |
Сериновая эндопептидаза |
|
Serine protease SplB |
3.4.21.- |
Сериновая эндопептидаза |
|
Sporulation-specific protease YabG |
||
|
Tail-specific protease |
3.4.21.102 |
Сериновая эндопептидаза Re |
|
Thermophilic metalloprotease (M29) |
||
|
Thermostable alkaline protease |
3.4.21.- |
Сериновая эндопептидаза |
|
Transglutaminase-activating metalloprotease |
||
|
Zinc metalloprotease Rip1 |
3.4.24.- |
Металлоэндопептидаза |
В природных местообитаниях гидролитические бактерии занимают нишу первичных деструкторов, благодаря способности гетеротрофно расти на биополимерах различной природы. Особенностью изученных микробных сообществ термальных источников Прибайкалья является его термофилия и алкалитолернат-ность, что предполагает термо- и рН стабильность соответствующих ферментов.
Проведенный метагеномный анализ позволил выявить гены пептидаз в природном образце микробного мата горячего источника Гарга. Анализ собранных метагеномных последовательностей позволил систематизировать и дать характеристику выявленных генов. Сравнение метагеномных последовательностей репрезентативных данных показало доминирование ферментов класса сериновых пептидаз. Ферменты, относящиеся к этому классу, ингибируются диизопропил-фторфосфатом и фенилметилсульфонилфторидом, а также субстратоподобными галоидметилкетонами, такими как тозиллизинхлорметилкетон (TLCK) или тозилфенилаланинхлорметилкетон (TPCK). Из литературных данных известно, что сериновые пептидазы обычно активны при нейтральных и щелочных значениях рН и имеют оптимум рН между 7 и 11 [6]. На основании аминокислотной последовательности, пептидазы делят на семейства и в настоящее время выделено более 20 семейств. В нашем исследовании было выявлено 7 представителей сериновых пептидаз (табл. 4). Принято считать, что эволюционное родство ферментов выражается в гомологии первичной и сходстве пространственной структур. Поэтому этим признакам придается большое значение. Известны случаи, когда сходство структуры каталитического центра не сопровождается гомологией пространственной и первичной структур. Вероятно, такое сходство является следствием конвергентной эволюции.
Метагеномный анализ позволил выявить распространение пептидаз класса металлопептидаз в изученных микробных сообществах. В классе металлопепти-дазы выделяют 25 семейств, обнаруженных в разных систематических группах. Металлопептидазы, как правило, синтезируются в неактивной форме и активируются в присутствии ионов металлов (магния, марганца, кобальта, цинка). Активность металлопротеиназ подавляется веществами, связывающими металлы — ЭДТА, 1,10-фенантролином, версеном, цитратом, фосфамидом и др. Оптимальные значения рН для металлопротеиназ также лежат в диапазоне 7–9. Также известны металлопротеиназы, обладающие свойствами термостабильности [3].
Обнаружены единичные последовательности генов класса цистеиновых пептидаз в микробном сообществе Гарга. Возможно, это связано с тем, что цистеиновые пептидазы эффективны при нейтральных значениях рН; реже зона оптимума лежит в слабокислой или слабощелочной среде (pH 4–9) в зависимости от природы гидролизуемого белка [3]. У изученного нами микробного сообщества диапазон развития находится в высокотемпературной зоне и щелочной области рН. В состав активного центра цистеиновых пептидаз входит цистеин и гистидин [7]. Цистеиновые пептидазы активируются синильной кислотой и сульфгидрильными соединениями — восстановленным глутатионом, дитиотреи-толом, 2-меркаптоэтанолом и цистеином.
Таким образом, на основе анализа препаратов тотальной ДНК микробных сообществ горячих источников Байкальской рифтовой зоны методом высокопроизводительного секвенирования были получены данные о высоком разнообразии природных пептидаз в исследуемом микробном сообществе, которые обеспечи- 51
вают гидролиз биополимеров на первых этапах деструкции органического вещества.
В метагеномных последовательностях были идентифицированы потенциальные пептидазы, которые могут представлять биотехнологический интерес. Их использование в разных областях промышленности, медицины, биоремедиации обусловлено несколькими факторами: снижением риска контаминации, увеличением скорости процессов и повышением общей стабильности ферментов.
Работа поддержана бюджетной темой ИОЭБ СО РАН АААА-А17-117011810034-9
Список литературы Поиск природных пептидаз в микробном мате горячего источника Гарга и их разнообразие
- Замана Л. В., Хахинов В. В., Данилова Э. В., Бархутова Д. Д. Гидрохимия минеральных вод // Геохимическая деятельность микроорганизмов гидротерм Байкальской рифтовой зоны. Новосибирск: Академическое изд-во "Гео". 2011. С. 62-101.
- Obayashi Y., Ueoka N., Suzuki S. Degradation and utilization of protein derived from Pseudomonas aeruginosa by marine microbial community // J. Oceanogr. 2010. V. 6. P. 513- 521.
- Oliveira A. S., Filho J. X., Sales M. P. Cysteine proteinases cystatins // Braz Arch Biol Technol. 2003. V. 46, № 1. P. 91-104.
- Orsi W. D., Smith J. M., Liu S. and oth. Diverse, uncultivated bacteria and archaea underlying the cycling of dissolved protein in the ocean // ISME J. 2016. V. 10. P. 2158-2173.
- Vranova V., Rejsek K., Formanek P. Proteolytic activity in soil: A review // Applied Soil Ecology. 2013. V. 70. P. 23-32.
- Rao M. B., Tanksale A. M., Ghatge M. S., Deshpande V. V. Molecular and biotechnological aspects of microbial proteases // Microbiol. Mol. Biol. Rev. 1998. V. 62, № 3. P. 597-635.
- Rawlings N. D. and Barrett A. J. Evolutionary families of peptidases // Biochem. J. 1993. V. 290. P. 205-218.


