Показатели химической контаминации областей быстрого обмена как критерии определения критических систем организма
Автор: Атискова Н.Г., Шарифов А.Т., Шур П.З.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Экология
Статья в выпуске: 3, 2010 года.
Бесплатный доступ
Изучение здоровья как интегрированного показателя требует установления закономерностей процессов биорегуляции организма в условиях химической контаминации областей быстрого обмена. В ходе исследования разработаны принципы и критерии математического моделирования зависимости «уровень химической контаминации - изменение процессов биорегуляции», выявлены критические органы и системы, установлены критические уровни контаминации сред быстрого обмена, вызывающие изменения процессов биорегуляции.
Химическая контаминация, быстрый обмен, критические системы организма
Короткий адрес: https://sciup.org/147204517
IDR: 147204517 | УДК: 614
Текст научной статьи Показатели химической контаминации областей быстрого обмена как критерии определения критических систем организма
Для изучения здоровья как интегрированного показателя, отражающего состояние экологических и медико-биологических процессов, важным является установление закономерностей процессов биорегуляции организма в условиях химической контаминации областей быстрого обмена. Изучение данных закономерностей позволит перейти к идентификации критических органов систем и прогнозированию нарушений здоровья, что в перспективе позволит целенаправленно проводить профилактические мероприятия.
Гипотеза формирования системы биорегуляции организма человека в условиях химической контаминации областей быстрого обмена предполагает, что определенный уровень контаминации области быстрого обмена вызывает нарушение процессов биорегуляции. Определение индикаторов химической контаминации может служить критерием вероятного начала и степени изменений процессов биорегуляции, то есть изменение механизма биорегуляции может рассматриваться как функция от химической контаминации.
В качестве инструмента для проверки данной гипотезы используются эпидемиологические исследования, включающие определение содержания вредных веществ в крови, как области быстрого обмена, и регистрация вероятных ответов (изменение биохимических, иммунологических и других показателей).
Чаще других используются экологическое и когортное исследования. Целью экологического исследования является определение контингента риска и ответов со стороны здоровья населения. Данный вид эпидемиологического исследования не требует больших финансовых и временных затрат, позволяет рассматривать большое количество событий. Однако в рамках этого метода сложно контролировать влияние вмешивающихся факторов, возникают систематические ошибки в ходе отбора популяции для исследования.
Выбор когортного исследования целесообразен при построении моделей зависимости «экспозиция – ответ»; кроме того, метод дает возможность изучать широкий спектр следствий заболеваний. Недостатками данного типа исследования являются длительное время сбора данных, возможность изучения только нескольких экспозиций.
При планировании эпидемиологического исследования необходимо учитывать факторы, способные исказить связь между экспозицией и ответом со стороны здоровья, к ним могут быть отнесены возраст, пол, наследственность, индивидуальные особенности.
При выборе экспонируемой популяции необходимо учитывать длительность контакта с неблагоприятным фактором среды обитания, так как развитие патологических изменений со стороны здоровья может возникнуть только после достижения определенного уровня физической и функциональной кумуляции токсиканта в организме.
Регистрация вероятных ответов со стороны здоровья (изменение биохимических, иммунологических и других показателей) проводится отдельно для различных контингентов населения.
В ходе проведения данного эпидемиологического исследования необходимо решить ряд задач:
-
1. Обоснование принципов выявления критиче ских органов и систем с идентификацией соответст вующих им показателей биорегуляции.
-
2. Классификация показателей биорегуляции с учетом механизмов их формирования и выделение маркерных тестов для углубленных исследований.
-
3. Проведение математического моделирования связи изменения уровня химической контаминации областей быстрого обмена с изменением процессов биорегуляции.
-
4. Определение критического уровня контаминации сред быстрого обмена, вызывающего изменение процессов биорегуляции.
Выбор и классификация показателей биорегуляции основывается на данных многочисленных зарубежных и отечественных исследований (Dy-kewicz et. al., 1991; Baj et. al., 1994; Katsouyanni et. al., 1997; Быков и др., 1999; Goldbohm et. al., 2000). Известно, что морфологические и функциональные нарушения определенных органов сопровождаются изменениями специфических биохимических и иммунологических показателей (маркеры). Так, например, для кроветворной системы это может быть уровень содержания гемоглобина, количество форменных элементов крови, лейкоцитарная формула, для пищеварительной системы – активность α-амилазы и щелочной фосфатазы крови, уровень холестерина, общего билирубина, АЛАТ, АСАТ и др.
Следующим этапом является разработка математических моделей, отражающих зависимости «маркер экспозиции – ответ» и/или «маркер экспозиции – маркер ответа» с использованием многоступенчатого вычисления показателя отношения шансов, что позволяет получить параметры, на основе которых становится возможным определение направленности действия контаминации. В качестве зависимых переменных могут быть приняты вероятности нарушения здоровья в виде заболеваний и донозологических изменений клиниколабораторных показателей, а в качестве независимых переменных – уровни экспозиции в виде концентраций в биологических средах человека (маркеры экспозиции). На основе этого устанавливается критический уровень содержания контаминанта в крови, как области быстрого обмена, вызывающий патологические сдвиги процессов биорегуляции (табл.). Величина критического уровня определялась верхней границей 95% доверительного интервала.
Критический уровень контаминации сред быстрого обмена по маркерам биорегуляции
|
Токсикант |
Маркер в крови |
Критический уровень (мг/дм3) |
|
Марганец |
IgG (г/дм3) |
0,047 |
|
АЛАТ (Е/дм3) |
0,026 |
|
|
АСАТ (Е/дм3) |
0,143 |
|
|
Тромбоциты(×109/дм3) |
0,039 |
|
|
Фагоцитарное число (у. е.) |
0,025 |
|
|
Цветной показатель крови |
0,046 |
|
|
Моноциты (%) |
0,016 |
|
|
Палочкоядерные нейтрофилы (%) |
0,033 |
|
|
Метанол |
IgG (г/дм3) |
3,269 |
|
Ретикулоциты (%) |
3,429 |
|
|
Гемоглобин (г/дм3) |
1,049 |
|
|
Эозинофилы (%) |
2,286 |
|
|
Свинец |
АЛАТ (Е/дм3) |
0,165 |
|
Общий билирубин (мкмоль/дм3) |
0,104 |
|
|
T-3 (нг/мл) |
0,115 |
|
|
T-4 (мкг%) |
0,118 |
|
|
ТТГ (мкМЕ/мл) |
0,124 |
|
|
Палочкоядерные нейтрофилы (%) |
0,127 |
|
|
Ретикулоциты (%) |
0,091 |
|
|
Формальдегид |
Гемоглобин (г/дм3) |
0,05 |
|
Лимфоциты (%) |
0,0189 |
|
|
CEA (карциноэмбриональный антиген) (нг/мл) |
0,029 |
|
|
Сегиментоядерные нейтрофилы (%) |
0,022 |
|
|
АЛАТ (Е/дм3) |
0,009 |
|
|
Малоновый диальдегид плазмы (мкмоль/дм3) |
0,018 |
На начальных этапах проведения работы целесообразным является детальное изучение закономерностей воздействия химической контаминации областей быстрого обмена на различных уровнях нарушения процессов биорегуляции (адаптационные сдвиги, донозологические и нозологические патологические реакции).
Предварительно необходимо проводить мониторинговые наблюдения за содержанием вредных веществ в крови и других биологических средах одновременно с изучением содержания вредных веществ или их метаболитов в организме, используя клинико-лабораторные тесты, адекватные вероятному действию исследуемых химических ве- ществ, а также углубленный анализ заболеваемости исследуемой популяции по основным нозологическим формам (группам) заболеваний за период мониторинговых наблюдений.
Кроме того, в качестве исходной информации могут быть использованы результаты углубленных эпидемиологических исследований заболеваемости, результаты клинико-лабораторных исследований состояния здоровья, маркеры ответа.
Данный методический подход был реализован на примере когортного исследования в г. Губахе, одном из промышленно развитых городов Пермского края, в ходе которого изучалось воздействие марганца, свинца, метанола и формальдегида. Для исследования, как самая чувствительная группа населения, были выбраны 1028 детей в возрасте от 5 до 14 лет, страдающих респираторными аллергозами, которые являются индикатором неблагоприятного действия аэрогенных экологических факторов на здоровье. Содержание данных веществ в биологических средах (крови) детей существенно превышало фоновый уровень для Пермского края.
В результате исследований, проведенных в г. Губахе, разработано и экспертно оценено шесть моделей зависимости для формальдегида. В качестве примера представлена модель, где лимитирующим показателем вредности явилось повышение АЛАТ (безопасный уровень формальдегида – 0,008 мг/дм3) (рис. 1).
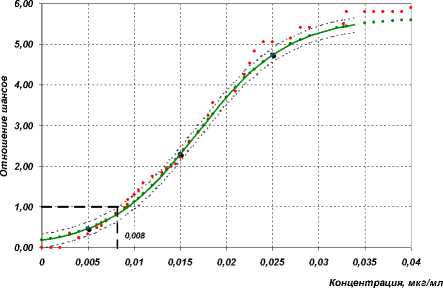
Рис. 1. Модель зависимости «концентрация формальдегида в крови – показатель риска повышения АЛАТ»
Сформировано четыре модели воздействия метанола на клинико-лабораторные показатели. Представлена модель зависимости с лимитирующим показателем вредности – снижение уровня IgG (безопасный уровень метанола – 0,653 мг/дм3) (рис. 2).
Кроме того, сформировано семь моделей зависимости изменения клинико-лабораторных показателей для свинца и восемь моделей зависимости между воздействием марганца и изменениями клинико-лабораторных показателей.
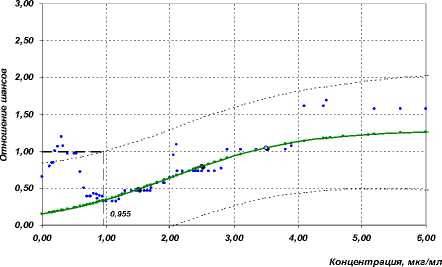
Рис. 2. Модель зависимости «концентрация метилового спирта в крови – показатель риска понижения IgG»
В результате проведенное исследование подтверждает выдвинутую гипотезу. Полученные данные дают возможность не только прогнозировать маркеры ответа, но и установить критический уровень содержания токсиканта, при котором возникает риск развития той или иной патологии, что позволит не только целенаправленно разрабатывать, но и оценивать эффективность профилактических мероприятий.
Список литературы Показатели химической контаминации областей быстрого обмена как критерии определения критических систем организма
- Быков А.А., Соленова Л.Г., Земляная Г.М., Фурман В.Д. Методические рекомендации по анализу и управлению риском воздействия на здоровье населения вредных факторов окружающей среды. М.: Анкил, 1999. 412 с.
- Baj Z., Majewska E., Zeman K. et al. The effect of chronic exposure to formalde hyde, phenol and organic chlorohydrocarbons on peripheral blood cells and the immune system in humans//J. Invest. Allergol. Clin. Immunol. 1994. Vol. 4. P. 186-191.
- Dykewicz M.S., Patterson R., Cugell D.W. et al. Serum IgE and IgG to formalde hyde-human serum albumin: Lack of relation to gaseous formaldehyde exposure and symptoms//J. Allergy Clin. Immunol. 1991. Vol. 87. P.48-57.
- Goldbohm R.A., Tielemans E.L.J.P., Heederik D. et al. Risk estimation for carcino gens based on epidemiological data: A structured approach, illustrated by an example on chromium//Regul. Toxicol. Pharmacol. 2006. Vol. 44. P. 294-310.
- Katsouyanni K., Touloumi G., Spix C. et al. Short term effects of ambient sulphur di oxide andparticulate matter on mortality in 12 European cities: Results from time series data from the APHEA project//B. M. J. 1997. Vol. 314. Р. 1658 -1663.


