Получение β-клеток поджелудочной железы новорожденных кроликов и межвидовых гибридных культур клеток - продуцентов инсулина
Автор: Шевцова Н.А.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Клеточные технологии
Статья в выпуске: 6 т.42, 2007 года.
Бесплатный доступ
Оценивали возможность гибридизации β-клеток поджелудочной железы новорожденных кроликов и мугантной культуры клеток почки овцы, дефектных по тимидинкиназе, с целью получения межвидовых гибридных культур клеток - продуцентов инсулина. Показано, что β-клетки поджелудочной железы новорожденных кроликов способны сливаться с эпите-лиоподобными клетками почки овцы. Полученная межвидовая гибридная культура имеет стабильную морфологию и кулътуральные свойства, продуцирует инсулин в культуральную среду, а также накапливает зерна инсулина в цитоплазме.
5-бром-2-дезоксиуридин (5-бду), гат - селективная среда, содержащая гипоксантин, аминоптерин, тимидин, крупный рогатый скот, мугантная культура клеток почки овцы (по тк-100), среда игла mem (минимальная среда игла), дмем (минимальная среда игла в модификации дюлъбеко), тк - тимидинкиназа
Короткий адрес: https://sciup.org/142133229
IDR: 142133229 | УДК: 57.085.23
Cultivation of pancreas β-cells of newborn rabbits and interspecific hybrid cell cultures - insulin producers
The author has estimated the possibility of hybridization of pancreas β-cells of newborn rabbits and mutant cell culture of sheep kidney defected on thymidine kinase for the purpose of creation of interspecific hybrid cells cultures - insulin producers. It was shown that newborn rabbit's pancreas β-cells can fuse with epitheliumlike cells of sheep kidney. Obtained interspecific hybrid culture has stabile morphology, cultural properties and secretes the insulin to cultural medium and also accumulates the insulin grains in cytoplasm.
Текст научной статьи Получение β-клеток поджелудочной железы новорожденных кроликов и межвидовых гибридных культур клеток - продуцентов инсулина
Число больных диабетом составляет 2-3 % населения планеты и, по прогнозам ученых, каждые 15 лет ожидается его 2-кратное увеличение.
Одно из разрабатываемых направлений эффективных методов лечения диабета — трансплантология, включающая аллогенную пересадку поджелудочной железы или ее фрагментов, пересадку островков поджелудочной железы, полученных от аллогенного или ксеногенного донора, конструирование и создание искусственной поджелудочной железы (1, 2).
Реальной альтернативой применения алло- или ксенотрансплантации культур или свежих островковых клеток, по нашему мнению, являются биотехнологические методы, позволяющие полностью компенсировать функцию естественных инсулинсекретирующих клеток, и в частности создание гибридных культур клеток, продуцирующих инсулин и обладающих гистосовместимостью с тканевыми антигенами различных видов животных и человека, что и послужило целью нашей работы.
Методика . В качестве партнеров по слиянию были взяты мутантная культура клеток почки овцы ПО ТК-100, хранившаяся в жидком азоте в криобанке Всероссийского НИИ экспериментальной ветеринарии им. Я.Р. Коваленко (получена А.С. Симоновой и др., 1998), и β -клетки поджелудочной железы 1-3-суточных кроликов. Гибридизацию β -клеток и клеток почки овцы, дефектных по тимидинкиназе, проводили согласно методическим рекомендациям по гибридизации соматических клеток сельскохозяйственных животных с использованием стандартных растворов (3); β -клетки поджелудочной железы кролика получали бесцентрифужным флотационным методом (4).
Применялись среды Игла МЕМ, Игла MEM с двойным набором аминокислот, ДМЕМ (минимальная среда Игла в модификации Дюльбеко), RPMI-1640, селективная среда ГAT, раствор версена (натриевая соль этилендиаминтетрауксусной кислоты), 0,25 % раствор трипсина на рабочем растворе Хенкса без Са2+ и Mg2+, сыворотка крови эмбрионов крупного рогатого скота (НПО «Биолот», Россия, «Sigma», США); в качестве необходимых добавок для роста мутантных клеток и гибридных культур — 0,05 % 2-меркаптоэтанол и 0,05 % пируват натрия; для предотвращения контаминации культур бактериями и грибами — этоний (из расчета 5-7 мкг/мл), энроксил и амфотерицин В (соответственно 0,05 и 0,01 %), пенициллин и стрептомицин (по 100 ЕД/мл), 5-бром-2-дезоксиуридин (5-БДУ) (500 мкг/20 мл). 5-БДУ использовали в концентрации от 4 до 150 мкг/мл для проверки на реверсию мутантных клеточных линий. Рабочие растворы стерилизовали фильтрацией (диаметр пор 0,22 мкм) («Millipore», США).
Культуры клеток поддерживали периодическим пассированием: пересев культуры осуществляли по мере формирования монослоя после обработки 0,02 % версеном и 0,25 % трипсином (в соотношении 7:1) бесцентрифужным методом с коэффициентом пересева 1:4-1:5 при титре посевного материала 105 кл/мл.
Для приготовления цитологических препаратов клетки выращивали на покровных стеклах в пенициллиновых флаконах (посевной титр — 1,5-2½105 кл/мл, объем суспензии — 1,5-2 мл), далее фиксировали в растворе Буэна или нейтральным формалином, обрабатывали метиловым спиртом и окрашивали гематоксилином с эозином или азур-эозином по Романовскому-Гимза. Препараты для кариологического анализа готовили по методу Мурхеда (1960), предусматривающему накопление в культуре клеток с метафазными пластинками под действием колхицина, обработку клеток гипотоническим раствором, фиксацию и окрашивание препаратов.
При иммуноцитохимическом и цитохимическом исследовании клеточных культур на продукцию инсулина выращивали монослой исследуемых клеток в пенициллиновых флаконах с покровными стеклами, как описано выше. Цитохимическое окрашивание клеток на инсулин проводили альдегидфуксином по Гомори. Для иммуноцитохимического окрашивания гибридных клеток на инсулин использовали моноклональные антитела к инсулину («Sigma», США), антивидовые (вторичные) антитела или антитела с флуоресцином (FITC), дающие зеленое свечение в ультрафиолетовом свете, а также антитела, конъюгированные с пероксидазой хрена. Иммуногистохимические методики описаны L. Andersen с соавт. (5).
Результаты. Полученные от слияния клеточные гибриды на первых пассажах содержали большое число ди- и поликарионов со смешанной морфологией (рис. 1). Кариотип в культуре был нестабильным, в монослое встречались крупные образования с гигантскими ядрами, представляющие собой слившиеся клетки, наблюдалась активная пролиферация.
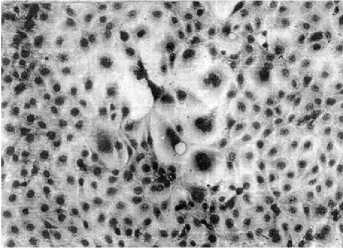
Рис. 1. Гибрид в -клеток кролика и мутантной культуры клеток почки овцы ПО ТК-100 (второй пассаж, окраска по Романовскому, ½200).
Клетки с высокой адгезивной способностью прикреплялись к субстрату, среди них встречались симпластные структуры, содержащие несколько ядер (слившиеся в результате гибридизации клетки, способные сохранять морфологию на протяжении нескольких пассажей). Крупные округлые лимфоцитоподобные клетки располагались на поверхности фибробластов одиночно или небольшими кластерами, иногда отрываясь и переходя в суспензию.
В процессе культивирования было проведено клонирование культур методом предельных разведений. Часть клонов выбраковывалась вследствие нестабильности, низкой адаптивности и других причин, влияющих на жизнеспособность культуры.
На начальных этапах продукцию инсулина гибридными клонами определяли радиоиммунным методом. Первоначальное тестирование провели на восьмом пассаже после перевода с селективной среды на обычную, когда наступила некоторая стабилизация генотипа вновь образующихся клеток и культура стала однородной.
Концентрация инсулина в культуральной жидкости к исходу 6 сут составила 156 нг/л. После этого провели клонирование культуры и отбор инсулинпродуцирующих клонов. Весь объем культуры (6,0 мл клеточной суспензии) ресуспендировали и высеяли в отдельные флаконы объемом 25 мл (по 103 клеток на флакон). Через 6 сут культивирования отобрали пробы культуральной жидкости и методом радиоиммунного анализа определили содержание инсулина в образцах. При концентрации инсулина в контроле 34,4 нг/л (культура клеток почки овцы ПО ТК-100) в 15 проанализированных гибридных клонах она составила от 120 (клоны 2Д и 2Ж) до 360 (клон 1Г) нг/л, то есть на 12-е сут все образцы гибридной культуры продуцировали инсулин в количестве, превышающем контрольный показатель в 3,5-11,5 раз.
Все 15 образцов были трижды реклонированы с криоконсервацией на каждой стадии получения клонов гибридных клеток. После третьего клонирования образцы высевали на планшеты (по 100 клеток на лунку) и на 6-е сут культивирования тестировали пробы культуральной жидкости иммунолюминесцентным методом. По результатам тестирования отобрали клоны, продуцирующие наибольшее количество инсулина.
Из 45 клонов 4 не продуцировали инсулин (клоны 17, 22, 1В и 4А), у остальных показатель варьировал от 1,7 (клон 16) до 42 пмоль/л. Для иммуноцитохимического и цитохимического определения содержания инсулина в клетках гибридных клонов суспензию клеток каждого клона максимально разводили питательной средой и высевали в многолуночные планшеты (1-10 клеток на лунку). В результате получили 24 жизнеспособные субпопуляции гибридной культуры, при этом клоны существенно различались между собой как по культуральным и морфологическим свойствам, так и по продукции инсулина, оцениваемой по содержанию зерен инсулина в клетках (рис. 2).
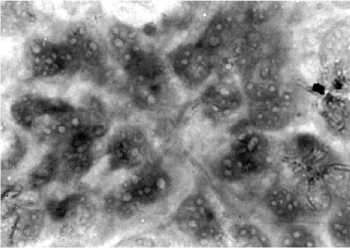
Рис. 2. Определение продукции инсулина межвидовой гибридной культурой ПО ТК-100 % в —клетки кролика. Окраска по Гомори, ^200.
Жизнеспособность клонов поддерживалась культивированием в термостате (СO 2 -инкубатор) при содержании СO 2 5 % и влажности воздуха 100 % (4-5 флаконов на клон) с пересевом каждые 5-7 сут. После 16-18 пассажей в результате селекции по культуральноморфологическим, кариологическим признакам и продукции инсулина были отобраны 10 наиболее перспективных клонов, из которых в результате выделили два наиболее перспективных — Г1 и Г2, которые одновременно реклонировали. К 18-му пассажу из клонов Г1 и Г2 жизнеспособными остались соответственно 10 и 16, но по продукции инсулина клоны Г2 были признаны неперспективными.
Из всех клонов поколения Г1 для дальнейшей работы выбрали клоны ГА2 и ГГ4. Однако у клеток клонов ГГ4 после реклонирования и 18 пассажей повышалась адгезивность, в связи с чем их трудно было отделять от подложки, и оказалась практически утраченной способность секретировать инсулин.
Клетки клона ГА2 сохранили как положительные культуральные характеристики, так и возможность продуцировать значительное количество инсулина в питательной среде.
Таким образом, β-клетки поджелудочной железы новорожденных кроликов способны сливаться с эпителиоподобными клетками почки овцы, дефектными по ферменту тимидинкиназе. Полученная межвидовая гибридная культура имеет стабильную морфологию, культуральные свойства и продуцирует инсулин в культуральную среду, а также накапливает зерна инсулина в цитоплазме, что подтверждается иммуноцитохимическим, гистологическим, иммунорадиологическим методом и методом флуоресцирующих антител. В результате выделены клоны с высоким уровнем продукции инсулина в культуральную среду.
Автор выражает благодарность профессору Н.Н. Скалецкому, сотрудникам Всероссийского НИИ экспериментальной ветеринарии им. Я.Р. Коваленко Т.В. Гальнбек, И.К. Абдрахманову, А.Н. Сафиной за помощь при проведении работы.
Л И Т Е Р А Т У Р А
-
1. Д е д о в И.И., Б а л а б о л к и н М.И., К л е б а н о в а Е.М. Современные аспекты трансплантации островков поджелудочной железы при сахарном диабете. М., 2001.
-
2. С к а л е ц к и й Н.Н., К и р с а н о в а Л.А., Б л ю м к и н В.Н. Проблемы трансплантологии и искусственных органов М., 1994: 73-80.
-
3. Д ь я к о н о в Л.П., К у щ А.К., Т у г и з о в Ш.М. др. Методические рекомендации по гибридизации соматических клеток сельскохозяйственных животных. М.,
-
4. С к а л е ц к и й Н.Н., К и р с а н о в а Л.А., Б а р а н о в а Н.В. и др. Получение культур островковых клеток для трансплантации: новые подходы и новое качество. Вестник трансплантологии и искусственных органов, 2002, 3: 86.
-
5. A n d e r s e n L., D i n e s e n В., J o r g e n s e n P.N. e.a. Enzime immunoassay for detekt human insulin in serum or plasma. Clin. Chem., 1993, 39(4): 578-582.
-
ГНУ Всероссийский НИИ животноводства Россельхозакадемии,


