Получение 2-фенилбензимидазола
Автор: Холхоев Бато Чингисович, Бурдуковский Виталий Федорович, Могнонов Дмитрий Маркович, Луцкая Мария Руслановна
Журнал: Вестник Бурятского государственного университета. Философия @vestnik-bsu
Рубрика: Химия
Статья в выпуске: 3, 2011 года.
Бесплатный доступ
2-фенилбензимидазол синтезирован окислительной дегидроциклизацией N-фенилбензамидина Последний получен взаимодействием бензонитрила и анилина в расплаве и в ионной жидкости гептахлордиалюминат 1-бутил-3-метилимидазолия.
2-фенилбензимидазол, n-фенилбензамидин, бензонитрил, анилин, ионные жидкости
Короткий адрес: https://sciup.org/148180224
IDR: 148180224 | УДК: 547.592
Synthesis of 2-phenilbenzimidazole
2-phenilbenzimidazole was synthesized by oxidative dehydrocyclization of N-phenilbenzamidine. The last was obtained by interaction of benzonitrile and aniline in melt and in ionic liquid of 1-butyl-3-metylimidazolium heptachlorodialuminate.
Текст научной статьи Получение 2-фенилбензимидазола
2-фенилбензимидазол широко применяется как отвердитель эпоксидных смол, для предохранения поверхности различных металлов от коррозии, в качестве биологически активного вещества и промежуточного продукта для получения мономеров. Однако традиционный метод его получения, основанный на взаимодействии о-фенилендиамина с бензойной кислотой в расплаве или в растворе поли-фосфорной кислоты, имеет существенные недостатки, связанные с тем, что синтез проводится в сравнительно жестких условиях, что в сочетании с высокой окисляемостью о-фенилендиамина приводит к снижению выхода и качества целевого продукта [1].
В то же время безрастворный способ осуществления реакций или замена токсичных, взрывоопасных реакционных сред на альтернативные сверхкритические (СО 2 , Н 2 О) или ионные жидкости (ИЖ) является одним из бурно развивающихся направлений «зеленой» химии, призванной устранить указанные недостатки [2].
В данной работе показана принципиальная возможность синтеза 2-фенилбензимидазола окислительной дегидроциклизацией предварительно полученного N-фенилбензамидина на основе бензо- нитрила и анилина, согласно схеме:
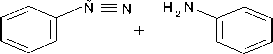
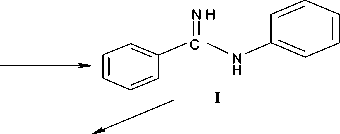
N
N H
C
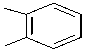
II
Известно [3], что на основе ароматических нитрилов и аминов в отсутствии кислых катализаторов не удается получить N-замещенные амидины с удовлетворительными выходами. В таких реакциях широко используются кислоты Льюиса. Наличие последних необходимо для увеличения полярности связи –C≡N, за счет координации вакантной орбитали кислоты с неподеленной парой электронов азота, что значительно усиливает электрофильность нитрильной группы.
Исследование процесса образования соединения I в расплаве показало, что наибольший выход (54% после перекристаллизации из бензола) достигается при эквимольном соотношении исходных веществ в присутствии 1 эквивалента хлорида алюминия за 30 мин при температуре 200оС. Тогда как изучение процесса амидинообразования в ИЖ показало, что целевой продукт образуется с большим выходом (83% после перекристаллизации из бензола) и в более мягких условиях (140оС, при концентрации исходных соединений 1 моль/л), при одинаковой продолжительности синтеза.
На основе полученного N-фенилбензамидина окислительной дегидроциклизацией получен 2-фенилбензимидазол. Циклизацию осуществляли действием на солянокислую соль амидина в растворе метанола гипохлоритом натрия и основанием, в результате чего удалось получить целевой продукт
ВЕСТНИК БУРЯТСКОГО ГОСУДАРСТВЕННОГО УНИВЕРСИТЕТА с выходом более 90%. Строение полученных соединений I, II подтверждено совокупностью методов ИК-, ЯМР- 13С и 1Н спектроскопии.
Таким образом, в работе продемонстрирован эффективный метод синтеза 2-фенилбензимидазола окислительной дегидроциклизацией N-фенилбензамидина. Последний образуется с хорошим выходом при сравнительно мягких условиях в ионной жидкости гептахлордиалюминат 1-бутил-3-метилимидазолия.


