Получение фосфорного удобрения с дополнительными питательными элементами
Автор: Самедов М.М., Мустафа Д.М., Мамедова Г.М., Джавадова С.Г.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Химическая технология
Статья в выпуске: 2 (96) т.85, 2023 года.
Бесплатный доступ
С целью получения фосфорного удобрения, обогащенного дополнительными питательными элементами, процесс разложения апатитового концентрата серной кислотой осуществляли с добавкой, в первом варианте - гидрофосфатом аммония, а во втором варианте - гидрофосфатами аммония и калия. Экспериментальными исследованиями изучено влияние добавок на процесс взаимодействия серной кислоты с фторапатитом, а также рентгенофазовыми и ИК-спектроскопическими анализами изучен структурный состав полученного продукта. Установлено, что с применением добавок, полученное фосфорное удобрение содержит наряду с дигидрофосфатом кальция, также дигидрофосфат аммония. Отличительной особенностью является разложение фосфатов сернокислотного типа, в результате чего получается переходящий в твердую фазу малорастворимый сульфат кальция, который имеет следы присутствия в полученном удобрении, а также может не входить в состав раствора. Процесс разложения фторапатита серной кислотой с использованием добавочной части (NH4)2HPO4, оптимальное количество добавочной части необходимо считать 12-18%-ную (от массы серной кислоты) добавку, при этом достигается наиболее высокая степень разложения апатитового концентрата, которая составляет 95-97%. Проведенные исследования установили, что введение добавки - гидрофосфатов аммония и калия - в процесс сернокислотного разложения апатитового концентрата также положительно влияет на продолжительность периода созревания суперфосфата. Для уточнения структурного состава готового продукта были проведены рентгенофазовые исследования и ИК-спектрометрический анализ порошкообразного продукта. Таким образом, минеральные удобрения, полученные с применением добавок, имеющим в своем составе дополнительный питательный элемент, а именно азот - в первом варианте, а азотом и калием - во втором варианте.
Фосфорные удобрения, интенсифицирующие добавки, разложение, фторапатит, обогащение, гидрофoсфаты аммония и калия
Короткий адрес: https://sciup.org/140303208
IDR: 140303208 | УДК: 661.632.2:631.841.1 | DOI: 10.20914/2310-1202-2023-2-198-204
Obtaining phosphate fertilizer with additional nutrients
In order to obtain phosphorus fertilizer enriched with additional nutrients, the decomposition process of apatite concentrate with sulfuric acid was carried out with an additive, in the first variant - ammonium hydrophosphate, and in the second variant - ammonium and potassium hydrophosphates. Experimental studies have studied the effect of additives on the interaction of sulfuric acid with fluorapatite, as well as X-ray phase and IR spectroscopic analyses have studied the structural composition of the resulting product. It was found that with the use of additives, the resulting phosphorus fertilizer contains, along with calcium dihydrophosphate, also ammonium dihydrophosphate. A distinctive feature is the decomposition of sulfuric acid phosphates, resulting in a poorly soluble calcium sulfate that passes into the solid phase, which has traces of its presence in the resulting fertilizer, and may also not be part of the solution. The process of decomposition of fluorapatite with sulfuric acid using an additional part (NH4)2HPO4, the optimal amount of the additional part should be considered 12-18% (by weight of sulfuric acid) additive, while the highest degree of decomposition of apatite concentrate is achieved, which is 95-97%. The conducted studies have established that the introduction of an additive - ammonium and potassium hydrophosphates - into the process of sulfuric acid decomposition of apatite concentrate also has a positive effect on the duration of the superphosphate maturation period. To clarify the structural composition of the finished product, X-ray phase studies and IR spectrometric analysis of the powdered product were carried out. Thus, mineral fertilizers obtained with the use of additives having an additional nutrient element in their composition, namely nitrogen - in the first variant, and nitrogen and potassium - in the second variant.
Текст научной статьи Получение фосфорного удобрения с дополнительными питательными элементами
Общепринято, что разложение апатитового концентрата кислотами приводит к образованию фосфорной кислоты, а также соответствующих солей кальция. Данные фосфорные кислоты и соли кальция отличаются высокой растворимостью (примером служит растворение в азотной или соляной кислотах). В результате дальнейшая переработка данных полученных растворов в получении удобрений производится с помощью выделения и связывания некоторых частей кальция с целью исключения превращений в сфере химических реакций, в результате которого появляются неусвояемые, трудноусвояемые растения соединений фосфата. Отличительной чертой является разложение фосфатов сернокислотного типа, в результате которого получаем малорастворимый сульфат кальция, переходящий в твердую фазу, который имеет следы присутствия в полученном удобрении, а также может не входить в состав раствора [1–4].
Материалы и методы
Интенсификационный процесс при разложении природного фосфата серной кислотой включает в себя использование 40%-ного раствора (NН 4 ) 2 НРО 4 как добавки. Экспериментальные исследования осуществляли по известной методике [5]. Схема процесса представлена на рисунке 1. Все применяемы в работе реактивы имели марку ХЧ и были приобретены посредством компании «АО Реахим» (Россия).
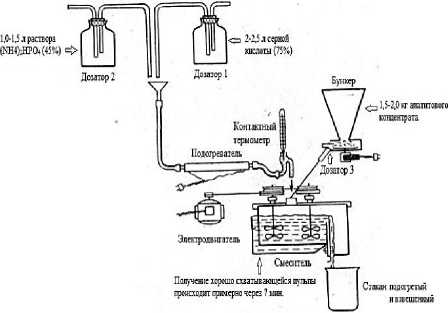
Рисунок 1. Схема получения суперфосфата с применением раствора (NН 4 ) 2 НРО 4 (40%) как интенсифицирующей добавки. Составлено по данным [6]
Figure 1. Scheme for obtaining superphosphate using a solution of (NН4) 2 НРО 4 (40%) as an intensifying additive. Compiled according to [6]
Ранее было установлено при 65ºС достигается максимальная (88,2%) степень разложения сырья через 90 мин. Поэтому подогрев выполняли до нужной температуры, а после заполнения стакана его выдерживали в термостате (1100 ºС) 90 мин. и получали готовое фосфорсодержащее минеральное удобрение [6]. Предложенный способ сравнивали с получением суперфосфата обычным способом, где для получения суперфосфата добавляли только серную кислоту в количестве 2,8–3,5 л на тот же вес апатитового концентрата (рисунок 1).
Проведены отдельные эксперименты по добавлению в качестве интенсифицирующей добавки смеси гидрофосфатов аммония / калия и воды следующих составов (% масс.): ( 1 ) 8, 2, 90; ( 2 ) 12, 4, 84; ( 3 ) 15, 6, 79; ( 4 ) 18, 8, 76; ( 5 ) 22, 10, 68; ( 6 ) 25, 12, 63; ( 7 ) 28, 14, 58; ( 8 ) 30, 16, 54.
Рентгенограммы образцов суперфосфата сняты на дифрактометре DРОН-3 при облучении СuК α в Ni фильтре. При снятии диффактограм образцов суперфосфата скорость движения счетчика составляла 2 и 4 град/мин; точность отсчета по диаграмме ±0,2 мм; погрешность определения межплоскостных расстояний равнялась 1%. Для объяснения вещественно-структурных особенностей полученного продукта использован метод ИК-спектроскопии. ИК-спектры были сняты на спектрометре марки ИР-20 (Россия).
Результаты
При обычном способе получения суперфосфата требуется повышенный объем серной кислоты, если сравнивать необходимое количество кислоты для связывания кальция в апатите [6, 7]:
2Са 5 (РО 4 ) 3 F + 7Н 2 SО 4 + 3Н 2 О → 3Са(Н 2 РО 4 ) 2 ∙Н 2 O + 7СаSО 4 + 2НF
В предложенном способе добавление в качестве реагента гидрофосфата аммония позволяет получить смесь дигидрофосфата кальция и аммония. Последний обогащает конечное удобрение азотом. Выяснено при процессе разложения фторапатита серной кислотой с добавкой гидрофосфата аммония и без нее включает в себя два процесса [8]. Фторапатит и серная кислота имеют реагирование до образования свободной фосфорной кислоты и сульфата кальция:
Са 5 F(РО 4 ) 3 + 5Н 2 SО 4 + (NН 4 ) 2 НРО 4 →
5СаSО 4 + 2NН 4 Н 2 РО 4 + 2Н 3 РО 4 + HF
Когда серная кислота полностью используется, появляется фосфорная кислота, которая вступает в реакцию с фторапатитом, образующий кальцийдигидрофосфат:
Са 5 F(РО 4 ) 3 + 7Н 3 РО 4 + 5Н 2 O → 5Са(Н 2 РО 4 ) 2 Н 2 O + HF
Полученный монокальцийфосфат держат сначала в растворе, в котором происходит процесс пересыщения – кристаллизации. Коэффициенты в уравнениях свидетельствуют о 70% реакции в первой стадии при наличии стехиометрических соотношений компонентов, а на второй стадии реагирует только 30% фторапатита. Отсюда получаем уравнение реакции в суммарном виде: 6Са 5 F(РО 4 ) 3 + 25Н 2 SО 4 + (NН 4 ) 2 НРО 4 + 5Н 2 O
→ 5Са(Н 2 РО 4 ) 2 ×Н 2 O + 2NН 4 Н 2 РО 4 + 25СаSО 4 + 7Н 3 РО 4 + 6НF
Количество суперфосфата и сама степень разложения апатитового концентрата имеет изменения при добавлении гидрофосфата аммония, которые отражены в таблице 1, из которой видно, что при использовании интенсифицирующей добавки гидрофосфата аммония процесс разложения фторапатита в суперфосфате при десятидневном дозревании ускоряется. Так, увеличение добавки до 18% от массы серной кислоты процесс разложения определяется до 96,04%.
Таблица 1.
Состав суперфосфата и степени разложения фторапатита в зависимости от количества добавки гидрофосфата аммония
Table 1.
The composition of superphosphate and the degree of decomposition of fluorapatite, depending on the amount of ammonium hydrophosphate additive
|
Количество (Quantity) (NН 4 ) 2 НРО 4 , % от m Н 2 SО 4 |
Состав суперфосфата после 10-ти суточного дозревания, масс. % Superphosphate composition after 10 days ripening, wt. % |
Степень разложения, % Degree of decomposition, % |
|||
|
Р 2 О 5 |
Р 2 О своб. |
N |
Н 2 O |
||
|
общ. / усв. / водн. |
|||||
|
0 |
21,32 / 9,59 / 18,66 |
7,23 |
– |
9,89 |
91,88 |
|
5 |
21,24 / 19,96 / 19,08 |
6,82 |
0,69 |
8,92 |
93,97 |
|
8 |
21,19 / 20,11 / 18,749 |
6,64 |
0,97 |
8,47 |
94,90 |
|
12 |
21,12 / 20,24 / 18,68 |
6,39 |
1,38 |
7,86 |
95,83 |
|
15 |
21,08 / 20,46 / 18,59 |
6,17 |
1,95 |
7,53 |
97,06 |
|
18 |
20,98 / 20,15 / 18,54 |
5,96 |
2,36 |
7,18 |
96,04 |
|
22 |
20,76 / 19,50 / 18,36 |
6,71 |
2,71 |
6,95 |
93,93 |
|
26 |
20,53 / 19,08 / 18,12 |
6,93 |
2,98 |
6,72 |
92,94 |
Данный показатель является повышенной степенью разложения и свидетельствует об использовании добавки (NН 4 ) 2 НРО 4 как реагента, стимулирующего введение дополнительных ионов НРО 4 2- и имеющего высокое влияние на водородные ионы, которые положительно воздействуют на глубину разложения апатитового концентрата. При этом, если увеличить массу добавки на 22% и выше, процесс считается нецелесообразным, так как приводит к снижению степени разложения фторапатита в суперфосфате. Большое использование данной добавки приводит к появлению к множеству мелких кристаллов сульфата кальция, которые осаждаются на поверхности частиц апатита, тем самым являются большим препятствием для диффузии кислоты к зернам апатита.
Анализ данных таблицы 1 показывает, что количественный состав добавки, находящийся в интервальном отрезке 12–18% от массы серной кислоты считается целесообразным, так как отличается высокой степенью разложения при сумме питательных составляющих, равной 21,62–22,51%. В итоге, оптимальный процесс разложения фторапатита серной кислотой с достигается при количестве добавочной части (NН4)2НРО4 12–18% от массы серной кислоты. При этом достигается наиболее высокая степень разложения апатитового концентрата, которая составляет 95–97%.
Далее исследовали влияние состава добавки на качественные показатели готового продукта и степень разложения апатитового концентрата. Полученные данные эксперимента представлены в таблице 2.
Как видно из таблицы 2, при низких концентрациях добавки (опыты 1–3) существенных изменений в составе полученного суперфосфата не происходит, но с увеличением концентрации добавки увеличивается степень разложения апатитового концентрата (опыты 4–6), а конечный продукт имеет добавки питательных элементов – азота и калия. Дальнейшее увеличение концентрации добавки (опыты 7, 8) является нецелесообразным, так как происходит некоторое снижение степени разложения сырья и уменьшение содержания Р 2 О 5усв в готовом суперфосфате. Следовательно, оптимальным составом добавки следует считать% масс.: NН 4 НSО 4 – 18–25;
К 2 СО 3 – 8–12; Н 2 O – 76–63.
Таблица 2.
Состав суперфосфата и степень разложения апатита в готовом продукте в зависимости от состава добавки Table 2.
The composition of superphosphate and the degree of decomposition of apatite in the finished product, depending on the composition of the additive
|
Состав добавки, % масс. Additive composition, % wt |
Показатели суперфосфата, % масс. Superphosphate parameters, % wt |
Степень разложения, % Degree of decomposition, % |
|||
|
(NН4) 2 НРО 4 / К 2 НРО 4 / Н 2 О |
Р 2 О 5 общ / усв. / своб. |
N |
К 2 O |
Н 2 O |
|
|
8 / 2 / 90 |
21,18 / 19,70 / 6,68 |
0,39 |
0,34 |
8,05 |
93,01 |
|
12 / 4 / 84 |
20,83 / 19,59 / 6,40 |
0,61 |
0,70 |
7,83 |
94,05 |
|
15 / 6 / 79 |
20,41 / 19,39 / 6,27 |
0,75 |
0,98 |
7,67 |
95,00 |
|
18 / 8 / 76 |
20,05 / 19,48 / 5,95 |
1,00 |
1,40 |
7,44 |
97,16 |
|
22 / 10 / 68 |
19,70 / 19,31 / 5,63 |
1,18 |
1,72 |
7,26 |
98,02 |
|
25 / 12 / 63 |
19,42 / 18,84 / 5,42 |
1,30 |
2,10 |
7,04 |
97,01 |
|
28 / 14 / 58 |
18,86 / 17,90 / 5,38 |
1,42 |
2,38 |
6,85 |
94,91 |
|
30 / 16 / 54 |
18,54 / 17,40 / 5,33 |
1,56 |
2,70 |
6,71 |
93,85 |
Проведенными исследованиями установлено, что введение добавок гидрофосфатов аммония и калия в процесс сернокислотного разложения апатитового концентрата оказывает положительное влияние также на продолжительность срока дозревания суперфосфата. При этом оптимальное значение количества добавки, равное 22 и 10% от массы серной кислоты для гидрофосфатов аммония и калия соответственно, способствует максимальному разложения апатита и дальнейшему процесса вызревания суперфосфата.
Предложенный метод получения суперфосфата, обогащенного добавками азота и калия, прошел испытания на Сумгаитском суперфосфатном заводе. Получено фосфорное удобрение с включением добавочных компонентов, а именно гидрофосфатов аммония и калия. Разработанная технология является легко осуществимой и целесообразной для решения задачи обогащения состава удобрения. При оптимальных количестве и составе добавки полученный продукт обладает хорошими физико-химическими свойствами, становится более рассыпчатым, пористым, устойчивым к механическим воздействиям с точки зрения тиксотропных свойств и обогащен добавочно питательными элементами – азотом (N – 1,0–1,3% масс.) и калием (К 2 О – 1,4–2,1% масс.). Для уточнения структурного состава готового продукта проведены рентгенофазовые исследования и ИК – спектрометрический анализ порошкообразного продукта. В качестве сравнения использовали образец суперфосфата, полученного обычным способом.
Из дифрактограммы образцов суперфосфата следует, что в обычном суперфосфате в основном содержатся дигидрофосфат кальция и сульфат кальция с различной степенью гидратации (рисунок 2, дифрактограмма № 1). При добавке гидрофосфата аммония в 8% от массы серной кислоты существенных изменений в фазовом составе суперфосфата не наблюдается, за исключением появления новых полос дигидрофосфата аммония – V (см. рисунок 2, дифрактограмма № 2). При добавлении гидрофосфата аммония с 12 и 15%-й концентрации (от массы серной кислоты) интенсивность полос дигидрофосфата аммония (V) увеличивается (рисунок 3).
На ИК-спектрограммах представлены спектры суперфосфата, полученного с 10 и 12%-ной добавкой раствора гидрофосфата аммония (рисунок 4, спектры 1 и 2) и суперфосфата, полученного обычным способом (рисунок 4, спектр 3).
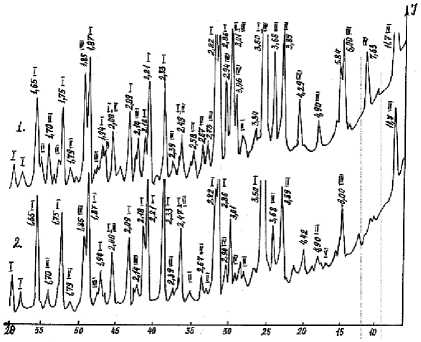
Рисунок 2. Дифрактограммы простого суперфосфата (№ 1) и суперфосфата, полученного с 8%-ной (от массы серной кислоты) добавкой гидрофосфата аммония (№ 2)
Figure 2. Diffractograms of simple superphosphate (No. 1) and superphosphate obtained with 8% (by weight of sulfuric acid) addition of ammonium hydrophosphate (No. 2): I – СаSО 4 ; II – Ca(Н 2 РО 4 ) 2 ; III – СаSО 4 × 0,5 Н 2 О; IV – СаНРО 4 × 2Н 2 О; V – NН 4 Н 2 РО 4
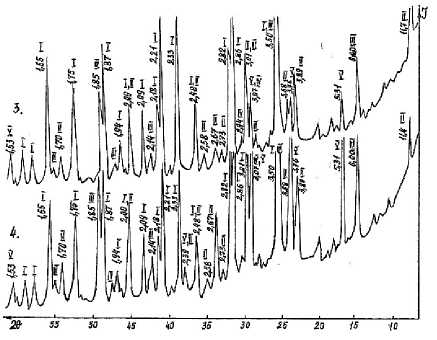
Рисунок 3. Дифрактограммы образцов суперфосфата, полученного с 12 и 15%-ной (от массы серной кислоты) добавкой гидрофосфата аммония (соответственно № 3 и № 4)
Figure 3. Diffractograms of samples of superphosphate obtained with 12 and 15% (by weight of sulfuric acid) addition of ammonium hydrophosphate (co-responsible No. 3 and No. 4): I – СаSО 4 ; II – Ca(Н 2 РО 4 ) 2 ; III – СаSО 4 × 0,5 Н 2 О; IV – СаНРО 4 × 2Н 2 О; V – NН 4 Н 2 РО 4
На рисунок 5 представлены спектры химически чистого дигидрофосфата кальция (рисунок 5. спектр 1), дигидрофосфата аммония (рисунок 5. спектр 2) и суперфосфата, полученного с 15-ти процентной добавкой гидрофосфата аммония (рисунок 5. спектр 3). При сравнении спектров суперфосфатов, полученных без добавки и с добавкой гидрофосфата аммония видно, что появляются линии поглощения 1405 и 1445 см-1, соответствующие NН 4 + иону и характерные для деформационных комбинаций, они не перекрываются другими полосами. Наличие данной полосы подтверждает присутствие дигидрофосфата аммония в исследуемом продукте.
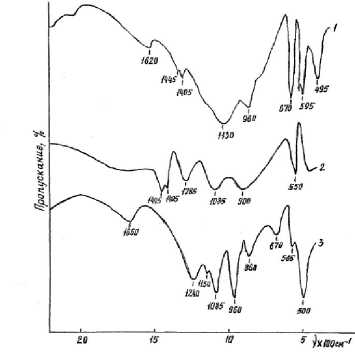
Рисунок 4. ИК – спектры суперфосфата, полученного с добавкой (10 и 12% от массы сернойкислоты) гидрофосфата аммония (спектры 1 и 2) и суперфосфата без добавки (спектр 3)
Figure 4. IR spectra of superphosphate obtained with the addition (10 and 12% by weight of sulfuric acid) of ammonium hydrophosphate (spectra 1 and 2) and super-phosphate without the addition (spectrum 3)
Таким образом, результаты рентгенографических и ИК–спектроскопических исследований подтвердили, что при введении гидрофосфата аммония в процесс разложения апатита серной кислотой полученный суперфосфат наряду с кальцийдигидрофосфатом содержит также аммонийдигидрофосфат.
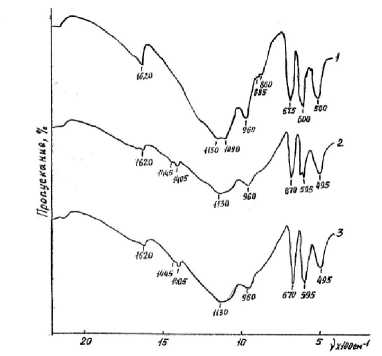
Рисунок 5. ИК–спектры дигидрофосфата кальция (спектр 1), дигидрофосфата аммония (спектр 2) и суперфосфата, полученного с добавкой (15% от массы кислоты серы) гидрофосфата аммония (спектр 3) Figure 5. IR spectra of calcium dihydrophosphate (spectrum 1), ammonium dihydrophosphate (spectrum 2) and su-perfosphate obtained with the addition (15% by weight of sulfur acid) of ammonium hydrophosphate (spectrum 3)
Обсуждение
Предложенный способ разложения апатита серной кислотой с интенсифицирующей добавкой гидрофосфатов аммония и калия отличается рядом преимуществ: снижение расхода кислоты, обогащение готового суперфосфата калием и азотом, ускорение созревания, повышение выхода готового продукта в связи с максимизацией разложения исходной породы. По анализу литературных данных установлено, что сведения по добавлению вышеуказанной добавки в качестве интенсифицирующего и обогащающего компонента отсутствуют. Описаны способы: активации низкосортных фосфоритовых руд концентрированными растворами сульфата аммония [9]; получения суперфосфата, обогащенного бором и молибденом [10]; нейтрализации свободной кислотности суперфосфата аммиаком [11]. Проведены исследования получения фосфорных удобрений из отходов производств, в частности из золы осадка сточных фосфатных минералов и закрытию цикла P [12]. Изучены возможности оптимизации производства обычного суперфсофата и его грануляции в зависимости от расхода серной кислоты [4] и разложения фосфоритов и апатитов, в том числе низкосортных фосфорной кислотой для получения суперфосфата [8, 13, 14]. Данный способ интенсификации получения суперфосфата не исследован в литературе. Способы оптимизации получения суперфосфата без добавок и с добавками интересны для поиска направления дальнейших исследований, включающих подбор источников фосфорных удобрений, анализ возможностей внедрения в состав конечного продукта других элементов, полезных для растений.
Анализ литературы показал отсутствие способов получения суперфосфата, аналогичных или близких к предложенному. Единственный пример, который отдаленно напоминает разработанный способ, заключается в получении фосфорно-калийного удобрения на основе сернокалийного раствора хлористого калия, что позволяет получить конечный продукт без содержания хлора [15–20].
Заключение
В результате проведенных исследований разработан метод получения суперфосфата из апатита. Посредством введения гидрофосфата аммония в качестве интенсифицирующей добавки позволило сократить объем используемой серной кислоты как основного компонента реакции, обеспечивающего разложение аппатита. Достигнуто сокращение времени созревания конечного продукта и внедрение в суперфосфат источника азота и калия при использовании в качестве интенсифицирующей добавки смеси гидрофосфатов аммония и калия. По нашим данным, интервальном отрезке 12–18% от массы серной кислоты считается целесообразным при использовании 45%-го раствора (NН4)2НРО4. При исследовании влияния интенсифицирующей добавки, состоящей из смеси гидрофосфатов аммония и калия, установлено, что максимальная (98,02%) степень разложения достигается при внесении компонентов 19,7 и 19,31% от массы серной кислоты соответственно.
Современные исследования в сфере получения суперфосфатов многогранны, однако направление применения гидрофосфатов аммония и калия не исследовано в литературе, поэтому разработанный способ является уникальным. Дальнейшие исследования могут быть направлены на оптимизацию получения суперфосфата из различных, в том числе обедненных пород и других фосфорсодержащих источников для организации безотходных технологий. Другое направление, которое следует учитывать, – применение других интенсифицирующих добавок, полезных для обогащения конечного удобрения дополнительными питательными элементами.
Выражаем благодарность сотрудникам Сумгаитского государственного университета и Азербайджанского университета нефти и промышленности за помощь в аналитических исследованиях.
Список литературы Получение фосфорного удобрения с дополнительными питательными элементами
- Сахаров Ю.Н., Махоткин А.Ф., Махоткин И.А., Ситкин А.И. Механизм и кинетика разложения фосфатного сырья // Вестник Казанского технологического университета. 2011. № 11. С. 18-22.
- Тлеуханова Г.Б., Касымова Ж.С. Изучение научно-производственных принципов химической технологии экстракционной фосфорной кислоты в лабораторных условиях // Матер. VIII Международной студенческой научной конференции «Студенческий научный форум» URL: https://scienceforum.ru/2016/article/2016020073
- Sherkuziev D. Simple superphosphate by two-stage acid treatment of phosphate raw materials // IOP Conference Series: Earth and Environmental Science. 2021. V. 939. P. 012057.
- Otaboev Kh., Sherkuziev D., Namazov Sh., Radjabov R., et al. Flow of simple superphosphate using two-stage decomposition of phosphorite // IOP Conference Series: Earth and Environmental Science. 2021. V. 939. P. 012055.
- Mahammadjanovich S.M., Muhitdinovich T.S., Elbekovich S.B. Obtainment of suspended phosphorus-potassium containing nitrate // Austrian Journal of Technical and Natural Sciences. 2016. №. 9-10. P. 95-100.
- Самедов М.М.О., Гасанова Т.Ш.Г., Мамедова Г.М.Г. Исследование процесса разложения природных фосфатов серной кислотой с применением интенсифицирующих добавок - (NH4) 2HPO4 // Elmi xəbərlər. Təbiət və texniki elmlər bölməsi. 2020. Т. 20. № 3. С. 19-23.
- Гумбатов М.О.о. Интенсификация процесса получения суперфосфата // Евразийский научный журнал. 2016. № 1. P. 1-4
- Усманов Б.С., Эргашев А.А, Исследование процесса разложения низкосортных фосфоритов // Scientific progress. 2021. № 7. P. 712-716.
- Atashev E. Production of azosuperphosphate in the participation of central Kyzylkum phospharites and ammonium sulphate // Journal of critical reviews. 2020. V. 7. №. 7. P. 358-362.
- Гумбатов М.О. Получение суперфосфата, обагащенного бор - молибденом // Актуальные проблемы гуманитарных и естественных наук. 2016. № 3-1. C. 1-3.
- Бадалова О.А., Отабоев Х.А., Намазов Ш.С., Сейтназаров А.Р. и др. Простой аммонизированный суперфосфат на основе забалансовой фосфоритной руды - минерализованной массы // Universum: технические науки: электрон. научн. журн. 2018. № 9 (54). C. 1-5.
- You Y., Klein J., Hartmann T.E., Nkebiwe P.M. et al. Producing Superphosphate with Sewage Sludge Ash: Assessment of Phosphorus Availability and Potential Toxic Element Contamination // Agronomy. 2021. V. 11. P. 1506.
- Молдабеков Ш.М., Жантасов К.Т., Жанмолдаева Ж.К., Алтыбаев Ж.М. и др. Кинетика разложения низкокачественных фосфоритов фосрной кислотой и получение двойного суперфосфата циклическим способом // Современные наукоемкие технологии. 2013. № 11. С. 107-112.
- Sabirov R., Makhotkin A., Sakharov Yu., Makhotkin I. et al. Mechanism of the process of decomposition of apatitis with phosphoric acid // Proceedings of the Voronezh State University of Engineering Technologies. 2019. V. 81. P. 294-297.
- Гумбатов М.О.о. Разложение апатитового концентрата с применениемсернокалийного раствора // Евразийский научный журнал. 2016. № 1. С. 1-4.
- Najmiddinov R., Shamshidinov I., Qodirova G., Sayfiddinov O. Purification of phosphoric acid from impurities in the extraction process and research of obtaining high-quality nitrogen-phosphoric fertilizers // Models and methods in modern science. 2022. V. 1. №. 16. P. 86-99.
- Rolewicz M., Rusek P., Mikos-Szymańska M., Cichy B. et al. Obtaining of suspension fertilizers from incinerated sewage sludge ashes (ISSA) by a method of solubilization of phosphorus compounds by Bacillus megaterium bacteria // Waste and Biomass Valorization. 2016. V. 7. №. 4. P. 871-877.
- Ryszko U., Rusek P., Kołodyńska D. Quality of Phosphate Rocks from Various Deposits Used in Wet Phosphoric Acid and P-Fertilizer Production // Materials. 2023. V. 16. №. 2. P. 793.
- Alzaky M.A.M., Li D. Sulfate of potash and yellow phosphorus to simultaneously remove SO2-NO and obtain a complete fertilizer // Atmospheric Pollution Research. 2021. V. 12. №. 2. P. 147-158. https://doi.org/10.1016/j.apr.2020.10.017
- Santos A.F., Almeida P.V., Alvarenga P., Gando-Ferreira L.M. et al. From wastewater to fertilizer products: Alternative paths to mitigate phosphorus demand in European countries // Chemosphere. 2021. V. 284. P. 131258. https://doi.org/10.1016/j.chemosphere.2021.131258


