Получение низкомолекулярного хитозана и его производных
Автор: Шагдарова Бальжима Цырендоржиевна, Левов Александр Николаевич, Варламов Валерий Петрович
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Биотехнология
Статья в выпуске: 3-5 т.15, 2013 года.
Бесплатный доступ
Методом кислотного гидролиза получена фракция хитозана с молекулярной массой 20 кДа, определены ее основные характеристики. Синтезирован ряд ацилированных производных низкомолекулярного хитозана, содержащих N-(2-гидрокси-3-триметиламмоний)пропильный фрагмент.
Хитозан, ацилированные производные, кватернизированные производные
Короткий адрес: https://sciup.org/148202076
IDR: 148202076 | УДК: 547.99
Preparation of low molecular weight chitosan and its derivatives
Method by acid hydrolysis was obtained low molecular weight chitosan fraction of 20 kDa, its main characteristics were determined. A series of acylated derivatives containing N-(2-hydroxy-3-trimethylammonium) propyl fragment were synthesized from low molecular weight chitosan.
Текст научной статьи Получение низкомолекулярного хитозана и его производных
Одним из достижений биотехнологического прогресса в области изыскания новых перспективных веществ за последние годы стало получение, изучение и внедрение в практику биополимеров хитина, хитозана и их производных. Природный полисахарид хитин, его дезацетилированное производное хитозан и продукты их химической модификации привлекают внимание исследователей благодарякомплексу уникальных физикохимических и биологических свойств, основными из которых являются – биодеградируемость, биосовместимость, низкая токсичность, а также широкий спектр антимикробного действия [1]. Хитин – линейный аминополисахарид, состоящий из N-ацетил-2-амино-2-дезокси-D-глюкопиранозных звеньев. Он служит основным структурным компонентом наружного скелета ракообразных и насекомых, а также входит в состав клеточных стенок грибов. Хитозан – обобщающее название частично (обычно на 70-90%) или полностью дезацетилиро-ванного хитина [2]. Хитин является полимером не растворимым в воде и большинстве органических растворителей, что существенно ограничивает его применение, в отличие от хитозана или его модификаций, которые растворимы в широком диапазоне pH и могут использоваться в различных областях.
Перспективным направлением использования хитозана и его производных является сфера охраны окружающей среды, а именно создание препаратов с радиопротекторными свойствами, сорбентов и композитов для выделения и концентрирования радионуклидов [3]. Также хитозан можно применять как флокулянт для водоподготовки, очистки промышленных стоков, содержащих ионы тяжелых металлов. При использовании его для очистки воды, значительно уменьшается мутность, химическая и биологическая потребность в кислороде [4]. Одной из проблем, возникающих на пути применения высокомолекулярного хитозана в экологии и биотехнологии является его плохая растворимость в воде. Для решения этой проблемы хитозан подвергается деполимеризации. Существует несколько
методов получения низкомолекулярного хитозана, например, ферментативный гидролиз с применением хитиназ, комплексов гепатопакреаса краба или криля [5]. В данном исследовании был использован химический гидролиз, главными преимуществами которого являются низкая степень полидисперсности получаемых фракций, отсутствие в них белковых примесей и низкая стоимость используемых реактивов [6]. Хитозан обладает свободной реакционноспособной аминогруппой, которая может быть использована для присоединения дополнительных функциональных групп (карбоксиметил-, сукцинил-, сульфо- групп, а также четвертичных аммониевых солей) к молекуле хитозана, за счет чего увеличивается его растворимость и улучшаются биологические свойства.
Целью данной работы являлось получение низкомолекулярного хитозана путем кислотного гидролиза и синтез ряда водорастворимых производных на его основе.
В качестве исходного материала был использован крабовый высокомолекулярный хитозан с молекулярной массой 200 кДа, со степенью дезацетилирования 86% (СД) производства ЗАО "Биопрогресс" (Московская область). Далее методом химической деполимеризации соляной кислотой высокомолекулярного хитозана была получена фракция с молекулярной массой 20 кДа (ММ). СД по данным 1Н-ЯМР-спектроскопии (рис. 1) и кондуктометрического титрования составляет 98-100%. Увеличение СД объясняется тем, что происходит расщепление ацетамидных связей в процессе химического гидролиза хитозана. Молекулярную массу образцов определяли методом высокоэффективной гель-проникающей хроматографии (рис. 2) [7]. Полученная фракция хитозана была использована для синтеза ряда производных. Наиболее используемым и легким подходом придания полимеру сильных катионных свойств является кватерни-зация хитозана, так как реакция протекает в мягких условиях с высоким выходом продукта. Ацилирование проводилось с целью увеличения сродства к мембранам бактериальных клеток, так как полученные производные планируется использовать в качестве антибактериального агента.
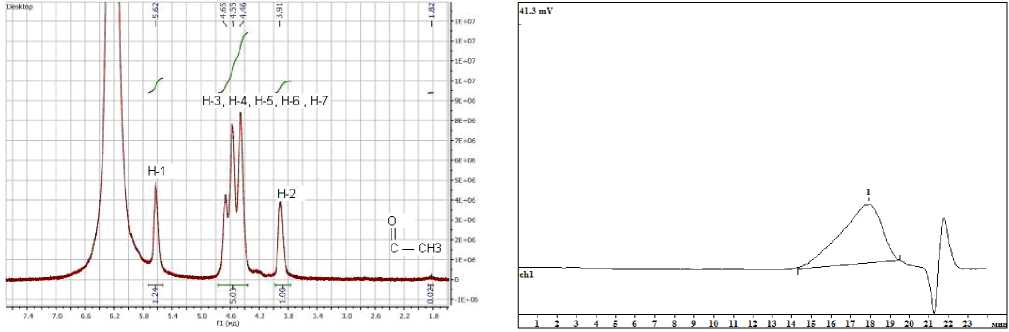
Рис. 2. Хроматограмма образца хитозана. Хроматограф: S 2100 (Sykam, Германия), колонка (7,8×300 мм), сорбент Ultahydrogel-250 (Waters, США) предколонка (4×3 мм) GFC-4000 (Phenomenex, USA) при элюировании раствором 0,05 М CH3COOH, 0,15 М CH3COONH4 (рН 5,1), с расходом 0,5 мл/мин при температуре 30˚C
Рис. 1. 1Н-ЯМР спектр хитозана СД=98%
Синтез производных проводился в две стадии:
-
1) Реакция ацилирования. Взаимодействие хитозана с капроновым, масляным и уксусным ангидридами в среде 1% уксусной кислоты и метанола при 200С, время реакции 5 мин (получены производные с длиной жирнокислотного остатка 6, 4, 2
атомов углерода, соответственно) [5];
-
2) Реакция кватернизации. Исчерпывающее алкилирование первичных аминогрупп хитозана и ацилированных производных глицидилтримети-ламмоний хлоридом проводилось в водной среде при температуре 850С в течение 5 ч [8].
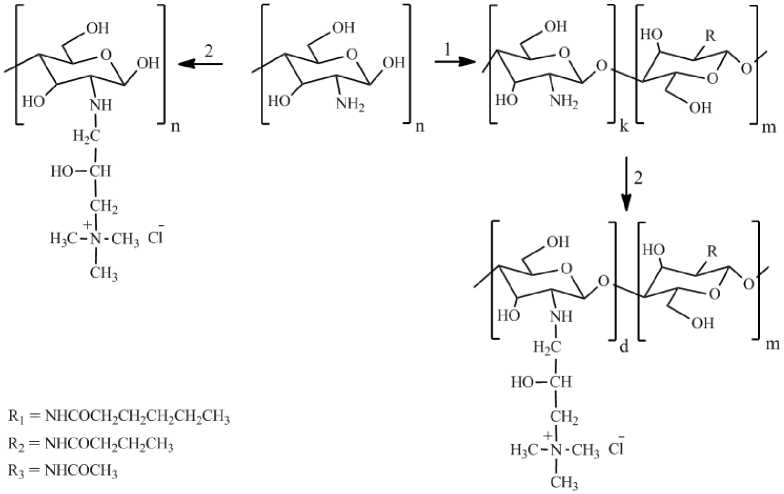
Рис. 3 . Схема химической модификации хитозана: 1 – реакция ацилирования, 2 – реакция кватернизации
В результате были получены производные, представленные на рис. 4.
Структура и степень замещения производных подтверждена с помощью 1Н-ЯМР-спектроскопии.
Таким образом, был получен ряд производных хитозана, которые за счет введённых функциональных групп имеют не только большую по сравнению с хитозаном растворимость в воде, а также будут обладать повышенными антибактериальны- ми свойствами. Перспективным является применение данных производных для использования в области биотехнологии и экологии. Возможно их использование в виде суспензий для защиты растений от болезней и стрессов, а также в качестве компонентов биодеградируемых материалов и защитных покрытий для пищевых продуктов.
На данный момент ведутся работы по изучению антибактериальных свойств полученных производных.
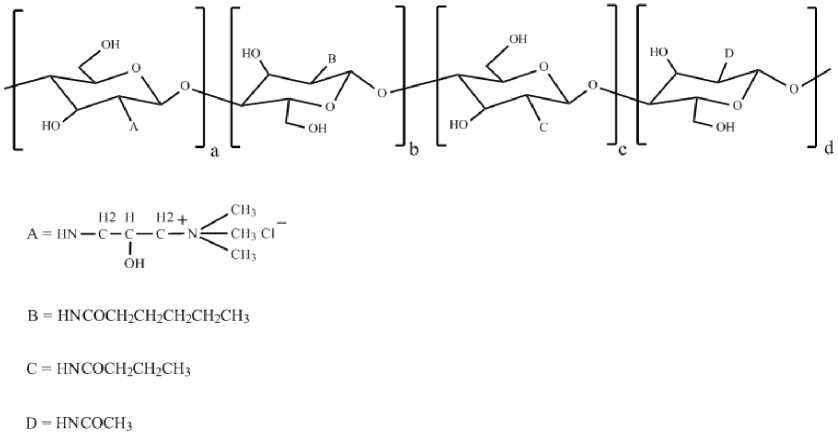
Рис. 4 . Структурная формула полученных производных хитозана
I. N-[(2-гидрокси-3-триметиламмоний)пропил]хитозан хлорид а=100%
II. N-гексаноилхитозан кватернизированный а=90%, b=10%
III. N-бутаноилхитозан кватернизированный а=90%, с=10%
IV. N-этаноилхитозан кватернизированный а=90%, d=10%
-
1. Хитин и хитозан: Получение, свойства и применение / Под ред. К.Г. Скрябина, Г.А. Вихоревой, В.П. Варламова. М.: Наука, 2002. 386 с.
-
2. Хитин и хитозан: Природа, получение и применение / Пер. с исп., под ред. В.П. Варламова, С.В. Немцева, В.Е. Тихонова. С. 292.
-
3. Велешко И.Е . Перспективы применения хитозана для выделения и концентрирования радионуклидов в растворах // Рыбпром: технологии и оборудование для переработки водных биоресурсов. 2010. № 2. С. 53-57.
-
4. Братская С.Ю., Червонецкий Д.В., Перфильев А.В., Юдаков А.А., Авраменко В.А. Применение хитозана и его производных в питьевом водоснабжении и переработке сточных вод различного состава // Рыбпром: технологии и оборудование для переработки водных биоресурсов. 2010. № 2. С. 58-63.
-
5. Ильина A.В., Варламов В.П . Влияние степени ацетилирования на ферментативный гидролиз хитозана препаратом Целловиридин Г20Х // Прикл. биохимия и микробиология. 2003. Т. 39. № 3. С. 273-277.
-
6. Новиков В.Ю., Долгопятова Н.В., Рипачева Е.Н., Коновалова И.Н., Путинцев Н.М. Деструкция хитина и хитозана при химическом гидролизе // Рыбпром: технологии и оборудование для переработки водных биоресурсов. 2010. № 2. С. 64-68.
-
7. Лопатин С.А . Проблемы определения молекулярномассовых характеристик хитозана // Рыбпром: техноло- гии и оборудование для переработки водных биоресур
сов. 2010. № 2. С. 82-85.
-
8. Sang-Hoon Lim, Samuel M. Hudson. Synthesis and antimicrobial activity of a water-soluble chitosan derivative with a fiber-reactive group // Carbohydrate Research. 2004. V. 339. Iss. 2. Р. 313-319.
PREPARATION OF LOW MOLECULAR WEIGHT CHITOSAN AND ITS DERIVATIVES
Список литературы Получение низкомолекулярного хитозана и его производных
- Хитин и хитозан: Получение, свойства и применение/Под ред. К.Г. Скрябина, Г.А. Вихоревой, В.П. Варламова. М.: Наука, 2002. 386 с.
- Хитин и хитозан: Природа, получение и применение/Пер. с исп., под ред. В.П. Варламова, С.В. Немцева, В.Е. Тихонова. С. 292.
- Велешко И.Е. Перспективы применения хитозана для выделения и концентрирования радионуклидов в растворах//Рыбпром: технологии и оборудование для переработки водных биоресурсов. 2010. № 2. С. 53-57.
- Братская С.Ю., Червонецкий Д.В., Перфильев А.В., Юдаков А.А., Авраменко В.А. Применение хитозана и его производных в питьевом водоснабжении и переработке сточных вод различного состава//Рыбпром: технологии и оборудование для переработки водных биоресурсов. 2010. № 2. С. 58-63.
- Ильина A.В., Варламов В.П. Влияние степени ацетилирования на ферментативный гидролиз хитозана препаратом Целловиридин Г20Х//Прикл. биохимия и микробиология. 2003. Т. 39. № 3. С. 273-277.
- Новиков В.Ю., Долгопятова Н.В., Рипачева Е.Н., Коновалова И.Н., Путинцев Н.М. Деструкция хитина и хитозана при химическом гидролизе//Рыбпром: технологии и оборудование для переработки водных биоресурсов. 2010. № 2. С. 64-68.
- Лопатин С.А. Проблемы определения молекулярно-массовых характеристик хитозана//Рыбпром: технологии и оборудование для переработки водных биоресурсов. 2010. № 2. С. 82-85.
- Sang-Hoon Lim, Samuel M. Hudson. Synthesis and antimicrobial activity of a water-soluble chitosan derivative with a fiber-reactive group//Carbohydrate Research. 2004. V. 339. Iss. 2. Р. 313-319.


