Получение осадков и пленок диоксида циркония из уротропиновой системы
Автор: Туленин С.С., Шварц С.К., Андреева А.А., Изотова О.М., Бочарова Е.Д., Игошкина Н.Ю.
Журнал: Журнал Сибирского федерального университета. Серия: Техника и технологии @technologies-sfu
Рубрика: Исследования. Проектирование. Опыт эксплуатации
Статья в выпуске: 2 т.19, 2026 года.
Бесплатный доступ
В статье представлены результаты исследования золь-гель синтеза пленок и осадков диоксида циркония (ZrO2) из уротропиновой системы. Основное внимание уделено оптимизации условий осаждения, включая подбор осадителей (уротропин и мочевина), контролю pH среды, а также изучению кинетики гелеобразования. Результаты работы имеют практическое значение для разработки технологий получения тонкопленочных материалов на основе ZrO2, применяемых в катализе, электронике и защитных покрытиях.
Диоксид циркония, золь-гель метод, тонкие пленки
Короткий адрес: https://sciup.org/146283265
IDR: 146283265 | УДК: 546.831.4
Sintesis Precipitates and Films of Zirconium Dioxide from a Urotripine System
This article presents the results of a study on the sol-gel synthesis of zirconium dioxide (ZrO2) films and precipitates from the urotropine system. The focus is on optimizing the precipitation conditions, including the selection of precipitating agents (urotropine and urea), pH control of the medium, and the investigation of gelation kinetics. The findings are of practical significance for the development of technologies for producing thin-film materials based on ZrO2, which are used in catalysis, electronics, and protective coatings.
Текст научной статьи Получение осадков и пленок диоксида циркония из уротропиновой системы
Цитирование: Туленин С. С. Получение осадков и пленок диоксида циркония из уротропиновой системы / С. С. Туленин, С. К. Шварц, А. А. Андреева, О. М. Изотова, Е. Д. Бочарова, Н. Ю. Игошкина // Журн. Сиб. федер. ун-та. Техника и технологии, 2026, 19(2). С. 202–215. EDN: AUWYKF мы. Подобные недостатки затрудняют промышленное применение рассмотренных методов и увеличивают себестоимость продукции.
В свою очередь, золь-гель метод является низкотемпературным, позволяет контролировать размер и морфологию частиц, а также легко модифицировать состав продукта. Эти преимущества делают золь-гель метод удобным и экономически выгодным решением.
Поэтому целью работы стало исследование возможности осаждения, получение и исследование осадков и пленок диоксида циркония золь-гель методом.
Материалы и методы
При получении осадков и пленок ZrO2 были использованы следующие реактивы: цирконил азотнокислый ZrO(NO3)2·2H2O (ч); мочевина CH4N2O (чда); уротропин (ГМТА) C6H12N4 (ч). Осаждение из растворов с участием соли циркония (при концентрации от 0.05 до 0.1 М) и уротропина (0.12 М) при температуре 298 K. В качестве подложек для золь-гель осаждения были использованы следующие материалы: стекло предметное, монокристаллический кварц, монокристаллический кремний, ситалл марки СТ-50-1. Оценка склонности к гидролизу нитратов циркония была проведена с использованием методик расчета [10, 11, 16].
В качестве методов нанесения слоев были применены методы заливки, центрифугирования, окунания, синтез в объеме и наложением. Отбор проб для нанесения проводился на 11–26 минуте синтеза, в момент появления максимального количества зародышей твердой фазы и минимального значения светопропускания, с последующей термообработкой образцов в печи SNOL 30/1300 при 700, 900, 1300 °C в течение 1 часа.
С целью вычисления времени гелеобразования составов была определена зависимость коэффициента светопропускания Т (%) от времени синтеза на спектрофотометре UNICO 2800 при длине волны 440 нм. Также для осадков диоксида циркония после термообработки был проведен рентгенофазовый анализ (РФА) на дифрактометре Rigaku D/MAX-2200VL в CuKα излучении в диапазоне 2θ от 10 до 90°. Для определения структуры частиц были использованы данные сканирующей электронной микроскопии (СЭМ) JEOL JSM-5900 LV. Для осадков из уротропиновой системы был проведен термогравиметрический анализ (ТГА) на приборе Netzsch STA 449 F3 Jupiter в среде аргона до 1300о, скорость нагрева – 30 °C/мин. Размер частиц в осадках определяли на ультразвуковом анализаторе Analysette 22 MicroTec plus (ФТИ, УрФУ) при мощности излучателя 70 % от максимальной и затемнении луча 17 %.
Результаты и их обсуждение
На первом этапе работы был проведен расчет граничных условий образования гидроксида циркония с учетом констант нестойкости и произведения растворимости всевозможных комплексных соединений, образующихся в исследуемой системе. Согласно [8, 9] в водной среде образуются гидроксосоединения циркония с координационными числами от 1 до 4 (табл. 1).
Долевую концентрацию ионов циркония aZr4+ можно выразить уравнением (1)
aZr4+ —
[Zr(OH)3+] [Zr(OH)|+]2 [Zr(OH)g]3 [Zr(0H)4]4 (1)
kHi
kH2
кнз
kH4
Долевая концентрация лиганда может быть найдена по уравнению (2)
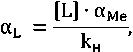
где αL – долевая концентрация лиганда; [L] – концентрация лиганда в растворе; αМе – доля свободных ионов металла; k н – константа нестойкости соединения.
Таблица 1. Константы нестойкости и произведения растворимости соединений циркония
Table 1. Constants of instability and solubility products of zirconium compounds
|
Соединение (комплексный ион) |
ПР |
рПР |
pk н |
k н |
|
Zr(OH) 3 + |
– |
– |
pK н1 = 14.32 |
4.79 ·10–15 |
|
Zr(OH) 2 2+ |
– |
– |
pK н2 = 28.26 |
5.50 ·10–29 |
|
Zr(OH) 3 + |
– |
– |
pK н3 = 41.91 |
1.23 ·10–42 |
|
Zr(OH) 4 |
1.10 · 10–54 |
53.96 |
pK н4 = 55.27 |
5.37 ·10–56 |
Анализ диаграммы распределения концентрационных долей комплексов циркония (рис. 1) показал, что в сильнокислой среде присутствуют все известные комплексы циркония, а также свободные ионы циркония. Гидролиз соли циркония начинается в сильнокислой среде при pH = 0. Доля остальных ионов с увеличением pH стремительно снижается до 0 за исключением доли ионов [Zr(OH)3+], которая увеличивается до 0.28 при pH = 1 и затем резко снижается при pH = 3.
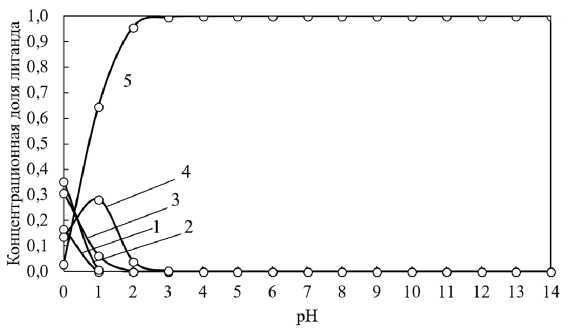
Рис. 1. Распределение концентрационных долей комплексов циркония в зависимости от pH. Линия 1 – долевая концентрация aZr4+ ; 2 – долевая концентрация ионов aZr(OH)3 +; 3 – долевая концентрация ионов aZr(OH^ + ; 4 – долевая концентрация ионов aZr(OH)J; 5 – долевая концентрация сольватированных молекул гидроксида aZr(0H)4
Fig. 1. Distribution of molar fractions of zirconium complexes as a function of pH. Line 1 – molar fraction “Zr44 ; 2 – molar fraction of ions aZr(01I)3+; 3 – molar fraction of ions aZr(OH)^+ ; 4 – molar fraction of ions aZr(OH)J; 5 – molar fraction of solvated hydroxide molecules aZr(OH)4
Общее уравнение для расчета граничных условий осаждения гидроксида металла будет иметь вид (3):
рСн = рПРМе(он)п - npKw + npH - paMen+, (3)
где p – обозначение отрицательного десятичного логарифма; ПРме(ОН) – произведение растворимости гидроксида металла; K w – константа ионизации воды, K w = 10–14; рH – водородный показатель; aMen+ – долевая концентрация незакомплексованного иона металла.
Приведенная на рис. 2 графическая зависимости граничных условий образования гидроксида циркония показывает сложность формирования осадка в данной системе при 298 K при низких концентрациях исходных солей, однако анализ ионных равновесий (рис. 1) говорит об обратном. Так, в предварительных экспериментах на образование коллоидного гидроксида циркония указывает появление эффекта Тиндаля при просвечивании лазером толщи раствора.
Полученное несоответствие может быть объяснено сложностью ионных процессов, происходящих в системах, содержащих ионы редкоземельных металлов, формированием полиядер-ных комплексов для выбранных элементов, которые склонны к гидролизу [10–12, 14]. Результаты расчетов получены без учета повышенной температуры и кристаллизационного фактора, указывающего на наличие пересыщения в системе, что, в свою очередь, на 3–6 порядков понижает начальную концентрацию соли металла [10–14]. С учетом этого линии на графике окажутся выше оси абсцисс, что будет соответствовать реальной возможности осаждения гидроксида циркония при повышенной температуре. Однако, несмотря на приведенный выше расчет области образования гидроксида циркония с учетом термодинамических констант, метод химического осаждения из водных растворов оказался малоэффективен на практике. Сложность контроля процесса и получение обильных осадков гидроксида циркония не позволяет осаждать его тонкие слои на подложечном материале.
Иным методом получения гидроксида циркония может быть золь-гель метод с использованием достаточно простых систем, включающих слабые органические основания (осадители).
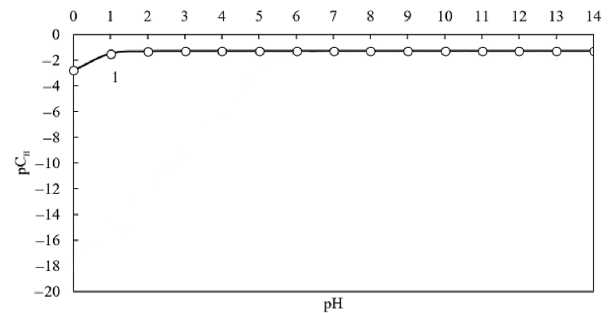
Рис. 2. Граничные условия образования гидроксидов Zr(OH)4 от pH при температуре 298 K. 1 – граничные условия образования Zr(OH)4
Fig. 2. Boundary conditions for the formation of Zr(OH)4 as a function of pH at a temperature of 298 K. 1 – boundary conditions for the formation of Zr(OH)4
Такие осадители должны удовлетворять определенным требованиям: хорошая растворимость в воде, безопасность при использовании, обеспечение полноты осаждения, отсутствие побочных реакций в растворе, приводящих к уменьшению его концентрации. Подходящими осадителями гидроксидов являются такие органические соединения, как мочевина, гексаметилентетрамин (ГМТА), формамид (ФА) и диметилформамид (ДМФА) [12–14]. Данные соединения гидролизуются в водных растворах с образованием продуктов (аммиак, диметиламин и др.), которые, являясь слабыми основаниями, вызывают плавное изменение величины pH раствора и постепенное осаждение катионов металлов в виде гидроокиси. Согласно предварительным экспериментам наиболее интересными осадителями для гидроксида циркония можно считать уротропин и мочевину.
С целью определения склонности к гидролизу солей циркония были выполнены расчеты ионных равновесных в системе Меn+ – Н2О – Х, где в качестве осадителя (Х) использовался уротропин. При расчетах принималось, что на начальной стадии гидролиза солей циркония идет образование моноядерного гидроксокомплекса. Итоговое расчетное уравнение для системы Меn+ – Н 2 О – Х имеет вид:
п [ЯН+]
pCMe =рай//++рС“ - paMe(0H)M)++2pH-p4^j, (4) где α – мольная доля металла и осадителя в растворе.
Используя уравнение (4), можно определить степень влияния применяемого осадителя на процесс образования твердой фазы гидроксида металла и сделать вывод о полноте его осаждения. На рис. 3 линия 1 разделяет плоскость графика на две части – на область ненасыщенного раствора (ниже линии) и область двухфазной системы «раствор-осадок» (выше линии). Так, при комнатной температуре синтеза и низких концентраций соли циркония можно работать в расчетной области рН вплоть до 12 (рис. 3). Для формирования гидроокиси циркония необходимо пересечение линии 3 снизу вверх, что обеспечивается плавным ростом рН.
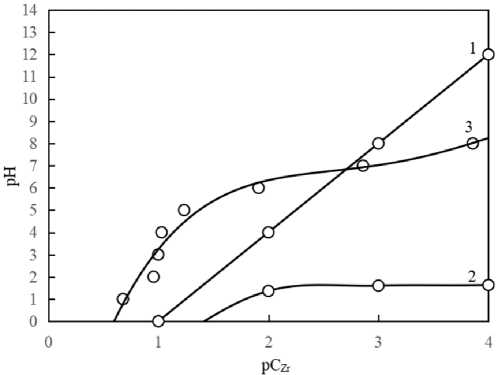
Рис. 3. Зависимость равновесных значений рН в системах Zr4+р-р – Zr(ОН)4ос (1); Zr4+ – ГМТА– Н2О при [ГМТА]=0.1 моль/л (2); равновесие Zr4+ – ZrОН3+– Н2О (3)
Fig. 3. Dependence of the equilibrium pH values in the systems Zr4+r-r – Zr(OH)4oc (1); Zr4+ – GMTA– H2O at [GMTA]=0.1 mol/l (2); equilibrium Zr4+ – ZrOH3+– H2O (3)
Наличие в реакционной смеси уротропина будет способствовать преждевременному образованию гидроксокомплексов циркония в области рН от 0 до 7. Поэтому осаждение предпочтительно вести до рН=7 и при малых концентрациях соли металла в растворе менее 0.1 моль/л.
Стоит отметить, что предварительные эксперименты показали возможность получения гелей гидроксида циркония с уротропином при комнатной температуре лишь при рН исходной смеси около 4 (с мочевиной образование гелей возможно лишь при температурах выше 323 K). При этом выявлено определяющее влияние начального значения рН смеси и плавности его изменения на образование гидроксида циркония и продолжительность процесса гелеобразования. В зависимости от соотношения концентраций соль циркония/уротропин в пределах от 4 до 8.5 были получены плотные гели (рис. 4a). При увеличении концентрации соли циркония наблюдалось обильное образование гидроксида циркония и выпадение его в осадок. При малых концентрациях зародышеобразование либо не наблюдалось, либо было крайне замедленно во времени.
Начало образования первых зародышей гидроксида циркония, а затем и плотной структуры геля определяли по плавному спаданию кривой пропускания (рис. 5). При этом для системы с участием ГМТА (0.12 М) и соли циркония (0.1 М) при температуре 298 K наблюдается плавное увеличение рН от 3.95 до 4.5 за 25 ч (рис. 4b), что способствует равномерному образованию гидроксида циркония во всем объеме раствора.
Получение кристаллического диоксида циркония для дальнейшего практического применения возможно только при высокотемпературной термообработке полученных гелей или осадков. По данным РФА при температурах до 100 °C определяется промежуточная аморфная фаза гидроксида циркония с остатками органического осадителя. Кубическая модификация
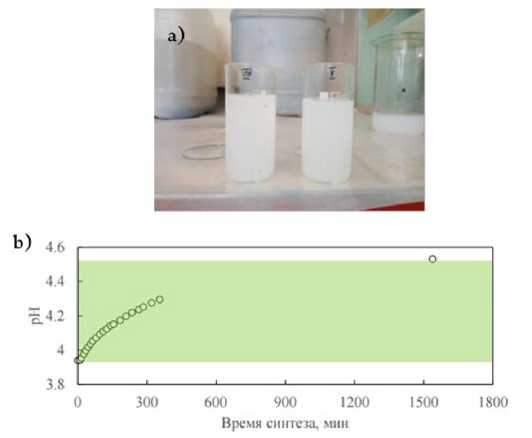
Рис. 4. а – образцы гелей гидроокиси циркония ZrO2, полученных из уротропиновой системы; b – зависимость рН в системе с участием ГМТА от времени синтеза при 298 K
Fig. 4. а – samples of zirconium hydroxide ZrO2 gels obtained from the urotropin system; b – dependence of the pH in the system with GMTA on the synthesis time at 298 K
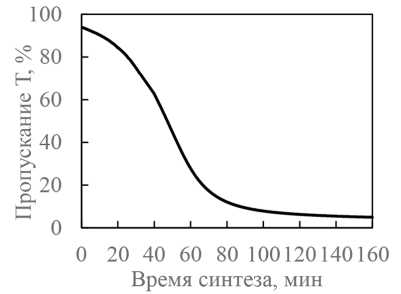
Рис. 5. Результаты спектрофотометрии (пропускание Т) для раствора, содержащего 0.1 М соль циркония – 0.14 М ГМТА. Длина волны 440 нм
Fig. 5. Spectrophotometry results (transmittance T) for a solution containing 0.1 M zirconium salt – 0.14 M
GMTA. Wave length 440 nm
ZrO2 (с постоянными решетки а = b = c = 5.12910 Å) является основной фазой в результате термообработки при 400 °C. С увеличением температуры отжига до 700 °C в образцах обнаружена единственная фаза тетрагонального диоксида циркония с постоянными решетки а = b = 3.6055(17) Å и c = 5.213(4) Å. Основной фазой термообработанного осадка при 900 °C является моноклинный бадделеит (собственно диоксид циркония), на долю которого приходится 84.5 мас.%, остальные 15.5 мас.% приходятся на остаточный тетрагональный диоксид цирконий (рис. 6). С увеличением температуры до 1300 °C в образах присутствует только фаза моноклинного бадделеита.
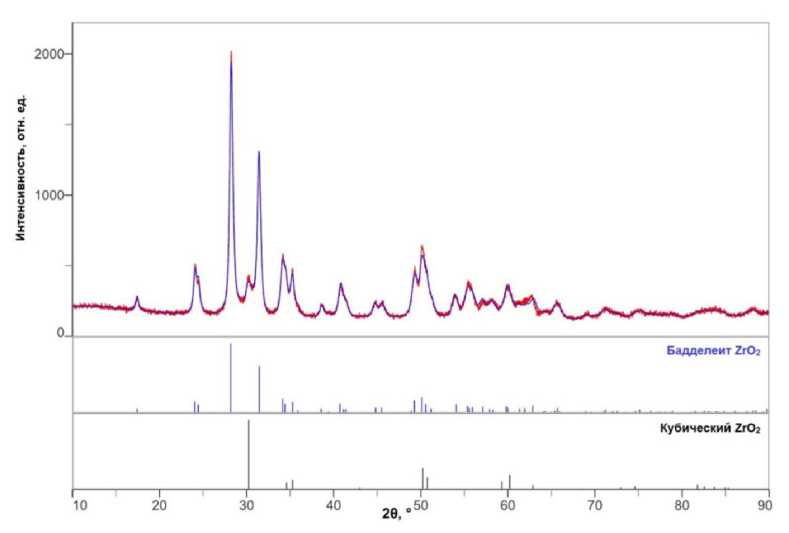
Рис. 6. РФА осадка, полученного из уротропиновой системы, после обработки при 900 °C
Fig. 6. XRD of the precipitate obtained from the urotropine system after treatment at 900 °C
В термообработанном при 900 °C осадке диоксида циркония наблюдается бимодальное распределение частиц с максимумом при 25 и 200 мкм – более 70 % частиц имеют размеры от 0.1 до 125 мкм и менее 30 % частиц имеют размеры от 100 до 500 мкм (рис. 7). Частицы без предварительного перемола достаточно крупные, чтобы их можно было использовать, например, для электрофоретического осаждения – приготовленные из таких порошков суспензии будут иметь низкую седиментационную устойчивость.
По данным СЭМ исходные химически осажденные порошки гидроксида циркония из уротропиновой системы состоят из частиц с размером от 3 до 30 мкм (рис. 8). После термообработки синтезированных образцов при 900 °C в них наблюдается наличие мелких и крупных частиц неправильной формы, основная масса которых приходится на 70–80 мкм, а средний
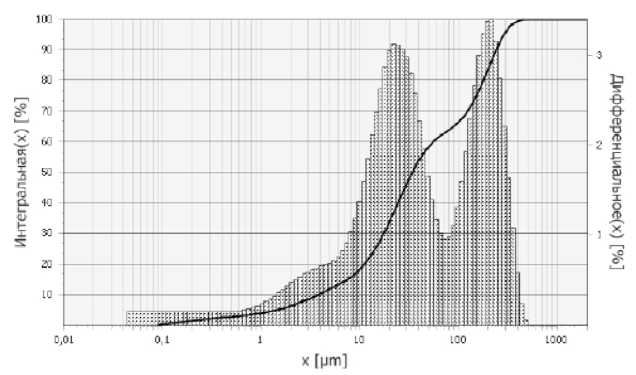
Рис. 7. Интегральное и дифференциальное распределение частиц по размерам в порошке оксида циркония после термообработки при 900 о
Fig. 7. Integral and differential particle size distribution in zirconia powder after thermal treatment at 900 о

Рис. 8. Результат СЭМ порошка диоксида циркония, полученного из уротропиновой системы до и после отжига при 900 и 1300 о
Fig. 8. SEM result of zirconium dioxide powder obtained from the urotropin system before and after annealing at 900 and 1300 о размер частиц составляет от 0.4 до 160 мкм. Морфология частиц практически не претерпевает изменений с увеличением температуры отжига – это, как правило, крупные неровные частицы с достаточно гладкой поверхностью и большим скоплением мелких частиц на них. Стоит отметить, что большинство крупных частиц имеет на поверхности глубокие трещины шириной более 1 мкм, число которых растет с увеличением температуры термообработки, что говорит о наличии внутренних напряжений. Увеличение температуры отжига приводит к растрескиванию частиц и уменьшению их линейного размера с 250 до 160 мкм.
Термогравиметрический анализ показал, что общая потеря массы составила 56.65 % от первоначальной. В интервале от 50 до 200 °C происходит удаление адсорбированной воды, а при 120–150 °C происходит термическое разложение остаточного уротропина. При повышении температуры до 300 °C гидроксидные группы переходят в кислородные мостики между ионами циркония (оксоляция), выделяется вода и образуется аморфный диоксид циркония [15]. Таким образом, более 40 % массы образца теряется до 400 °C (рис. 9).
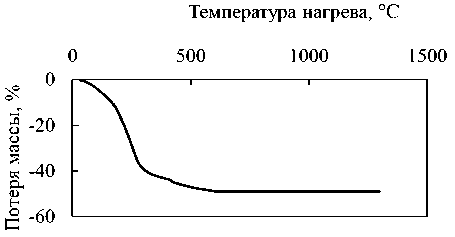
Рис. 9. Результат термогравиметрического анализа осадка, полученного из уротропиновой системы
Fig. 9. The result of thermogravimetric analysis of sediment obtained from the urotropin system
Наличие тепловых эффектов на термограмме указывает на различные фазовые превращения в образце. Так, возгонка уротропина наблюдается при 263 °C с разложением в газовой фазе, а потеря молекул уротропина из комплекса с цирконием будет происходить выше 270 °C, что характеризуется эндоэффектом. Дополнительная потеря молекул уротропина в структуре возможна и в области до 600 °C. При 380–430 °C происходит кристаллизация диоксида циркония в кубической структуре (экзоэффект на ДТА). Увеличение температуры до 630 °C приводит к необратимому переходу кубического диоксида циркония в тетрагональную модификацию, который идентифицирован по РФА при 700 °C. Фазовый переход из тетрагональной в моноклинную фазу и изменение формы частиц наблюдаются на участке от 600 до 1300 °C, что также подтверждается данными РФА.
В работе важным являлся подбор методики нанесения слоев в процессе золь-гель синтеза. На выбор метода сильное влияние оказывает используемый объем раствора, процесс сушки и старения геля. Центрифугирование без пленкообразующих веществ приводит к быстрому испарению водного растворителя в результате вращения и формированию островковых структур по краям подложки. Пленки имеют симметричную картину относительно центра вращения, но крайне неоднородны. Метод накатки является более эффективный ввиду получения равномерных слоев как до, так и после термообработки.
В процессе получения слоев важно контролировать объем нанесения раствора, скорость высыхания геля и качество материала основы. Результаты СЭМ полученных на ситалле после термообработки пленок диоксида циркония из уротропиновой системы показывают важность подбора условий нанесения (рис. 10). Полученные слои при большом увеличении имеют трещины шириной до нескольких сотен нанометров, что связанно с быстрым высыханием и большим содержанием воды (растворителя) в образцах.
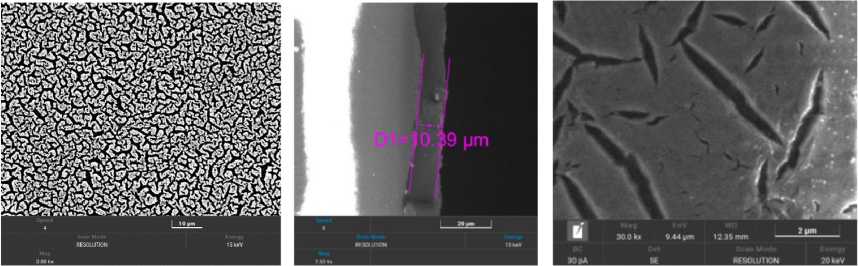
Рис. 10. СЭМ-изображения пленки диоксида циркония, полученного на ситалле, после термообработки при 900 о и торцевого слома подложки с пленкой, полученные методом накатки и центрифугирования
Fig. 10. SEM images of a zirconium dioxide film obtained on a sitall after heat treatment at 900 °C and the end break of the substrate with the film obtained by knurling and centrifugation
Лучший результат показал метод накатки с последующей сушкой слоя и термообработкой. Однако ввиду того, что гели были получены на водной основе, пленка крайне неоднородна после термообработки. Слои имеют мозаичную структуру с большим количеством трещин. Толщина таких пленок составила 10.39 мкм.
Выводы
Расчеты граничных условий образования и ионных равновесий для свободных и закомплексованных форм циркония показали, что для данной системы характерно сложное ионное взаимодействие, также существенное влияние на процесс осаждения оказывает гидролиз соли циркония, который начинается в кислой среде при pH = 0. По результатам расчетов было установлено, что оптимальное начальное значение процесса осаждения гидроксида циркония возможно при pH = 3, а для процесса формирования геля и пленок на подложечном материале необходим плавный рост pH.
В результате проведенных исследований методом золь-гель были получены осадки и пленки гидроксида циркония из уротропиновой системы. В термообработанных образцах средний размер частиц составляет от 0.4 до 160 мкм, в синтезированных осадках размер частиц варьируется от 3 до 30 мкм. Основной фазой после термообработки при 900 °C по данным РФА является моноклинный ZrO2, на долю которой приходится 84.5 мас.%, остальные 15.5 мас.% приходятся на тетрагональный ZrO2. По данным РФА были идентифицированы фазовые переходы при температуре 630 °C (необратимый переход части кубического диоксида циркония – 212 – в тетрагональную), и на участке от 600 до 1300 °C фазовый переход тетрагональной в моноклинную фазы, происходящий с изменением формы частиц.
Среди методов нанесения слоев из водных растворов наилучший результат был продемонстрирован методом накатки с последующей сушкой и термообработкой. Полученные пленки имеют мозаичную структуру с большим количеством пустот, толщина пленок составила 10.39 мкм.
Полученные результаты имеют практическое значение для разработки технологий получения тонкопленочных материалов на основе ZrO2, которые могут быть применены в катализе, электронике и защитных покрытиях.


