Получение стеклоуглеродных микросфер для электрохимического анализа
Автор: Матвеев К.В., Бежин В.К., Гейнц Н.С., Жеребцов Д.А.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Физическая химия
Статья в выпуске: 3 т.16, 2024 года.
Бесплатный доступ
В статье рассмотрена новая методика получения стеклоуглеродных микросфер в растворах, содержащих фурфуриловый спирт, этиленгликоль, изооктилфенолдекаэтиленгликоль (ОП-10) и серную кислоту, приведена морфология микросфер, а также результаты их электрохимического тестирования в растворе 0,1 M KCl, 0,005 M K3[Fe(CN)6], 0,005 M K4[Fe(CN)6. С помощью бесконтактного термометра была установлена зависимость между температурой раствора в процессе синтеза (выделяющейся в ходе теплотой реакции поликонденсации) и объемом добавляемой кислоты. Полученные в растворе полимерные микросферы отмывались, сушились и прокаливались при температуре 900 °С. Полученные материалы исследовались методами сканирующей электронной микроскопии, рентгенофлуоресцентного элементного анализа. Элементный анализ показал, что материалы содержат около 98 % углерода, а также менее 2 % калия, меди, кислорода, серы и железа. Сканирующая электронная микроскопия показала, что микросферы имеют правильную сферическую форму, развитую поверхность и диаметр от 0,5 до 10 мкм. На основании данных о характерных размерах микросфер, определенных методом динамического рассеяния света, были построены зависимости их размеров от соотношения реагентов при синтезе. На основе микросфер готовили пасту для электрода с массовым соотношением микросферы : вакуумное масло = 80 : 10. Данную смесь перемешивали до однородной пасты и набивали в трубчатый электрод диаметром 3 мм. Методом циклической вольтамперометрии определены значения пикового тока и пикового потенциала электрода с чистыми микросферами, а для лучшего образца - еще и с добавлением гексаферрита бария как электрохимического катализатора. Из девятнадцати исследованных растворов для синтеза наиболее перспективным является раствор, содержащий 100 мл этиленгликоля, 5 мл фурфурилового спирта, 5 мл ОП-10, 50 мл серной кислоты.
Стеклоуглерод, микросферы, электрохимия
Короткий адрес: https://sciup.org/147244647
IDR: 147244647 | УДК: 542.06, | DOI: 10.14529/chem240310
Preparation of glassy carbon microspheres for use in electrochemical analysis
The article considers a new method for producing glassy carbon microspheres in solutions containing furfuryl alcohol, ethylene glycol, iso-octylphenol decaethylene glycol (OP-10) and sulfuric acid. The morphology of the microspheres is presented, as well as the results of their electrochemical testing in a solution of 0.1 M KCl, 0.005 M K3[Fe(CN)6], 0.005 M K4[Fe(CN)6]. Using a non-contact thermometer, the dependence of the solution temperature during synthesis (the heat released during the polycondensation reaction) on the volume of added acid was established. The polymer microspheres obtained in the solution were washed, dried, and calcined at 900 °C. The obtained materials were investigated using scanning electron microscopy and X-ray fluorescence elemental analysis. The elemental analysis showed that the materials contained about 98 % carbon, as well as less than 2 % potassium, copper, oxygen, sulfur, and iron. Scanning electron microscopy revealed that the microspheres had a regular spherical shape, well-developed surface and a diameter ranging from 0.5 to 10 microns. On the basis of the data summarizing the characteristic sizes of the microspheres determined by dynamic light scattering, the dependences of their sizes on the ratio of reagents during synthesis were constructed. The microspheres were used for preparation of the paste for an electrode with a mass ratio of microspheres : vacuum oil = 80 : 10. This mixture was stirred into a homogeneous paste and stuffed into a tubular electrode with the 3 mm diameter. The peak current and peak potential values of the electrode with pure microspheres were determined using cyclic voltammetry, with addition of barium hexaferrite as an electrochemical catalyst for the best sample. Among the nineteen solutions studied during synthesis, the most promising is the solution containing 100 mL of ethylene glycol, 5 mL of furfuryl alcohol, 5 mL of OP-10, and 50 m> of sulfuric acid.
Текст научной статьи Получение стеклоуглеродных микросфер для электрохимического анализа
В связи с возрастанием антропогенной нагрузки на окружающую среду с каждым годом происходит накопление и концентрирование загрязняющих веществ в среде обитания живых организмов. Существует множество методов обнаружения вредных веществ в воде, однако электрохимический анализ имеет ряд преимуществ: низкая стоимость, высокая скорость анализа, чувствительность и компактность оборудования. Открытие углеродных нанотрубок (УНТ) и нановолокон привело к их использованию в таких областях, как электрохимия, адсорбция, катализ, хранение водорода и электроника [1]. Среди нанообъектов выделяются наносферы разного состава, методика их получения описана из таких прекурсоров, как глюкоза и фурфуриловый спирт [2,3], 3-аминофенол с формальдегидом [4], 3-аминофенол с гексаметилентетрамином [5] и другие [6], также была описана методика допирования углеродных наносфер никелем [7]. Углеродные наносферы представляют особый интерес, так как они имеют важное применение в составе пастовых электродов [8]. Известно применение модифицированных углеродных наносфер для определения широкого спектра органических веществ: глюкозы [9, 10], допамина [11, 12], различных антибиотиков, в том числе тобрамицина [13] и триметоприма [14], таких лекарственных веществ, как ацетаминофен [15, 16] и прогестерон [17], а также красителя родамина Б [18] и мальтола [19]. Из неорганических веществ, определяемых с использованием углеродных наносфер, можно выделить перекись водорода [20]. Помимо датчиков, наносферы также находят применение в иони-сторах [21]. В данной работе было исследовано влияние параметров синтеза на размер углеродных наносфер, получаемых с использованием фурфурилового спирта, так как этот спирт является дешёвым однокомпонентным прекурсором для реактопласта, способного превращаться при прокаливании в стеклоуглерод. В качестве материала, которым допируются наносферы, был использован гексаферрит бария, на основе которого были созданы датчики для определения таких соединений, как ацетаминофен [22] и озон [23].
Экспериментальная часть
Для синтеза эмульсии (и далее – суспензии) полимера на основе фурфурилового спирта был избран раствор на основе воды или этиленгликоля. Роль катализатора поликонденсации играла соляная или серная кислота, а в качестве неионогенного поверхностно активного вещества выступал изооктилфенолдекаэтиленгликоль (ОП-10). Все реактивы были квалификации «хч». Реакцию поликонденсации проводили в полипропиленовой посуде емкостью 500 мл при переменном количестве компонентов (табл. 1, 2).
Таблица 1
Составы растворов для синтеза образцов (серия 1)
|
Растворитель [мл] |
Объем ФС, мл |
Количество ОП-10, г |
Объем кислоты, мл |
Выход микросфер, % |
|
Вода 150 |
5 |
0,1 |
100 HCl |
1,2 |
|
Вода 150 |
5 |
0,1 |
50 HCl + 10 H 2 SO 4 |
1,5 |
|
Вода 150 |
5 |
1 |
50 HCl |
1,6 |
|
Вода 150 |
5 |
1 |
100 HCl |
1,7 |
|
Этиленгликоль 100 |
20 |
2,5 |
50 HCl |
3,4 |
|
Этиленгликоль 100 |
5 |
5 |
50 HCl |
4,5 |
|
Этиленгликоль 100 |
5 |
5 |
50 H 2 SO 4 |
15,1 |
|
Этиленгликоль 100 |
5 |
20 |
100 HCl |
2,6 |
|
Этиленгликоль 100 |
20 |
5 |
50 HCl |
6,3 |
|
Этиленгликоль 100 |
10 |
5 |
50 HCl + 10 H 2 SO 4 |
3,4 |
|
Этиленгликоль 100 |
10 |
2,5 |
50HCl |
4,7 |
К навеске поверхностно активного вещества добавлялся растворитель (150 мл воды или 100 мл этиленгликоля), затем приливался фурфуриловый спирт. После этого смесь перемешивалась без нагревания и затем небольшими порциями вливалась кислота в течение 10–60 минут. Цвет при этом переходил от бледно-желтого до черно-коричневого (рис. 1). С помощью бесконтактного термометра определяли температуру раствора каждые 2–3 минуты. Через сутки часть образцов коагулировала в крупные капли, часть образовала донный слой полимера, другая осталась в виде эмульсии полимера. В случае низкого содержания кислоты в исходной смеси ряд растворов оставался мало измененным в течение часа, поэтому в них была добавлена дополнительная порция кислоты.

Рис. 1. Цвет продукта через сутки после синтеза
Затем полученная суспензия полимера выдерживалась при 80 °С в течение 2–7 суток, после чего трижды промывалась водой и центрифугировалась в течение 5 мин при 8000 оборотов в минуту. После этого образец переносился в стеклянную склянку, высушивался и прокаливался при 900 °С в защитной атмосфере. Полученный стеклоуглеродный материал исследовали методом сканирующей электронной микроскопии (Jeol JSM-7001F) и рентгенофлуоресцентного анализа с помощью рентгеновского энергодисперсионного спектрометра Oxford INCA X-max 80.
Поскольку опыты с водой в качестве растворителя, а также с соляной кислотой в качестве катализатора дали в большинстве своем слой полимера вместо эмульсии, было принято решение скорректировать состав и поставить синтез ещё 8 образцов (табл. 2). Серная кислота имеет то преимущество, что не требует улавливания коррозионноактивных паров при выдержке при 80 °С. Далее название образцов было сформировано по следующей схеме: буквы В или ЭГ относятся к типу растворителя – вода или этиленгликоль, следующее за буквами число – к объему растворителя, затем объем фурфурилового спирта, объем ОП-10 и объем кислоты. Например, 100ЭГ-3ФС-3ОП-30H 2 SO 4 или в случае растворов на основе этиленгликоля (серия 2) – еще короче: 100ЭГ-3-3-30. Можно отметить, что выход микросфер максимален в двух сериях при составе ЭГ100-5-5-50 и ЭГ100-8-3-30.
Таблица 2
Составы растворов для синтеза образцов (серия 2)
|
Растворитель [мл] |
Объем ФС, мл |
Количество ОП-10, г |
Объем серной кислоты, мл |
Выход микросфер, % |
|
Этиленгликоль 100 |
3 |
3 |
30 |
2,3 |
|
Этиленгликоль 100 |
3 |
8 |
30 |
4,7 |
|
Этиленгликоль 100 |
8 |
3 |
30 |
7 |
|
Этиленгликоль 100 |
8 |
8 |
30 |
2,1 |
|
Этиленгликоль 100 |
3 |
3 |
80 |
0 |
|
Этиленгликоль 100 |
3 |
8 |
80 |
0 |
|
Этиленгликоль 100 |
8 |
3 |
80 |
0 |
|
Этиленгликоль 100 |
8 |
8 |
80 |
0,1 |
Для серии 2 было проведено измерение размера частиц суспензии полимера методом динамического рассеяния света с помощью Photocor Compact-Z, ООО «Фотокор».
Качество пастовых электродов, в том числе значения пикового анодного и катодного тока и потенциала, определяли методом циклической вольтамперометрии (ЦВА) в растворе красной и желтой кровяных солей, так как на них протекает простой одноэлектродный переход Fe2+/3+, на котором удобно тестировать электродный материал [24, 25].
Для электрохимического исследования использовался потенциостат-гальваностат Р-150Х. Электрохимическая ячейка подключалась по трёхэлектродной схеме. При этом противоэлектро-дом являлся стеклоуглеродный стакан, а электродом сравнения – хлорид-серебряный электрод, параметры съёмки: от –0,4 до +0,8 В (относительно ХСЭ), скорость развертки – 50 мВ/с, количество циклов – 3. Вольтамперограммы снимались в водном растворе с 0,1 M KCl, 0,005 M K 3 [Fe(CN) 6 ] и 0,005 M K 4 [Fe(CN) 6 ].
Обсуждение результатов
Для двух серий синтеза были построены зависимости температуры от объема серной кислоты, добавляемой порциями по 3 мл (рис. 2, 3). Обе они имеют схожий экстремальный вид, свидетельствующий о том, что через 20–25 минут достигается значительная полнота реакции, так что новые порции кислоты не вызывают дальнейшего роста температуры. Впрочем, следовало бы учесть еще и теплоту гидратации (сольватации) кислоты. Из двух графиков следует, что, как и должно следовать из констант скорости и из закона действующих масс, увеличение концентраций ФС и кислоты приводит к увеличению выделения теплоты и, соответственно, к росту температуры. ОП-10 практически не влияет на скорость реакции.
Результаты сканирующей электронной микроскопии прокаленных продуктов показали, что частицы имеют развитую поверхность и форму правильных сфер диаметром от 0,5 до 10 мкм (рис. 4). Состав образцов близок к ожидаемому для чистого стеклоуглерода (табл. 3). Примеси металлов имеют случайное происхождение. Важно, что кислород и сера достаточно полно удаляются.
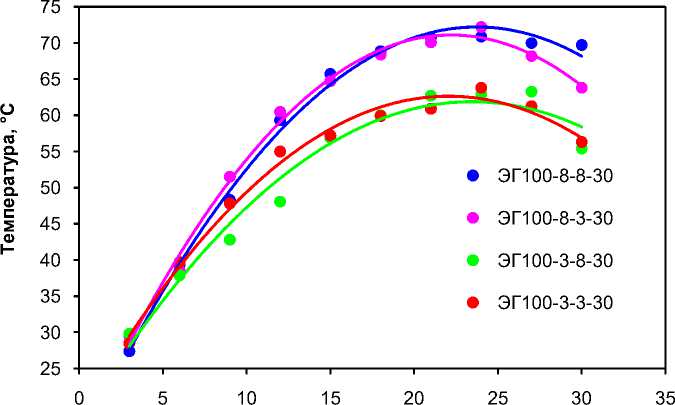
Объем H2SO4, мл
Рис. 2. Зависимость температуры от объема добавляемой серной кислоты (серия 1)
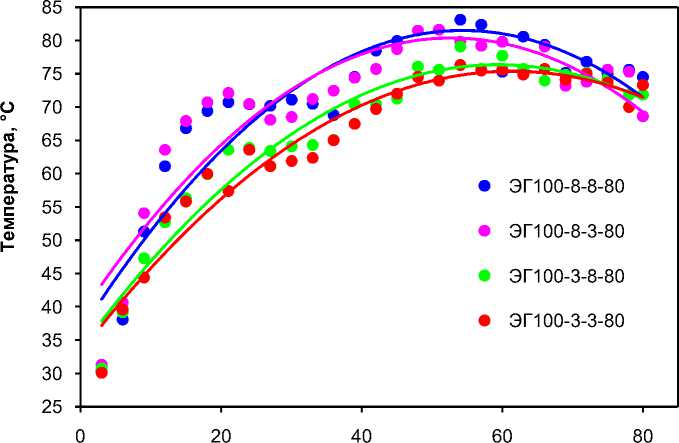
Объем H2SO4, мл
Рис. 3. Зависимость температуры от объема добавляемой серной кислоты (серия 2)

а)
б)
в)
Рис. 4. Морфология образца ЭГ100-5-5-50 по данным электронной микроскопии: при увеличении х5000 (а), х10000 (б) и х50000 (в)
Таблица 3
|
Название образца |
C |
O |
S |
Cl |
K |
Fe |
Cu |
Сумма |
|
В150-5ФС-0,1ОП-50HCl-10H 2 SO 4 |
98,83 |
0,30 |
0,34 |
0,03 |
0,34 |
0,05 |
0,11 |
100,00 |
|
В150-5ФС-0,1ОП-100HCl |
99,13 |
0,71 |
0,01 |
0,01 |
0,07 |
0,02 |
0,06 |
100,00 |
|
В150-5ФС-1OП-50HCl |
99,59 |
0,21 |
0,01 |
0,03 |
0,11 |
0,00 |
0,04 |
100,00 |
|
В150-5ФС-1OП-100HCl |
98,47 |
0,36 |
0,06 |
0,01 |
0,27 |
0,02 |
0,81 |
100,00 |
|
ЭГ100-20ФС-5OП-50HCl-100C |
99,64 |
0,27 |
0,01 |
0,00 |
0,05 |
0,00 |
0,02 |
100,00 |
|
ЭГ100-20ФС-2,5OП-50HCl-100C |
99,45 |
0,44 |
0,00 |
0,00 |
0,07 |
0,00 |
0,03 |
100,00 |
|
ЭГ100-5ФС-5OП-50HCl |
97,06 |
2,24 |
0,02 |
0,48 |
0,15 |
0,00 |
0,04 |
100,00 |
|
ЭГ100-5ФС-20OП-100HCl |
98,47 |
1,21 |
0,03 |
0,11 |
0,13 |
0,02 |
0,04 |
100,00 |
|
ЭГ100-5ФС-5OП-50H2SO4 |
99,95 |
0,00 |
0,00 |
0,00 |
0,03 |
0,01 |
0,01 |
100,00 |
|
ЭГ100-5ФС-20OП-50HCl |
99,70 |
0,09 |
0,01 |
0,02 |
0,11 |
0,00 |
0,07 |
100,00 |
|
ЭГ100-10ФС-5ОП-50HCL+10H 2 SO 4 |
96,24 |
1,73 |
0,03 |
0,24 |
0,69 |
0,47 |
0,60 |
100,00 |
|
ЭГ100-10ФС-2,5OП-50HCl |
98,44 |
1,47 |
0,00 |
0,01 |
0,04 |
0,01 |
0,04 |
100,00 |
Данные элементного анализа образцов, масс. %
По данным динамического рассеяния света удалось определить размеры частиц суспензии полимера (табл. 4, рис. 5). При этом в таблице приведены значения размера частиц и содержания для наиболее характерной фракции, а также средний размер частиц. Размер точек на графиках пропорционален размеру частиц. Из измерений можно заключить, что рост содержания ФС в целом приводит к увеличению размера капель эмульсии (и далее частиц суспензии), что следует избегать при получении наиболее мелких микросфер. К данным DLS следует относиться с осторожностью, поскольку, например, для образца ЭГ100-3-8-30 электронная микроскопия его не подтверждает. Хорошее совпадение размеров по DLS и электронной микроскопии следует отнести к более надежным данным. В других случаях следует предполагать, что завышенные значения размеров по DLS вызваны слипанием частиц в агломераты.
Определение дзета-потенциала частиц суспензии полимера позволяет определить интервал рН, при котором эта суспензия наименее устойчива, что удобно использовать для ее центрифугирования и очистки. При рН=1 дзета-потенциал частиц полимера составил около +50 мВ, а при рН=12 – около –30 мВ, что позволяет заключить, что изоэлектрическая точка суспензии находится около рН=4.
Таблица 4
Размер частиц суспензии по данным DLS и СЭМ
|
Название образца |
Размер частиц фракции, нм |
Содержание фракции, масс. % |
Средний размер, нм |
Средний размер по данным СЭМ, нм |
|
ЭГ100-3ФС-3ОП-30H 2 O |
573 |
50 |
496 |
500–600 |
|
419 |
50 |
|||
|
ЭГ100-3ФС-8ОП-30H 2 O |
9,13 |
100 |
9,13 |
500–1000 |
|
ЭГ100-8ФС-8ОП-80H 2 O |
5410 |
35 |
1902 |
10000 |
|
13,86 |
65 |
|||
|
ЭГ100-8ФС-8ОП-30H 2 O |
1854 |
89 |
1700 |
900–1000 |
|
462 |
11 |
|||
|
ЭГ100-8ФС-3ОП-30H2O |
5600 |
35 |
3107 |
600–900 |
|
1765 |
65 |
|||
|
ЭГ100-3ФС-3ОП-80 H 2 O |
2736 |
11 |
351 |
10000 |
|
56,9 |
89 |
|||
|
ЭГ100-3ФС-8ОП-80 H 2 O |
5600 |
29 |
2214 |
400–600 |
|
2680 |
17 |
|||
|
249 |
54 |
|||
|
ЭГ100-8ФС-3ОП-80 H 2 O |
5650 |
16 |
2935 |
700–900 |
|
2419 |
84 |
|||
|
ЭГ100-5ФС-5ОП-50 H 2 O |
1970 |
58 |
1193 |
600–1000 |
|
561 |
9 |
|||
|
1,13 |
33 |
о
При 30 мл H2SO4


•ЭГ100-3-3-30
•ЭГ100-3-8-30
•ЭГ100-8-8-30
•ЭГ100-8-3-30
•ЭГ100-5-5-50
Объём ФС, мл
а)
о W
ф ю О
При 3 г ОП


•ЭГ100-3-3-30
•ЭГ100-8-3-30
•ЭГ100-5-5-50
•ЭГ100-3-3-80
•ЭГ100-8-3-80
Объём ФС, мл
б)
о W
Ф ю О


При 8 г ОП


•ЭГ100-8-8-80
•ЭГ100-3-8-80
•ЭГ100-5-5-50
•ЭГ100-8-8-30
•ЭГ100-3-8-30
Объём ФС, мл
в)
Рис. 5. Зависимость среднего размера частиц суспензии (серия 2) от объема ФС при переменных: а) 30 мл H 2 SO 4 , б) 3г ОП-10, в) 8 г ОП-10
Методом циклической вольтамперометрии были получены вольтамперограммы пастового электрода на основе ЭГ100-5-5-50 без добавок и с добавлением 5 % BaFe12O19 с соотношением твердый материал : масло = 80 : 10 для обоих электродов (рис. 6). Положения максимумов пиковых токов при введении гексаферрита бария существенно сближаются, что косвенно свидетельствует о высокой пригодности полученных микросфер для изготовления пастовых электродов с вводимыми частицами катализаторов. Удобно сравнить результаты тестирования электрода на основе ЭГ100-5-5-50 без добавок с таким же электродом, приготовленным из молотого графита ВПГ-4, показавшего намного большее перенапряжение (см. рис. 6).
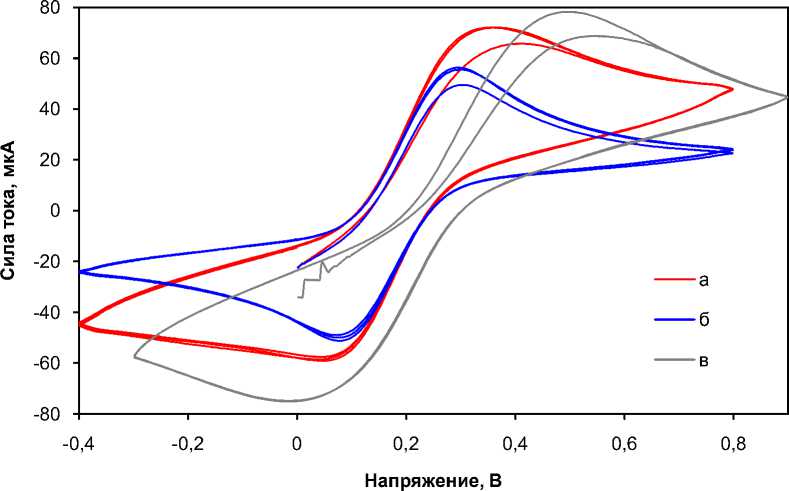
Рис. 6. Кривые ЦВА пастовых электродов (относительно ХСЭ):
на основе ЭГ100-5-5-50 без добавок (а), на основе ЭГ100-5-5-50 с добавлением 5% BaFe 12 O 19 (б), на электроде с молотым графитом (в)
Заключение
В работе был получен и исследован материал, состоящий из стеклоуглеродных микросфер. Выявлено, что рост содержания фурфурилового спирта приводит к росту размера частиц эмульсии. ОП-10 повышает устойчивость против слияния капель. Из всех изученных материалов по малому размеру и высокому выходу наиболее перспективным получился образец из раствора с содержанием 100 мл этиленгликоля, 5 мл фурфурилового спирта, 5 мл ОП-10, 50 мл серной кислоты. Электрохимическое тестирование показало пригодность микросфер для применения в пастовых электродах. Тем не менее, сравнение с литературными данными для аминофенольных смол дает основание полагать, что их следует рассматривать как объект для более пристального исследования, дающий без использования органических растворителей и без высокой концентрации кислот более мелкие сферы углерода с более высоким выходом.
Список литературы Получение стеклоуглеродных микросфер для электрохимического анализа
- Antonio N.-M., Rub R.A.N.-M. // Journal of Materials Chemistry. 2010. V. 21, No. 6. P. 1664. DOI: 10.1039/C0JM01350A
- Zhang P., Qiao Z. A., Dai S. // Chemical Communications. 2015. V. 51, No. 45. P. 9246. DOI: 10.1039/C5CC01759A
- Díez N., Sevilla M., Fuertes A.B. // Materials Today Nano. 2021. V. 16. P. 100147. DOI: 10.1016/j.mtnano.2021.100147
- Yang T., Liu J., Zhou R., Chen Z., Xu H. // Materials Chemistry A. 2014 V. 2. P. 18139 DOI: 10.1039/C4TA04301D
- Yu Q., Guan D., Zhuang Z., Li J. // ChemPlusChem. 2017. V. 82. P. 1. DOI: 10.1002/cplu.201700182
- Cho I.W., Son Seung Uk, Yang MinHo et al. // Journal of Electroanalytical Chemistry. 2020. V. 876. P. 114739. DOI: 10.1016/j.jelechem.2020.114739
- Wei N., Li X., Yin H. et al. // Journal of Materials Science. 2023. V. 58, No. 12. P. 5244. DOI: 10.1007/s10853-023-08347-0
- Fan L., Xin Y., Xu Y. et al. // Microchemical Journal. 2021. V. 170. P. 106770. DOI: 10.1016/j.microc.2021.106770
- Peer M., Qajar A., Rajagopalan et al. // Carbon. 2013. V. 51. P. 85. DOI: 10.1016/j.carbon.2012.08.015
- Yao J., Wang H., Liu J. et al. // Carbon. 2005. V. 43, No. 8. P. 1709. DOI: 10.1016/j.carbon.2005.02.014
- Guaraldo T.T., Goulart L.A., Moraes F.C. et al. // Applied Surface Science. 2019. V. 470. P. 555. DOI: 10.1016/j.apsusc.2018.09.226
- Zhang D., Qian J., Yi Y. et al. // Journal of Electroanalytical Chemistry. 2019. V. 847. P. 113229. DOI: 10.1016/j.jelechem.2019.113229
- Jayaraman S., Rajarathinam T., Chang S. C. // Chemosensors. 2023. V. 11, No. 4. P. 254. DOI: 10.3390/chemosensors11040254
- Yi Y., Sun H., Zhu G. et al. // Analytical Methods. 2015. V. 7, No. 12. P. 4965. DOI: 10.1039/C5AY00654F
- Zhao X., Zhang L., Chu Z. et al. // Molecules. 2023. V. 28, No. 7. P. 3006. DOI: 10.3390/molecules28073006
- Gan T., Sun J., Yu M. et al. // Food chemistry. 2017. V. 214. P. 82. DOI: 10.1016/j.foodchem.2016.07.054
- Wang M., Hu B., Yang C. et al. // Biosensors and Bioelectronics. 2018. V. 99. P. 176. DOI: 10.1016/j.bios.2017.07.059
- Astruc J., Nagalakshmaiah M., Laroche G. et al. // Carbohydrate polymers. 2017. V. 178. P. 352. DOI: 10.1016/j.carbpol.2017.08.138
- Li C., Li J., Wang Z. et al. // Inorganic Chemistry Frontiers. 2017. V. 4, No. 2. P. 309. DOI: 10.1039/C6QI00502K
- Zubizarreta L., Arenillas A., Pis J. J. // Applied surface science. 2008. V. 254, No. 13. P. 3993. DOI: 10.1016/j.apsusc.2007.12.025
- Liu J., Wang X., Gao J. et al. // Electrochimica Acta. 2016. V. 211. P. 183. DOI: 10.1016/j.electacta.2016.05.217
- Granja-Banguera C.P., Silgado-Cortázar D.G., Morales-Morales J.A. // Molecules. 2022. V. 27, No. 5. P. 1550. DOI: 10.3390/molecules27051550
- Ziegler D., Marchisio A., Montanaro L. et al. // Solid State Ionics. 2018. V. 320. P. 24. DOI: 10.1016/j.ssi.2018.02.028
- Mikysek T., Stočes M., Švancara I. et al. // RSC advances. 2012. V. 2, No. 9. P. 3684. DOI: 10.1039/C2RA20202F
- Švancara I., Vytřas K., Barek J. et al. // Critical Reviews in Analytical Chemistry. 2001. V. 31, No. 4. P. 311. DOI: 10.1080/20014091076785


