Постчернобыльские раки щитовидной железы в Украине: фоновые и радиоиндуцированные случаи
Автор: Лихтарев И.А., Ковган Л.Н., Вавилов С.Е., Тронько Н.Д., Богданова Т.И., Олейник В.А., Чорнобров А.И., Гулак Л.О.
Статья в выпуске: S3, 2005 года.
Бесплатный доступ
Короткий адрес: https://sciup.org/170169891
IDR: 170169891
Текст статьи Постчернобыльские раки щитовидной железы в Украине: фоновые и радиоиндуцированные случаи
В результате аварийного радиоактивного выброса на Чернобыльской АЭС, 26 апреля -10 мая 1986 г., практически на всей территории Украины произошли выпадения йода-131, явившиеся источником внутреннего (в результате ингаляционного и перорального поступления) облучения щитовидной железы (ЩЖ) практически всего населения страны. Уровни выпадений йода-131 по территории Украины были крайне неравномерными [1, 2] и среднеобластные их значения варьировали от 0,01 МБк/м2 (Ивано-Франковская область) до 2,02 МБк/м2 (Киевская область). При этом наиболее интенсивно загрязненными (0,16-2,02 МБк/м2) оказались северные области: Киевская, Житомирская, Ровенская, Черниговская, Черкасская, Волынская (карта-схема на рис. 1).
Рис. 1. Территориальное распределение кумулятивных выпадений йода-131 в результате чернобыльского аварийного выброса по территории Украины [1,2].
Как и ожидалось, одним из последствий массового облучения ЩЖ йодом-131 стал регистрируемый с 1990 г. рост заболеваемости раком ЩЖ детей и подростков Украины [3-9]. Наиболее поздние оценки рисков возникновения раков ЩЖ в результате чернобыльского облучения применительно к населению северной части трех наиболее пострадавших областей (Киевская, Житомирская и Черниговская) были представлены в работе [10]. Именно у этих лиц в 1986 г. было проведено более чем 150 тыс. измерений активности радиойода в ЩЖ. При этом оценки рисков [10] основывались на среднегрупповых (для каждого пола и возраста) дозах облучения ЩЖ, выполненных для населенных пунктов (НП) северных районов трех указанных областей. Для каждого НП определялись 38 среднегрупповых доз (для 19 возрастов в интервале 0-18 лет отдельно для мальчиков и девочек) [11]. Оценки абсолютного и относительного рисков, полученные в в результате исследований [10], составили 2 на 104 чел.^лет^Гр и 13 Гр-1, соответственно.
Однако в цитированной работе [10] остался открытым вопрос о временной динамике и региональной структуре фоновой заболеваемости раком ЩЖ в Украине. Важность этой проблемы связана, в частности, с тем, что после 1990 г. рост заболеваемости раком ЩЖ стал регистрироваться не только на территориях, которые подверглись интенсивным радиойодным выпадениям и население которых получило значительные дозы внутреннего облучения ЩЖ, но и в тех областях Украины, где уровни выпадений йода-131 (и, соответственно, дозы облучения ЩЖ) были крайне низкими (например, в Херсонской, Одесской, Николаевской и др., рис. 2).
Рис. 2. Средняя заболеваемость раком ЩЖ в периоды 1981-1989 гг. и 1990-2000 гг. в разных областях Украины (возрастная группа 0-18 лет).
Помимо радиационного фактора, на наблюдаемый рост выявляемой заболеваемости раком ЩЖ в этот период могли оказывать влияние ряд процессов нерадиационной природы, в частности:
-
- Во-первых, с 1990 г. началась повсеместная и интенсивная технологическая модернизация диагностики различных видов тиреопатологии и, в частности, узелковой: произошел постепенный переход от пальпаторной к ультразвуковой (УЗ) технике индикации узелковых образований.
-
- Во-вторых, серьезным фактором роста выявляемости тиреоонкопатологий стала возникшая после чернобыльской аварии повсеместная обеспокоенность населения (и в том числе врачей ), а также введение ряда административных мер 1, ставших причиной массовых эндокринологических обследований детей и подростков практически на всей территории Украины.
Учитывая вышеизложенное, далее эффект роста наблюдаемой заболеваемости ЩЖ, связанный с вышеперечисленными факторами, будем определять как «скрининг-технологический эффект» роста заболеваемости (или кратко, скрининг-технологический эффект ). При этом важной особенностью скрининг-технологического эффекта является то, что влияние его на уровень наблюдаемой заболеваемости не зависит от природы возникновения рака ЩЖ (фоновой или радиоиндуцированной).
Одной из главных задач настоящего сообщения является:
-
- выделение регионов (областей) Украины, где наблюдаемый рост заболеваемости раком ЩЖ обусловлен, в основном, скрининг-технологическим эффектом, и
-
- определение половозрастной структуры и временной динамики фоновой заболеваемости раком ЩЖ в различных регионах Украины.
Уровни фоновой заболеваемости раком ЩЖ для отдельных областей в различных половозрастных группах после 1990 г. восстанавливались с учетом заболеваемости, которая регистрировалась до 1990 г. (минимальный латентный период для возникновения радиоиндуцирован-ных раков ЩЖ), «поправленной» на независимо полученную оценку величины область-специфичного скрининг-технологического эффекта.
Модель область-специфичного скрининг-технологического эффекта базировалась на результатах анализа временной динамики среднеобластной заболеваемости узловым зобом среди детей и взрослых в период 1990-2001 гг., поскольку технологически диагностика узлов и раков ЩЖ имеют общую начальную стадию.
С целью проверки адекватности разработанных моделей скрининг-технологического эффекта и фоновой заболеваемости, выполнена оценка радиационных рисков возникновения раков ЩЖ для населения северных, наиболее пострадавших регионов Украины, охваченных прямыми измерениями. Применялась, так называемая, модель «внешнего фона», в которой пара- метризованные модели скрининг-технологического эффекта и фоновой заболеваемости использовались для моделирования ожидаемой заболеваемости. Полученные таким образом оценки радиационных рисков довольно удовлетворительно совпали с аналогичными оценками, представленными в работе [10], где для оценки радиационных рисков использовалась модель «внутреннего фона».
Материалы и методы
Соотношение заболеваемости узловым зобом и фоновой заболеваемости раком ЩЖ
Обнаружение узла (пальпаторно или с помощью УЗ) всегда является самым первым шагом в диагностике любого новообразования в ЩЖ (рис. 3). Поэтому, принимая во внимание то, что рак ЩЖ является довольно редким (в сравнении с узловым зобом) событием, статистически намного более эффективно осуществить оценку величины и временной динами ки скрининг-технологического эффекта для разных областей Украины, основываясь на анализе временной динамики среднеобластной заболеваемости узловым зобом за период 1990-2001 гг.
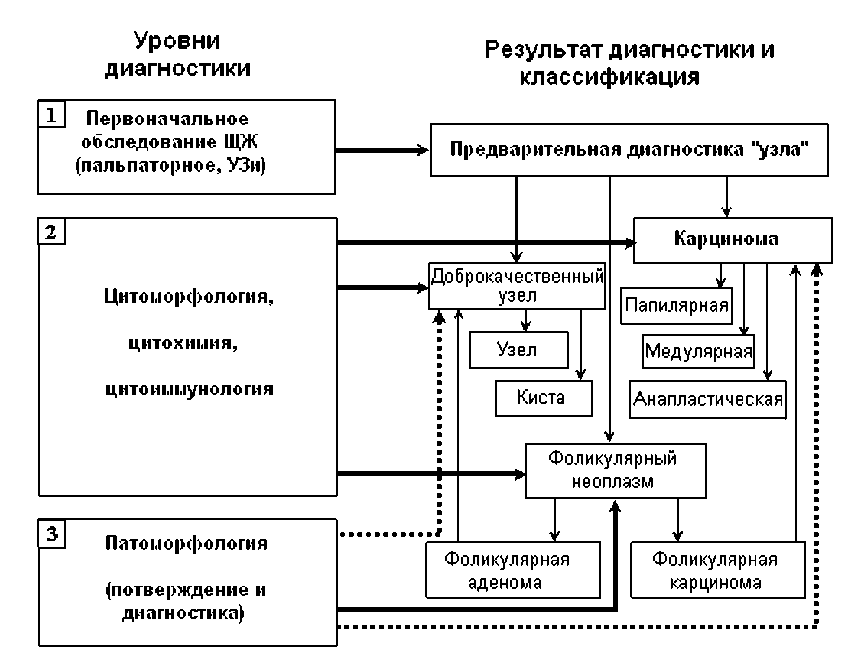
Рис. 3. Основные этапы диагностики и классификации узловой тиреопатологии.
К несомненным преимуществам подобного подхода следует отнести следующее:
-
- обнаружение первичного узла является существенно более простой и надежной процедурой по сравнению с конечной диагностикой тиреоидного рака;
-
- соотношение между окончательно подтвержденными диагнозами: «рак щитовидной железы» с одной стороны и всеми первично регистрируемыми узловыми патологиями - с другой, как правило, довольно устойчиво;
-
- статистическая мощность анализа случаев узловой патологии по сравнению с подобным анализом такого (довольно редкого) заболевания, как рак ЩЖ, существенно выше;
-
- влияние облучения на частоту узлового зоба значительно меньше по сравнению с радиоиндукцией тиреоидных раков [13-23].
На рис. 4 визуализирована корреляция заболеваемости раком ЩЖ (в возрастной группе 0-18 лет) с заболеваемостью узловым зобом в различных областях Украины за 1990-2001 гг. При сравнении значений заболеваемости раком ЩЖ и узловым зобом, зарегистрированных в каждой области Украины в одном и том же временном интервале, коэффициент корреляции между этими тиреопатологиями оказался равным 0,81 .
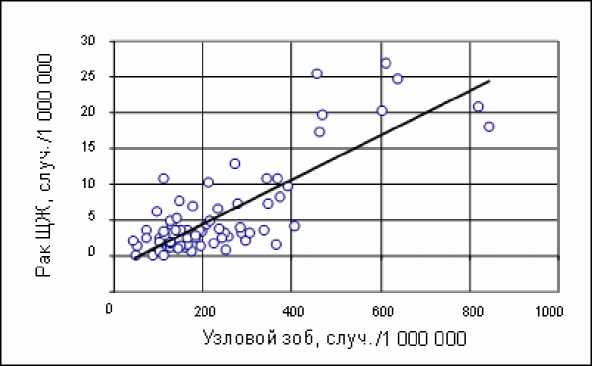
Рис. 4. Корреляция среднеобластной заболеваемости раком ЩЖ (в возрастной группе 0-18 лет) с заболеваемостью узловым зобом за период 1990-2001 гг. Кружки соответствуют заболеваемости в отдельной области в одном и том же трехлетнем интервале времени.
«Радиационный» и «нерадиационный» периоды наблюдения
В настоящем сообщении рассматривается 21-летний интервал времени: с 1981 по 2001 годы, для которого имеются данные о случаях рака ЩЖ. Этот интервал разделен на два периода:
-
- «нерадиационный» период , в пределах которого заболеваемость раком ЩЖ может рассматриваться как заведомо не связанная с облучением (он включает шесть доаварийных лет (1981-1985 гг.) и четыре года после аварии, связанных с минимальным латентным периодом возникновения рака ЩЖ (1986-1989 гг.);
-
- «радиационной» период (1990-2001 гг.), в течение которого наблюдаемые случаи раков ЩЖ могут иметь как фоновую, так и радиационную природу.
Временная динамика УЗ-обследований и наблюдаемая заболеваемость узловым зобом
Первые УЗ-аппараты стали поступать в медицинскую сеть Украины (в первую очередь в «околочернобыльские» районы и области) примерно в 1990-м году. Но уже спустя несколько лет (таблица 1) насыщенность этими приборами во многих областях достигла столь высокого уровня, что практически все узелки в ЩЖ детектировались с помощью этого современного метода (хотя темп перехода на УЗ-технологию в разных областях был неодинаков).
Из данных таблицы 1 следует, что если в 1990 г. только в пяти областях и в Киеве интенсивность УЗ-обследований в год превышала 100 на 100 000 жителей, то уже через 5 лет этот показатель возрос более, чем в 6 раз (521), достигнув к 2002 г. значения 1392. При этом наибольший темп внедрения УЗ-технологии наблюдался как раз в «околочернобыльских» областях: Волынской, Сумской, Ровенской, Житомирской и Киевской. Тогда как, например, в Тернопольской, Закарпатской, Харьковской, Ивано-Франковской областях этот процесс развивался заметно медленнее.
Таблица 1
Временная динамика УЗ-обследований (на 100 000 жителей) в 1990, 1995 и 2002 гг. в различных областях Украины
|
Область |
УЗ-обследования на 100 000 населения |
||
|
Годы |
|||
|
1990 |
1995 |
2002 |
|
|
Житомирская |
121 |
1815 |
2647 |
|
Киевская |
108 |
667 |
2021 |
|
Черниговская |
93 |
1066 |
2171 |
|
Киев |
507 |
1614 |
3697 |
|
Винницкая |
5 |
417 |
1328 |
|
Волынская |
19 |
1007 |
4309 |
|
Днепропетровская |
5 |
457 |
1328 |
|
Донецкая |
298 |
674 |
1289 |
|
Закарпатская |
- |
91 |
598 |
|
Запорожская |
20 |
394 |
1252 |
|
Ивано-Франковская |
- |
264 |
997 |
|
Кировоградская |
- |
445 |
1186 |
|
Луганская |
323 |
506 |
1105 |
|
Львовская |
186 |
806 |
1301 |
|
Николаевская |
- |
327 |
1004 |
|
Одесская |
39 |
449 |
1186 |
|
Полтавская |
- |
726 |
1429 |
|
Ровенская |
9 |
1141 |
2518 |
|
Сумская |
65 |
715 |
2834 |
|
Тернопольская |
9 |
240 |
478 |
|
Харьковская |
55 |
390 |
776 |
|
Херсонская |
25 |
884 |
1572 |
|
Хмельницкая |
7 |
350 |
775 |
|
Черкасская |
- |
304 |
1288 |
|
Черновицкая |
- |
1051 |
1669 |
Одним из следствий увеличения массовости применения УЗ-технологии (и вообще скрининга) среди населения стало то, что, начиная с 1990 г., практически во всех 24 областях Украины и в Киеве стала расти выявляемость заболеваемости всеми узелковыми формами тиреопа-тологии (таблица 2). При этом, если при пальпаторной индикации обычно выявлялись узлы раз- мером не менее 10-15 мм, то УЗ-технология позволяла визуализировать в 2-3 раза более мелкие новообразования. По действующим в настоящее время в Украине правилам, дальнейшей проверке подлежат узелки не менее 5 мм.
Обязательная регистрация и требование единой формы отчетности обо всех видах тире-опатологии было введено на Украине с 1990-1991 гг. Ежегодные отчетные формы эндокринологической службы, поступающие в Министерство здравоохранения Украины и Институт эндокринологии и обмена веществ после 1990 г., содержали данные о среднеобластной заболеваемости и распространенности различных видов тиреопатологий (включая первично диагностируемые узлы) как для детей (0-14 лет), так и для и взрослых.
Важным является то, что в системе отчетности первично регистрируемые узлы ЩЖ (до завершения окончательной дифференциальной диагностики) определяются как «узловой зоб». Поэтому рост узелковой тиреопатологии (независимо от наличия радиационного фактора) вре-зультате модернизации технологии диагностики проявился, прежде всего, в виде роста (от 2-х до 10 и более раз) среднеобластной заболеваемости узловым зобом в период с 1991 до 2001 гг.
Таким образом, узловой зоб является весьма перспективным «индикатором» скрининг-технологического эффекта. Более того, использование именно этого индикатора открывает возможность построения количественной модели скрининг-технологического эффекта.
Таблица 2
Среднеобластная заболеваемость узловым зобом у детей в разных областях Украины в 1990-2001 гг.
|
Область |
Годы |
||
|
1990-1993 |
1994-1997 |
1998-2001 |
|
|
Случаев на 100 000 |
|||
|
Житомирская |
24 |
47 |
61 |
|
Киевская |
47 |
64 |
82 |
|
Черниговская |
27 |
46 |
61 |
|
Киев |
21 |
37 |
84 |
|
Винницкая |
17 |
26 |
39 |
|
Волынская |
29 |
59 |
77 |
|
Днепропетровская |
13 |
25 |
41 |
|
Донецкая |
11 |
15 |
30 |
|
Закарпатская |
9 |
17 |
25 |
|
Запорожская |
5 |
10 |
14 |
|
Ивано-Франковская |
10 |
16 |
24 |
|
Кировоградская |
10 |
13 |
21 |
|
Луганская |
10 |
12 |
23 |
|
Львовская |
13 |
20 |
24 |
|
Николаевская |
4 |
7 |
17 |
|
Одесская |
8 |
13 |
18 |
|
Полтавская |
11 |
14 |
31 |
|
Ровенская |
11 |
18 |
34 |
|
Сумская |
14 |
38 |
64 |
|
Тернопольская |
5 |
11 |
20 |
|
Харьковская |
13 |
17 |
19 |
|
Херсонская |
18 |
35 |
46 |
|
Хмельницкая |
15 |
29 |
37 |
|
Черкасская |
15 |
28 |
35 |
|
Черновицкая |
13 |
15 |
22 |
Функция скрининг-технологического эффекта Zj (τ) и скрининг-технологический фактор RSTFj
Принимая, что в отсутствии радиоиндуцирования, темп нарастания наблюдаемой заболеваемости узловым зобом пропорционален темпу нарастания наблюдаемой заболеваемости раком ЩЖ, параметры функции скрининг-технологического эффекта Zj(T) определялись по дан ным о временной динамике наблюдаемой заболеваемости узловым зобом.
Если временную динамику наблюдаемой заболеваемости узловым зобом в j -й области представить в виде функции Z,( t ) = Z 0 j • exp( - b j • т) , где ZQ j - заболеваемость узловым зобом, зарегистрированная в 1990 г., то функция относительного роста заболеваемости узловым зобом ( функция скрининг-технологического эффекта ) Z j (T) за период наблюдения 1990-2001 гг. будет иметь вид: ~
Zj(T) = Zj(T)/Zo,j • exp(bj • т), (1)
где параметр bj характеризует область-специфичную скорость нарастания заболеваемости. При этом символы функций Zj(T), Zj(T) и их параметры Z0,j и bj будем сопровождать нижними символами ch или ad в зависимости от того, принадлежит ли член рассматриваемой субпопу ляции в текущем году тсоответственно к детям или ко взрослым.
Интегральное, усредненное за 12 лет наблюдений, значение функции Z j (T) назовем относительным скрининг-технологическим фактором j -й области RSTF j и определим как:
RSTF, = ,, , J Z,(T)dT.
12 ⋅ Z j,0 0
Далее принимается, что функция Z j (T) и значения RSTF j , полученные при анализе ежегодной заболеваемости узловым зобом для детей и взрослых, применимы также и для описания скрининг-технологического эффекта выявляемости рака ЩЖ у детей и у взрослых.
Возрастная динамика фоновой заболеваемости
Зона фоновой заболеваемости. При установлении межвозрастных отличий заболеваемости раком ЩЖ использованы данные о случаях рака ЩЖ, зарегистрированные в различных возрастных группах в течение «нерадиационного» (1981-1989 гг.) и «радиационного» (1990-2001 гг.) периодов наблюдения. При этом информация о случаях в течение «радиационного» периода анализировалась лишь применительно к областям, отнесенным к, так называемой, «зоне фоновой заболеваемости», определяемой как такие территории, на которых радиа- ционно-индуцированная компонента заболеваемости раком ЩЖ в этот период была статистически незначимой на фоне общей наблюдаемой заболеваемости.
Таким образом, к « зоне фоновой заболеваемости» были отнесены области, в которых различие между наблюдаемыми и ожидаемыми случаями рака ЩЖ в радиационный период отвечало условию t st < 1,96, где t st - критерий Стьюдента. При этом число ожидаемых случаев в j -й области в радиационной период вычислялось как произведение величины RSTF j , определенное для этой области, на среднегодовое число случаев рака, зарегистрированное в течение нерадиационного периода в этой же области (с учетом длительности радиационного периода).
Возрастная функция относительного изменения заболеваемости раком ЩЖ, λzsone(аges). Для параметризации этой функции анализировались случаи, зарегистрирован ные в «зоне фоновой заболеваемости» в различных половозрастных группах 0-49 лет в течение периода 1990-2001 гг. Для снижения возможного влияния скрининг-технологического эффекта случаи объединялись для областей, которые характеризовались близкими значениями средней заболеваемости раком ЩЖ в период 1990-2001 гг. в возрастной группе 0-18 лет.
Таким образом, средняя за период наблюдения (1990-2001 гг.) заболеваемость раком ЩЖ Az°ne(ages) в возрастной группе ages во всей зоне фоновой заболеваемости (либо в группе областей зоны) можно представить в виде:
λ zsone (аges) = A z(io)ne,s,0
⋅ exp(As(i)
⋅ ages)
' i = 1, для ages < agesb i = 2, для ages > agesb
где A ^' - характеризует относительный темп нарастания фоновой заболеваемости с возрастом ages в s -й половой группе; A ZO)ne,s,0 — характеризует среднюю для зоны фоновой заболеваемости (или ее части) заболеваемость раком ЩЖ новорожденных s -го пола (возраст 0 лет); ages b - характеризует пограничный возраст между младшими ( i =1) и старшими ( i =2) возрастными группами, по достижении которого темп нарастания заболеваемости раком ЩЖ с возрастом может изменяться.
Временная динамика фоновой заболеваемости раком ЩЖ в субпопуляции возраста age на момент аварии
С использованием функции скрининг-технологического эффекта Zj(t) (уравнение 1) и параметров возрастной зависимости заболеваемости раком ЩЖ изменение со временем (t=0 в 1986 г.) фоновой заболеваемости раком ЩЖ Aexpae f(t,T) членов субпопуляции s-го пола и s,age, j возраста age в 1986 г. в той или иной j-й области (как в зоне фоновой, так и в зоне радиоинду-цированной заболеваемости раком ЩЖ) можно представить в виде:
^ sXPge,j (t,T) = A s,0,j . f s,age (t) - Z j ( t ) , (4)
где A s,0,j - область-специфичный параметр, соответствующий фоновой заболеваемости в j -й области у новорожденных ( age =0 в 1986 г.); A s,0,j определялся по соотношению 81 - 89
Aλ 0 - 18,s,j 81 - 89
s,0,j = Azone,s,0 • Jzone , где Л-i8,s,j — усредненная по всему нерадиационному периоду λ0-18,s заболеваемость раком ЩЖ детей и подростков в возрасте 0-18 лет в j-й области, Л0ОПе s - заболеваемость детей и подростков в возрасте 0-18 лет в областях зоны фоновой заболеваемости, оцененная с использованием уравнения; fs age (t) = exp(Asi • ages) - безразмерная функция, описывающая возрастание со временем фоновой заболеваемости, обусловленное «старением», при этом ages = age+t; Zj(T) - функция скрининг-технологического эффекта для j-й области (т=0 в 1990 г.).
Модель скрининга узловой тиреопатологии и рака ЩЖ
Суммарную (обобщенную) величину скрининг-технологического эффекта в той или иной j -й области можно представить как результат взаимодействия трех различных факторов:
-
1) Технологический , связанный с переходом от пальпаторной к УЗ-диагностике узловой тиреопатологии, во всех областях Украины . Этот фактор стал причиной повсеместного роста выявляемости различных видов узловой тиреопатологии у населения всех возрастов, а для взрослых - это практически единственная причина наблюдавшегося роста. Параметр функции скрининг-технологического эффекта, описывающей эту компоненту, будем обозначать b jad .
-
2) Встревоженность населения всех областей Украины относительно возможного негативного влияния последствий чернобыльского аварийного облучения на здоровье детей, и, как следствие, рост самообращаемости в эндокринологические кабинеты. Это сформировало скрининг-компоненту роста выявляемости тиреопатологии у детей дополнительную к той, которая была обусловлена внедрением УЗ-технологии. Параметр функции скрининг-технологического эффекта, описывающей эту компоненту, будем обозначать b jch .
-
3) Административный фактор, обусловленный Приказом Министерства здравоохранения Украины (1990 г.) [12], согласно которому в пяти наиболее пострадавших северных областях Украины все дети и подростки дважды в год обязаны были проходить эндокринологическую диспансеризацию . Это обусловило еще более высокий скрининг-эффект среди детского и подросткового населения в указанных областях в сравнении со взрослыми и детьми других областей, на которые действие Приказа Минздрава не распространялось. Параметр функции скрининг-технологического эффекта, описывающей эту компоненту, будем обозначать b jch .
Реально действие административного фактора локализовалось в основном в пределах северных районов (районы « повышенного внимания » ) Киевской, Житомирской и Черниговской областей , которые характеризовались наибольшими уровнями загрязнения и были охвачены прямыми измерениями в 1986 г. Это, в свою очередь, обусловило то, что помимо неизбежных межобластных различий в величине и интенсивности скрининг-технологического эффекта, можно ожидать различия величины этого эффекта между районами внутри одной и той же области: Киевской, Житомирской и Черниговской.
Поскольку реально доступными для анализа были лишь среднеобластные значения заболеваемости узловой тиреопатологии, оценка интенсивности скрининг-технологического эффекта Zj(z) в районах «повышенного внимания» оценивалась с учетом уравнений (1) и (2) по соот- ношению:
b .= j,ch
•
T screen
T screen
I
Т = 1
In [exp^ • т) - (1- K* )exp( bch • Kch/ad • т)]
*
iz * l,ch где K = Ъ—
P j,ch
определяет отношение численности детского населения в районах с обычным уровнем скрининга (Pj,ch) к численности детского населения во всей области (Pj,ch); Kch/ad -отношение значений среднеобластных параметров, характеризующих скрининг-технологический эффект у детей (bjch) и у взрослых (bj,ad), усредненное по всем областям, в которых админи- стративная компонента скрининга практически отсутствовала.
Оценки радиологического риска с использованием модели «внешнего фона»
Представленные выше модели фоновой заболеваемости и скрининг-технологического эффекта, при соответствующей их параметризации, дают возможность оценить уровни ожидаемой заболеваемости раком ЩЖ на территориях, которые оказались в сфере интенсивных ради-ойодных выпадений в 1986 г. и, следовательно, население которых получило заметные дозы облучения ЩЖ. Сравнение оцененной таким образом ожидаемой заболеваемости с наблюдаемой, позволяет оценить величину эксцесса радиологических рисков возникновения рака ЩЖ на единицу дозы внутреннего облучения этого органа.
Оценка величины эксцесса абсолютного и относительного риска на единицу дозы в зависимости от пола s и возраста age на момент аварии ( age = 0,1,...,18 лет) выполнялась на основе линейной Пуассоновской регрессии:
^ = ^ SXPge + « s ' D * e z ' age , (6)
^SbSge = ^SXe ‘ d + в * D * ' age), где λobs и λexp – соответственно наблюдаемая и ожидаемая заболеваемость раком ЩЖ s ,age s ,age членов облученной субпопуляции за период наблюдения; as и вз — оцениваемые параметры модели, соответствующие эксцессу абсолютного (EAR/106 чел.·лет·Гр) и относительного (ERR/Гр) риска на единицу дозы; D - доза облучения ЩЖ йодом-131 (Гр); zs,a и zs,e - модификаторы соответственно параметров as и вз, отражающие влияние на величину риска возраста на момент облучения.
Оценка риска проводилась для радиационного периода 1990-2001 гг.
Весь статистический (включая регрессионный) анализ данных о заболеваемости узловым зобом и раком ЩЖ, и анализ доза-эффект проводились средствами пакета Epicure (модуль AMFIT) [24], а также с помощью специальных программ, созданных в среде MatLab 6.0 [25].
Изучаемая популяция
При моделировании и параметризации функции скрининг-технологического эффекта и половозрастной функции заболеваемости раком ЩЖ, в качестве изучаемой популяции рассматривалось все население 24 областей Украины и Киева. Автономная Республика Крым и Севастополь были исключены из рассмотрения, в связи с высоким и трудно учитываемым уровнем миграции жителей этих территорий.
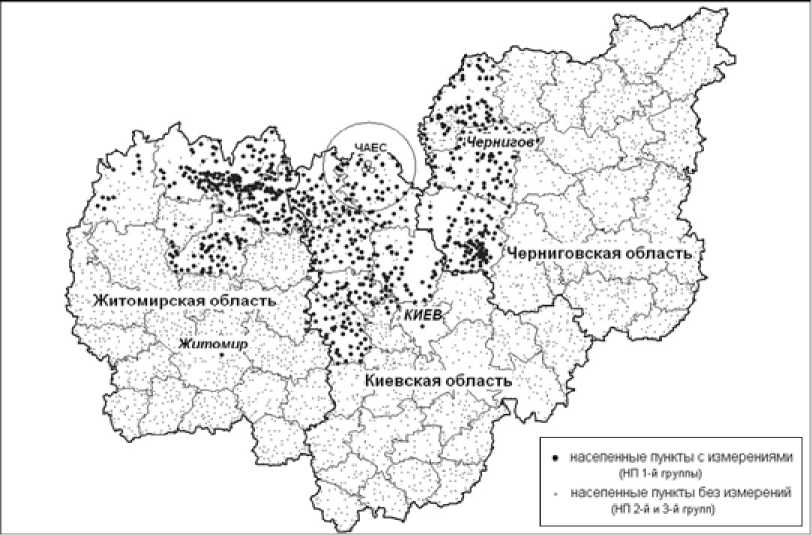
Рис. 5. Локализация районов «повышенного внимания» Киевской, Житомирской и Черниговской областей, где проводились прямые измерения активности ЩЖ у населения в 1986 г.
При оценке радиологических рисков возникновения рака ЩЖ в исследования было вовлечено лишь ~314 тыс. детей и подростков, которые в период радиойодных выпадений проживали в тех северных районах Киевской, Житомирской и Черниговской областей, где в мае-июне
1986 г. были проведены прямые измерения активности радиойода в ЩЖ (рис. 5). Члены этой субпопуляции с одной стороны подверглись сравнительно высокому радиационному воздействию, а с другой – именно для них была осуществлена достаточно надежная реконструкция дозовых оценок [11].
Случаи рака ЩЖ в Украине
После чернобыльской аварии 1986 г. Институтом эндокринологии и обмена веществ АМН Украины был организован централизованный сбор, обработка и хранение информации, касающейся регистрируемых случаев рака ЩЖ в Украине [26]. В рамках этого Института была сформирована и продолжает работать, так называемая, клинико-морфологическая база данных, которая содержит сведения о зарегистрированных случаях:
-
- у детей и подростков в возрасте 0-18 лет за период 1981-1985 гг.;
-
- среди лиц 1968-1986 гг. рождения после 1986 г.;
-
- у лиц, рожденных после 1987 г.
С 1995 г. начал активно функционировать Национальный канцер-регистр Украины, являющийся одним из подразделений Института онкологии АМН Украины. В этом Регистре накапливается и обобщается информация обо всех видах онкозаболеваемости (включая рак ЩЖ) у населения всех половозрастных групп во всех областях Украины [27-29]. Этот регистр тесно взаимодействует с областными специализированными онкологическими диспансерами, откуда по единым унифицированным формам региональные данные направляются в Национальный канцер-регистр.
В настоящем исследовании используется и анализируется информация о случаях рака ЩЖ, содержащаяся как в базе данных Института эндокринологии, так и в Национальном канцер-регистре Украины.
В таблице 3 приведены агрегированные по каждой области Украины данные о численности детей и подростков (0-18 лет) в 1986 г., количестве случаев рака ЩЖ, зарегистрированных в области в «нерадиационный» (до 1990 г.) и «радиационный» (после 1990 г.) периоды в возрастной группе 0-18 лет и в субпопуляции возраста 0-18 лет в 1986 г.
Сведения о количестве случаев рака ЩЖ в возрастной группе 0-18 лет в период 1981-1989 гг. для Житомирской и Закарпатской областей отсутствовали. Поэтому для «нерадиационного» периода применительно к возрастной группе 0-18 лет Житомирской и Закарпатской областей были приняты значения заболеваемости, усредненные по заболеваемости раком ЩЖ в пограничных областях, для которых подобная информация имелась. Кроме того, Киев рассматривался как отдельная административная единица.
Таблица 3
Численность населения и количество раков ЩЖ, зарегистрированные в «нерадиационный» (1981-1989 гг.) и «радиационный» (1990-2001 гг.) периоды в возрастной группе 0-18 лет и в субпопуляции возраста 0-18 лет на момент облучения в разных областях Украины
|
Области |
Численность населения в возрастной группе 0-18 лет в 1986 г. |
Количество выявленных случаев рака ЩЖ |
|||
|
В возрастной группе 0-18 лет |
В субпопуляции возраста 0-18 лет на момент облучения |
||||
|
1981-1989 |
1990-2001 |
1986-1989 |
1990-2001 |
||
|
Житомирская |
418900 |
- |
75 |
- |
124 |
|
Киевская |
494300 |
10 |
132 |
9 |
284 |
|
Черниговская |
333300 |
3 |
81 |
1 |
145 |
|
Киев |
721900 |
13 |
116 |
9 |
300 |
|
Винницкая |
486500 |
9 |
31 |
7 |
104 |
|
Волынская |
314700 |
2 |
10 |
1 |
22 |
|
Днепропетровская |
1029200 |
14 |
44 |
11 |
149 |
|
Донецкая |
1360900 |
12 |
41 |
9 |
159 |
|
Закарпатская |
404400 |
0 |
3 |
1 |
16 |
|
Запорожская |
551400 |
11 |
9 |
11 |
65 |
|
Ивано-Франковская |
416300 |
4 |
11 |
1 |
27 |
|
Кировоградская |
313700 |
3 |
19 |
2 |
45 |
|
Луганская |
740500 |
8 |
14 |
7 |
48 |
|
Львовская |
789500 |
4 |
16 |
7 |
48 |
|
Николаевская |
368200 |
2 |
10 |
1 |
29 |
|
Одесская |
709600 |
3 |
16 |
2 |
71 |
|
Полтавская |
431600 |
5 |
20 |
3 |
52 |
|
Ровенская |
356900 |
2 |
29 |
3 |
69 |
|
Сумская |
357000 |
4 |
21 |
2 |
35 |
|
Тернопольская |
316500 |
2 |
4 |
1 |
5 |
|
Харьковская |
820500 |
13 |
21 |
6 |
104 |
|
Херсонская |
354900 |
5 |
27 |
4 |
93 |
|
Хмельницкая |
396300 |
2 |
16 |
0 |
43 |
|
Черкасская |
384100 |
3 |
33 |
2 |
64 |
|
Черновицкая |
279000 |
4 |
8 |
5 |
27 |
|
Всего |
13150100 |
138 |
807 |
105 |
2128 |
Оценка доз облучения ЩЖ
Трехуровневая система реконструкции доз облучения ЩЖ у всего населения Украины детально описана в [11]. В соответствии с этой системой первый уровень реконструкции включает оценку инструментально-индивидуализированных доз для жителей с прямыми измерениями активности радиойода в ЩЖ в мае-июне 1986 г. Второй уровень охватывает оценки среднегрупповых инструментальных доз для жителей тех НП, где активность радиойода в ЩЖ была измерена хотя бы у части жителей. Эти НП отнесены к так называемым НП 1-й группы. В рамках третьего уровня оцениваются среднегрупповые дозы для детей и подростков различных половозрастных групп тех НП, где измерения активности ЩЖ в 1986 г. не проводились вовсе. Эти НП, в свою очередь, разделяются на НП 2-й группы, у жителей которых измерения, хотя и не проводились, но сами НП находятся в тех районах Киевской, Житомирской и Черниговской областей, в которых хотя бы часть НП была охвачена прямыми измерениями. К НП 3-й группы отнесены НП, которые находятся в тех районах Киевской, Житомирской и Черниговской областей, где измерений не было ни в одном НП. В 3-ю группу НП включены также НП всех других (помимо указанных выше) областей Украины. Локализация НП 1, 2 и 3 групп на территории Киевской, Житомирской и Черниговской областей показана на рис. 5.
Для оценки радиационных рисков рассматривалось население 738 сельских НП 1-й группы и 548 НП 2-й группы северных районов Киевской, Житомирской и Черниговской областей (рис. 5). Численность детей и подростков возраста 1-18 лет, проживающих в этих НП, составило 296 147 человек. Из них 73 216 человек (35% детей и подростков НП 1-й группы) имели прямые измерения в 1986 г. Распределение НП 1-й группы в зависимости от процента детского и подросткового населения, охваченного прямыми измерениями, приведено в таблице 4. С учетом результатов прямых измерений, посуточной динамики выпадений 131I на почву [1,2], а также экологической модели, описывающей миграцию радиойода по звеньям пищевой цепочки [10, 30, 31], для каждого НП оценивалось 38 половозрастных среднегрупповых доз облучения ЩЖ. Учитывались три пути поступления: ингаляционный, «молочный» (с молоком и молокопродуктами) и «овощной» (с листовой зеленью).
Таблица 4 Распределение НП 1-й группы в зависимости от процента жителей возраста 1-18 лет, охваченных прямыми измерениями активности радиойода в ЩЖ в 1986 г.
|
Процент жителей с прямыми измерениями в отдельном НП |
Количество НП 1-й группы |
|
<1% |
6 |
|
1-5% |
20 |
|
5-10% |
29 |
|
10-20% |
68 |
|
20-30% |
82 |
|
30-40% |
100 |
|
40-50% |
102 |
|
50-100% |
331 |
Результаты и обсуждение
Параметры функции скрининг-технологического эффекта для детского и взрослого населения и значения RSTFj для различных областей Украины
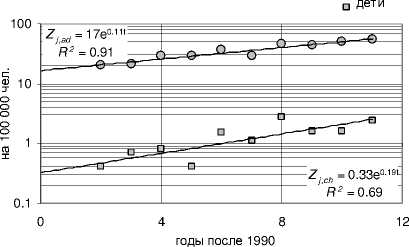
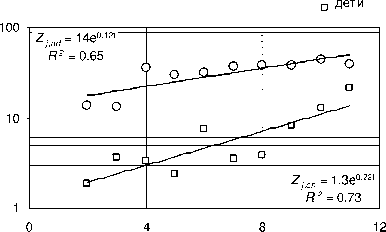
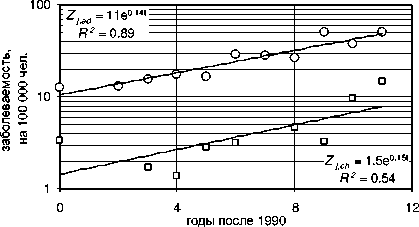
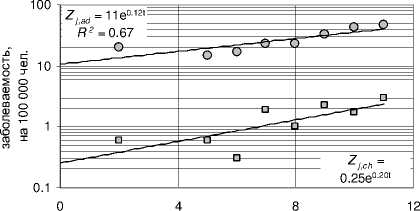
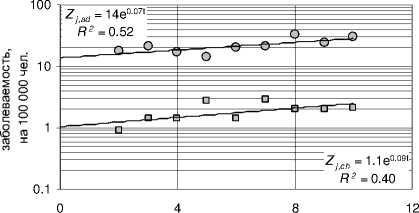
Графики на рис. 6 иллюстрируют примеры роста заболеваемости узловым зобом среди детского и взрослого населения в течение 1990-2001 гг. в ряде областей Украины. Там же приводятся вид и параметры соответствующих аппроксимационных функций скрининг-технологического эффекта для детей ( Z j,ch (T) = exp(b jch • т) ) и взрослых ( z~ j,ad (T) = exp(b j,ad • т) ) . На рис. 7 приведены аналогичные данные для трех северных (наиболее пострадавших) областей Украины: Киевской, Житомирской и Черниговской, а также показана динамика заболеваемости узловым зобом среди детей и взрослых для всей Украины в целом.
взрослые
Днепропетровская область
взрослые
Черкасская область
годы после 1990
Ровенская область взрослые дети
Тернопольская область взрослые дети
Полтавская область взрослые дети
годы после 1990
= 3.90.17t
2 =
Z j,ad

0.1
j,ch
R2 = 0.72
Черновецкая область взрослые дети
годы после 1990
48 годы после 1990
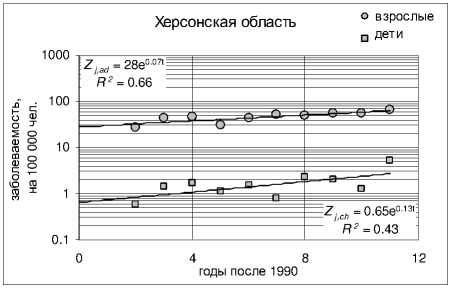
Рис. 6. Примеры изменения со временем среднеобластной заболеваемости узловым зобом в период 1990-2001 гг. (случаев на 100 000 чел.) среди детей и взрослых в ряде областей Украины. Сплошные прямые соответствуют среднеобластным функциям изменения заболеваемости узловым зобом среди взрослых ( Z jad (T) верхняя прямая и уравнение) и среди детей ( Z ,ch (T) нижняя прямая и уравнение).
Одесская область взрослые дети
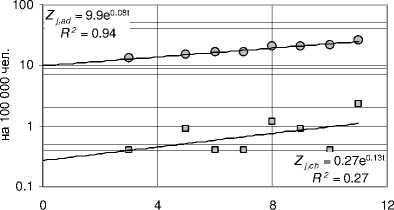
годы после 1990
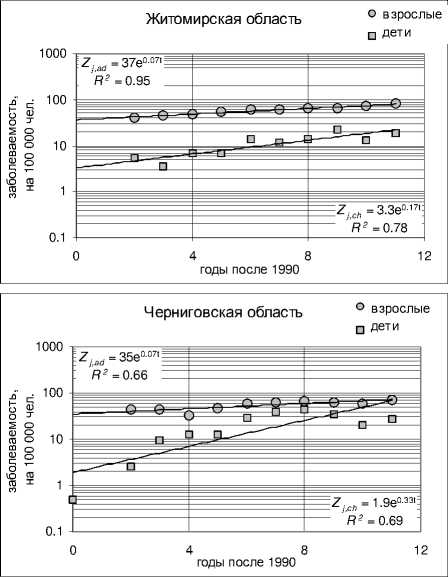
Рис. 7. Изменение со временем среднеобластной заболеваемости узловым зобом в период 1990-2001 гг. (случаев на 100 000 чел.) среди детей и взрослых в трех наиболее пострадавших областях: Житомирской, Киевской и Черниговской, а также для всей Украины в целом. Сплошные прямые соответствуют среднеобластной (или среднеукраинской) функциям изменения заболеваемости узловым зобом среди взрослых ( Z j,ad (τ) верхняя прямая и уравнение) и среди
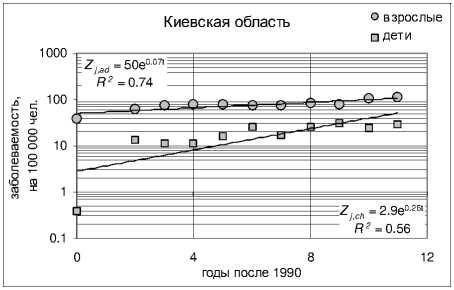
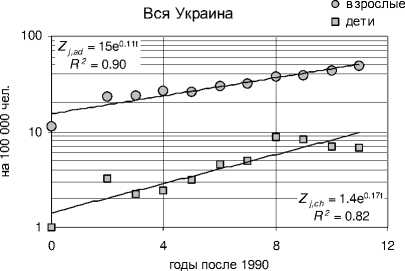
детей ( Z j,ch (τ) нижняя прямая и уравнение).
В таблице 5 приведены численные оценки параметров b j,ch и b j,ad соответственно
~~ функций Zj,ch(τ) и Zj,ad
(τ) для каждой области, а также рассчитанные по величине bj,ch значения область-специфичного скрининг-технологического фактора RSTFj,ch. Там же даны от- ношения
b j,ch b j,ad
Как видно из данных, представленных на рис. 6, 7 и в таблице 5, практически во всех областях имеет место рост заболеваемости узловым зобом в период с 1990 до 2001 гг. как среди детей (bj,ch), так и среди взрослых (bj,ad ). При этом, хотя абсолютный уровень заболеваемости детей почти повсюду ниже, чем взрослых, однако темп роста заболеваемости детей заметно bj,ch выше. Отношение для всех областей (кроме северных – Киевской, Житомирской и Чер-bj,ad ниговской) лежит в довольно узком интервале значений: 1÷1,8, а среднее этого отношения со- ставляет 1,45±0,25. Это свидетельствует о наличии среди детского населения дополнительной технологической компоненты скрининга, связанной с общей встревоженностью населения после аварии. Наибольшее различие между темпами роста заболеваемости узловым зобом среди детей и взрослых наблюдается в трех северных областях – Житомирской, Киевской и bj,ch
Черниговской, для которых отношение составило 2,4; 3,7 и 4,7, соответственно. Это, в bj,ad свою очередь, подтверждает наличие в этих трех областях более высокого уровня скрининга среди детей по сравнению с уровнем детского скрининга в остальных областях Украины. Подобное усиление скрининга в модели скрининг-технологического эффекта связывается с наличием дополнительной административной компоненты.
Таблица 5 Параметры скрининг-технологического эффекта для детей (bj ch), взрослых (bjad) и их bj,ch отношение —'—, оцененные для различных областей Украины (и для всей Украины в bj,ad целом)
|
Область |
Дети |
Взрослые |
b j,ch b j,ad |
95% ДИ |
RSTF j,ch |
||
|
b h j,ch |
95% ДИ |
ь j,ad |
95% ДИ |
||||
|
Житомирская |
0,17 |
0,09; 0,25 |
0,07 |
0,06; 0,08 |
2,43 |
1,71; 2,96 |
3,1 |
|
Киевская |
0,26 |
0,09; 0,44 |
0,07 |
0,04; 0,10 |
3,71 |
2,31; 4,47 |
6,2 |
|
Черниговская |
0,33 |
0,16; 0,49 |
0,07 |
0,03; 0,10 |
4,71 |
5,78; 4,68 |
11,1 |
|
Киев |
0,24 |
0,13; 0,36 |
0,21 |
0,13; 0,29 |
1,14 |
1,02; 1,26 |
5,3 |
|
Винницкая |
0,14 |
0,02; 0,27 |
0,10 |
0,08; 0,12 |
1,40 |
0,18; 2,32 |
2,5 |
|
Волынская |
0,13 |
-0,001; 0,26 |
0,11 |
0,05; 0,18 |
1,18 |
-0,02; 1,50 |
2,3 |
|
Днепропетровская |
0,19 |
0,09; 0,29 |
0,11 |
0,08; 0,14 |
1,73 |
1,03; 2,07 |
3,6 |
|
Донецкая |
0,16 |
-0,03; 0,35 |
0,12 |
0,09; 0,15 |
1,33 |
-0,32; 2,40 |
2,9 |
|
Закарпатская |
0,20 |
-0,02; 0,42 |
0,16 |
0,09; 0,22 |
1,25 |
-0,20; 1,86 |
3,9 |
|
Запорожская |
0,10 |
-0,03; 0,23 |
0,10 |
0,05; 0,15 |
1,00 |
-0,62; 1,55 |
1,9 |
|
Ивано-Франковская |
0,19 |
0,04; 0,35 |
0,13 |
0,08; 0,18 |
1,46 |
0,46; 1,95 |
3,6 |
|
Кировоградская |
0,13 |
-0,07; 0,32 |
0,10 |
0,07; 0,13 |
1,30 |
-1,01; 2,49 |
2,3 |
|
Луганская |
0,13 |
-0,28; 0,54 |
0,08 |
0,04; 0,11 |
1,63 |
-6,54; 4,81 |
2,3 |
|
Львовская |
0,07 |
-0,08; 0,22 |
0,05 |
0,03; 0,08 |
1,40 |
-2,69; 2,87 |
1,5 |
|
Николаевская |
0,22 |
0,04; 0,41 |
0,18 |
0,11; 0,25 |
1,22 |
0,33; 0,66 |
4,5 |
|
Одесская |
0,13 |
-0,08; 0,34 |
0,08 |
0,06; 0,10 |
1,63 |
-1,34; 3,26 |
2,3 |
|
Полтавская |
0,20 |
0,02; 0,38 |
0,12 |
0,04; 0,21 |
1,67 |
0,62; 1,87 |
3,9 |
|
Ровенская |
0,15 |
0,03; 0,28 |
0,14 |
0,10; 0,18 |
1,07 |
0,26; 1,61 |
2,7 |
|
Сумская |
0,25 |
0,06; 0,43 |
0,14 |
0,10; 0,17 |
1,79 |
0,60; 2,51 |
5,8 |
|
Тернопольская |
0,25 |
0,13; 0,37 |
0,17 |
0,02; 0,33 |
1,47 |
1,12; 7,02 |
5,8 |
|
Харьковская |
0,06 |
-0,21; 0,32 |
0,04 |
0,01; 0,07 |
1,50 |
-16,7; 4,75 |
1,4 |
|
Херсонская |
0,13 |
0,01; 0,25 |
0,07 |
0,03; 0,12 |
1,86 |
0,29; 2,16 |
2,3 |
|
Хмельницкая |
0,19 |
0,00; 0,37 |
0,11 |
0,07; 0,16 |
1,73 |
-0,02; 2,37 |
3,6 |
|
Черкасская |
0,22 |
0,11; 0,33 |
0,12 |
0,05; 0,19 |
1,83 |
2,34; 1,75 |
4,5 |
|
Черновицкая |
0,09 |
-0,01; 0,19 |
0,07 |
0,01; 0,13 |
1,29 |
-0,87; 1,36 |
1,8 |
|
Всего по Украине |
0,17 |
0,11; 0,24 |
0,11 |
0,08; 0,14 |
1,55 |
1,39; 1,69 |
|
RSTF j,ch – область-специфический относительный скрининг-технологический фактор.
Как уже указывалось, даже в пределах каждой отдельной области (Житомирской, Киевской, Черниговской) уровень скрининга в различных административных районах мог существенно отличаться. С самого начала аварии наибольшее внимание уделялось районам, где имели место особенно интенсивные радиоактивные выпадения. Население этих районов было охвачено прямыми измерениями активности радиойода в ЩЖ в мае-июне 1986 г., а позже, именно это население стало объектом особо пристальных медицинских (включая эндокринологические) обследований. Полученные оценки b j,ch и b j,ad для Житомирской, Киевской и Черниговской областей (таблица 5) позволяют применить описанную выше модель скрининга узловой тирео-паталогии для определения параметров скрининг-технологического эффекта b * j * ,ch (уравнение 5) в районах «повышенного внимания» (рис. 5). Результаты подобного анализа приведены в таблице 6.
Таблица 6 Параметры, характеризующие интенсивность скрининга у детей и подростков, оцененные для районов Житомирской, Киевской и Черниговской областей с различными уровнями скрининга
|
Область |
Отношение населения |
Параметры, характеризующие интенсивность скрининга |
||
|
P *j,ch P j,ch |
Среднеобластной |
Районы с обычным скринингом |
Районы с интенсивным скринингом |
|
|
Ь к j,ch |
b j „ j ,ch |
b j\ j,ch |
||
|
Киевская |
0,7 |
0,26 |
0,11 |
0,30 |
|
Житомирская |
0,5 |
0,17 |
0,11 |
0,22 |
|
Черниговская |
0,6 |
0,33 |
0,11 |
0,40 |
P^ ch и P j ch — численность населения в возрасте 0-18 лет в районах обычного скрининга ( b j ch ) и во всей области ( b j ch ), соответственно; b j Ch - параметр, относящийся к районам с особо интенсивным скринингом (районы «повышенного внимания»).
При получении оценок параметров, приведенных в таблице 6, принималось, что среднее по 21 области (исключены Житомирская, Киевская и Черниговская области, а также Киев) зна- чение отношения интенсивности скрининга детского и взрослого населения составляет
K ch / ad
_ 1 2С bj,ch21k bjad
_ 1,5.
Значения b j ch и b j* ch , приведенные в таблице 6, использовались далее для моделирования «внешнего фона» у членов изучаемой субпопуляции детей и подростков Житомирской, Киевской и Черниговской областей.
«Зона фоновой заболеваемости»
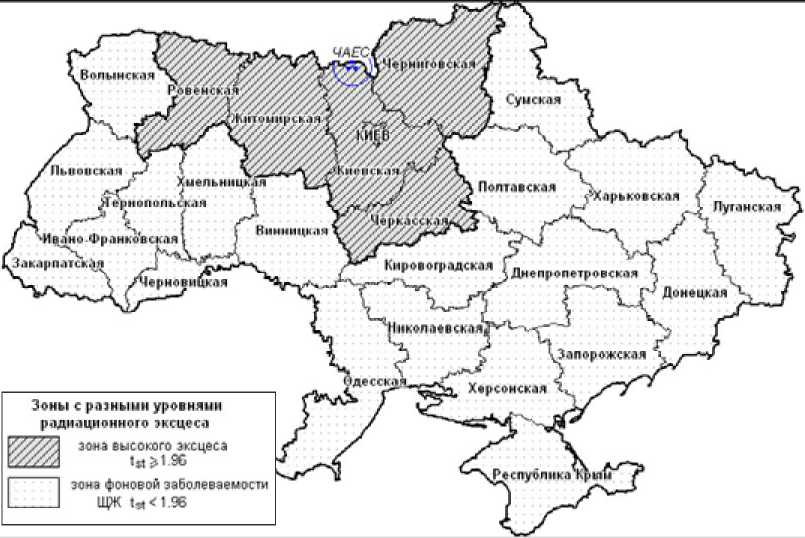
В соответствии с принятым выше определением «зоны фоновой заболеваемости», а также с использованием значений RSTFj,ch (таблица 5) и данных о заболеваемости раком ЩЖ в «нерадиационный» период, были определены области Украины, заболеваемость раком ЩЖ в которых в «радиационный» период (1990-2001 гг.) очень слабо (статистически незначимо) связана с влиянием радиационного фактора. Оказалось, что «зона фоновой заболеваемости» покрывает большую часть территории Украины (19 областей и Киев), на которой проживали ~82% жителей в возрасте 0-18 лет в 1986 г. Как видно из карты-схемы на рис. 8, к этой «зоне фоновой заболеваемости» относится практически вся западная, восточная, центральная и южная часть территории Украины.
ЧАЕС.
Вплынскля
Хмельницкая
Полтавская
1ерновицкая школ аве ска я.
Запорожская
•десп
Херсонская Д
Республика
J *Ивано Франковская
Закарпатская I '
KwpoeoipwKM ^.^.„„ро,^,.,, Г Ч
Г5 Донецкая
.арьковская < „
-_г Луганская
Зоны с ратными уровнями радиационного эксцеса эона высокого аксцеса lM>19G
- зона фоновой заболеваемости __ ЩЖ 1^^196
Рис. 8. Зоны «фоновой» и «радиоиндуцированной» заболеваемости раком ЩЖ в возрастной группе 0-18 лет в «радиационный» период (1990-2001 гг.).
Параметры функции половозрастной зависимости заболеваемости раком ЩЖ λzsone ( аges)
Для параметризации функции λzsone ( аges) (уравнение 3) анализировались случаи рака ЩЖ, зарегистрированные в «радиационный» период в областях «зоны фоновой заболеваемости» в различных возрастных группах отдельно для мальчиков и девочек. В анализ вовлекались данные по 9 областям «зоны фоновой заболеваемости» с близкими значениями средней наблюдаемой заболеваемости раком ЩЖ в возрастной группе 0-18 лет в 1990-2001 гг. (λ09-0-1--80,1s,j ), лежащими в интервале 1,6-2,6 случая на 106 чел.-лет (таблица 3). Использовалась информа- ция, содержащаяся как в Национальном канцер-регистре [27-29], так и в специальной клиникоморфологической базе данных Института эндокринологии и обмена веществ АМН Украины [26]. В таблице 7 приводится число случаев и количество человеко-лет наблюдения в возрастных группах 0-49 лет для двух полов. Оценки параметров функции λzsone ( аges) , полученные для 9-ти областей (Волынская, Луганская, Донецкая, Ивано-Франковская, Львовская, Николаевская, Одесская, Харьковская и Черновицкая), приведены в таблице 8.
Таблица 7
Число случаев рака ЩЖ, зарегистрированных в разных возрастных группах в интервале 0-49 лет у мужчин и женщин в 1990-2001 гг., и соответствующее количество человеко-лет наблюдения в 9-ти областях «зоны фоновой заболеваемости», в которых средняя наблюдаемая заболеваемость раком ЩЖ в возрастной группе 0-18 лет в этот период составляет 1,6-2,6 случая на 106 чел.-лет
|
Возраст ( age )* |
Число случаев* |
Млн чел.-лет |
||||
|
F II |
M II |
F+M |
F |
II M |
F+M |
|
|
0 |
0 |
0 |
0 |
1.16 |
1.22 |
2.38 |
|
1 |
0 |
0 |
0 |
1.22 |
1.29 |
2.51 |
|
2 |
0 |
0 |
0 |
1.30 |
1.37 |
2.67 |
|
3 |
0 |
0 |
0 |
1.38 |
1.45 |
2.82 |
|
4 |
0 |
0 |
0 |
1.45 |
1.52 |
2.98 |
|
5 |
0 |
0 |
0 |
1.53 |
1.59 |
3.12 |
|
6 |
1 |
2 |
3 |
1.59 |
1.66 |
3.26 |
|
7 |
2 |
3 |
5 |
1.66 |
1.73 |
3.39 |
|
8 |
3 |
0 |
3 |
1.71 |
1.78 |
3.49 |
|
9 |
2 |
0 |
2 |
1.75 |
1.81 |
3.56 |
|
10 |
3 |
2 |
5 |
1.78 |
1.84 |
3.62 |
|
11 |
6 |
1 |
7 |
1.80 |
1.87 |
3.67 |
|
12 |
7 |
5 |
12 |
1.82 |
1.88 |
3.70 |
|
13 |
12 |
2 |
14 |
1.82 |
1.89 |
3.71 |
|
14 |
8 |
5 |
13 |
1.82 |
1.88 |
3.70 |
|
15 |
11 |
3 |
14 |
1.82 |
1.87 |
3.69 |
|
16 |
10 |
7 |
17 |
1.81 |
1.86 |
3.67 |
|
17 |
17 |
3 |
20 |
1.79 |
1.86 |
3.65 |
|
18 |
23 |
9 |
32 |
1.79 |
1.85 |
3.64 |
|
19 |
21 |
6 |
27 |
1.77 |
1.83 |
3.61 |
|
20 |
18 |
4 |
22 |
1.76 |
1.82 |
3.58 |
|
21 |
31 |
9 |
40 |
1.74 |
1.80 |
3.55 |
|
22 |
33 |
2 |
35 |
1.73 |
1.78 |
3.51 |
|
23 |
34 |
6 |
40 |
1.61 |
1.66 |
3.27 |
|
24 |
33 |
9 |
42 |
1.46 |
1.51 |
2.97 |
|
25 |
29 |
5 |
34 |
1.32 |
1.36 |
2.67 |
|
26 |
26 |
3 |
29 |
1.17 |
1.20 |
2.37 |
|
27 |
34 |
5 |
39 |
1.02 |
1.05 |
2.07 |
|
28 |
27 |
6 |
33 |
0.97 |
0.90 |
1.77 |
|
29 |
19 |
6 |
25 |
0.73 |
0.75 |
1.47 |
|
30-34 |
104 |
24 |
128 |
2.82 |
2.86 |
5.68 |
|
35-39 |
172 |
38 |
210 |
3.22 |
3.24 |
6.46 |
|
40-44 |
218 |
44 |
262 |
3.39 |
3.36 |
6.76 |
|
45-49 |
295 |
38 |
333 |
3.26 |
3.14 |
6.40 |
|
Всего |
1199 |
247 |
1446 |
58.96 |
60.51 |
119.37 |
Таблица 8 Оценки параметров половозрастной функции фоновой заболеваемости раком ЩЖ λ z s one ( а ges) в возрастном интервале 0-49 лет для 9-ти областей Украины со средней заболеваемостью в возрастной группе 0-18 лет λ 0 9 - 0 1 - 8 0 , 1 s, j = 1,6-2,6 случая на 106 чел.-лет
|
Пол |
ages b (лет) |
Возрастной интервал (лет) |
Параметры функции λ z s one ( а ges) |
||||
|
(i) zone,s,0,9obl случаев на 10 6 чел.-лет |
(i) s,9obl лет -1 |
||||||
|
GM |
GSD P value |
Mean |
STD |
P value |
|||
|
F |
21 |
0 – 21 21 – 49 |
0,40 4,66 |
1,30 0,006 1,11 <0,001 |
0,18 0,06 |
0,02 0,003 |
<0,001 <0,001 |
|
M |
- |
0 – 49 |
0,93 |
1,29 0,849 |
0,06 |
0,008 |
<0,001 |
λzsone(аges) = Az(io)ne,s,0,9obl ⋅ exp(As(i,9)obl ⋅ ages), s – пол, ages – достигнутый возраст, 9obl agesb - «пограничный» возраст, разделяющий два возрастных интервала (i=1,2) с различным темпом возрастного нарастания заболеваемости раком ЩЖ; Az(io) ne,s,0,9obl , As(i,9) obl – параметры, gm – геометрическое среднее, GSD – стандартное отклонение среднегеометрического, STD – стандартное отклонение среднеарифметического, F - женщины, M - мужчины.
Анализ показал, что в старших возрастных группах темп прироста фоновой тиреоонкоза-болеваемости с возрастом довольно резко снижается по сравнению с темпом возрастного прироста заболеваемости у детей и подростков. Оказалось, что «двухинтервальная» функция с пограничным возрастом ages b (уравнение 3) хорошо описывает данные, относящиеся к женщинам. При этом пограничный возраст ages b составляет 21 год. Что касается мужчин, то более подходящей оказалась моноинтервальная функция λ z s one ( а ges) , описывающая изменение фоновой заболеваемости на всем рассматриваемом интервале возрастов 0-49 лет. На рис. 9 визуализированы модельные кривые и данные наблюдений для двух полов.
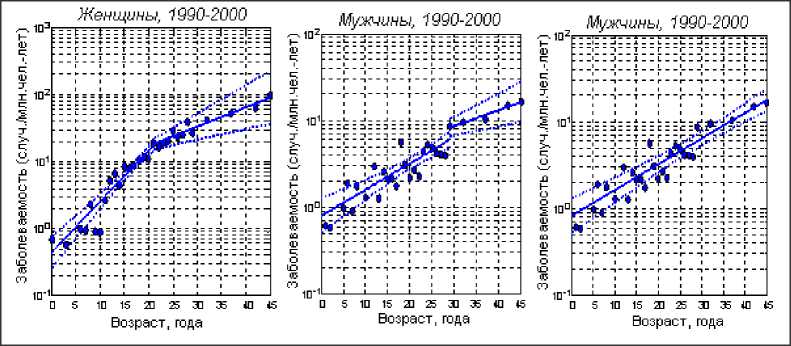
Рис. 9. Заболеваемость раком ЩЖ и аппроксимационные кривые λ z s one ( а ges) для возрастного интервала 0-49 лет для женщин (двухинтервальная кривая) и для мужчин (одно- и двухин-тервальная кривые) для периода 1990-2001 гг. в 9-ти областях «фоновой заболеваемости».
В дальнейшем анализе использовалось предположение о едином для всей территории Украины характере относительного межвозрастного изменения фоновой заболеваемости раком ЩЖ в отдельной гендерной группе. То есть, принималось, что в уравнении 3 значения b s (i) близки к значениям b s (i , ) 9obl , приведенным в таблице 8. Для проверки правомерности подобного допущения, представленные в таблице 8 оценки b s (i , ) 9obl , сравнивались с аналогичными оценками, полученными из анализа двух других массивов данных, а именно:
-
( i) Массив случаев рака ЩЖ, наблюдавшихся в «радиационный» период у жителей 15 областей (возраста 0-49 лет) зоны «фоновой заболеваемости», где средняя наблюдаемая заболеваемость раком ЩЖ в возрастной группе 0-18 лет в 1990-2001 гг., λ 0 9 - 0 1 - 8 0 , 1 s, j , была ниже, чем 4 случая на 106 чел.-лет. Кроме анализированных выше девяти областей, в рассмотрение были включены также Днепропетровская, Закарпатская, Запорожская, Полтавская, Тернопольская и Хмельницкая области.
-
( ii) Массив со случаями рака ЩЖ, наблюдавшимися в «радиационный» период у населения возраста 0-49 лет в пределах всей территории Украины в целом.
Обработка этих двух массив также проводилась с использованием уравнения 3. Параметры соответствующих функций, λzsone ( аges) и λs ( аges )I , описывающих соответст венно изменение с возрастом фоновой заболеваемости в 15 областях с λ09-01-80,1s, j ≤ 4 случая на 106 чел.-лет и во всей Украине в целом, представлены в таблицах 9 и 10.
Результаты, приведенные в таблицах 7-9, отчетливо демонстрируют следующее:
-
- оцененные значения параметров b s (i , ) 9obl , b s (i , ) 15obl и b s (i , ) Ukr близки как для мужчин, так и для женщин;
-
- для всех проанализированных массивов данных «пограничный возраст» ages b у женщин составляет 21 год;
-
- в младших возрастах (до 21 года) темп роста с возрастом фоновой заболеваемости раком ЩЖ у женщин выше, чем у мужчин;
-
- численные оценки параметров A z (i o ) ne,s,0,9obl , A z (i o ) ne,s,0,15obl и A z (i o ) ne,s,0,Ukr существенно зависят от того, к какой зоне принадлежит анализируемый информационный массив.
Таким образом, выполненный сравнительный анализ в целом свидетельствует о правомерности использования единой для всех территорий относительной возрастной зависимости фоновой заболеваемости раком ЩЖ, количественно описываемой параметрами b s (i , ) 9obl , приведенными в таблице 8.
Таблица 9
Оценки параметров половозрастной функции фоновой заболеваемости раком ЩЖ λ z s one ( а ges) в возрастном интервале 0-49 лет для 15-ти областей со средней заболеваемостью в возрастной группе 0-18 лет λ 0 9 - 0 1 - 8 0 , 1 s, j ≤ 4 случая на 106 чел.-лет
|
Пол |
ages b (лет) |
Возрастной интервал (лет) |
zone ~ Параметры функции λ s ( а ) |
|||||
|
(i) zone,s,0,9obl случаев на 10 6 чел.-лет |
(i) b s,9obl лет -1 |
|||||||
|
GM |
GSD P value |
Mean |
STD |
P value |
||||
|
F |
21 |
0 – 21 21 – 49 |
0,49 6,27 |
1,33 0,002 1,16 <0,001 |
0,18 0,06 |
0,02 0,004 |
<0,001 <0,001 |
|
|
M |
- |
0 – 49 |
1,01 |
1,26 0,80 |
0,06 |
0,008 |
<0,001 |
|
λzsone(аges) = Az(io)ne,s,0,15obl ⋅ exp(bs(i,1)5obl ⋅ ages), s – пол, ages – достигнутый возраст, 15 obl agesb - «пограничный» возраст, разделяющий два возрастных интервала (i=1,2) с различным темпом возрастного нарастания заболеваемости раком ЩЖ; Az(io)ne,s,0,9obl , bs(i,9) obl – параметры, GM – геометрическое среднее, GSD – стандартное отклонение среднегеометрического, STD – стандартное отклонение среднеарифметического, F - женщины, M - мужчины.
Таблица 10
Оценки параметров половозрастной функции фоновой заболеваемости раком ЩЖ λ s ( а ges) в возрастном интервале 0-49 лет для всей Украины
|
Пол |
ages b (лет) |
Возрастной интервал (лет) |
zone ~ Параметры функции λ s ( а ) |
|||||
|
(i) zone,s,0,9obl случаев на 10 6 чел.-лет |
(i) s,9obl лет -1 |
|||||||
|
GM |
GSD P value |
Mean |
STD |
P value |
||||
|
F |
21 |
0 – 21 21 – 49 |
0,38 5,93 |
1,30 0,002 1,14 <0,001 |
0,18 0,06 |
0,02 0,003 |
<0,001 <0,001 |
|
|
M |
- |
0 – 49 |
0,90 |
1,28 0,680 |
0,06 |
0,008 |
<0,001 |
|
A s (ages) Ukr = A ^krsy • exp( b sUkr • ages) , s - пол, ages - достигнутый возраст, ages b - «пограничный» возраст, разделяющий два возрастных интервала ( i =1,2) с различным темпом возрастного нарастания заболеваемости раком ЩЖ; A z (i o ) ne,s,0,Ukr , b s ( i ,U ) kr – параметры, GM – геометрическое среднее, GSD – стандартное отклонение среднегеометрического, STD – стандартное отклонение среднеарифметического. F - - женщины , M - мужчины.
Оценка рисков с использованием «внешнего фона»
Результаты оценки риска в варианте «внешнего фона», когда фоновый уровень заболеваемости рассчитывался с учетом изложенных выше моделей скрининг-технологического эффекта и относительной половозрастной зависимости заболеваемости раком ЩЖ, представлены в таблице 11.
Таблица 11
Оценки абсолютного (EAR/106 чел.-лет Гр) и относительного (ERR/Гр) рисков в модели
«внешнего спонтана»: λobs = λexp +α ⋅ D ⋅ ezs,α⋅age и λobs = λexp ⋅(1+β ⋅D⋅ezs,β⋅age) s,age s,age s s,age s,age s соответственно
|
Оценка эксцесса абсолютного риска, EAR/106 чел.-лет Гр |
||
|
Параметры модели |
F |
M |
|
α s ± std |
193 ± 38 |
135 ± 29 |
|
95% ДИ |
119 – 267 |
78 – 192 |
|
t stas |
5,095 |
4,65 |
|
Pv |
< 0,001 |
< 0,001 |
|
z s, α ± std |
-0,034 ± 0,037 |
-0,036 ± 0,031 |
|
95% ДИ |
-0,107 – 0,039 |
-0,098 – 0,025 |
|
t stas |
0,90 |
1,15 |
|
Pv |
0,366 |
0,249 |
|
Оценка эксцесса относительного риска, ERR/Гр |
||
|
Параметры модели |
F |
M |
|
β s ± std |
9,4 ± 2,0 |
13,0 ± 2,9 |
|
95% ДИ |
5,5 – 13,3 |
7,4 – 18,6 |
|
t stas |
4,76 |
4,56 |
|
Pv |
< 0,001 |
< 0,001 |
|
z s, β ± std |
-0,185 ± 0,049 |
-0,078 ± 0,034 |
|
95% ДИ |
-0,282 – 0,089 |
-0,144- 0,011 |
|
t stas |
3,78 |
2,30 |
|
Pv |
< 0,001 |
0,022 |
|
Количество случаев |
||
|
Фоновые* |
137 |
32 |
|
Радиоиндуцированные* |
23 |
42 |
|
Всего |
160 |
74 |
|
Численность населения |
||
|
Всего |
155141 1 |
159139 |
* расчетные значения;
F – женщины, M – мужчины.
Как видно из представленных данных:
-
(a) оценки и абсолютных, и относительных рисков статистически высоко достоверны;
-
(b) оценки абсолютных и относительных рисков достаточно близки к тем, которые получены в варианте «внутреннего фона» в работе [10];
-
(c) абсолютные риски для женщин на 40% выше, а относительные риски на 25-27% ниже, чем у мужчин;
-
(d) оценки возраст-зависимых модификаторов как абсолютных, так и относительных рисков отрицательны (для случая абсолютного риска достоверны), причем возрастная зависимость для женщин существенно более выражена, чем для мужчин.
Сопоставляя два варианта анализа рисков (с «внутренним» и «внешним» фоном) необходимо подчеркнуть, что удовлетворительное согласие между рисковыми оценками и оценками возрастных модификаторов, позволяет считать принятые модели фоновой заболеваемости и скрининг-технологического эффекта как такие, которые вполне адекватно описывают моделируемые процессы.
Список литературы Постчернобыльские раки щитовидной железы в Украине: фоновые и радиоиндуцированные случаи
- Talerko N. Mesoscale modelling of radioactive contamination formation in Ukraine caused by the Chernobyl accident//J. Environ. Radioactivity. -2005. -V. 78. -P. 311-329.
- Likhtarev I., Talerko N., Bouville A., Vailleque P., Lukyanov N., Kuzmenko A., Shedemenko I. Radioactive contamination of Ukraine caused by Chornobyl accident using atmospheric transport modeling. Draft report available at http//dceg.cancer.gov/radia.html.
- Jacob P., Goulko G., Heidenreich W.F., Likhtarev I.A., Kairo I.A., Tronko N.D., Bogdanova T.I., Kenigsberg J., Buglova E., Drozdovitch V., Beral V. Thyroid cancer risk to children calculated//Nature. -1998. -V. 392. -P. 31-32.
- Likhtarev I.A., Sobolev B.G., Kairo I.A., Tronko N.D., Bogdanova T.I., Oleinic V.A., Epshtein E.V., Beral V. Thyroid cancer in the Ukraine//Nature. -1995. -V. 375. -P. 365.
- Тронько Н.Д., Богданова Т.И. Рак щитовидной железы у детей Украины (последствия чернобыльской катастрофы). -Киев: Чернобыльинтеринформ, 1997. -200 с.
- Tronko N.D., Bogdanova T.I., Komissarenko I., Rybakov S., Kovalenko A., Epshtein O., Oliynik V., Tereshchenko V., Likhtarev I.A., Kairo I., Chepurnoy M. The Post-Chernobyl incidence of Childhood thyroid cancer in Ukraine. In: Radiation and Thyroid Cancer. Proceedings of an International Seminar. EUR 18552 EN. -1999. -P. 61-69.
- Tronko M.D., Bogdanova T.I., Komissarenko I.V., Epstein O.V., Oliynik.V.A., Kovalenko A.Ye., Likhtarev I.A., Kairo I.A., Peters S.B., LiVolsi V.A. Thyroid carcinoma in children and adolescents in Ukraine after the Chernobyl accident: statistical data and clinicomorphologic characteristics//Cancer. -1999. -V. 86, N 1. -P. 149-156.
- Tronko N.D., Bogdanova T.I., Likhtarev I.A., Kairo I.A., Shpak V.I. Summary of the 15 year observation of thyroid cancer among Ukrainian children after the Chernobyl accident/Chernobyl: Message for the 21st Century/Editors S.Yamashita, Y.Shibata, M.Hoshi, K.Fujimura. Excerpta Medica. International Congress Series. -Elsevier, Amsterdam, 2002. -P. 77-83.
- Ivanov V.K., Gorski A.I., Pitkevitch V.A., Tsyb A.F., Cardis E., Storm H. Risk of radiogenic thyroid cancer in Russia following the Chernobyl accident/Eds. Thomas G., Karaoglou A., Willliams E.D. Proceedings of an International Seminar on Radiation and Thyroid Cancer. -Brussels-Luxembourg: World Scientific Publishing, 1999. -P. 89-96.
- Likhtarov I., Kovgan L., Vavilov S., Chepurny M., Ron E., Lubin J., Bouville A., Tronko N., Bogdanova T., Gulak L., Zablotska L., Howe G. Report 2 Post-Chornobyl thyroid cancers in Ukraine. Report 2: Risk Analysis//Radiation Research (in press).
- Likhtarov I., Kovgan L., Vavilov S., Chepurny M., Bouville A., Luckyanov N., Jacob P., Volleque P., Voigt G. Post-Chornobyl thyroid cancers in Ukraine. Report 1. Estimation of thyroid doses//Radiation Research. -2005. -V. 163. -P. 125-136.
- О совершенствовании эндокринологической помощи населению: Приказ МОЗ Украины. -Киев, 1992.
- Shore R.E., Hildreth N., Dvoretsky P., Andresen E., Moseson M., Pasternack B. Thyroid cancer among persons given x-ray treatment in infancy for an enlarged thymus gland//Am. J. Epidemoil. -1993. -V. 137. -P. 1068-1080.
- Ron E., Modan B., Preston D.L., Alfandary E., Stovall M., Boice J.D. Thyroid neoplasia following lowdose radiation in childhood//Radiation Research. -1989. -V. 120. -P. 516-531.
- Schneider A.B., Ron E., Lubin J., Stovall M., Gierlowski T.C. Dose-response relationships for radiation-induced thyroid cancer and thyroid nodules: evidence for the prolonged effects of radiation on the thyroid//J. Clin. Endocrinol. Metab. -1993. -V. 77. -P. 362-369.
- Pottern L.M., Kaplan M.M., Larsen P.R., Silva J.E., Koenig R.J., Lubin J.H., Stovall M., Boice J.D.Jr. Thyroid nodularity after irradiation for lymphoid hyperplasia: A comparison of questionnaire and clinical findings//J. Clin. Epidemiol. -1990. -V. 43. -P. 449-460.
- Holm L.E. Thyroid cancer after diagnostic and therapeutic use of radionuclides: a review of the association: Radiation and Thyroid Cancer. Proceedings of an International Seminar. EUR 18552 EN, 1999. -P. 13-20.
- Hall P., Furst C.J., Mattsson A., Holm L.E., Boice J.D.Jr., Inskip P.D. Thyroid nodularity after diagnostic administration of iodine-131//Radiation Research. -1996. -V. 146. -P. 673-682.
- Shore R.E. Studies in Utah thyroid tumors following Nevada Test Site Fallout: Radiation and Thyroid Cancer. Proceedings of an International Seminar. EUR 18552 EN, 1999. -P. 29-34.
- Kerber R.A., Till J.E., Simon S.L., Lyon J.L., Thomas D.C., Preston-Martin S., Rallison M.L., Lloyd R.D., Stevens W. A cohort study of thyroid disease in relation to fallout from Nuclear Weapons Testing//JAMA. -1993. -V. 270, N. 17. -P. 2076-2082.
- Trott K.R., Schoemaker M.J., Takahashi T., Fujimori K., Nakashima N., Ohtomo H., Watanabe N., Satomi S., Simon S.L. Thyroid cancer and thyroid nodules in the people of the Marshall Islands potentially exposed to fallout from Nuclear Weapons Testing//Radiation and Thyroid Cancer. Proceedings of an International Seminar. EUR 18552 EN. -1999. pp. 41-50.
- Howard J.E., Vaswani A., Heotis P. Thyroid disease among the Rongelap and Utirik population -an update//Health Physics. -1997. -V. 73, N 1. -P.190-198.
- Takahashi T., Trott K.R., Fujimori K., Simon S.L., Ohtomo H., Nakashima N., Takaya K., Kimura N., Satomi S., Schoemaker M.J. An investigation into the prevalence of thyroid disease on Rwajalein Atoll, Marshall islands//Health Physics. -1997. -V. 73, N 1. -P.199-213.
- Preston D.L., Lubin J.H., Pierce D.A. and McConney M.E. EPICURE. -Seatle, USA: Hirosoft International Corporation, 1993.
- Дьяконов В.П. MATLAB 6/6.1/6.5 + SIMULINK 4/5. Основы применения. Полное руководство пользователя. -М.: СОЛОН-Пресс, 2002. -768 с.
- Tronko N.D., Bogdanova T.I., Komissarenko I. et al. Thyroid cancer in children and adolescents in Ukraine after the Chernobyl accident (1986-1995). Proceedings of the first international conference Minsk, Belarus 18 to 22 March 1996. -P. 683-690.
- Рак в Україні, 2000-2001. Захворюваність, смертність, показники діяльності онкологічної служби/Під ред. С.О.Шалімова//Бюлетень Національного Канцер-реєстру України: Інститут онкології та радіології АМН України. -Київ, 2002. -108 с.
- Winkelmann R.A., Okeanov A., Gulak L., Remennik L., Rahu M., Storm H.H. Cancer registration techniques in the New Independent States of the former Soviet Union: IARC Technical Report No 35. -Lyon: IARC, 1998. -P. 22-43.
- Рак в Україні, 1998-2000. Захворюваність, смертність, показники діяльності онкологічної служби/Під ред. С.О.Шалімова//Бюлетень Національного Канцер-реєстру України: Інститут онкології та радіології АМН України. -Київ, 2001. -117 с.
- Likhtarev I., Minenko V., Khrouch V., Bouville A. Uncertainties in thyroid dose reconstruction after Chernobyl//Radiation Protection Dosimetry. -2003. -V. 105, N 1-4. -P. 601-608.
- Likhtarev I., Bouville A., Kovgan L., Luckyanov N., Voilleque P., Chepurny M. Questionnaire -and measurement -based individual thyroid doses in Ukraine resulting from the Chornobyl nuclear reactor accident//Radiation Research (in press).


