Поверхность растворимости углерода, кислорода и хрома в жидкой меди
Автор: Михайлов Геннадий Георгиевич, Макровец Лариса Александровна, Самойлова Ольга Владимировна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Рубрика: Физическая химия и физика металлургических систем
Статья в выпуске: 2 т.17, 2017 года.
Бесплатный доступ
Выполнено термодинамическое моделирование фазовых равновесий в металлическом расплаве для систем Cu-C-O и Cu-Cr-C-O в интервале температур 1100-1300 °С. Термодинамический анализ процессов взаимодействия в исследуемых системах был проведен с использованием методики построения поверхности растворимости компонентов в металле. Диаграмма такого вида позволяет связать составы металлического расплава с видом продуктов взаимодействия, включающих не только твердые частицы оксидов, но и компоненты оксидного расплава, а также газообразные продукты взаимодействия. В ходе моделирования были уточнены температурные зависимости констант равновесия реакций, протекающих в медном расплаве исследуемых систем. Также были оценены параметры взаимодействия первого порядка (по Вагнеру) элементов в жидкой меди. Результаты моделирования представлены в виде графиков, на которых отражены составы металлического расплава (в зависимости от температуры), который находится в равновесии с тем или иным продуктом взаимодействия. По результатам проведенного моделирования определено, что образование частиц оксида меди в присутствии углерода и хрома, растворенных в жидкой меди, термодинамически маловероятно. При использовании графита в качестве элемента-раскислителя необходимо учитывать малую растворимость углерода в медном расплаве.
Система cu-c-o, система cu-cr-c-o, термодинамическое моделирование, поверхность растворимости компонентов в металле, хромовые бронзы
Короткий адрес: https://sciup.org/147157088
IDR: 147157088 | УДК: 669.35 | DOI: 10.14529/met170201
Carbon, oxygen and chromium solubility surface in liquid copper
Thermodynamic modeling of phase equilibria in the liquid metal of Cu-C-O and Cu-Cr-C-O systems was done for the temperature range 1100-1300 °С. Thermodynamic analysis of interaction processes in the investigated systems was performed using the method of constructing of the components’ solubility surface in the metal melt. Such diagram allows connecting the compositions of the metal melt with the type of products of interaction, including solid particles of oxides, components of oxide melt and gaseous reaction products. Temperature dependences of the equilibrium constants of the reactions, which are taking place in the copper melt of the investigated systems, was clarified during thermodynamic modeling. The first order interaction parameters (Wagner) of elements in the liquid copper were evaluated during simulation. The thermodynamic modeling results are presented in the form of graphs on which the compositions of the metallic melt (depending on the temperature) are reflected. On these graphs metal melt compositions are in equilibrium with one or another interaction product. Based on the results of the simulation, it was determined that the formation of copper oxide particles in the presence of carbon and chromium dissolved in liquid copper is thermodynamically unlikely. Using graphite as a deoxidizing element, it is necessary to take into account the low solubility of carbon in liquid copper.
Текст научной статьи Поверхность растворимости углерода, кислорода и хрома в жидкой меди
Бронзы системы Cu–Cr отличаются высокими механическими свойствами, высокой электропроводностью и теплопроводностью, повышенной температурой рекристаллизации. Эти сплавы применяют для изготовления электродов электросварочных аппаратов, а также для изготовления различных деталей, работающих при повышенных температурах. В основном хромовые бронзы содержат порядка 0,4–1,0 мас. % хрома [1–4]. При производстве таких бронз графит используют не только как составную часть сплавов для раскисления, но и как покров, который помещают на зеркало металла для предотвращения окисления металлического расплава [5].
В литературе имеются сведения по термодинамике процессов взаимодействия в системе Cu–Cr–O, согласно которым хром взаимодействует с растворенным в медном расплаве кислородом с образованием частиц оксида хрома Cr2O3 [5, 6]. Для системы Cu–C–O большинство литературных данных посвяще- но описанию раскисления медного расплава монооксидом углерода CO [7–9]. Только в работах [6, 10] представлены некоторые сведения о термодинамических и диффузионных аспектах процессов взаимодействия растворенных в медном расплаве углерода и кислорода. Следует отметить, что для системы Cu– Cr–C–O в литературе нет данных, описывающих взаимодействие компонентов в жидкой меди.
Целью данной работы является термодинамическое моделирование процессов взаимодействия в системах Cu–C–O и Cu–Cr–C–O в условиях существования металлического расплава на основе меди.
Термодинамический анализ в данной работе выполнялся с использованием методики построения поверхности растворимости компонентов в металле (ПРКМ) [11, 12], которая позволяет связать количественные изменения в составе металлического расплава с изменениями в составе продуктов взаимодействия, которые могут быть представлены как твердыми частицами, так и компонентами оксидного расплава, а также газом.
На начальной стадии моделирования рассматривались бинарные диаграммы состояния (Cu–C, Cu–O и Cu–Cr), составляющие исследуемые системы, для определения пределов растворимости компонентов в жидкой меди в интересующем интервале температур (в данной работе этот интервал составляет 1100– 1300 °С).
Согласно литературным данным [13, 14] углерод обладает ограниченной растворимостью как в твердой, так и в жидкой меди. Растворимость углерода в жидкой меди в интересующем нас интервале температур 1100– 1300 °С крайне мала и составляет для температуры 1100 °С величину порядка 10–5 мас. %, а для температуры 1300 °С не превышает 10–4 мас. %.
Данные по диаграмме состояния системы Cu–O обобщены в работе [15], согласно этим сведениям для температуры 1100 °С растворимость кислорода в медном расплаве состав- ляет 0,64 мас. %; для 1200 °С – порядка 1,66 мас. %; для 1300 °С – порядка 3,10 мас. %.
Согласно фазовой диаграмме Cu–Cr [16], хром обладает ограниченной растворимостью в металлическом расплаве на основе меди: для температуры 1100 °С растворимость хрома в жидкой меди составляет порядка 2 мас. %; для температуры 1200 °С – порядка 4 мас. %; для температуры 1300 °С – не более 7 мас. %.
При моделировании системы Cu–Cr–C–O также учитывалась возможность образования соединения CuCrO 2 [17–19].
Для расчета координат ПРКМ исследуемых систем необходимы сведения о константах равновесия реакций, протекающих в металлическом расплаве (табл. 1), а также данные по параметрам взаимодействия первого порядка по Вагнеру (табл. 2).
Следует отметить, что для сильных раскислителей возможна не только температурная, но и концентрационная зависимость для параметра взаимодействия первого порядка (по Вагнеру) элемента-раскислителя с кислородом в жидкой меди [12, 22], что учитывалось для
Таблица 1
Константы равновесия процессов взаимодействия медного расплава и сопряжённых фаз (lg K = -AIT + B) [6]
|
Уравнение реакции* |
A |
B |
|
(Cu 2 O) = 2 [Cu]+ [O] |
3141 |
2,251 |
|
(Cr 2 O 3 ) = 2 [Cr]+ 3 [O] |
45 292 |
13,123 |
|
|Cu 2 O| = 2 [Cu] + [O] |
6500 |
4,468 |
|
|Cr 2 O 3 | = 2 [Cr] + 3 [O] |
50 760 |
15,248 |
|
|CuCrO 2 | = [Cu] + [Cr] + 2 [O] |
30 631 |
9,638 |
|
{CO} = [C] + [O] |
13 170 |
–1,930 |
|
{CO 2 } = [C] + 2 [O] |
23 660 |
1,858 |
* В квадратных скобках приведены компоненты металлического расплава, в круглых – оксидного расплава, в прямых скобках указаны чистые твердые вещества, в фигурных – газ.
Параметры взаимодействия первого порядка в медном расплаве e i j [6, 20, 21]
Таблица 2
Активности компонентов оксидного шлакового расплава Cu 2 O–Cr 2 O 3 , который может находиться в равновесии с металлическим расплавом системы Cu–Cr–C–O, рассчитывались по теории субрегулярных ионных растворов [11]. Энергетические параметры теории оказались равными (Дж/моль): Q 1112 = –61 304; Q 1122 = –51 688; Q 1222 = –22 300.
Результаты моделирования поверхности растворимости компонентов в металле системы Cu–C–O приведены на рис. 1. Описать ПРКМ можно следующим образом. В области I представлены составы металлического расплава, в равновесии с которым находится чистый твердый оксид меди; в области II – оксидный расплав, представленный оксидом меди (Cu 2 O); в области III – газ, представленный смесью {CO, CO 2 }, с общим давлением P общ = 1 атм. Линия a–b соответствует равновесию «металлический расплав – чистый твердый оксид меди – газ»; линия b–c – «металлический расплав – оксидный расплав – газ»; линия b–d – «металлический расплав – чистый твердый оксид меди – оксидный рас-
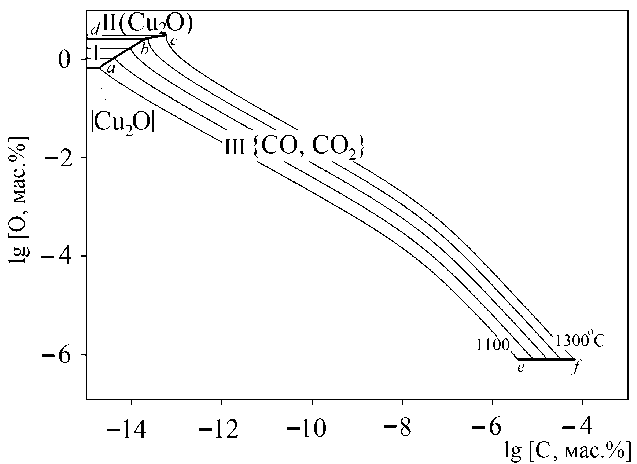
а)
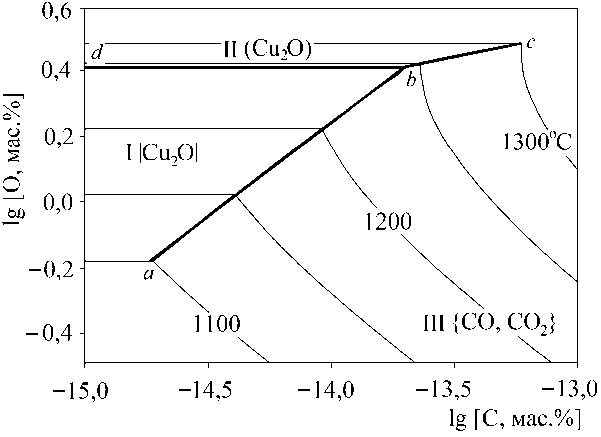
б)
Рис. 1. ПРКМ системы Cu–C–O: а – общий вид; б – увеличенный фрагмент с высокой концентрацией кислорода в металлическом расплаве
плав»; линия e–f ограничивает предельную растворимость углерода в жидкой меди при разных температурах.
Следует отметить, что линия b–d фактически соответствует процессу плавления оксида меди и реализуется при температуре 1242 °С, соответствующей литературным данным [23] о температуре плавления Cu 2 O.
Результаты моделирования поверхности растворимости компонентов в металле системы Cu–Cr–C–O приведены на рис. 2–4. Помимо известных областей I–III на ПРКМ добавились: область IV, определяющая составы металлического расплава, равновесного с чистым твердым соединением CuCrO 2 , и область V – с чистым твердым оксидом хрома Cr 2 O 3 . Также следует отметить, что в области II представлен оксидный расплав переменного состава (Cu 2 O,
Cr 2 O 3 ). На рис. 2–4 линия g–h соответствует равновесию «металлический расплав – чистое твердое соединение CuCrO 2 – чистый твердый Cr 2 O 3 »; линия g–i – «металлический расплав – чистый твердый Cr 2 O 3 – газ». На рис. 2 линия j–k определяет составы «металлический расплав – чистый твердый оксид меди – чистое твердое соединение CuCrO 2 »; линия j–l – «металлический расплав – чистый твердый оксид меди – газ». На рис. 3 линия o–k определяет составы «металлический расплав – оксидный расплав – чистый твердый оксид меди»; линия o–l – «металлический расплав – чистый твердый оксид меди – газ». На рис. 3, 4 линия m–n определяет составы «металлический расплав – оксидный расплав – чистое твердое соединение CuCrO 2 »; линия o–m – «металлический расплав – оксидный расплав – газ».
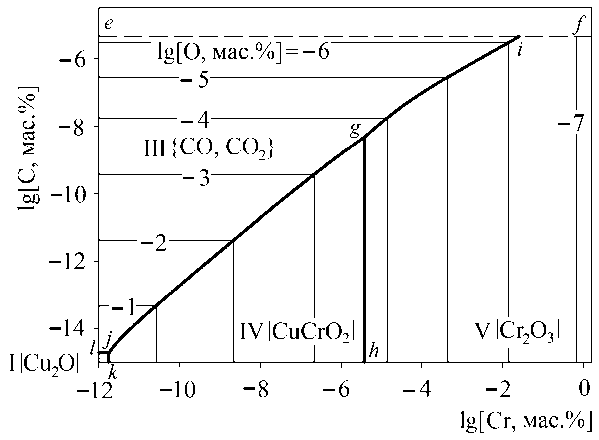
Рис. 2. ПРКМ системы Cu–Cr–C–O для температуры 1100 °С
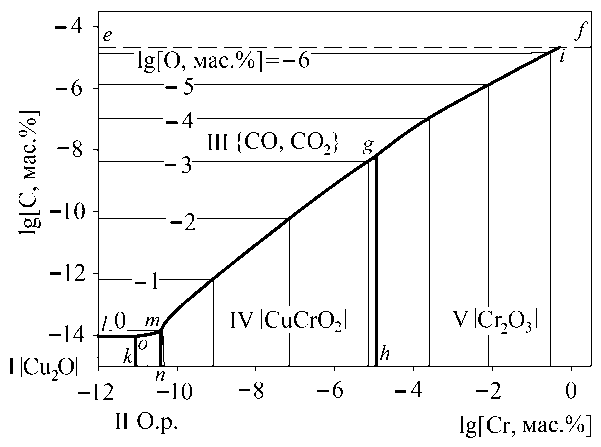
Рис. 3. ПРКМ системы Cu–Cr–C–O для температуры 1200 °С
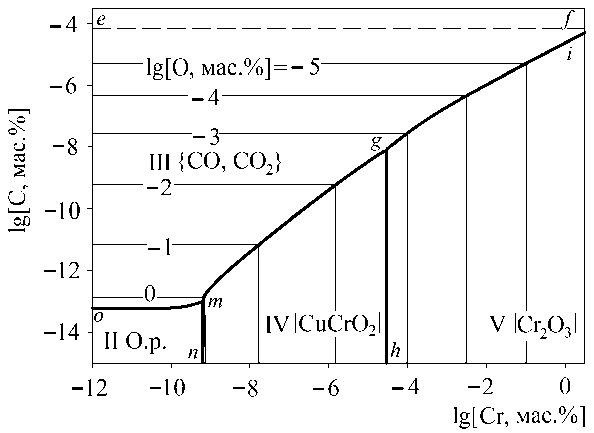
Рис. 4. ПРКМ системы Cu–Cr–C–O для температуры 1300 °С
Согласно рис. 2–4 углерод является в медном расплаве сильным раскислителем. При одних и тех же концентрациях углерода и хрома в медном расплаве (например, 10–6 мас. %) основным продуктом взаимодействия в системе Cu–Cr–C–O будет являться газ {CO, CO 2 }. Однако вследствие малой растворимости углерода в медном расплаве его раскислитель-ная способность ограничена пределом его растворимости. Для температуры 1100 °С при концентрациях хрома, соответствующих составу хромовых бронз (0,4–1,0 мас. % Cr), основным продуктом взаимодействия будет являться оксид хрома Cr 2 O 3 . И лишь только для температуры 1300 °С (с увеличением растворимости углерода в жидкой меди с ростом температуры) для интересующих концентраций хрома в металлическом расплаве системы Cu–Cr–C–O основным продуктом взаимодействия будет газ {CO, CO 2 }.
Выводы
Проведено термодинамическое моделирование процессов взаимодействия в системах Cu–C–O и Cu–Cr–C–O в условиях существования металлического расплава на основе меди для интервала температур 1100–1300 °С. Результаты моделирования представлены в виде диаграмм поверхности растворимости компонентов в металле. Установлено, что углерод является сильным раскислителем в медном расплаве, однако его раскислительная способность ограничена пределом его растворимости в жидкой меди. В системе Cu–Cr–C–O в интервале концентраций хрома в меди, соответствующих хромовым бронзам (0,4–1,0 мас. %), при температуре 1100 °С в качестве неметаллических включений образуются частицы Cr2O3. При более высоких температурах (1300 °С) раскислителем медно-хромового сплава является углерод.
Работа осуществлена при финансовой поддержке РФФИ, грант № 16-08-00133 а.
Список литературы Поверхность растворимости углерода, кислорода и хрома в жидкой меди
- Осинцев, О.Е. Медь и медные сплавы. Отечественные и зарубежные марки: справ./О.Е. Осинцев, В.Н. Федоров. -М.: Машиностроение, 2004. -336 с.
- On the use of alloying elements for Cu interconnect applications/K. Barmak, C. Cabral Jr., K.P. Rodbell, J.M.E. Harper//Journal of Vacuum Science & Technology B. -2006. -Vol. 24, no. 6. -P. 2485-2498 DOI: 10.1116/1.2357744
- Watanabe, Ch. Mechanical properties of Cu-Cr system alloys with and without Zr and Ag/Ch. Watanabe, R. Monzen, K. Tazaki//Journal of Materials Science. -2008. -Vol. 43, no. 3. -P. 813-819 DOI: 10.1007/s10853-007-2159-8
- Nanostructured Cu-Cr alloy with high strength and electrical conductivity/R.K. Islamgaliev, K.M. Nesterov, J. Bourgon et al.//Journal of Applied Physics. -2014. -Vol. 115. -P. 194301-194301-4 DOI: 10.1063/1.4874655
- Производство отливок из сплавов цветных металлов: учеб. для вузов/А.В. Курдюмов, М.В. Пикунов, В.М. Чурсин, Е.Л. Бибиков. -М.: Металлургия, 1986. -416 с.
- Куликов, И.С. Раскисление металлов/И.С. Куликов. -М.: Металлургия, 1975. -504 с.
- Sano, K. Physico-chemical investigation on copper smelting (2nd report). Thermodynamical consideration for the experimental results of the equilibrium between liquid copper and CO-CO2 gas mixtures/K. Sano, H. Sakao//Journal of the Japan Institute of Metals. -1955. -Vol. 19. -P. 435-438.
- Nanda, Ch.R. The kinetics of deoxidation of copper and copper alloys by carbon monoxide/Ch.R. Nanda, G.H. Geiger//Metallurgical Transactions. -1971. -Vol. 2, no. 4. -P. 1101-1106 DOI: 10.1007/BF02664242
- Andreini, R.J. Copper deoxidation kinetics utilizing carbon monoxide/R.J. Andreini, J.S. Foster, R.B. Phillips//Metallurgical Transactions B. -1977. -Vol. 8, no. 4. -P. 633-638 DOI: 10.1007/BF02669341
- Жуков, В.П. Математическое моделирование кинетики раскисления жидкой черновой меди углеродом/В.П. Жуков//Известия вузов. Цветная металлургия. -2016. -№ 4. -С. 13-16 DOI: 10.17073/0021-3438-2016-4-13-16
- Михайлов, Г.Г. Термодинамика металлургических процессов и систем/Г.Г. Михайлов, Б.И. Леонович, Ю.С. Кузнецов. -М.: Издат. Дом МИСиС, 2009. -520 с.
- Михайлов, Г.Г. Фазовые равновесия в многокомпонентных системах с жидкими цветными металлами/Г.Г. Михайлов, Е.А. Трофимов, А.Ю. Сидоренко. -М.: Издат. Дом МИСиС, 2014. -158 с.
- Oden, L.L. Cu-C and Al-Cu-C phase diagrams and thermodynamic properties of C in the alloys from 1550 °С to 2300 °С/L.L. Oden, N.A. Gokcen//Metallurgical Transactions B. -1992. -Vol. 23, no. 4. -P. 453-458 DOI: 10.1007/BF02649664
- Okamoto, H. Supplemental literature review of binary phase diagrams: Ag-Cl, Br-Pb, Br-Zn, C-Cu, Ce-Zr, Cl-Zn, Fe-Lu, Fe-Tm, Ga-V, Nd-Ti, Nd-Zr, and Si-Ta/H. Okamoto//Journal of Phase Equilibria and Diffusion. -2016. -Vol. 37, no. 2. -P. 246-257 DOI: 10.1007/s11669-015-0433-z
- Thermodynamic description of the Cu-O system/M.T. Clavaguera-Mora, J.L. Touron, J. Rodríguez-Viejo, N. Clavaguera//Journal of Alloys and Compounds. -2004. -Vol. 377. -P. 8-16 DOI: 10.1016/j.jallcom.2004.01.031
- Chakrabarti, D.J. The Cr-Cu (chromium-copper) system/D.J. Chakrabarti, D.E. Laughlin//Bulletin of Alloy Phase Diagrams. -1984. -Vol. 5, no. 1. -P. 59-68.
- Gadalla, A.M.M. The system CuO-Cu2O-Cr2O3 and its bearing on the performance of basic refractories in copper-melting furnaces/A.M.M. Gadalla, J. White//Transactions of the British Ceramic Society. -1964. -Vol. 63, no. 10. -P. 535-552.
- Vlach, K.C. A thermodynamic study of the Cu-Cr-O system by the EMF method/K.C. Vlach, Y.-Z. You, Y.A. Chang//Thermochimica Acta. -1986. -Vol. 103, no. 2. -P. 361-370 DOI: 10.1016/0040-6031(86)85173-5
- Revisiting the properties of delafossite CuCrO2: a single crystal study/M. Poienar, V. Hardy, B. Kundys et al.//Journal of Solid State Chemistry. -2012. -Vol. 185. -P. 56-61. DOI: 10.1016/j.jssc.2011.10.047
- Линчевский, Б.В. Термодинамика и кинетика взаимодействия газов с жидкими металлами/Б.В. Линчевский. -М.: Металлургия, 1986. -222 с.
- Standard Gibbs free energy of formation of MnO-saturated MnO•Cr2O3 solid solution at 1873 K/M. Tanahashi, N. Furuta, T. Taniguchi et al.//ISIJ International. -2003. -Vol. 43, no. 1. -P. 7-13 DOI: 10.2355/isijinternational.43.7
- Взаимодействие лития с кислородом в жидкой меди/О.В. Самойлова, Г.Г. Михайлов, Л.А. Макровец, Е.А. Трофимов//Расплавы. -2017. -№ 1. -С. 83-92.
- Химическая энциклопедия: в 5 т./под ред. И.Л. Кнунянца. -М.: Сов. энцикл. -1990. -Т. 2. -671 с.


