Повторные реконструктивные операции при инфекции синтетических протезов в аорто-подвздошно-бедренной позиции
Автор: Хамитов Ф. Ф., Маточкин Е. А., Чельдиев К. В., Фомин В. С., Бобылев А. А., Белышев С. Ю.
Журнал: Московский хирургический журнал @mossj
Рубрика: Сердечно-сосудистая хирургия
Статья в выпуске: 2 (80), 2022 года.
Бесплатный доступ
Введение. Цель - улучшение результатов хирургического лечения пациентов с инфекцией аортобедренно-бифуркационного протеза.Материалы и методы. В городской клинической больницы им. В.В. Вересаева с 2002 года по 2022 г. были повторно оперированы на аорто-подвздошно-бедренной зоне 70 пациентов в связи с инфицированием аорто-бедренных бифуркационных протезов (68 больных) и эндографтов (2 больных). У 15 (21,4 %) пациентов первичные операции были выполнены по поводу аневризм инфраренальной аорты, остальным в связи с окклюзионно-стенотическими поражениями брюшной аорты и подвздошных артерий. У 37 (84 %) пациентов первичные операции были выполнены по поводу окклюзионно-стенотических поражений аорто-подвздошной зоны. 38 (69 %) из 55 больных с окклюзионно-стенотическими поражениями брюшной аорты и артерий конечностей были оперированы в связи с хронической ишемией 3-й и 4-й степени.Результаты. В ближайшем послеоперационном периоде погибло 7(10 %) больных. Основной причиной летального исхода явился сепсис с полиорганной недостаточностью - 6. В одном наблюдении у пациента с сепсисом на 4-е сутки после операции развилась клиническая картина перитонита, причиной которого стали острые язвы тощей кишки с перфорацией. Тромбоз одной из бранш протеза развился в 3(4,2 %) наблюдениях. Во всех наблюдениях кровообращение в конечностях было восстановлено.Заключение. Методом выбора при инфицировании синтетических протезов и эндопротезов в аорто-подвздошно-бедренной позиции является использование принципов активного хирургического лечения, с полным удалением инфицированного синтетического протеза с одномоментной заменой in-situ аутовенозными шунтами из поверхностных бедренных вен, активной до- и послеоперационной антибиотикотерапией.
Аорто-бедренное бифуркационное шунтирование, синтетические протезы, сепсис, аутовенозные шунты
Короткий адрес: https://sciup.org/142235286
IDR: 142235286 | УДК: 616.136, | DOI: 10.17238/2072-3180-2022-2-58-66
Repeated reconstructive operations for infection of synthetic prostheses in the aorto-ilio-femoral position
Introduction. The Aim. Improving the results of surgical treatment of patients with infection of the aortobedreno-bifurcation prosthesis.Materials and methods. In the V.V. Veresaev City Clinical Hospital from 2002 to 2022, 70 patients were re-operated on the aorto-iliac-femoral zone due to infection of aorto-femoral bifurcation prostheses (68 patients) and endografts (2 patients). 15 (21.4%) patients underwent primary surgery for aneurysms of the infrarenal aorta, the rest due to occlusive stenotic lesions of the abdominal aorta and iliac arteries. In 37 (84%) patients, primary operations were performed for occlusive-stenotic lesions of the aorto-iliac zone. 38 (69%) of 55 patients with occlusive-stenotic lesions of the abdominal aorta and limb arteries were operated due to chronic ischemia of the 3rd and 4th degree.Results. In the immediate postoperative period, 7 (10%) patients died. The main cause of death was sepsis with multiple organ failure - 6. In one observation, a patient with sepsis on the 4th day after surgery developed a clinical picture of peritonitis, which was caused by acute ulcers of the jejunum with perforation. Thrombosis of one of the branches of the prosthesis developed in 3 (4.2%) cases. In all observations, blood circulation in the extremities was restored.Conclusion. The method of choice for infection of synthetic prostheses and endoprostheses in the aorto-iliac-femoral position is the use of the principles of active surgical treatment, with complete removal of the infected synthetic prosthesis with simultaneous in-situ replacement with autovenous shunts from the superficial femoral veins, active pre- and postoperative antibiotic therapy.
Текст научной статьи Повторные реконструктивные операции при инфекции синтетических протезов в аорто-подвздошно-бедренной позиции
Оперативные вмешательства на инфраренальном отделе брюшной аорты и подвздошных артериях считаются наиболее распространенными в практике сосудистых отделений страны. Среди всех видов операций ведущее место занимает аорто-бедренное бифуркационное шунтирование (АББШ) или протезирование (АББП) с применением синтетических протезов различных производителей. Результаты лечения при тотальном инфицировании аортобедренно-бифуркационного протеза неутешительны, общая летальность по данным разных авторов составляет при этом 16,8–88,0 % [1, 2]. В случае возникновения осложнений в раннем периоде смертность достигает 43–50 %, поздних –28,6 % [3].
Активная тактика лечения данной группы больных предусматривает обязательное раннее, до развития аррозивного кровотечения и сепсиса, удаление/резекцию инфицированного протеза с одномоментной или отсроченной реваскуляризацией конечности или ампутацией. Сторонников этой тактики большинство [4, 5]. Удаление инфицированного эксплантата большинством авторов считается обязательным [6].
Самым актуальным вопросом при хирургическом лечении больных с инфицированным аорто-бедренным синтетическим эксплантантом остается выбор материала нового протеза. Так, Torsello и соавторы [7] использовали дакро-новый протез, пропитанный желатином с рифампицином, для протезирования аневризм, вызванных золотистым стафилококком.
Также встречаются сообщения об удачном решунтировании через очаг воспаления с использованием аллотрансплантатов [8, 9]. Авторы, использующие эту методику, сообщают о недостаточной стойкости аллографтов к инфекции [9, 10].
Использование эндартерэктомированных аутоартерий для замены инфицированного синтетического протеза встречается как самостоятельный метод [11], так и в случае невозможности использовать аутовены нижних конечностей [12]. Для замены инфицированных в паховой области протезов аорто- и подвздошно-бедренного сегментов используют эверсированные поверхностные бедренные артерии этой же зоны.
Использование аутовен при наличии гнойной раны в условиях клиники и эксперимента позволяет избежать аррозивных кровотечений почти полностью, вплоть до 100 % успеха [2, 3]. Использование аутовен следует разделить на варианты: во-первых, применяются подкожные вены, во-вторых, – глубокие вены бедра: в частности, поверхностные бедренные вены.
Большие подкожные вены имеют больший диаметр, но их использование для замены аорты и подвздошно-бедренных инфицированных протезов также осложняет их выраженное несоответствие диаметров. Поверхностная бедренная вена в этом отношении более предпочтительна [13].
Также различаются мнения о порядке выполнения этапов хирургического лечения при замещении инфицированного протеза: через очаг инфекции аутотрансплантатом или экс-транатомически синтетическим шунтом. Так, Леменев В.Л. и соавторы [3] осуществляли внеочаговое шунтирование и по возможности перевязывали на протяжении сосуды, с которыми анастомозирован вовлеченный в гнойный процесс синтетический имплантат. Вторым этапом, который производят через 2–3 недели с момента прекращения кровотока по эксплантату, подлежащему удалению, захватывают стенку протеза в гнойной ране и путем тракции просто отрывают его от проксимального и дистального анастомозов. Некоторые авторы настаивают на одновременной эктраанатомической реконструкции и удалении инфицированного синтетического имплантата [14].
Но внеанатомическое шунтирование несет опасность развития синдрома перетока в той или иной степени [3]. После удаления инфицированного синтетического аортобифемо-рального протеза для внеанатомического шунтирования использовали протез Goore- tex из политетрафлюороэтилена. В 16 описанных случаях неудач не было. Однако, при лучших результатах в раннем послеоперационном периоде отдаленные результаты экстраанатомических шунтирований уступают анатомическим реконструкциям [15, 16, 17].
Oбобщая немногочисленные данные литературы по данному вопросу можно сделать вывод, что лучшие результаты получены при замене in situ на новый синтетический протез. Но, имеющиеся в отдаленном периоде повторные инфицирования, несмотря на антибиотикотерапию, заставляют искать новые пути. Экстраанатомические шунтирования характеризуется высокой частотой тромбозов протезов в ближайшем и отдаленном послеоперационном периодах. У трети выживших пациентов из-за ишемии требуется ампутация конечности. Наиболее стойкими к реинфицированию являются аутогенные материалы, а при их расположении in situ ишемических осложнений меньше.
L. Kubicek с соавторами на ежегодной конференции ESVS в Гамбурге (2019 г.) поделились опытом 35 повторных операций АББП с использование поверхностных бедренных вен. Благодаря этой тактики авторам удалось снизить послеоперационную летальность до 6,3 %, а частоту высоких ампутаций до 7,8 %.
Инфекция эндотрнасплантатата – редкое осложнение, заболеваемость <1% [15, 16]. Частота инфекции сосудистого трансплантата брюшной аорты у пациентов с аневризмой аорты, перенесших открытую операцию и эндоваскулярное лечение аневризмы, не имеет существенной разницы. Большинство авторов считают, что одной из ведущих причин развития инфекции эндопротезов становится формирование аорто-кишечных фистул, которые выявляются в 1 %–2 % до 23,9 % случаях [15, 17, 18]. В многоцентровом реестре в США, включающем 180 инфицированных стент-графтов, сообщалось о 43 инфекций эндотронсплантата (23,9 %) с аорто-кишечной фистулой [18]. Развитие инфекции приводит к таким осложнениям, как кровотечение, что стало наиболее частым симптомом (71,7 %), сепсис (39,7 %) и геморрагический шок (33,1 %). В связи с чем, актуальность проблемы не вызывает сомнения. Безусловно, достигнуты большие успехи в лечении инфекции синтетических протезов в условиях общей воспалительной реакции организма благодаря новейшим антибактериальным препаратам, применению различных гомографтов, аутографтов и протезов с ионами серебра, но опыт их применения в отдельности пока еще недостаточен, а результаты нельзя считать удовлетворительными, чтобы рекомендовать их к широкому применению[3, 6, 7, 12, 13]. Что касается лечения инфекции эндопротезов, то в литературе встречаются единичные сообщения, свидетельствующие о высокой хирургической летальности и неудовлетворительных результатах [15, 16, 17].
Материалы и методы
В отделении сосудистой хирургии городской клинической больницы им. В.В. Вересаева в период с 2002 года по 2022 г. были повторно оперированы на аорто-подвздошно-бедренной зоне 70 пациентов (66 мужчин и 4 женщины) в связи с инфицированием аорто-бедренных бифуркационных протезов (68 больных) и эндографтов (2 больных). 15 (21,4 %), включая эндопротезирование, пациентам первичные операции были выполнены по поводу аневризм инфраренальной аорты, остальным в связи с окклюзионно-стенотическими поражениями брюшной аорты и подвздошных артерий.
42 (60 %) пациентов были реоперированы в ближайшем послеоперационном периоде, 28 – в отдаленные сроки после первичной операции. Из них 3 пациента уже были повторно оперированы в связи с инфекцией бифуркационных протезов с повторным замещением синтетическими протезами, импрегнированными ионами серебра. У 37 (84 %) пациентов первичные операции были выполнены по поводу окклюзион-но-стенотических поражений аорто-подвздошной зоны. У 13 (18, 5%) больных выполнялась резекция аневризм инфрареналь-ного отдела брюшной аорты и подвздошных артерий. 38 (69 %) из 55 больных с окклюзионно-стенотическими поражениями брюшной аорты и артерий конечностей были оперированы в связи с хронической ишемией 3-й и 4-й степени по классификации Фонтейна-Покровского.
Таким образом, большинство пациентов были оперированы с использованием синтетических протезов в условиях гнойнонекротических процессов на дистальных отделах конечностей, т.е. при состояниях высокой угрозы потери конечностей.
Следует отметить, что при первичной операции использовались синтетические протезы всех известных производителей, как тканные и вязаные, так и ПТФЭ.
По данным анализов инфицирование бифуркационных протезов из ПТФЭ наблюдались только в ближайшем послеоперационном периоде.
Диагностика инфицирования синтетических протезов основывались на клинической картине, данных ультразвукового исследования, мультиспиральной КТ, двукратного микробиологического исследования содержимого парапротезного пространства и крови, маркеров сепсиса.
Инфекция сосудистых протезов, как правило, характеризовалась сочетанием трех постоянных признаков: жидкость в парапротезном пространстве по данным УЗИ и МСКТА, гнойные свищи в области послеоперационных ран, положительный микробиологический анализ отделяемого из ран (табл. 1).
Микробиологическое исследование парапротезной жидкости и содержимого из области дистальных анастомозов показало, что доминирующим инфекционным агентом стал MRSA (метициллинрезистентный золотистый стафилококк), который выявлен у 41 (58,5 %) пациентов, S. Еpidermidis был высеян у 9 (12,8 %) больных, Proteus Vulgaris также у 9 (12,8 %)
больных, Pseudomonas аeruginosa у 7 (10 %), E.Coli у 4, сочетание 2 микроорганизмов было отмечено в 7 (10 %) наблюдениях.
Таблица 1
Клинико-диагностическое критерии инфекции сосудистых протезов
Table 1
Clinical and diagnostic criteria for vascular prosthesis infection
|
Симптомы Symptoms |
№ |
% |
|
Жидкость в парапротезном пространстве Fluid in the paraprosthetic space |
70 |
100 |
|
Гнойный свищ, рана Purulent fistula, wound |
68 |
100 |
|
Псевдоаневризма проксимального анастомоза Pseudoaneurysm of proximal anastomosis |
28 |
41,1 |
|
Псевдоаневризма дистального анастомоза Pseudoaneurysm of distal anastomosis |
24 |
35,2 |
|
Аррозивное кровотечение Arrosive bleeding |
24 |
34,2 |
|
Положительный микробиологический анализ Positive microbiological analysis |
61 |
87,1 |
|
Симптомы сепсиса Symptoms of sepsis |
15 |
21,4 |
«Золотым» стандартом в диагностике инфицирования протезов и эндопротезов является МСКТ-ангиография (рис. 1А, Б).
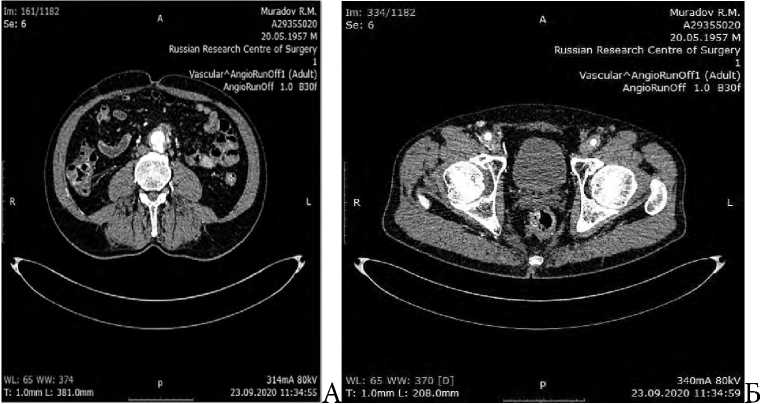
Рис. 1 А, Б. МСКТА больного с инфицированием. Стрелками указано наличие жидкости вокруг основной бранши (А) и по ходу обеих браншей (Б)
Fig. 1 A, Б. MSCTA of a patient with infection. The arrows indicate the presence of liquid around the main branch (A) and along the course of both branches (Б)
После проведения предоперационной подготовки все 70 пациентов были оперированы в объеме удаления синтетического аорто-бедренного бифуркационного протеза, аортобедренное бифуркационное аутовенозное репротезирование (ре-шунтирование – 4) «in situ».
Операция состоит из 3 основных этапов.
1-й этап: забор поверхностной бедренной вены (ПБВ) и подколенной вены (ПКВ) на обеих нижних конечностях от устья глубокой вены бедра (ГВБ) до уровня щели коленного сустава. Длина каждой забранного аутовенозного трансплантата составляла в среднем 28–33 см (рис. 2 А, Б).
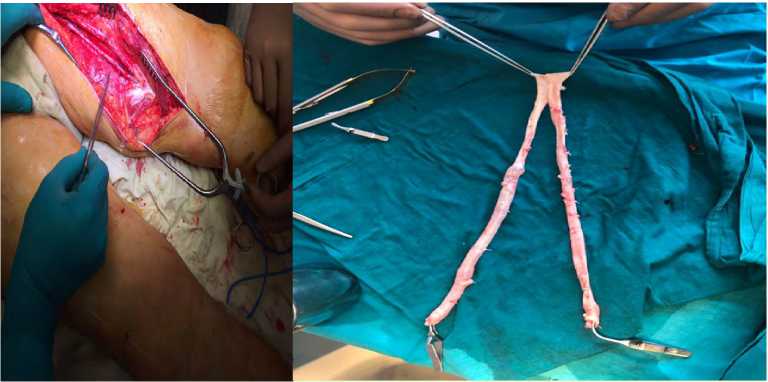
Рис. 2 А, Б. 1 этап операции: Выделение поверхностных бедренных с двух сторон и формирование бифуркационного протеза
Fig. 2 A, Б. 1 stage of the operation: Isolation of the superficial femoral from both sides and the formation of a bifurcation prosthesis
Следует отметить зависимость от диаметра инфраренального отдела аорты и необходимой длины браншей аутовенозного протеза для дистальных анастомозов с общими или глубокими бедренными артериями (рис. 3).
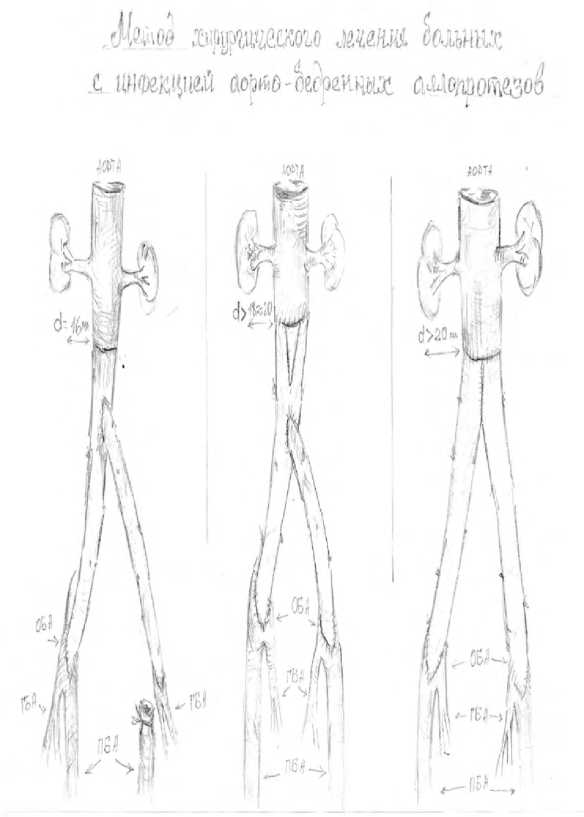
А Б В
Рис. 3 А, Б, В. Варианты формирования аутовенозных бифуркационных протезов Fig. 3 A, Б, В. Variants of the formation of autovenous bifurcation prostheses
Вариант А формируется при диаметре аорты до 16 мм и дистальных анастомозах на глубокие артерии бедра или с отдельной реконструкции ПБА и ГБА, вариант Б с клиновидной аутовенозной вставкой применяется при диаметре аорты до 20 мм и пролонгированных дистальных анастомозах, вариант В, как наиболее универсальный использовался при любом диаметре аорты и дистальных анастомозах на общие бедренные артерии. И в 2 наблюдениях, в связи с недостаточной длиной поверхностных бедренных вен, использовалась в качестве основной бранши внутренняя яремная вена.
-
2 этап : Релапаротомия или лапаротомия (если при первой операции был использован забрюшинный доступ), выделение проксимального анастомоза (рис. 4), с последующим выделением дистальных анастомозов АББШ на бедре (рис. 5). Этап завершается полным удалением бифуркационного протеза (рис. 6.).
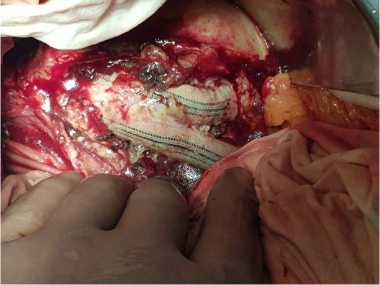
Рис. 4. Этап выделения проксимального анастомоза АББШ (гной и фибрин вокруг основной бранши протеза)
Fig. 4. Stage of isolation of the proximal anastomosis of ABS (pus and fibrin around the main branch of the prosthesis)
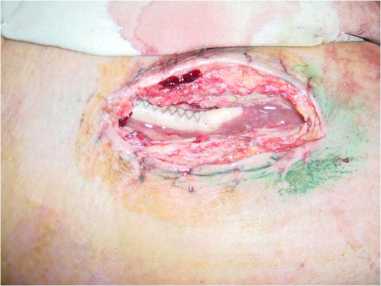
Рис. 5. Этап выделения дистальных анастомозов АББШ на бедре Fig. 5. Stage of isolation of distal anastomoses of ABBE on the thigh
Основной задачей при выделении проксимального анастомоза является выделение аорты в ее неизмененном участке для надежного контроля и профилактики массивного кровотечения, а лишь затем выполнение удаления протеза. Очень важно после удаления бифуркационного протеза произвести тщательную механическую, физическую и химическую санацию ложа инфицированного графта.
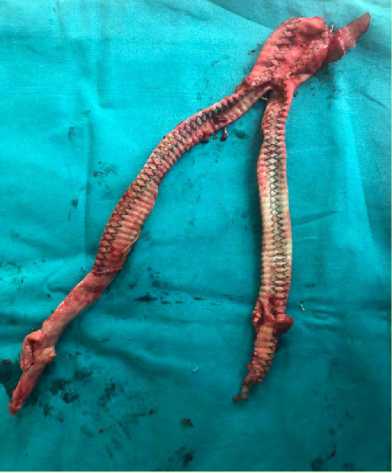
Рис. 6. Удаленный инфицированный бифуркационный протез
Fig. 6. Removed infected bifurcation prosthesis
-
3 этап: Формирование проксимального анастомоза аутовенозного шунта (протеза) с аортой по типу «конец в конец» или «конец в бок», проведение браншей протеза на бедра и формирование дистальных анастомозов (рис. 7, 8 А, Б, 9).
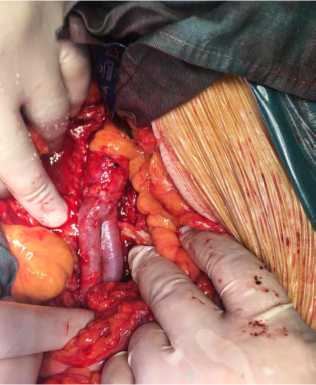
Рис. 7. Сформированный проксимальный анастомоз между аутовенозным протезом и аортой по типу «конец в конец» Fig. 7. The formed proximal anastomosis between the autovenous prosthesis and the aorta according to the “end to end” type
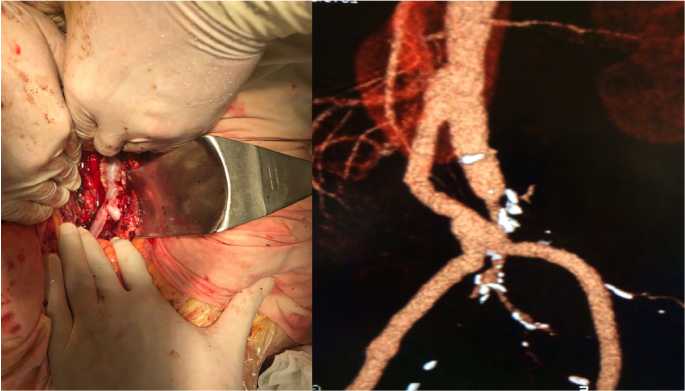
Рис. 8 А. Сформированный проксимальный анастомоз между аутовенозным шунтом и аортой по типу «конец в бок», 8 Б МСКТА аутовенозного ре-АББШ Fig. 8 A. The formed proximal anastomosis between the autovenous shunt and the aorta according to the type “end to side”, 8 Б MSCTA autovenous re-ABBSH
Необходимо отметить, что шунтирующие операции возможны при инфицировании протезов в раннем послеоперационном периоде.
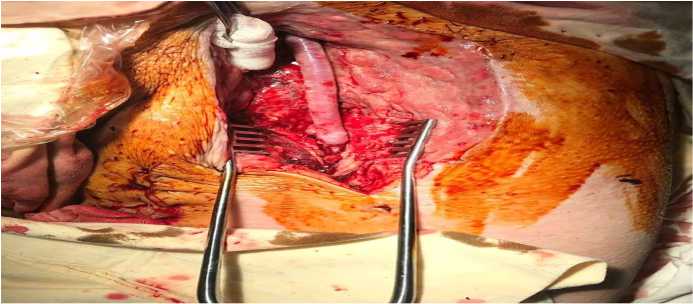
Рис. 9. Сформированный дистальный анастомоз между аутовенозным шунтом и глубокой бедренной артерией по типу «конец в бок» Fig. 9. The formed distal anastomosis between the autovenous shunt and the deep femoral artery of the “end to side” type
Оперативное вмешательство завершается дренированием брюшной полости, бедренных ран, отдельно ложа после поверхностных бедренных вен и области дистальных анастомозов. Для профилактики послеоперационной лимфорреи используется препарат «Лимфоблок» в дозировке по 25 мл на рану.
Результаты
В ближайшем послеоперационном периоде погибло 7 (10%) больных. Анализ показал, что основной причиной летального исхода был сепсис с развитием полиорганной недостаточности – 6 и лишь у 1 пациента причиной летального исхода стал инфаркт миокарда на 12-е сутки после операции.
Характер послеоперационных осложнений представлен в таблице 2.
Таблица 2
Осложнения в ближайшем послеоперационном периоде
Table 2
Complications in the immediate postoperative period
|
Результаты/ Results |
№ |
% |
|
Аррозивное кровотечение Аrrosive bleeding |
4 |
5,7 |
|
Перфорация тощей кишки Perforation of the jejunum |
1 |
1,4 |
|
Тромбоз бранши Branchy thrombosis |
1 |
1,4 |
|
Тромбоз + ампутация Thrombosis + amputation |
2 |
2,8 |
|
Септический шок Septic shock |
3 |
4,2 |
|
Инфаркт миокарда Myocardial infarction |
1 |
1,4 |
Как видно из таблицы, наиболее частым осложнением послеоперационного периода стало аррозивное кровотечение на фоне сепсиса – 3 (4,2 %), без сепсиса – 1 (1,5 %). В одном наблюдении у пациента с сепсисом на 4-е сутки после операции развилась клиническая картина перитонита, причиной которого стали острые язвы тощей кишки с перфорацией. Тромбоз одной из браншей протеза развился в 3 (4,2 %) наблюдениях: одному пациенту успешно была выполнена тромбэктомия, в 2 других в связи с безуспешностью восстановления кровообращения – ампутация на уровне бедра. Следует отметить, что в послеоперационном периоде не было клинических проявлений острой венозной недостаточности ни в одном наблюдении, но во всех наблюдениях отмечалась лимфоррея в течение 2–4 недель. С 2021 года для профилактики лимфорреи успешно применяется препарат «Лимфоблок».
В послеоперационном периоде всем пациентам проводилась комплексное лечение: антибактериальная в соответствии с результатами посева, коррекция гомеостаза и сопутствующей патологии. С целью контроля аутовенозных трансплантатов перед выпиской проводилась МСКТ-ангиография.
Отдаленные результаты прослежены у 57 пациентов в сроки от 8 месяцев до 13 лет.
В течение года после операции у 2 больных образовались аневризмы дистальных и проксимального анастомозов (рис. 14) и у 2 развился тромбоз одной из браншей протеза. Эти больные были оперированы: резекция аневризм с реконструкцией дистальных анастомозов аллонадставками, тромбэктомия с реконструкцией дистальных анастомозов аллонадставкой – 1, аутовенозной надставкой – 1. Ложная аневризма проксимального анастомоза имела размеры до 3,0–2,5–2,8 см, не увеличивалась в течение длительного времени (6 лет), поэтому было решено не проводить активных эндоваскулярных процедур.
Во всех наблюдениях кровообращение в конечностях было восстановлено. У 3 пациентов тромбоз бранши бифуркационного протеза развился через 4, 5 и 9 лет соответственно вследствие неудовлетворительного дистального русла. Из них двум пациентам была выполнена ампутация на уровне бедра, у одного больного симптомы острой ишемии регрессировали на фоне консервативного лечения.
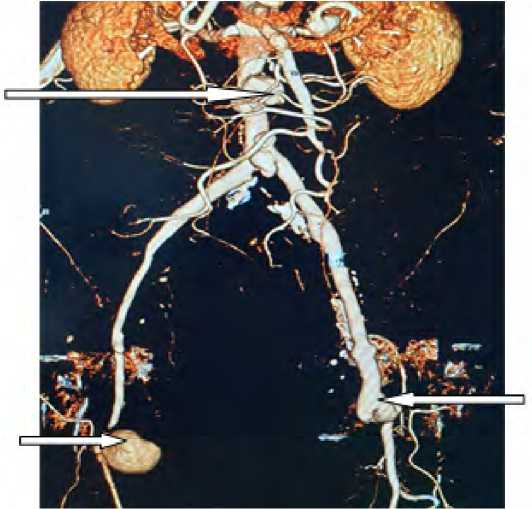
Рис. 10. Через 1 год после аутовенозного ре-АББП. Ложные аневризмы проксимального дистальных анастомозов (стрелками указаны ложные аневризмы)
Fig. 10. 1 year after autovenous re-ABBP. False aneurysms of proximal distal anastomoses (arrows indicate false aneurysms)
Таким образом, проходимость аутовенозных протезов в отдаленные сроки составила 92,5 %, что подтверждалось выполнением МСКТ-ангиографии (рис. 11 А, Б).
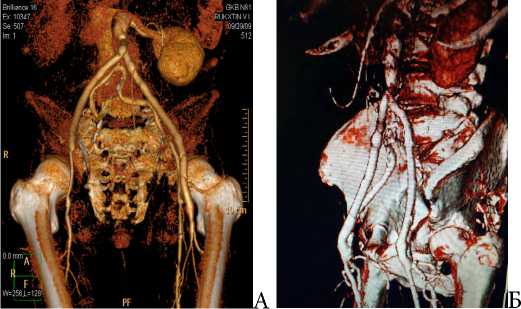
Рис. 11 А, Б . МСКТА больных через 8 и 12лет после аутовенозного ре-АББП
Fig. 11 A, B. MSCTA of patients 8 and 12 years after autovenous re-ABBP
Всего за время наблюдения в отдаленном послеоперационном периоде умерло 3 больных от причин, несвязанных с оперативным вмешательством и инфекцией: ОНМК по геморрагическому типу – 1, онкология – 1, цирроз печени – 1.
Использование в качестве бифуркационного протеза аутоматериала из поверхностных бедренных вен является рутинным в нашей клинике при замене инфицированных синтетических бифуркационных или линейных аорто-бедренных протезов.
Следует лишь подчеркнуть, что выделение брюшной аорты, а точнее шейки аневризмы характеризовалось выраженными трудностями из-за инфильтративного процесса, который распространялся на почечные и висцеральные сосуды чего мы не наблюдали при стандартных инфекциях синтетических протезов.
Заключение
Таким образом, по нашему мнению, методом выбора при инфицировании синтетических протезов и эндопротезов в аорто-подвздошно-бедренной позиции является использование принципов активного хирургического лечения, с полным удалением инфицированного синтетического протеза с одномоментной заменой in-situ аутовенозными шунтами из поверхностных бедренных вен, активной до- и послеоперационной антибиотикотерапией.
Список литературы Повторные реконструктивные операции при инфекции синтетических протезов в аорто-подвздошно-бедренной позиции
- Клиническая ангиология. Руководство для врачей. Под редакцией академика РАМН Покровского А.В. М. : Медицина, 2009. Т. 1, 2. 808 с.
- Белов Ю.В., Степаненко А.Б. Повторные реконструктивные операции на аорте и магистральных артериях. М. : МИА. 2009. 175 с.
- Щербюк А.Н., Индербиев Т.С., Ульянов Д.А., Васильев СВ. Повторные реконструктивные операции на аорте и артериях нижних конечностей. Хирургия, 2002. № 9. С. 64–69.
- Леменев В. Л., Михайлов И.П. Хирургическая тактика при инфицировании сосудистого протеза. Хирурги, 1997. № 3. С. 10–12.
- Hart J.P., Eginton M.T., Brown K.R., Seabrook G.R., Lewis B.D., Edmiston C.E., Jr., et al. Operative strategies in aortic graft infections: is complete graft excision always necessary? Ann Vasc Surg., 2005, Mar; № 19(2), рр. 154–160.
- Biro G., Szeberin Z., Nemes A., Acsady G. Cryopreserved homo-graft and autologous deep vein replacement for infrarenal aorto and iliaco-femoral graft infection: early and late results. J Cardovasc Surg (Torino), 2011, № 52(2), рр. 169–176.
- Pupka A., Skora J., Janczak D., et al. In situ revascularization with silver coated polyester prosthesis and arterial homografts in patients with aortic graft infection – a prospective, comparative, single-centre study. Europen Journal of Vascular et Endovascular Surgery, 2011, Jan; № 41(1), рp. 61–67.
- Seeger, J.M., Pretus, H.A., Welborn, M.B., Ozaki, C.K., Flynn, T.C., and Huber, T.S. Long-term outcome after treatment of aortic graft infection with staged extra-anatomic bypass grafting and aortic graft removal. (discussion 459-60). J Vasc Surg., 2000, № 32, рр. 451–459.
- McKinsey J.F. Extra-Anatomic Reconstruction. Surgical Clinics of North America, 1995, № 75, (4,5), рр. 731–740.
- Oderich, G.S., Panneton, J.M., Bower, T.C., Cherry, K.J. Jr, Rowland, C.M., Noel, A.A. et al. Infected aortic aneurysms: aggressive presentation, complicated early outcome, but durable results. J Vasc Surg., 2001, № 34, рр. 900–908.
- Frankini A.D.; Lichtenfels E.; Frankini A.; Frankini T. Extra-anatomical arterial bypass of the aortoiliac segment: 15-year experience. J. vasc. bras., 2007, vol. 6, № 3, рр. 240–210.
- Тorsello G., Sandmann W. In situ replacement of infected vascular prostheses with rifampin-soaked vascular grafts: Early results. J VAsc Surg., 1993, № 17, рр. 768–73.
- Gabriel M., Pukacki F., Dzieciuchowicz L., Oszkinis G., Checinski P. Cryopreserved arterial allografts in the treatment of prosthetic graft infections. European Journal of Vascular and Endovascular Surgery, 2004, № 27(6), рр. 590–596.
- Benjamin M.E., Cohn E.J. Jr, Purtill W.A., Hanna D.J., Lilly M.P., Flinn W.R. Arterial reconstruction with deep leg veins for the treatment of mycotic aneurysms. J Vasc Surg., 1999, Dec; № 30(6), рр. 1004–1015.
- .Argyriou C., Georgiadis G.S., Lazarides M.K., Georgakarakos E., Antoniou G.A. Endograft infection after endovascular abdominal aortic aneurysm repair: a systematic review and meta-analysis. J Endovasc Ther., 2017, № 24, рр. 688–697.
- Smeds M.R., Duncan A.A., Harlander-Locke M.P., Lawrence P.F., Lyden S., Fatima J. et al. Treatment and outcomes of aortic endograft infection. J Vasc Surg., 2016, № 63, рр. 332–340.
- Vogel T.R., Symons R., Flum D.R. The incidence and factors associated with graft infection after aortic aneurysm repair. J Vasc Surg., 2008, № 47, рр. 264–269.
- Kakkos S.K., Bicknell C.D., Tsolakis I.A., Bergqvist D. Hellenic Cooperative Group on Aortic Surgery. Editor’s Choice – Management of secondary aorto-enteric and other abdominal arterio- enteric fistulas: a review and pooled data analysis. Eur J Vasc Endovasc Surg., 2016, № 52, рр. 770–786.


