Повышение анодной устойчивости свинца легированием барием
Автор: Ганиев Изатулло Наврузович, Муллоева Нукра Мазабшоевна, Обидов Фатхулло Убайдович, Махмадуллоев Хайрулло Амонуллоевич
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Физика и электроника
Статья в выпуске: 4-1 т.15, 2013 года.
Бесплатный доступ
Потенциостатический методом исследовано анодное поведение сплавов системы Pb – Ba в среде электролита NaCl, в области концентрации бария до 0,5мас% и показано, что сплавы характеризуются повышенной коррозионной устойчивостью, чем чистый свинец.
Сплавы cвинца, стронций, электролит, потенциостатический метод, анодное поведение, коррозионная стойкость
Короткий адрес: https://sciup.org/148202260
IDR: 148202260 | УДК: 620.193
The anodic conduct stability of lead resistance of barium
Potentiyostatic methods is researched anodic the conduct of alloy systems Pb-Ba in environment electrolyte NaCl, in tract concentrations barium till 0,5mass % and showed, that alloys charactering heighten corrosion stability than clean lead.
Текст научной статьи Повышение анодной устойчивости свинца легированием барием
Коррозионное поведение сплавов определяется их химическим и фазовым составом. Фазовый состав, в свой очередь, зависит от характера физико-химического взаимодействия компонентов сплава, т.е. структуры образования (эвтектика, твердый раствор, интерметаллическое соединение и т.д.). Легирующий элемент сплава может выступить либо в роли модификатора, либо структурообразователя. Модификатор воздействует на размеры фазовых включений независимо от числа фаз в сплаве, возникающих при легировании. Щелочноземельные металлы, в частности барий, во многих сплавах выступают в роли модификатора структуры [1]. Механизм влияния модификаторов заключаются в том, что, распределяясь по границам зарождающихся при затвердевании сплава зёрен, они затрудняют собирательную рекристаллизацию (или коагуляцию фазовых составляющих) при кристаллизации сплава. Модификатор препятствует также росту зерен, укрепляет их границы и затрудняет процесс рекристаллизации в твердом состоянии, к чему склонны многие сплавы свинца. Если количества вводимого компонента превышает его предел растворимости в свинце, то могут образоваться интерметаллические соединения, т.е. в структуре сплава наряду с твёрдыми растворами предельной концентрации будут появляться новые фазы [2].
Муллоева Нукра Мазабшоевна, аспирантка.
Обидов Фатхулло Убайдович, кандидат технических наук, старший научный сотрудник.
Махмадуллоев Хайрулло Амонуллоевич, кандидат технических наук, старший научный сотрудник.
терметаллид Ва5Рb3 плавится конгруэнтно, остальные соединения инконгруэнтно. Эвтектика кристаллизуется со стороны свинца при 7 ат. % Рb и 2900С. Растворимость бария в свинце в твердом состоянии при температуре эвтектики составляет 0,8 ат.%.
На положительную роль бария в повышении защитных свойств фазового слоя на сплаве и снижении перехода свинца в раствор давно было обращено внимание [2]. Исследованиями, выполненными в среде 2н раствора серной кислоты, показано, что присутствие большего количества бария в свинце ( > 1мас%) приводит к увеличению во времени скорости анодной реакции. При указанных концентрациях бария сплавы являются двухфазными Рb + ВаРb3. Интерметаллид ВаPb3, являясь нестойким в среде серной кислоты, вызывает межкристаллидную коррозию, т.е. наблюдается преимущественное растворение этой фазы, что приводит к развитию поверхности, глубокому проникновенно коррозионных процессов и усиленному осыпанию окисленных продуктов [1].
Сплавы, содержащие <1 мас.% бария, по составу соответствуют области твердого раствора бария в свинце и являются однофазными. Для данных сплавов отмечено заметное повышение стойкости, стабильной в ходе длительной поляризации [2].
Сведений о коррозионном поведении свинца, легированного барием в нейтральной среде электролита NaCl, нами не обнаружено. Подобные сведения необходимы при разработке состава свинцовых сплавов, предназначенных в качестве защитной оболочки силовых и телефонных кабелей.
Сплавы для исследования были получены нами с учётом имеющихся в литературе данных, а также исходя из диаграммы состояния системы Pb – Ba. Сплавы содержали барий в пределах 0,005 – 5 мас.%, что предусматривало десяти- и стократное увеличение концентрации легирующего компонента в свинце и по структуре соот- ветствовали области твердого раствора бария в свинце [3].
Сплавы для исследования получали из свинца марки СО и его лигатуры с 5 мас.% бария, из которых отливались цилиндрические стрежни диаметром 8 мм и длиной 100 мм. Торцевая часть стрежня служила рабочим электродом.
Исследования выполнены в среде электролита NaCl с помощью потенциостата ПИ -50-1.1. в потенциостатическом режиме. Электродом сравнения служил хлорсеребряный, стандартным – платиновый. Скорость развёртки потенциала составляла 2мВ/с. Результаты исследования представлены в табл. 1, 2 и на рис. 1-3. В качестве примере на рис. 1 представлена полная поляризационная кривая металлического свинца, где показана последовательность снятия кривых. При электрохимических исследованиях образцы поляризовали в положительном направлении от потенциала, установившегося при погружении в исследуемый раствор (Есв. кор – потенциал свободной коррозии, или стационарный) до значения
Таблица 1. Изменение потенциала свободной коррозии сплавов системы Pb- Ba в среде электролита 0,3% - ного NaCl
|
Время, мин. |
Содержание бария в свинце, масс.% |
|||||
|
Рb |
0,005 |
0,01 |
0,05 |
0,10 |
0,50 |
|
|
0 |
0,670 |
0,680 |
0,676 |
0,662 |
0,660 |
0,650 |
|
1/8 |
0,662 |
0,656 |
0,660 |
0,654 |
0,652 |
0,648 |
|
1/4 |
0,645 |
0,643 |
0,650 |
0,642 |
0,638 |
0,632 |
|
1/2 |
0,628 |
0,635 |
0,630 |
0,624 |
0,620 |
0,616 |
|
1 |
0,614 |
0,618 |
0,615 |
0,610 |
0,600 |
0,594 |
|
2 |
0,592 |
0,600 |
0,592 |
0,588 |
0,582 |
0,580 |
|
3 |
0,584 |
0,580 |
0,574 |
0,570 |
0,566 |
0,570 |
|
4 |
0,580 |
0,572 |
0,562 |
0,556 |
0,553 |
0,548 |
|
5 |
0,573 |
0,566 |
0,548 |
0,542 |
0,538 |
0,530 |
|
10 |
0,555 |
0,560 |
0,540 |
0,536 |
0,525 |
0,522 |
|
15 |
0,550 |
0,557 |
0,535 |
0,534 |
0,520 |
0,516 |
|
20 |
0,548 |
0,550 |
0,530 |
0,526 |
0,516 |
0,508 |
|
30 |
0,546 |
0,544 |
0,528 |
0,520 |
0,514 |
0,505 |
|
40 |
0,545 |
0,540 |
0,525 |
0,518 |
0,510 |
0,500 |
|
50 |
0,543 |
0,536 |
0,522 |
0,516 |
0,510 |
0,500 |
|
60 |
0,543 |
0,536 |
0,522 |
0,516 |
0,510 |
0,500 |
Таблица 2. Корозионно-электрохимические характеристики сплавов системы Pb-Ba в среде электролита NaCl. Скорость развёртки потенциала 2мВ/с
|
гЗ о |
Содержание Ва, мас. % |
Электрохимические свойства |
Скорость коррозии |
||||
|
-Есв.корр. |
-Екорр. |
-Еп.о. |
-Ереп. |
Iкор• 10-2 |
К ∙10-3 |
||
|
В |
А/м2 |
г/м2∙час |
|||||
|
§2 |
- |
0,524 |
0,716 |
0,380 |
0,450 |
0,80 |
15,44 |
|
0,005 |
0,512 |
0,714 |
0,340 |
0,420 |
0,71 |
13,70 |
|
|
0,01 |
0,484 |
0,680 |
0,330 |
0,415 |
0,57 |
11,00 |
|
|
0,05 |
0,464 |
0,672 |
0,310 |
0,400 |
0,54 |
10,42 |
|
|
0,10 |
0,442 |
0,650 |
0,300 |
0,400 |
0,45 |
8,68 |
|
|
0,50 |
0,428 |
0,630 |
0,280 |
0,360 |
0,40 |
7,72 |
|
|
o' |
- |
0,543 |
0,720 |
0,420 |
0,510 |
0,85 |
16,40 |
|
0,005 |
0,536 |
0,720 |
0,380 |
0,435 |
0,74 |
14,28 |
|
|
0,01 |
0,522 |
0,714 |
0,360 |
0,420 |
0,60 |
11,58 |
|
|
0,05 |
0,516 |
0,710 |
0,340 |
0,412 |
0,56 |
10,80 |
|
|
0,10 |
0,510 |
0,700 |
0,340 |
0,410 |
0,48 |
9,26 |
|
|
0,50 |
0,500 |
0,686 |
0,320 |
0,400 |
0,43 |
8,30 |
|
|
- |
0,562 |
0,780 |
0,450 |
0,548 |
0,98 |
18,91 |
|
|
0,005 |
0,560 |
0,740 |
0,400 |
0,450 |
0,86 |
16,60 |
|
|
0,01 |
0,550 |
0,734 |
0,380 |
0,440 |
0,65 |
12,55 |
|
|
0,05 |
0,546 |
0,725 |
0, 360 |
0,430 |
0,60 |
11,58 |
|
|
0,10 |
0,530 |
0,712 |
0,340 |
0,430 |
0,52 |
10,04 |
|
|
0,50 |
0,524 |
0,700 |
0,340 |
0,420 |
047 |
9,07 |
|
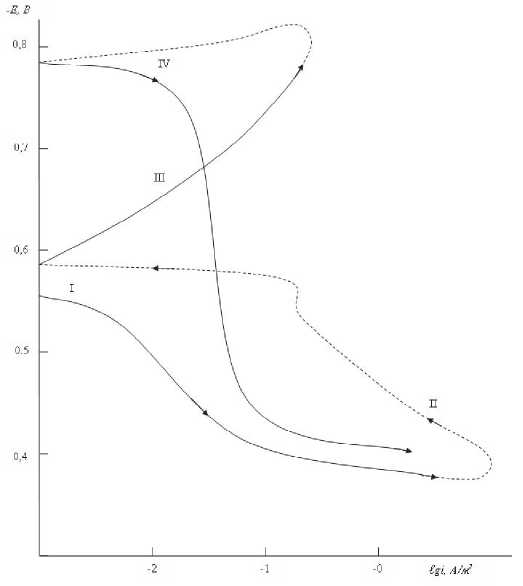
Рис. 1. Полная поляризационная кривая чистого свинца в среде электролита 3% NaCl (Скорость развёртки потенциала 2мВ’”сек-1) потенциала, при котором происходит резкое возрастание тока растворения (кривая I). Затем образцы поляризовали в обратном направлении до потенциала -0,8В, в результате чего происходило подщелачивание приэлектродного слоя поверхности сплава и удаление оксидного слоя (кривые II и III). Наконец, образцы повторно поляризовали в положительном направлении (кривая IV), при этом определялись потенциалы коррозии (Екорр), питтингообразования (Еп.о) и репассивации (Ер.п.) [4].
Зависимость потенциала свободной коррозии сплавов системы Pb – Ва в среде электролита NaCl
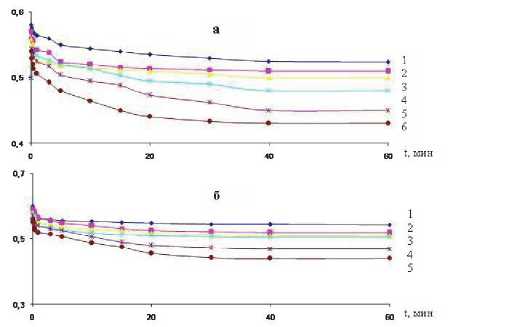
Рис. 2. Временная зависимость потенциала свободной коррозии сплавов системы Pb-Ba, содержащих бария, масс. %:
1-0,0; 2-0,005; 3-0,01; 4-0,05; 5-0,1; 6-0,5;
в средах 0,03% NaCl (а) и 3% NaCl (б)
представлена на рис. 1 и в табл. 1. Видно, что как для свинца, так и для сплавов с различным содержанием бария наблюдается смещение потенциала в положительную область по мере выдержки в среде электролита. Наибольший сдвиг величины потенциала происходит в первые 5-10 минут от начала погружения, что свидетельствует о динамике формирования защитного оксидного слоя на поверхности образца, которое завершается к 20-й…30-й минуте после погружения электрода в электролит. Добавки бария к свинцу незначительно сдвигают его потенциал свободной коррозии в положительную область, т.е. при увеличении содержании легирующего компонента наблюдается монотонный рост величины потенциала свободной коррозии сплавов во всех исследованных средах (табл. 1, рис. 2).
Коррозионно-электрохимические характеристики сплавов системы Pb-Ba в среде электролита NaСl представлены в табл. 2. Потенциалы
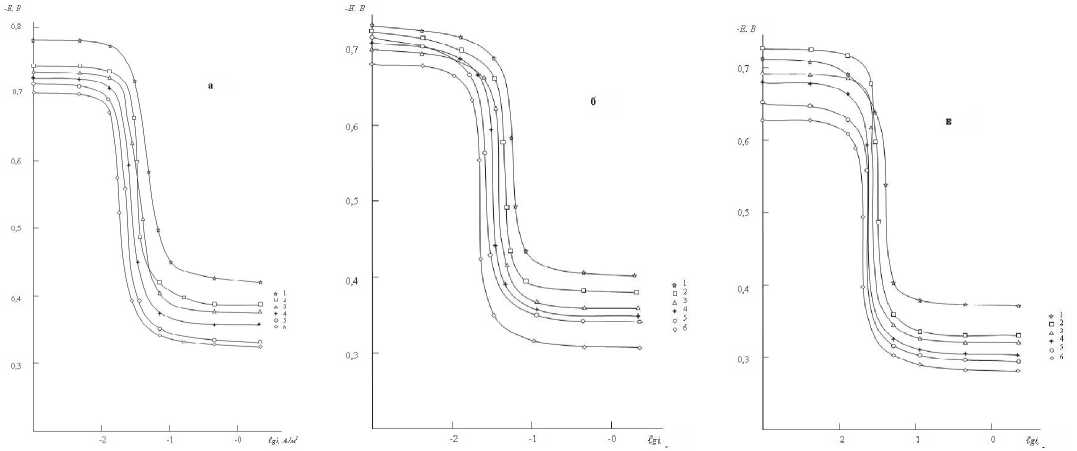
Рис. 3. Анодные ветви потенциодинамических кривых сплавов ситемы Pb-Ва, содержащих бария, масс.%: 1-0,0; 2-0,05; 3-0,01; 4-0,05; 5-0,1; 6-0,5 при скорости развёртки потенциала 2мВ’”сек ,-1 в средах 3% NaCl (а) 0,3% NaCl (б) и 0,03,% NaCl(в)
коррозии, питтингообразования и репассивации с ростом концентрации бария в свинце смещаются в положительную область. Данная зависимость имеет место во всех исследованных средах 0,03; 0,3 и 3,0% NaCl. Добавки бария почти в два раза снижают скорость коррозии свинца в исследованных средах. При увеличении концентрации бария до 0,5 мас. % монотонно снижается скорость коррозии свинца.
Данный факт свидетельствует о том, что предельная растворимость бария в свинце может превышать 0,5 мас. %, т.к. при переходе границы растворимости обычно наблюдается скачкообразное изменение физико- химических свойств сплавов.
Анодные ветви потенциадинамики кривых сплавов системы Pb- Ba представлены на рис. 3. Кривые, относящиеся к сплавам располагаются левее от кривых свинца во всех исследованных средах, что свидетельствует о снижении скорости анодной коррозии при легировании свинца барием.
С ростом концентрации хлор ионов наблюдается некоторый рост скорости коррозии свинца и сплавов. Ускоряющее действие ионов хлора на коррозию свинца связывают с их адсорбцией, что может привести к образованию на поверхно- сти и в порах внешнего слоя фазовых окислов адсорбированных комплексов типа PbСl4, оксихлорида PbOCl2, кислот Н[PbCl3], Н2[PbCl6 ] или их солей Pb[PbCl3], Pb[PbCl6] [2].
Адсорбированные комплексы, устраняя пассивирующее действие кислорода, могут легко терять связь с основой электролита и переходить в приэлектродный слой.
Таким образом, улучшение коррозионной стойкости свинца при легировании барием объясняется его модифицирующим действием на структуру твердого раствора на основе свинца, а также увеличением истинной поверхности анода или же уплотнением защитного фазового слоя окислов малорастворимыми продуктами окисления.
Список литературы Повышение анодной устойчивости свинца легированием барием
- Ганиев И.Н., Порхутик П.А., Вахобов А.В., Куприянова А.В. Модифицирование силуминов стронцием. Минск: Наука и техника, 1985. 152 с.
- Дунаев Ю.Д. Нерастворимые аноды из сплавов на основе свинца. Алма-Ата: Наука, 1978. 316 с.
- Вахобов А.В., Ганиев И.Н. Диаграммы состояния двойных и тройных систем с участием бария и стронция. Душанбе: Дониш, 1992. 296 с.
- Умарова Т.М., Ганиев И.Н. Анодные сплавы алюминия с марганцем, железом и редкоземельными металлами. Душанбе: Дониш, 2009. 232 с.


