ПОВЫШЕНИЕ ДОСТОВЕРНОСТИ МЕТОДА ПЛАВЛЕНИЯ ДНК ПУТЕМ ПРОВЕДЕНИЯ ПОВТОРНЫХ АНАЛИЗОВ
Автор: Д. А. Белов, Ю. В. Белов, А. Н. Зубик, В. Е. Курочкин
Журнал: Научное приборостроение @nauchnoe-priborostroenie
Рубрика: Физика и химия приборостроения
Статья в выпуске: 4 т.32, 2022 года.
Бесплатный доступ
В статье изучена возможность использования повторных анализов методом плавления ДНК для повышения их достоверности, а именно уменьшения погрешности определения температуры плавления ДНК Tm. Экспериментально выявлено статистически значимое различие значений Tm анализируемых образцов в последовательно проведенных анализах, препятствующее повышению достоверности. Показано, что увеличение температуры плавления Tm в проведенной серии экспериментов в среднем на 0.12 град. обусловлено испарением 1.65% воды из пробирки. Экспериментально выявлено изменение массы на 0.8 ± 0.1% от общей массы воды в пробирках в результате теплового режима, аналогичного анализу методом плавления, что частично подтверждает предположение. Рекомендовано при повторных анализах методом плавления ДНК учитывать этот эффект и реализовывать мероприятия, препятствующие испарению воды. Приведены аналитические выражения для относительной оценки изменения концентрации ионов натрия и объема воды в пробе.
Метод плавления ДНК, HRMA, испарение
Короткий адрес: https://sciup.org/142235502
IDR: 142235502 | УДК: 543.426; 543.9 | DOI: 10.18358/np-32-4-i1119
INCREASING THE DNA MELTING METHOD VALIDITY BY RE-ANALYSIS IMPLEMENTATION
The article explores the possibility of using repeated analyses based on the DNA melting method to increase their validity, namely, to reduce the error in determining the DNA melting temperature Tm. A statistically significant difference in the Tm values of the analyzed samples in successive analyses was experimentally revealed, which prevents the validity increase. It is shown that an increase in the temperature Tm on average by 0.12 deg. in the series of experiments is due to the evaporation of 1.65% of water from the test tube. A change in mass by 0.8 ± 0.1% of the total mass of water in test tubes was experimentally revealed as a result of a thermal regime similar to the analysis by the melting method, which partially confirms the assumption. It is recommended to take into account this effect during re-analyses using the DNA melting method and to implement measures that prevent water evaporation. Analytical expressions are given for the relative assessment of the sodium ion concentration changes and the water volume in the sample.
Текст статьи ПОВЫШЕНИЕ ДОСТОВЕРНОСТИ МЕТОДА ПЛАВЛЕНИЯ ДНК ПУТЕМ ПРОВЕДЕНИЯ ПОВТОРНЫХ АНАЛИЗОВ
Современный метод плавления ДНК выполняется после полимеразной цепной реакции в реальном времени (ПЦР-РВ) на детектирующих амплификаторах, при этом для генерации флуоресцентного сигнала используются интеркали-рующие красители, молекулы которых присоединяются к двойной цепи ДНК. При повышении температуры двойная цепь ДНК постепенно распадается на две одноцепочечные молекулы, вызывая отсоединение молекул красителя и спад интенсивности флуоресценции [1].
Графики плавления ДНК (ГП) представляют собой зависимости флуоресцентного отклика пробы от температуры и отличаются друг от друга формой и значением температуры плавления T m , что позволяет определять различия во фрагментах ДНК по их составу, длине и статусу метилирования и применять метод во множестве прикладных задач, таких как геномное сканирование, генотипирование, сопоставление последовательностей и эпигенетические исследования [2].
Значение Tm соответствует температуре, при которой 50% нуклеотидов в молекулах ДНК теряют водородные связи [3], и традиционно определяется как координата точки перегиба ГП, что соответствует значению максимума отрицательной производной ГП по температуре [4]. В ряде задач требуется высокая точность определения температуры Tm, например, для достоверного генотипиро- вания штаммов M. tuberculosis необходимо выявлять различия в значениях Tm менее 0.1 град. [5].
С целью уменьшения погрешности измерения температуры T m применяются известные методики, основанные на фильтрации и/или аппроксимации ГП различными непрерывными функциями, например полиномом третьей степени в ограниченном диапазоне изменения температуры, как в программе ANK_Melting [6], или усовершенствованной сигмоидальной функцией (СФ) [7]. В статьях [8–10] рекомендуется после предварительной нормализации выполнять численное дифференцирование графиков плавления с помощью полиномов Савицкого – Голея второй степени в каждой точке [11].
Метод плавления ДНК является неразрушающим, поэтому одним из дополнительных способов повышения достоверности результатов анализа может быть повторение экспериментов для накопления статистики. В настоящей статье рассматривается возможность применения такого подхода.
ПОЛУЧЕНИЕ И ОБРАБОТКА ИСХОДНЫХ ДАННЫХ
Для получения исходных данных выполнен трехкратный анализ методом плавления ДНК трех известных образцов ампликонов цитокератина (CK-19) на анализаторе нуклеиновых кислот АНК-32, который серийно выпускается в Институте аналитического приборостроения РАН (Россия). Ампликоны были получены в результате 50 циклов ПЦР-РВ с интеркалирующим красителем SYBR Green I ("ПЦР-Микс" М-427, ООО "Синтол", Россия) и специально разработанными праймерами (ООО "ДНК-Синтез", Россия). Образцы 1, 2 и 3 в четырех пробирках каждый анализирова- лись в диапазоне температур 70–95 °C с шагом 0.5 град. и длительностью выдержки на каждом шаге 30 с. Образцы 1, 2 и 3 имеют соответственно содержание нуклеотидов гуанина и цитозина во фрагменте ДНК [G + C], равное 53, 59 и 58% при длине фрагментов Lp, равной 103, 209 и 309 пар нуклеотидов (п. н.). Начальная концентрация ионов натрия во всех пробах равна 0.125 моль/л.
Табл. 1. Значения температур плавления анализируемых образцов (°C)
|
№ эксперимента |
№ образца |
||
|
1 |
2 |
3 |
|
|
1 |
84.37 ± 0.04 |
90.55 ± 0.10 |
90.72 ± 0.08 |
|
2 |
84.53 ± 0.05 |
90.68 ± 0.09 |
90.85 ± 0.06 |
|
3 |
84.65 ± 0.09 |
90.83 ± 0.12 |
90.98 ± 0.06 |
Примечание . Уровень значимости 0.05, объем выборки 4
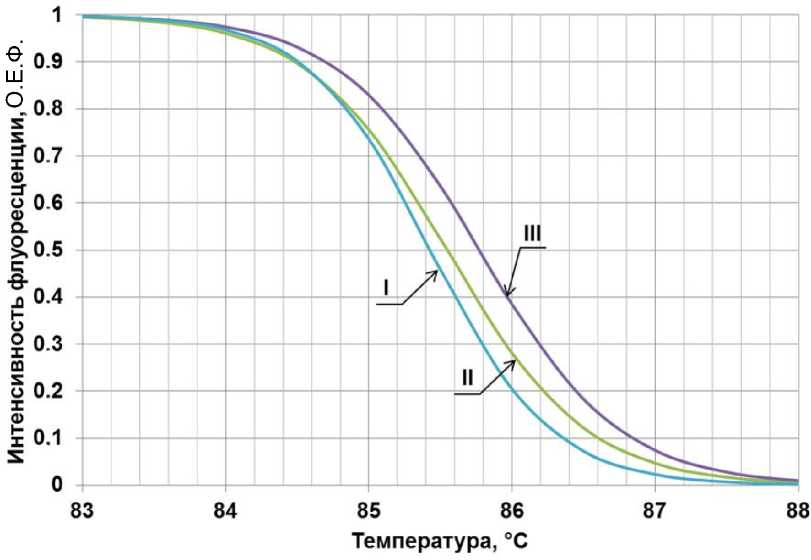
Рис. Графики плавления образца 1 по результатам первого (I), второго (II) и третьего (III) анализов
Значения температур плавления образцов были определены путем применения методики на основе СФ [7]. В табл. 1 приведены средние значения температур плавления трех образцов в трех последовательных анализах.
На рисунке изображены графики плавления от одной пробирки с образцом 1, полученные в результате трех последовательных анализов после нормализации модельной функцией СФ. Графики позволяют наглядно сравнить различия значений T m , соответствующих температуре, при которой интенсивность флуоресценции равна 0.5. Видно, что при каждом следующем анализе значение Tm увеличивается.
На основе вычисленных значений парного t-критерия Стьюдента выявлено статически значимое различие между результатами последовательных экспериментов с уровнем значимости р < 0.05. Эти различия не позволяют использовать повторные анализы методом плавления ДНК для увеличения их достоверности. Актуальным является определение причин изменения значений T m образцов при повторных анализах.
ПРИЧИНЫ ИЗМЕНЕНИЯ ТЕМПЕРАТУР ПЛАВЛЕНИЯ ОБРАЗЦОВ ПРИ ПОВТОРНЫХ АНАЛИЗАХ
В соответствии с работой [12], значение T m определяется по формуле:
T m = 81.5 + 16.6 • lg[Na + ] +
+ 0.41 • [ G + C ] - 675 / L p , (1)
где [Na+] — концентрация ионов натрия, моль/л.
Слагаемое 16.6∙lg [Na+] включено и в другие известные модели [13, 14].
Изменение значений T m может быть обусловлено испарением воды из анализируемой пробы. Так как значения [ G + C ] и L p из формулы (1) остаются постоянными, изменение значений Tm сопровождается увеличением концентрации ионов натрия [Na+].
Сравнение существующих моделей для вычисления температуры плавления ДНК показало значительное расхождение результатов применения моделей с экспериментальными данными [15]. В статьях [16, 17] предложено применять модели, учитывающие зависимость температуры Tm только от факторов, величина которых изменяется в серии экспериментов. Авторы представили формулу (1) в виде упрощенной модели:
T m = T - "Л + 0.41 • [ G + C ]. (2) Lp
Здесь значение параметра Т 1 равно сумме 81.5 + 16.6∙lg([Na+]) .
В табл. 2 приведены вычисленные параметры T 1 и различия параметров T 1 , определенных при повторных анализах. В столбце d103 находятся: значение 0.08 — это разность параметров T 1 при втором и первом анализах образца 1, значение 0.11 этой разницы при третьем и втором анализах и значение 0.19 — при третьем и первом анализах. Аналогично определены изменения параметров T 1 в столбцах d209 и d309 для образцов 2 и 3 (d209 и d309 соответственно).
Изменения параметров T 1 для образцов 1, 2 и 3 после проведения трех анализов направлены в сторону увеличения Т 1 : 0.19; 0.27 и 0.26 град. соответственно. Среднее изменение температуры T m между последовательными анализами составило 0.12 град.
Начальная концентрация натрия во всех пробах равна 0.125 моль/л, что соответствует: 16.6∙lg[0.125] = T 1 – 81.5. Увеличение концентрации натрия на 2% вызывает увеличение параметра T m на 0.14 град. Следовательно, испарение воды в пробирке и увеличение концентрации натрия составляют примерно 2%.
Для проверки этого предположения проанализировано изменение массы заполненных дистиллированной водой тонкостенных пробирок на 0.2 мл (SSI, США) до и после нагрева. 32 пробирки (4 стрипа по 8 шт.) заполняли дистиллированной водой по 25 мкл, закрывали крышки и выдерживали в эксикаторе для удаления мелких капель воды с внешней поверхности пробирок. Нагрев проводили в АНК-32 по программе плавления от 70 °С до 95 °С с шагом 0.5 град. и продолжительностью 30 с на каждой температуре. Взвешивание до и после нагрева, а также до и после заполнения водой
Табл. 2. Различия параметров T 1 при проведении повторных анализов (°С)
|
№ анализа |
103 |
d103 |
209 |
d209 |
309 |
d309 |
|
1 |
69.09 |
0.08 |
69.83 |
0.12 |
69.15 |
0.13 |
|
2 |
69.20 |
0.11 |
69.95 |
0.16 |
69.28 |
0.13 |
|
3 |
69.28 |
0.19 |
70.11 |
0.27 |
69.41 |
0.26 |
(для определения суммарной массы воды) проводили на аналитических весах высшего I специального класса точности (ЗАО "САРТОГОСМ", Россия), дискретность измерений которых составляет d = 0.1 мг, предельно допустимая погрешность e = = 1 мг.
Эксперимент проводили на трех сериях образцов. Итоговое изменение массы 32 пробирок после нагрева составило 6.0 ± 0.5 мг (n = 3), что соответствовало 0.8 ± 0.1% от общей массы воды в пробирках.
Чтобы удостоверится, что полученный результат действительно связан с испарением воды через закрытую крышку пробирки, дополнительную серию из 32 пробирок заполнили водой с минеральным маслом (25 мкл воды и 15 мкл масла). Изменение массы таких пробирок после нагрева было сопоставимо с погрешностью весов и составило 0.5 мкл (0.06% от расчетной массы воды).
ОЦЕНКА ИЗМЕНЕНИЯ КОНЦЕНТРАЦИИ ИОНОВ НАТРИЯ
В соответствии с формулой (1) при неизменных параметрах [ G + C ] и L p изменение температуры плавления образца определяется следующим образом:
A T m = 16.6 - lg( A [Na + ]), (3)
где A [Na+ ] — изменение концентрации ионов натрия в пробе.
Отсюда:
A T m
A [Na + ] = (10 16.6 - 1) - 100%. (4)
Долю испарившейся воды A VH2O оценить по следующей формуле:
V
A V H2o = (1-- H^ ) - 100%.
2 m
10 16.6
можно
С помощью формул (4) и (5) можно более точно оценить значения A [Na + ] и A V HO , соответствующие среднему изменению температуры T m на 0.12 град. в проведенной серии экспериментов: A [Na + ] = 1.68%, A V HzO = 1.65%.
ЗАКЛЮЧЕНИЕ
Использование повторных анализов методом плавления ДНК для увеличения их достоверности, а именно уменьшения погрешности температуры плавления ДНК Tm, затруднено вследствие изме- нения значений Tm с каждым повтором. Для успешного использования описанного подхода необходимо предотвратить процесс испарения воды из пробы, однако полностью исключить испарение является сложной задачей [18].
В проведенной серии экспериментов выявлено среднее увеличение значений T m на 0.12 град., что объясняется увеличением концентрации ионов натрия на 1.68% и уменьшением объема воды на 1.65%. Изменение массы 32 пробирок с водой в результате теплового режима, аналогичного анализу методом плавления, составило 0.8 ± 0.1% от общей массы воды в пробирках, что частично подтверждает предположение.
Выявление различий температур плавления образцов может использоваться для оценки количества испарившейся воды в емкостях, где оценка другими способами, как путем измерения массы пробы, затруднена или невозможна. Примером таких емкостей являются микрофлюидные чипы.
Работа выполнена в ИАП РАН в рамках государственного задания № 075-00761-22-00 Министерства науки и высшего образования РФ.
Список литературы ПОВЫШЕНИЕ ДОСТОВЕРНОСТИ МЕТОДА ПЛАВЛЕНИЯ ДНК ПУТЕМ ПРОВЕДЕНИЯ ПОВТОРНЫХ АНАЛИЗОВ
- 1. Ririe K.M., Rasmussen R.P., Wittwer C.T. Product differentiation by analysis of DNA melting curves during the
- polymerase chain reaction // Anal Biochem. 1997. Vol. 245, is. 2. P. 154–160. DOI: 10.1006/abio.1996.9916
- 2. Montgomery J.L., Sanford L.N., Wittwer C.T. Highresolution DNA melting analysis in clinical research and diagnostics // Expert Rev Mol Diagn. 2010. Vol. 10, is. 2. P. 219–240. DOI: 10.1586/erm.09.84
- 3. Wright T.A., Stewart J.M., Page R.C., Konkolewicz D. Extraction of thermodynamic parameters of protein unfolding using parallelized differential scanning fluorimetry // J Phys Chem Lett. 2017. Vol. 8, is. 3. P. 553–558. DOI: 10.1021/acs.jpclett.6b02894
- 4. Веденов А.А., Дыхне А.М., Франк-Каменецкий М.Д. Переход спираль – клубок в ДНК // Успехи физических наук. 1971. Т. 105, № 11. С. 479–519. DOI: 10.3367/UFNr.0105.197111d.0479
- 5. Pholwat S., Liu J., Stroup S. et al. Integrated microfluidic card with TaqMan probes and high-resolution melt analysis to detect tuberculosis drug resistance mutations across 10 genes // mBio. 2015. Vol. 6, is. 2. e02273. DOI: 10.1128/mBio.02273-14
- 6. Альдекеева А.С., Белов Д.А., Белов Ю.В., Широкорад А.Л. Разработка экспериментальной версии программного обеспечения на основе новой методики определения температуры плавления ДНК // Научное приборостроение. 2019. Т. 29, № 2. С. 22–29. DOI: 10.18358/np-29-2-i2229
- 7. Белов Д.А., Корнева Н.А., Альдекеева А.C., Белов Ю.В., Киселев И.Г. Повышение разрешающей способности генетических анализаторов при определении температуры плавления ДНК // Научное приборостроение. 2016. Т. 26, № 2. С. 17–22. URL: http://213.170.69.26/mag/2016/abst2.php#abst2
- 8. Wittwer C.T., Reed G.H., Gundry C.N., Vandersteen J.G., Pryor R.J. High-resolution genotyping by amplicon melting analysis using LCGreen // Clinical Chemistry. 2003. Vol. 49, is. 6. P. 853–860. DOI: 10.1373/49.6.853
- 9. Gundry C.N., Vandersteen J.G., Reed G.H., et al. Amplicon melting analysis with labeled primers: A closed-tube
- method for differentiating homozygotes and heterozygotes // Clinical Chemistry. 2003. Vol. 49, is. 3. P. 396–406. DOI: 10.1373/49.3.396
- 10. Herrmann M., Durtschi J., Bromley L., Wittwer C., Voelkerding K. Amplicon DNA melting analysis for mutation scanning and genotyping: Cross-platform comparison of instruments and dyes // Clinical chemistry. 2006. Vol. 52, is. 3. P. 494–503. DOI: 10.1373/clinchem.2005.063438
- 11. Press W.H., Teukolsky S.A., Vetterling W.T., Flannery B.P. Numerical recipes in C. 2nd ed., 1992. Cambridge University Press, New York. 994 p.
- 12. Календарь Р.Н., Сиволап Ю.М. Полимеразная цепная реакция с произвольными праймерами // Biopolymers and cell. 1995. Т. 11, № 3-4. С. 55–65. URL: https://www.elibrary.ru/item.asp?id=23336409
- 13. Howley P.M., Israel M.F., Law M.-F., Martin M.A. A rapid method for detecting and mapping homology between heterologous DNAs. Evaluation of polyomavirus genomes // J. Biol. Chem. 1979. Vol. 254, is. 11. P. 4876–4883. DOI: 10.1016/S0021-9258(17)30093-5
- 14. SantaLucia J., Allawi H.T., Seneviratne P.A. Improved nearest-neighbor parameters for predicting DNA duplex stability // Biochemistry. 1996. Vol. 35, is. 11. P. 3555–3562. DOI: 10.1021/bi951907q
- 15. Panjkovich A., Melo F. Comparison of different melting temperature calculation methods for short DNA sequences // Bioinformatics. 2005. Vol. 21, is. 6. P. 711–722. DOI: 10.1093/bioinformatics/bti066
- 16. Курочкин В.Е., Белов Д.А., Белов Ю.В., Зубик А.Н. Определение модельных констант при вычислении температуры плавления ДНК // Научное приборостроение. 2020. Т. 30, № 2. С. 10–16. DOI: 10.18358/np-30-2-i1016
- 17. Belov D.A., Belov Yu.V., Kiselev I.G. Modeling of the DNA melting point dependence on various analysis factors // IEEE 2020 International Multi-Conference on Industrial Engineering and Modern Technologies (FarEastCon). 2020. P. 1–3. DOI: 10.1109/FarEastCon50210.2020.9271634
- 18. Polini A., Mele E., Sciancalepore A.G., et al. Reduction of water evaporation in polymerase chain reaction microfluidic devices based on oscillating-flow // Biomicrofluidics. 2010. Vol. 4, is. 3. Id. 036502. DOI: 10.1063/1.3481776


