Повышение эффективности распознавания желудочно-кишечных заболеваний в автоматическом режиме на основе анализа изображений эндоскопической капсулы
Автор: Жуков Игорь Юрьевич, Михайлов Дмитрий Михайлович, Федоров Евгений Дмитриевич, Иванова Екатерина Викторовна, Кукушкин Александр Викторович, Стариковский Андрей Викторович, Толстая Анастасия Михайловна
Журнал: Спецтехника и связь @st-s
Статья в выпуске: 3, 2013 года.
Бесплатный доступ
Данная статья посвящена описанию модулей, повышающих эффективность распознавания патологий и морфологических изменений в желудочно-кишечном тракте по изображениям, полученным с беспроводной эндоскопической капсулы. В основе метода распознавания кровотечений лежит пиксельный анализ изображения. По специальной классификационной системе, зависящей от интенсивности кровотечения, принимается решение о наличии или отсутствии кровотечения в рассматриваемом участке ЖКТ. Обнаружение полипов происходит посредствам анализа выпуклости поверхности. Строятся 3D картины, измеряется кривизна поверхности. В результате отбора получаются элементы, которые превышают заранее заданную границу. Это означает, что в исходном изображении в точке, соответствующей этому элементу, находится полип.
Капсульная эндоскопия, кровотечение, полип, яркость, насыщенность, пиксель, анализ, кривизна
Короткий адрес: https://sciup.org/14967165
IDR: 14967165
Текст научной статьи Повышение эффективности распознавания желудочно-кишечных заболеваний в автоматическом режиме на основе анализа изображений эндоскопической капсулы
Беспроводная капсульная эндоскопия – это современный метод диагностики желудочно-кишечного тракта (ЖКТ) человека, позволяющий визуализировать области, недоступные для традиционных методов исследования. Автоматический анализ гастроэнтерологического тракта и его болезней представляет большой интерес благодаря его потенциалу в распознавании патологий и морфологических изменений.
У беспроводной эндоскопии есть важное преимущество по сравнению с традиционной – капсула может достичь двенадцатиперстной и тонкой кишки, не доставляя при этом дискомфорта пациенту. Более того, это единственный неинвазивный метод осмотра тонкой кишки [1, 2].
Исследование проводится следующим образом: пациент проглатывает маленькую капсулу 11х26 мм со встроенной видеокамерой, которая медленно проходит сквозь желудочно-кишечный тракт, захватывая изображения со скоростью два кадра в секунду.
Полученные изображения передаются на переносной жесткий диск, находящийся у пациента на поясе, с исполь- зованием специальных систем и протоколов передачи изображений с эндоскопической капсулы. Вся процедура длится около 8 ч, в течение которых пациент может заниматься обычными повседневными делами [3].
За это время запоминающее устройство накапливает более 57 тысяч изображений, которые по окончании исследования передаются на стационарный компьютер для дальнейшего анализа. Обычно на просмотр изображений врач-гастроэнтеролог тратит около 2 ч. Чтобы уменьшить это время, в программу, через которую врач просматривает эти изображения, встраиваются модули автоматического распознавания патологий [4].
Данная статья посвящена описанию модулей, определяющих наличие полипов и кровотечений в желудочно-кишечном тракте человека в автоматическом режиме. Модули представляют собой наборы функций и структур данных на языке программирования, которые принимают на вход изображение участка ЖКТ, анализируют его и выдают информацию о том, есть ли на данном участке аномалия или нет. Эти математические алгоритмы позволяю повысить эффективность распознавания желудочно-кишечных заболеваний в автоматическом режиме на основе анализа изображений эндоскопической капсулы, значительно сократив время обработки информации врачом-эндоскопистом.
В перспективе планируется усовершенствование описанных алгоритмов для определения других видов патологических и морфологических изменений в желудочно-кишечном тракте человека.
Распознавание полипов в ЖКТ
Предположим, что имеется цветное изображение, полученное эндоскопической капсулой, которое содержит полип. Оно переводится в черно-белую цветовую схему. В результате этой операции получается изображение, приближенное к тому, что приведено на рис. 1 .
Математическая модель подразумевает, что полип является выпуклостью по отношению к окружающему лан-

Рис. 1. Предполагаемая приближенная модель полипа
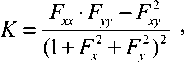
от того, как расстояния измеряются на поверхности.
В результате формируются два двумерных массива G (Gaussian) и M (Mean) размерностью m×n ( m – количество пикселей в исходном изображении по горизонтали; n – по вертикали). Элементами массива G(i,j) являются значения гауссовской кривизны в точках ( i , j ). Аналогично для массива M .
Значение массива G тем больше, чем сильнее изогнута поверхность. Значение массива M положительно, если поверхность выпуклая, и отрицательно, если поверхность вогнута [6]. Из полученных массивов G и M формируется массив P (Polyp Curvature), элементы которого определяются по следующему закону:
P(i,j) = –G(i,j) × min(0; M(i,j)). (2)
Если какой-то элемент массива P превышает заранее заданную границу α, то это означает, что в исходном изображении в точке, соответствующей этому элементу, находится полип.
Однако в реальном случае при переводе цветовой схемы изображения в черно-белую становится заметно так называемое «зерно» или «шум». Это очень часто чередующиеся точки со сравнительно большим и маленьким значением яркости. При переводе в трехмерную модель эти точки превратятся в ступень с очень большой разницей по высоте, что, в свою очередь, скажется на вычисленной кривизне. Подобное зерно может привести к обнаружению полипа там, где его на самом деле нет. Чтобы это предотвратить, используется сглаживание (Gaussian Blur). Оно применяется как к исходному изображению, так и к массивам производных, необходимых для вычисления кривизны [7]. Для сглаживания изображения и его производных экспериментально определены радиусы rI и rdI . Использовались значения:
rI = 3; rdI = 27; α = 0,9.
Метод распознавания полипов в желудочно-кишечном тракте был экспериментально проверен на материалах тестируемой выборки. Были проанализированы 76 изображений, из которых 26 содержали полипы и 50 без признаков патологии. В результате эксперимента была выявлена следующая неточность:
-
♦ на 4 изображениях из тестируемой выборки, содержащих полипы, алгоритм их не выявил;
-
♦ на 5 изображениях алгоритм выявил наличие полипа, хотя его там не было.
На точность выполнения алгоритма влияет качество камеры, принимающей изображение ЖКТ.
С учетом описанных ограничений был реализован программный модуль, обнаруживающий выпуклости на снимках с беспроводной эндоскопической капсулы и показывающий их местоположение на снимке. В результате значительно сокращается время поиска полипов желудочно-кишечном тракте пациента.
Распознавание кровотечений в ЖКТ
Предлагаемый метод распознавания кровоточащих областей разделен на два основных шага. Первый шаг разделяет фрагменты видео, содержащие признаки кровотечения, от не содержащих. На втором шаге происходит дальнейший анализ изображений кровотечений, подтверждающий, действительно ли данные изображения содержат признаки активного кровотечения.
При просмотре гастроэнтерологических изображений наиболее характерный признак, определяющий присутствие кровотечения, – это яркий красный цвет или присутствие темнокрасных областей [8]. Важно отметить, что в большей части желудочно-кишечного тракта превалирует красный цвет. Но красные оттенки в некровоточащих участках имеют меньшую цветовую насыщенность, чем в кровоточащих. Таким образом, автоматическое распознавание кровоточащих областей можно свести к распознаванию участков изображения с насыщенным красным цветом.
Цветовую насыщенность и оттенок можно легко узнать, преобразив цветовую схему изображения в HSV (Hue, Saturation, Value – тон, насыщенность, значение). Цвета, превалирующие в кишечнике, варьируются от оранжевого до желто-зеленого из-за присутствия остатков фекалий, что делает
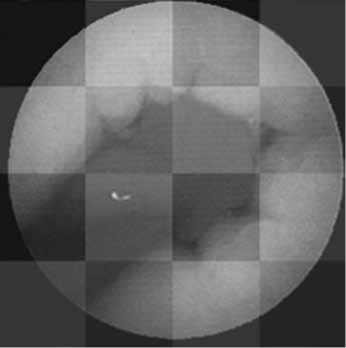
Рис. 2. Изображение, разбитое на блоки

Рис. 3. Блоки с подсчитанными значениями средней цветовой насыщенности по насыщенности блок из двенадцати оставшихся (B2–min). Блок с наименьшей насыщенностью не рассматривается, так как обычно он соответствует просвету в желудочно-кишечном тракте, через который продвигается капсула. Изображение распознается как содержащее кровотечение, если хотя бы один блок, содержащий кровь, удовлетворяет следующему условию.
Кровотечение есть:
Is(Bi) > Is (B2–min) + m, где Is – среднее значение цветовой насыщенности в блоке, а m – граница надежности. Во время тестирования она устанавливалась равной 0,15.
В случае несоответствия изображения данному условию можно считать, что кровотечения оно не содержит. Для иллюстрации на рис. 3 приведена визуализация цветовой насыщенности в каждом блоке исходного изображения. Чем блок светлее, тем цветовая насыщенность пикселей, содержащихся в нем, больше.
Блок, соответствующий Is ( B2–min ), отмечен белой рамкой.
Однако некоторые изображения, не содержащие реальных признаков кровотечения, могут быть ошибочно классифицированы как содержащие кровотечение. Далее они будут перепроверены, а их статус пересмотрен.
На втором шаге рассматриваются только те эндоскопические изобра-

Рис. 4. Иллюстрация второго шага распознавания: белые пиксели соответствуют кровотечению жения, которые были помечены как содержащие кровотечение. Производится дальнейший анализ изображений, который подтверждает или опровергает решение, полученное на шаге 1. Шаг 2 проиллюстрирован на рис. 4.
Здесь проводится пиксельный анализ яркости и цветовой насыщенности, тогда как предыдущий шаг оперировал только значениями средней насыщенности в крупных блоках (64×64 = 4096 пикселей в каждом блоке).
Кровотечения в изображениях с беспроводной эндоскопической капсулы обычно соответствуют диапазону относительно небольших значений яркости. Первичный анализ показал, что кровоточащие зоны чаще всего содержат значения яркости пикселей между 30 и 80. В результате можно вычислить два уровня границ: T l в следующем условии соответствует нижней границе, Th – верхней.
Кровотечение есть:
Th > I(x,y) > Tl.
Кровотечения нет: во всех остальных случаях.
Однако из-за того, что освещение различных участков может быть разным, выставление фиксированных границ в эндоскопических изображениях не всегда корректно. Таким образом, границы лучше задавать динамически. Параметр Iave , соответствующий среднему пиксельному значению яркости для каждого изображения, используется для автоматической установки границ [8].
Th = Iave + 10, Tl = Iave – 30.
Цветовая насыщенность снова используется здесь, но уже для пиксельного анализа. Стоит заметить, что для хорошо освещенных изображений, в которых доминирует красный цвет, цветовая насыщенность может достигать очень больших значений. Это основная причина ошибок, связанных с пропуском кровотечения на изображении, реально его содержащем. Кровоточащие участки с высокой насыщенностью выявляются, благодаря применению следующего условия.
Таблица 1. Классификация уровней кровотечения
|
Уровень |
0 |
1 |
2 |
3 |
|
Цветовой код |
Кровотечение есть:
0,95 > Is(x,y) > 0,7;
кровотечения нет: во всех остальных случаях.
Предложенная классификация включает комбинацию анализов по яркости и насыщенности. Окончательное решение зависит от того, как эти результаты соотносятся с различными условиями освещения. Оно может быть выражено с помощью нижеописанных условий:
-
1 Iave < 60: изображение имеет недостаточную освещенность, следовательно, эффективным будет анализ только по критерию насыщенности;
-
2 Iave ∈ [60,75]: критерии яркости и насыщенности используются в комбинации. Классификация кровотечений требует совпадения по обоим критериям;
3 Iave > 75: критерий яркости и насыщенности используются в комбинации, но из-за того, что изображение слишком яркое, вычисление SAT( x,y ) теперь отбирается по модифицированному критерию: 0,95 > Is(x,y) > 0,85.
Для того чтобы сделать классификацию более точной, изображения разделяются по уровню интенсивности кровотечения. Используется четырх-уровневая классификация, в которой каждому уровню соответствует определенный цветовой код ( табл. 1 ). Для этих целей анализируется общее количество пикселей Ns2 , отмеченных после шага 2 как кровотечение. Ns2 сравнивается с Nmin – параметром, используемым для разграничения изображений по уровням. По умолчанию значение Nmin установлено равным 450, если был применен только критерий цветовой насыщенности.
При применении обоих критериев – насыщенности и яркости – параметр выставляется равным 5000. Решение о принадлежности изображения, содержащего кровотечение, принимается по следующим правилам:
1 уровень 0 (кровотечение отсутствует):
N s2 < N min ;
2 уровень 1 (кровотечение малой интенсивности):
N min < N s2 ≤ 1,8N min ;
3 уровень 2 (кровотечение умерен- ной интенсивности):
1,8Nmin < Ns2 ≤ 2,6Nmin;
4 уровень 3 (кровотечение большой интенсивности):
N s2 > 2,6N min .
Примеры использования классификации по цветовому коду показаны в табл. 1 .
Метод распознавания кровотечений в желудочно-кишечном тракте был экспериментально проверен на материалах тестируемой выборки. Были проанализированы 72 изображения, из которых 22 содержали кровотечение и 50 были без признаков кровотечения. В результате эксперимента была выявлена следующая неточность:
-
♦ на 3 изображениях из тестируемой выборки, содержащих кровотечение, алгоритм их не выявил;
-
♦ на 13 изображениях алгоритм выявил наличие кровотечения, хотя его там не было.
Эта неточность вызвана значительным числом используемых констант, несмотря на это, планируется дальнейшее усовершенствование алгоритма и повышение его точности. Как уже было отмечено выше, на точность выполнения алгоритма также влияет качество камеры, принимающей изображение желудочно-кишечного тракта.
Таким образом, беспроводная капсульная эндоскопия позволяет не только целиком и полностью исследовать ЖКТ, но и автоматически выявлять

кровотечения и такие тканевые образования, как полипы.
Анализ медицинских изображений часто требует применения ряда техник анализа, учитывающих различные особенности изображений. Нужно также принимать во внимание анатомическую и патологическую важность просматриваемых участков.
Описанные методы распознавания полипов и кровотечений в желудочно-кишечном тракте учитывают эти особенности. В результате были осуществлены программные модули, способные практически безошибочно определять указанные патологии ЖКТ человека в автоматическом режиме и указывать на место их расположения. Для это- го используются математические методы, преобразующие получаемые с капсулы изображения в программную модель.
Данная технология также позволит значительно сократить время, необходимое врачам для анализа изображений, определения патологий и постановку диагноза ■
Список литературы Повышение эффективности распознавания желудочно-кишечных заболеваний в автоматическом режиме на основе анализа изображений эндоскопической капсулы
- Иванова Е.В. Федоров Е.Д. Тимофеев М.Е. Современные видеоэндоскопические технологии в диагностике и лечении заболеваний тонкой кишки./Кремлевская медицина, 2011. -Т. 3.
- Е.А. Распереза Д.В. Сишкова. Видеокапсульная эндоскопия в диагностике заболеваний тонкой кишки./Клиническая эндоскопия, 2008. -Т. 14.
- Waterman M, Eliakim R. Capsule enteroscopy of the small intestine. Abdom Imaging, 2008. -405: Epub ahead of print.
- Иванова Е.В., Жуков Ю.И., Федоров Е.Д. Программное обеспечение для программно-аппаратного эндоскопического капсульного комплекса для проведения безболезненного исследования желудочно-кишечного тракта, включая области, недоступные с помощью методов традиционной эндоскопии. Свидетельство № 2011610692об официальной регистрации программы для ЭВМ. Зарегистрировано в реестре программ для ЭВМ 11.01.2011.
- Klaus Engel, Markus Hadwiger, Joe M. Kniss. Real-Time Volume Graphics. A K Peters, 2006.
- Kühnel, Wolfgang. Differential Geometry: Curves -Surfaces -Manifolds./American Mathematical Society, 2006.
- Mark S. Nixon and Alberto S. Aguado. Feature Extraction and Image Processing./Academic Press, 2008. -P. 88.
- P.Y. Lau, P.L. Correia. Detection of bleeding patterns in WCE video using multiple features./Proceedings of the 29th Annual International Conference of the IEEE EMBS; Cite Internationale, Lyon, France; August 23-26, 2007. -PP. 5601 -5604.
- Nikos Paragios, Yunmei Chen and Olivier Faugeras: The Handbook of Mathematical Models in Computer Vision, Springer 2005. -596 p


