Повышенный уровень Са125 (МUC16) при метастатическом раке желудка - мощный фактор негативного прогноза выживаемости
Автор: Семнов Н.Н., Далгатов К.Д.
Журнал: Злокачественные опухоли @malignanttumors
Рубрика: Собственные исследования
Статья в выпуске: 1 т.12, 2022 года.
Бесплатный доступ
Введение: СА125 является экстрацеллюлярным доменом гликопротеина MUC16. Клиническое значение сывороточного СА125 наиболее широко изучено при раке яичников. Значение уровня сывороточного СА125 при раке желудка практически не отражено в литературе. Имеются данные о негативном прогнозе в отношении общей выживаемости при гиперэкспрессии MUC16 у больных метастатическим раком желудка. Работ по корреляции уровня сывороточного СА125 и гиперэкспрессии MUC16 в литературе не обнаружено. Цель: целью исследования являлась оценка влияния на отдаленные результаты (время до прогрессирования и общая выживаемость) повышенного уровня СА125 у больных метастатическим раком желудка. Материалы и методы: СА125 определялся в сыворотке до начала I линии химиотерапии у 75 больных метастатическим раком желудка. Возраст составил 61,3 (26,7-84,9) года, мужчины/женщины - 45/30. Синхронные метастазы 85%, локализация: брюшина 57,3%, печень 37,3%, другие локализации 5,4%. Паллиативная гастрэктомия выполнена у 28%, метастазэктомии у 20% больных. Монохимиотерапия использовалась у 6,7%; дублетные режимы у 58,7%; триплетные - у 36% больных. Результаты: при анализе было показано, что повышенный уровень СА125 (>37 МЕ/мл) ассоциировался со значительным уменьшением медианы времени до прогрессирования (3,5 мес. (ДИ 2,87-9,53) против 6,2 мес., р=0,001, ДИ 2,02-4,9) и общей выживаемости (5,1 мес. (ДИ 6,07-28,1) против 17,1 мес. (ДИ 3,5-6,67), р=0,001). При однофакторном анализе показано, что влияние на общую выживаемость имели локализация метастазов (брюшина), тип опухоли (аденокарцинома/перстневидноклеточный рак), проведение паллиативной гастрэктомии и резекции метастазов. При проведении многофакторного анализа было показано, что благоприятными прогностическими факторами в отношении общей выживаемости оказались только нормальный уровень СА125 (HR 0,39 (95% ДИ 0,18-0,84), р=0,001) и выполнение паллиативной гастрэктомии (HR 0,23 (95% ДИ 0,1-0,58), р=0,001). Применение тройных комбинаций позволяло несколько улучшить показатели общей выживаемости в группе больных с повышенным СА125, но различия не были статистически значимыми (6,7 мес. против 4,0 мec., р=0,29). Заключение: Высокий уровень СА125, в известной степени отражающий гиперэкспрессию MUC16, является мощным независимым фактором негативного прогноза при метастатическом раке желудка. В настоящее время возможным фактором преодоления негативного влияния остается, вероятно, интенсификация режимов химиотерапии. Однако в будущем решение проблемы лежит в поисках адекватных мишеней и способах нейтрализации негативного влияния гиперэкспрессии МUС16 у больных метастатическим раком желудка.
Са125, рак желудка, muc16, химиотерапия, гастрэктомия, метастазы
Короткий адрес: https://sciup.org/140293846
IDR: 140293846
Elevated levels of Ca125 (MUC16) in metastatic gastric cancer as a strong predictor of poor survival
CA125 is an extracellular domain of MUC16 glycoprotein. The clinical significance of serum CA125 has been most extensively studied in ovarian cancer. The significance of serum CA125 in gastric cancer has not been fully elucidated. There is evidence that MUC16 overexpression is associated with poor survival in patients with metastatic gastric cancer. We have not found any research papers on the correlation between the levels of serum CA125 and MUC16 overexpression. Objective: The objective of the study was to assess the effects of elevated CA125 levels in patients with metastatic cancer on the long-term results (time to disease progression and overall survival). Materials and methods: CA125 was determined in the serum before the start of first-line chemotherapy in 75 patients (45 males and 30 females) with metastatic gastric cancer. The mean age of the patients was 61,3 (26,7-84,9) years. Synchronous metastases were observed in 85 % of patients: 57,3 % in the peritoneum, 37,3 % in the liver, 5,4 % at other sites. Palliative gastrectomy and metastasectomy were performed in 28 % and 20 % of patients, respectively. Monotherapy, doublet and triplet chemotherapy regimens were used in 6,7 %, 58,7 % and 36,0 % of patients, respectively. Results: the analysis showed that elevated levels of CA125 (> 37 IU/mL) were associated with a significant reduction in median time to progression (3,5 months (CI 2,87-9,53) vs 6,2 months, р = 0.001 (CI 2,02-4,9)) and overall survival (5,1 months (CI 6,07-28,1) vs 17,1 months (CI 3,5-6,67), р = 0.001). One-factor ANOVA showed that factors with the strongest effects on the survival rates included the location of metastases (peritoneum), tumor histology (adenocarcinoma/signet ring cell carcinoma), the use of palliative gastrectomy and metastasis resection. A multi-factor ANOVA showed that the only favorable prognostic factors in terms of overall survival rates were normal CA125 levels (HR 0,39 (95 % CI 0,18-0,84), р = 0.001) and the use of palliative gastrectomy (HR 0,23 (95 % CI 0,1-0,58), р = 0.001). The use of triplet chemotherapy regimens allowed to slightly improve the overall survival rates in the group of patients with elevated CA125 levels; however, the differences were not statistically significant (6,7 months vs 4Ю0 months, p = 0.29). Conclusion: Elevated levels of CA125, which reflect MUC16 overexpression to a certain extent, is a strong independent predictor of poor outcome in metastatic gastric cancer. Currently, a possible way to overcome this negative impact is to use more intensive chemotherapy regimens. However, further research should be aimed at finding adequate targets and ways of neutralizing the negative impact of MUC16 overexpression in patients with metastatic gastric cancer.
Текст научной статьи Повышенный уровень Са125 (МUC16) при метастатическом раке желудка - мощный фактор негативного прогноза выживаемости
CA125 был открыт в 1981 году, когда Bast RC et al. [1] обнаружили моноклональное антитело ОС125, которое селективно определялось на поверхности клеток яичников. Далее было определено, что этот антиген может обнаруживаться в сыворотке большинства больных раком яичников [2]. Однако точная биохимическая характеристика СА125 была неизвестна до 2001 года, когда Yin BW [3] секвенировали первый клеточный клон ДНК и определили, что он соответствует экстарцеллюлярному домену нового муцинового протеина, который они назвали MUC16.
Дальнейшие исследования показали, что эктопическая экспрессия MUC16 может отвечать за резистент- ность к цитостатикам, например, цисплатину, и подавляет процесс апоптоза [4,5], хотя точный механизм до сих пор неизвестен. Также показано, что С-концевой пептид MUC16 взаимодействует с Sгс-семейством киназ, и это ведет к дерегуляции В-катенина и Е-кадгерина [6], что может способствовать развитию отдаленных метастазов.
В целом, муцины, кодируемые MUC генами, представляют собой гликопротеины и могут быть подразделены на 4 категории: образующие муцинозные структуры (MUC 2, -5АС, -5В, -6, и -19), образующие немуцинозные структуры (MUC7, -8, и -9), трансмембранные (MUC1, -ЗА, -ЗВ, -4, -12, -13, -14, -15, -16, -17, -20, и -21) и неклассифи-цируемые (MUC 11) [7]. Трансмембранные муцины обнаруживаются на апикальных отделах эпителиальных клеток и подслизистой оболочки респираторного и гастроинтестинального тракта [8]. Также исследования показали, что мезотелий (брюшина, плевра. перикард) сам может является существенным источником СА125 [9,10,11].
Гиперэкспрессия муцинов выявляется в злокачественных опухолях ЖКТ, и считается, что она может быть ответственна за рост и выживаемость опухолевых клеток [12], а также за подавление противоопухолевого иммунитета [13]. В частности, MUC16 показал способность оказывать негативное влияние на формирование иммунного ответа против клеток рака яичников путем прямого подавления функции NK-клеток [14,15].
Таблица 1. Характеристика больных, вошедших в оценку
Материалы и методы
Из представленных данных очевидно, что большинство больных имели синхронные метастазы, в основном в печень и брюшину, диссеминация распространялась на 1–2 зоны (включая и первичную опухоль), чаще всего при аденокарциноме, подавляющее большинство с низко-и недифференцированной формами. Части больных (28%) при достижении хорошего клинического эффекта было выполнено паллиативное удаление первичной опухоли.
Повышенным уровнем СА125 считался уровень выше 37 МЕ/мл. Повышенный уровень отмечался у 39 больных (52%), максимально до 7871 Ме/мл.
В качестве химиотерапии I линии применялась монотерапия у 4 больных (у двоих — капецитабин, у одного — паклитаксел еженедельно и у одного — иринотекан), двухкомпонентные режимы использованы у 44 больных (у 39 — FOLFOX/САРОХ, цисплатин + капецитабин/5-ФУ, у 5 — FOLFIRI), трехкомпонентные режимы — у 27 больных (24 FLOT, 3 FOLFIRINOX). Применение неплатиновых режимов в основном было обусловлено ранним прогрессированием после адъювантной химиотерапии. Трастузумаб при HER2/neu 3+ был использован у 3 больных. Распределение режимов химиотерапии в группах больных с повышенным и нормальным СА 125 представлено в табл. 2.
Результаты
При оценке влияния уровня СА125 на время до прогрессирования и общую выживаемость были получены следующие результаты (рис. 1 и 2).
Оказалось, что повышенный уровень СА125 значимо негативно влиял как на медиану времени до прогрессирования (3,5 мес. (ДИ 2,87–9,53) против 6,2 мес.,
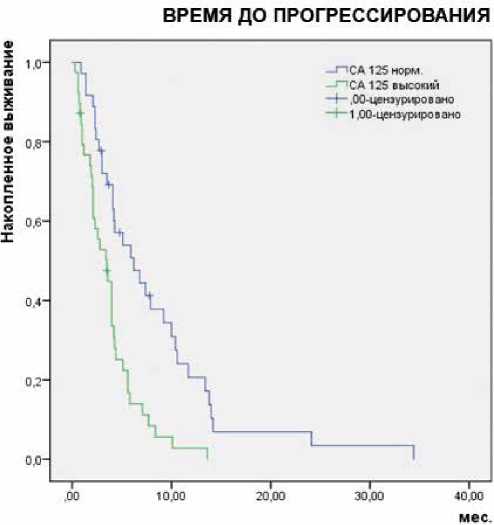
Таблица 2. Режимы химиотерапии в группах больных
|
СА 125 норма (n=36) |
СА 125 повышен (n=39) |
р |
|
|
Монотерапия |
4 (11%) |
1 (2,5%) |
0,8 |
|
|Дублеты |
20 (55,5%) |
22 (56,4%) |
1 |
|
Триплеты |
12 (33,3%) |
16 (38,4%) |
0,63 |
Таким образом, больные в группах получали сходную по интенсивности химиотерапию, в основном двух- и трехкомпонентную.
Статистический анализ
Статистическая обработка проводилась с использованием программ IВМ SPSS Statistics v. 23. Различия в частоте встречаемости оценивались тестом Фишера, время до прогрессирования и общая выживаемость по методу Каплана–Майера, многофакторный анализ и соотношение рисков регрессией Кокса.
ОБЩАЯ ВЫЖИВАЕМОСТЬ
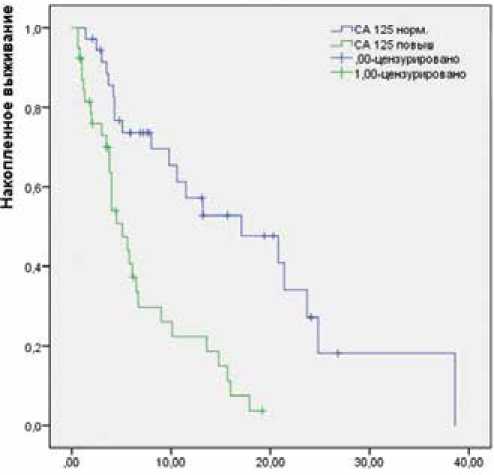
Рисунки 1, 2. Время до прогрессирования и общая выживаемость больных в зависимости от уровня СА125.
р=0,001, (ДИ 2,02–4,9), так и общую выживаемость (5,1 мес. (ДИ 6,07–28,1) против 17,1 мес. (ДИ 3,5–6,67), р=0,001).
Мы провели оценку влияния интенсивности химиотерапии (дублеты или триплеты) в группе больных с повышенным уровнем СА125. Оказалось, что триплетные режимы (FLОТ и FOLFIRINOX) демонстрировали несколько лучшее время до прогрессирования (4,0 против 2,7 мес.) и выживаемость (6,7 мес. против 4,0 мec.) по сравнению с дублетами, однако различия были статистически не достоверными (р=0,29).
При оценке числа больных, получавших 2 и более линии химиотерапии, было показано, что у больных с нормальным (при первичном диагнозе) уровне СА125 химиотерапию II линии получали 18 из 36 больных (50%), в то время как с повышенным уровнем маркера — 11 из 39 (28%), р=0,06.
С учетом того, что повышение СА125 может быть связано с метастазами в брюшину, мы оценили чувствительность и специфичность уровня СА125 для диагностики канцероматоза.
При наличии метастазов в брюшину уровень СА125 был повышен в 62% случаев. При отсутствии —у 39,4% больных. Таким образом, уровень СА125 не продемонстрировал ни чувствительности, ни специфичности в отношении диагностики метастазов в брюшину. Это говорит о том, что основным источником маркера являлась первичная опухоль и метастазы, но не результат связывания MUC16 с мезотелином.
Обсуждение
Значимость СА125 как фактора негативного прогноза в основном изучалась при раке яичников. В качестве попыток преодоления негативного влияния СА125 (МUС16) были разработаны несколько стратегий, направленных на связывание в сыворотке СА125 или индукцию иммунного ответа.
Список литературы Повышенный уровень Са125 (МUC16) при метастатическом раке желудка - мощный фактор негативного прогноза выживаемости
- Bast RC, Jr., Feeney M, Lazarus H, et al. Reactivity of a monoclonal antibody with human ovarian carcinoma. J Clin Invest 1981;68 (5): 1331-7. [PubMed: 7028788]
- Klug TL, Bast RC, Jr., Niloff JM, et al. Monoclonal antibody immunoradiometric assay for an antigenic determinant (CA 125) associated with human epithelial ovarian carcinomas. Cancer Res 1984;44 (3):1048—53. [PubMed: 6198078]
- Yin BW, Dnistrian A, Lloyd KO. Ovarian cancer antigen CA125 is encoded by the MUC16 mucin gene. Int J Cancer 2002;98 (S): 737—40. [PubMed: 11920644]
- S. Das, S. Rachagani, M. P. Torres-Gonzalez et al. Carboxyl-terminal domain of MUC16 imparts tumorigenic and metastatic functions through nuclear translocation of JAK2 to pancreatic cancer cells. Oncotarget. 2015 Mar 20;6 (8):5772-87. doi: 10.18632/oncotarget. 3308.
- M. Boivin, D. Lane, A. Piche CA125 (MUC16) tumor antigen selectively modulates the sensitivity of ovarian cancer cells to genotoxic drug-induced apoptosis. Gynecol Oncol. 2009 Dec;115 (3):407-13. doi:10.1016/j. ygyno. 2009.08.007. Epub 2009 Sep 10.
- C. Theriault, M. Pinard, M. Comamala et al. MUC16 (CA125) regulates epithelial ovarian cancer cell growth, tum-origenesis and metastasis Gynecol Oncol. 2011 Jun 1;121 (3):434-43. doi: 10.1016/j. ygyno. 2011.02.020. Epub 2011 Mar 21.
- S. Senapati, P. Sharma, S. Bafna, et al. The MUC gene family: their role in the diagnosis and prognosis of gastric cancer. Histol Histopathol. 2008; 23:1541-52. [PubMed: 18830939]
- 8. S. Bafna, S. Kaur, S. K. Batra. Membrane-bound mucins: the mechanistic basis for alterations in the growth and survival of cancer cells. Oncogene. 2010; 29:2893-904. [PubMed: 20348949]
- Kabawat, S. E., Bast, R. C., Bahn, A. K. et al. (1983) Tissue distribution of acoelomic-epithelium-related antigen recognized by the monoclonal antibody OC 125. Int.J. Gynecol. Pathol., 2, 275-285.
- Zeillemaker, A. M., Verbrugh, H. A., Hoynck van Papendrecht, A. A. G. M. et al. CA125 secretion by peritoneal me-sothelial cells. J. Clin. Pathol 47, 263-265.
- Zeimet, A. G., Offner, F. A., Muller-Holzner, E. et al. (1998) Peritoneum and tissues of the female reproductive tract as physiological sources of CA125. Tumor Biol., 19, 275-282
- Jonckheere, I. Van Seuningen The membrane-bound mucins: how large O-glycoproteins play key roles in epithelial cancers and hold promise as biological tools for gene-based and immunotherapies. Crit Rev Oncog. 2008: 14:177—96. (PubMed: 19409062]
- RC. Bast Jr, D. R. Spriggs. More than a biomarker: CA125 may contribute to ovarian cancer pathogenesis. Gynecol Oncol 2011, 121:429-430
- Gubbels JA, Felder M, Horibata S, et al. MUC16 provides immune protection by inhibiting synapse formation between NK and ovarian tumor cells. Mol Cancer 2010;9:11. [PubMed: 20089172]
- Belisle JA, Horibata S, Jennifer GA, et al. Identification of Siglec-9 as the receptor for MUC16 on human NK cells, B cells, and monocytes. Mol Cancer 2010;9:118. [PubMed: 20497550]
- M. M. Streppel, A. Vincent, R. Mukherjee, et al. Mucin 16 (cancer antigen 125) expression in human tissues and cell lines and correlation with clinical outcome in adenocarcinomas of the pancreas, esophagus, stomach, and colon. Hum Pathol. 2012 October; 43 (10): 1755-1763. doi:10.1016/j. humpath. 2012.01.005
- Kim DH, Yun HY, Ryu DH et al. Preoperative CA 125 is significant indicator of curative resection in gastric cancer patients. World J Gastroenterol. 2015 Jan 28;21 (4):1216-21. doi: 10.3748/wjg. v21. i4.1216.
- Namikawa T, Kawanishi Y, Fujisawa K, et al. Serum carbohydrate antigen 125 is a significant prognostic marker in patients with unresectable advanced or recurrent gastric cancer. Surg Today. 2018 Apr;48 (4):388-394. doi: 10.1007/ s00595-017-1598-3. Epub 2017 Oct 17.
- A. Perrier, J. Gligorov, G. Lefèvre, The extracellular domain of Her2 in serum as a biomarker of breast cancer. Lab Invest. 2018 Jun;98 (6):696-707. doi: 10.1038/s41374-018-0033-8. Epub 2018 Feb 28.
- K. Moreno-Aspitia, D. W. Hillman, S. H. Dyar et al. Soluble human epidermal growth factor receptor 2 (HER2) levels in patients with HER2-positive breast cancer receiving chemotherapy with or without trastuzumab: results from North Central Cancer Treatment Group adjuvant trial N9831. Cancer. 2013 Aug 1;119 (15):2675-82. doi: 10.1002/cncr. 28130. Epub 2013 Jun 6.
- K. Oyama, S. Fushida, T. Tsukada et al. Evaluation of serum HER2-ECD levels in patients with gastric cancer J Gastroenterol. 2015 Jan;50 (1):41-5. doi: 10.1007/s00535-014-0941-3. Epub 2014 Feb 21.
- H.-Z Shi, Y.-N. Wang, X.-H. Huang et al. Serum HER2 as a predictive biomarker for tissue HER2 status and prognosis in patients with gastric cancer. World J Gastroenterol. 2017 Mar 14;23 (10):1836-1842. doi: 10.3748/wjg. v23. i10.1836.
- M. Saito, K. Yamashita, Y. Arimura et al. Serum HER2 as an adjunct to assess HER2 status for advanced gastric cancer: A prospective multicenter trial (SHERLOCK). Acta Oncol. 2016;55 (3):309-17. doi: 10.3109/0284186X. 2015.1107189. Epub 2016 Jan 12.
- J. Berek, P. Taylor, W. McGuire, et al. Oregovomab maintenance monoimmunotherapy does not improve outcomes in advanced ovarian cancer. J Clin Oncol. 2009 Jan 20;27 (3):418-25. doi: 10.1200/jœ. 2008. 17.8400. Epub 2008 Dec 15.
- P. Sabbatini, P. Harter, G. Scambia, et al. Abagovomab as maintenance therapy in patients with epithelial ovarian cancer: a phase III trial of the AGO OVAR, COGI, GINECO, and GEICO--the MIMOSA study. J Clin Oncol. 2013 Apr 20;31 (12):1554-61. doi: 10.1200/jCO. 2012.46.4057. Epub 2013 Mar 11.


