Поздняя диагностика болезни Данона: морфологическая характеристика LAMP2-кардиомиопатии (клиническое наблюдение)
Автор: Мотина Наталья Владимировна, Веселовская Надежда Григорьевна, Костюченко Геннадий Иванович, Чумакова Галина Александровна, Отт Анна Владимировна, Мотин Юрий Григорьевич
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 3 т.30, 2022 года.
Бесплатный доступ
Болезнь Данона является редким и сложным для диагностики Х-сцепленным наследственным заболеванием, обусловленным дефицитом лизосом-ассоциированного мембранного протеина 2 или LAMP2. Основные клинические симптомы включают поражение миокарда с развитием гипертрофической LAMP2-кардиомиопатии, скелетную миопатию и интеллектуальные нарушения. Заболевание характеризуется быстро прогрессирующим течением, что требует динамического наблюдения пациентов. Наиболее значимым неблагоприятным прогностическим фактором и основной причиной смерти является развитие кардиомиопатии. Однако, лизосомальное накопление гликогена в кардиомиоцитах часто остается не распознанным в качестве причины развития гипертрофической кардиомиопатии. Целью исследования явилось проведение клинико-морфологического анализа случая поздней диагностики LAMP2-кардиомиопатии у пациента-женщины 44 лет. Использовались данные истории болезни, результаты прижизненных лабораторно-инструментальных исследований, качественные и количественные морфологические исследования эндомиокардиальных биоптатов. В результатах исследования представлены клинические признаки, результаты морфологического исследования на светооптическом и электронно-микроскопическом уровнях, показаны особенности структурной перестройки кардиомиоцитов. Обнаружено формирование мультиламеллярных миелиноподобных структур под сарколеммой кардиомиоцитов. Наблюдались признаки повреждения клеток - значительная неравномерная вакуолизация саркоплазмы с выявлением в отдельных вакуолях фрагментов PAS-позитивного содержимого, дисторсия кардиомиоцитов. Отмечалось исчезновение поперечной исчерченности и локальные нарушения целостности сарколеммы. Интерстиций характеризовался рыхлой лимфомононуклеарной инфильтрацией с примесью одиночных сегментоядерных лейкоцитов, явлениями отека, мелкоочаговым склерозом преимущественно по перимускулярному типу. В элементах микроциркуляторного русла на светооптическом уровне наблюдались признаки активации эндотелия. По совокупности клинико-анамнестических данных, результатов молекулярно-генетического, морфологического исследования была установлена метаболическая причина гипертрофии миокарда, ранее клинически не распознанная, с морфологической картиной LAMP2-кардиомиопатии - болезни Данона и выставлен сответствующий диагноз. Авторами представлен редкий случай позднего выявления болезни Данона (LAMP2-кардиомиопатии) с накоплением в саркоплазме кардиомиоцитов аутофагоцитарного материала, гликогена, формированием осмиофильных миелиноподобных структур. Представленный клинический случай наглядно демонстрирует практическую значимость ультраструктурного патоморфологического исследования эндомиокардиального биоптата для определения истинной формы метаболической гипертрофии и оценки степени морфологической перестройки миокарда.
Болезнь данона, гипертрофическая кардиомиопатия, лизосом-ассоциированный мембранный протеин 2, патологическая анатомия, электронная микроскопия
Короткий адрес: https://sciup.org/143178912
IDR: 143178912 | DOI: 10.20340/mv-mn.2022.30(3).638
The late diagnosis of Danon disease: the morphological characteristics of LAMP2-cardiomyopathy (case report)
Danons disease is a rare and difficult-to-diagnose X-linked hereditary disease caused by a deficiency of lysosome-associated membrane protein 2 or LAMP2. The main clinical symptoms include myocardial damage with the development of hypertrophic LAMP2 cardiomyopathy, skeletal myopathy, and intellectual impairment. The disease is characterized by a rapidly progressive course, which requires dynamic monitoring of patients. The most significant adverse prognostic factor and the main cause of death is the development of cardiomyopathy. But lysosomal accumulation of glycogen in cardiomyocytes often remains unrecognized as the cause of hypertrophic cardiomyopathy. The aim of the study was to conduct a clinical and morphological analysis of a case of late diagnosis of LAMP2 cardiomyopathy in a 44-year-old female patient. We used data from the medical history, the results of intravital laboratory and instrumental studies, qualitative and quantitative morphological studies of endomyocardial biopsy. The results of the study present clinical signs, the results of a morphological study at the light-optical and electronic microscopic levels, and show the features of the structural rearrangement of cardiomyocytes. The formation of multilamellar myelin-like structures under the sarcolemma of cardiomyocytes was found. There were signs of cell damage - significant uneven vacuolization of the sarcoplasm with the detection of fragments of PAS-positive content in individual vacuoles, distortion of cardiomyocytes. There was a disappearance of transverse striation and local violations of the integrity of the sarcolemma. The interstitium was characterized by loose lymphomononuclear infiltration with an admixture of single segmented leukocytes, edema, and small-focal sclerosis, predominantly of the perimuscular type. In the elements of the microvasculature at the light-optical level, signs of endothelial activation were observed. Based on the combination of clinical and anamnestic data, the results of molecular genetic, morphological studies, a metabolic cause of myocardial hypertrophy, previously not clinically recognized, was established with a morphological picture of LAMP2 cardiomyopathy - Danon disease, and an appropriate diagnosis was made. The authors present a rare case of late detection of Danon disease (LAMP2-cardiomyopathy) with the accumulation of autophagocytic material, glycogen in the sarcoplasm of cardiomyocytes, and the formation of osmiophilic myelin-like structures. The presented clinical case clearly demonstrates the practical significance of ultrastructural pathological examination of endomyocardial biopsy to determine the true form of metabolic hypertrophy and assess the degree of morphological myocardial rearrangement.
Текст научной статьи Поздняя диагностика болезни Данона: морфологическая характеристика LAMP2-кардиомиопатии (клиническое наблюдение)
Введение. Болезнь Данона – тяжелое метаболическое заболевание, связанное с первичным дефицитом лизосом-ассоциированного мембранного протеина 2 (LAMP2), важного структурного компонента мембран лизосом. Первое описание этой патологии было дано M. Danon в 1981 г., когда он опубликовал результаты морфологического исследования мышечных тканей двух мальчиков, страдающих кардиомиопатией, скелетной миопатией и отставанием в умственном развитии [1]. Позднее была установлена связь между развитием заболевания и мутацией в гене LAMP2 и высказано предположение, что в основе патогенеза лежит нарушение процессов аутофагии [2-3]. Нарушение функции протеина LAMP2 ведет к накоплению в мышечных клетках аутофагоцитарного материала и гликогена, что служит причиной увеличения размеров клеток, их гибели, развития гипертрофических и фиброзных изменений в миокарде [4]. Заболевание наследуется доминантно, сцеп-ленно с Х-хромосомой, поэтому клиническая картина у мужчин и женщин значительно отличается [5-6]. У мужчин наблюдается более тяжелое течение и ранняя манифестация. Клиническая картина болезни у женщин в силу гетерозиготности и поздней пенетрантности часто характеризуется стертой клинической симптоматикой, не полной выраженностью классической триады заболевания – скелетная миопатия и когнитивные нарушения у женщин встречаются гораздо реже, чем у мужчин, что в ряде случаев затрудняет диагностику, особенно при невозможности выполнения генетического исследования.
В отечественной литературе публикации о случаях диагностики болезни Данона встречаются не часто, еще реже публикуются работы с описанием результатов морфологического и ультраструк-турного исследования биопсийного материала миокарда. В связи с редкостью заболевания и сложностью диагностики распространенность болезни Данона в популяции достоверно не известна. По данным разных исследователей LAMP2 мутации обнаруживаются у 2-6% больных с гипертрофической кардиомиопатией [5-6]. В этой связи высказано предположение о минимальной распространенности болезни Данона в европейской популяции от 2 до 6 случаев на 100000 населения [7]. Необходимо отметить, что в работах K. Suigie с соавт. указывается на возможную гиподиагностику данного состояния у пациентов с гипертрофической кардиомиопатией, особенно у женщин при стертой клинической картине заболевания [8]. Поэтому мы сочли возможным представить собственный опыт наблюдения гипертрофической кардиомиопатии, связанной с мутацией в гене LAMP2.
Цель исследования: описать структурную перестройку миокарда при исследовании клинического случая поздней диагностики болезни Данона.
Материалы и методы исследования. В настоящей работе клиникоморфологическое исследование образцов биоптата миокарда проведено у пациентки с клиническим подозрением на кардиомиопатию при болезни Данона. В исследовании использованы сведения из истории болезни и результаты лабораторных и инструментальных данных. Пациент – жен- щина, 44 года. В анамнезе с детства беспокоили приступы учащенного сердцебиения, по поводу которых обследовалась у детского кардиолога, в процессе диагностики был исключен синдром Вольфа-Паркинсона-Вайта. Далее не наблюдалась, приступы сердцебиения были кратковременными, беспокоили редко. В возрасте 39 лет наступило ухудшение состояния в виде учащения приступов сердцебиения, при трансторакальном эхокардиографическом обследовании (далее - ЭХОКГ) выявлена гипертрофия миокарда левого желудочка с утолщением межжелудочковой перегородки (далее - МЖП) и задней стенки левого желудочка (далее - ЗСЛЖ) до 13 мм, характер нарушений ритма не верифицирован, генетическое исследование не проводилось. По результатам обследования пациентке выставлен диагноз - гипертрофическая кардиомиопатия без обструкции выходного отдела левого желудочка, назначена медикаментозная терапия □ -блокаторами. В возрасте 43 лет пароксизмы нарушения ритма стали чаще, со слов пациентки, через день. По результатам ЭКГ впервые была верифицирована пароксизмальная форма фибрилляции-трепетания предсердий, по поводу чего проведена радиочастотная аблация (далее - РЧА) устьев правых и левых легочных вен, зоны предсердной тахикардии, перешейка между устьем нижней полой вены и фиброзным кольцом трехстворчатого клапана.
В возрасте 44 лет появилась клиника декомпенсации хронической сердечной недостаточности в виде одышки, ортопноэ. Пациентка была госпитализирована в отделение некоронарогенной патологии миокарда Алтайского краевого кардиологического диспансера. Из анамнеза жизни известно, что отец умер внезапно во сне в возрасте 60 лет, у старшего сына в возрасте 1,5 лет была диагностирована дилатационная кардиомиопатия, далее верифицирована болезнь Данона, мальчик погиб в возрасте 16 лет. Несмотря на очевидную отягощенную наследственность – обследование на генетические аномалии среди родственников первой линии не проводилось. В период госпитализации по результатам трансторакальной ЭХОКГ у пациентки обнаружена расширение ле- вых отделов сердца: расширение левого предсердия до 46 мм, конечнодиастолический размер левого желудочка составил 56 мм. Величина фракции выброса левого желудочка составила 45%, систолическое давление в правом желудочке 48 мм рт. ст. Наблюдались признаки гипертрофии миокарда левого желудочка с толщиной МЖП 11 мм, ЗСЛЖ 11 мм, увеличение индекса массы миокарда левого желудочка до 133 гр/м2. С учетом анамнеза жизни (нарушения ритма с детского возраста, сын страдал болезнью Данона), клинической картины (гипертрофический фенотип по ЭХОКГ в течение 5 лет без явных причин для гипертрофии миокарда с исходом в расширение камер сердца, отсутствие типичных признаков гипертрофической кардиомиопатии по ЭКГ, нарушения ритма, устойчивые к РЧА) образцы биологического материала пациентки были направлены на молекулярно-генетическое исследование и выполнена эндомиокардиальная биопсия с целью исключения болезни накопления миокарда.
После изучения биопсийного материала в диссекционном микроскопе был отобран один фрагмент для электронномикроскопического исследования, два фрагмента для проведения прямого им-мунофлюоресцентного исследования с использованием антител к иммуноглобулинам M, G, C3c, C4d, λ- и k- легким цепям, фибриногену. Оставшийся материал после фиксации в 10% растворе формалина обезвоживали, заливали в парафин. Полученные срезы окрашивали гематоксилином и эозином, по Массону, конго-красным, ставили PAS-реакцию. Для электронно-микроскопического исследования образцы тканей фиксировали в 3% растворе глутарового альдегида, приготовленном на фосфатном буфере (pH 7,2), с дофиксацией в 1% растворе ОsO4, дегидратировали в этиловом спирте возрастающей концентрации и заключали в эпон. Из полученных блоков готовили полутон-кие срезы толщиной 1 мкм, окрашивали толуидиновым синим, изучали под световым микроскопом и выбирали необходимые участки тканей для исследования в электронном микроскопе. Из отобранного материала получали ультратонкие срезы толщиной 55 нм на ультратоме Leica EM UC7, контрастировали насыщенным водным раствором уранилацетата, цитратом свинца и изучали в электронном микроскопе Libra 120 (Carl Zeiss, Германия) при ускоряющем напряжении 120кВ с последующим фотографированием при увеличениях от 1985 до 20000.
Результаты исследования и обсуждение. При гистологическом исследовании эндокард в изучаемых фрагментах тонкий, ровный, в них определялись дистрофические изменения кардиомиоцитов с просветлением перинуклеарной зоны и оттеснением сократительных элементов на периферию, неравномерная гипертрофия отдельных групп кардиомиоцитов с увеличением размеров до 35-40 мкм, перинуклеарное накопление липофусцина. Наблюдались признаки повреждения клеток – значительная неравномерная вакуо- дельных вакуолях фрагментов PAS-позитивного содержимого (рис. 1), дисторсия кардиомиоцитов. Отмечалось исчезновение поперечной исчерченности и локальные нарушения целостности сарколеммы. Интерстиций характеризовался рыхлой лимфомононуклеарной инфильтрацией с примесью одиночных сегментоядерных лейкоцитов, явлениями отека, мелкоочаговым склерозом преимущественно по перимускулярному типу (рис. 2). В элементах микроциркуляторного русла на светооптическом уровне наблюдались признаки активации эндотелия.
Прямое иммунофлюоресцентное исследование биоптатов показало картину схожую с аутоиммунным повреждением миокарда: фиксацию IgM и C3 c мелкогранулярного характера в зоне до 20-30% капилляров, фиксацию С3 с субэндокардиаль-но очагово по сарколемме и саркоплазме отдельных групп кардиомиоцитов [9].
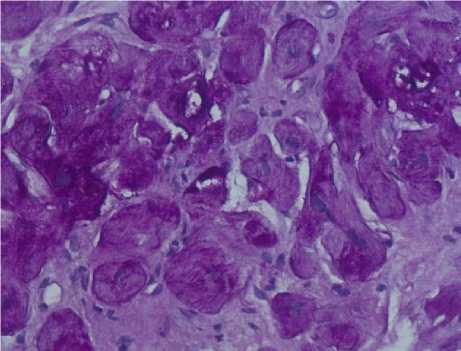
Рис. 1. Микрофото препарата миокарда пациентки. В саркоплазме гипертрофированных кардиомиоцитов определяются многочисленные различного размера вакуоли, часть из которых содержит неоднородное PAS-позитивное содержимое. Окр.: PAS-реакция. Ув.: ×400
лизация саркоплазмы с выявлением в от-
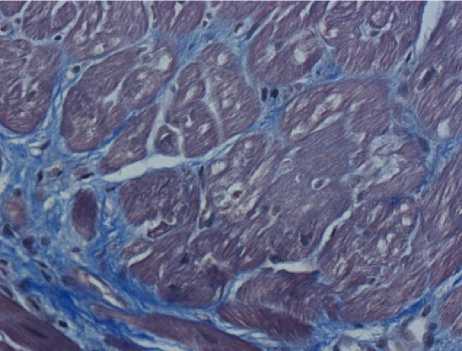
Рис. 2. Микрофото препарата миокарда пациентки. Мелкоочаговый склероз ин-терстиция. Неоднородная вакуолизация саркоплазмы кардиомиоцитов. Окр.: по Массону. Ув.: ×400
При электронномикроскопическом исследовании в кардиомиоцитах определялись многочисленные включения гликогена, располагающиеся преимущественно в периферических участках саркоплазмы и под сарколеммой. Наблюдалось расширение элементов саркоплазматической сети, аппарата Гольджи, вакуо- лизация цитоплазмы, скопление включений липофусцина. Отмечалось оттеснение сократительных элементов на периферию, участки дисторсии миофибрилл, их дезорганизации. Определялись группы митохондрий с явлениями набухания, снижением плотности матрикса, нарушением ориентации крист, их отеком и ва- куолизацией, фрагментацией, деструкцией мембран с высвобождением липидов и формированием одиночных мелких липидных капель в саркоплазме. Преимущественно в периферических участках саркоплазмы наблюдались многочисленные различные по размеру вакуоли, содержащие аутофагоцитарые элементы, гранулы гликогена (рис. 3). Между миофиламентами располагались многочисленные рибосомы, одиночные вторичные лизосомы с электронно-контрастным неоднородным содержимым. В периферических участках саркоплазмы отмечалось формирование электронноплотных образований, представленных концентрически расположенными мембранными элементами по типу миелиноподобных структур (рис. 4). Локально определялось нарушение целостности сарколеммы, разволокнение, нечеткость структуры базальной мембраны.
В результате молекулярногенетического исследования образцов биологического материала пациентки методом прямого секвенирования по Сэнгеру был обнаружен генетический вариант NM_002294.3:c.893_923del(p.E298Afs*38) в гетерозиготном состоянии последовательности гена LAMP2.
Основным морфологическим проявлением болезни Данона является развитие гипертрофической кардиомиопатии вследствие отложения в кардиомиоцитах и их лизосомах аномальных продуктов метаболизма. При этом по клиническим проявлениям болезнь Данона практически не отличается от других форм гипертрофических кардиомиопатий. В типичных случаях LAMP2-кардиомиопатия проявляется концентрической симметричной гипертрофией миокарда со значительным увеличением толщины стенки левого желудочка, по данным литературы до 29-65 мм [7].
Однако в описанном нами случае наблюдается поздний дебют заболевания, стертая клиническая картина с отсутствием выраженной гипертрофии миокарда левого желудочка по результатам ЭХОКГ, отсутствие скелетной миопатии и когнитивных нарушений, что вероятно связано с полом пациента и может объяснять позднюю диагностику заболевания.
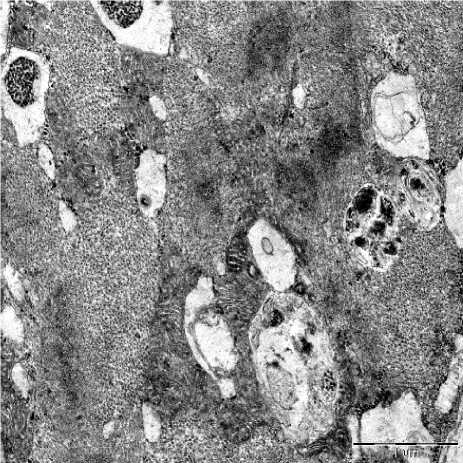
Рис. 3. Ультрамикрофото препарата миокарда пациентки. В саркоплазме кардиомиоцита содержатся многочисленные аутофагоцитарные включения. Электронная микроскопия. Ув.: ×6300
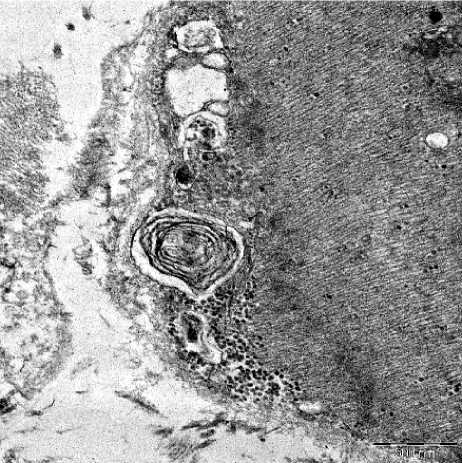
Рис. 4. Ультрамикрофото препарата миокарда пациентки. Формирование муль-тиламеллярной миелиноподобной структуры в периферических участках саркоплазмы кардиомиоцита. Участки разволокнения базальной мембраны. Электронная микроскопия. Ув.: ×10000
При этом морфологически в тканях миокарда наблюдались типичные признаки LAMP2-кардиомиопатии с выраженной гипертрофией кардиомиоцитов, наличием цитоплазматических вакуолей различного размера и фиброзом интер-стиция. При проведении ультраструктур-ного исследования в саркоплазме кардиомиоцитов были выявлены многочисленные включения аутофагоцитарного материала и гликогена, признаки дезорганизации миофибрилл, что также соответствует морфологической картине болезни Данона. Однако в большинстве исследований не описывается наличие миелиноподобных структур, которые обнаруживались нами под сарколеммой кардиомиоцитов. Вероятно, формирование этих образований можно связать с имевшими место процессами развивающегося аутофагоцитоза вследствие частичного сохранения функций мутантных LAMP2 белков, что подтверждается обнаружением в саркоплазме вторичных лизосом [12].
По совокупности клиникоанамнестических данных, результатов молекулярно-генетического, морфологического исследований, включавшего имму-
Список литературы Поздняя диагностика болезни Данона: морфологическая характеристика LAMP2-кардиомиопатии (клиническое наблюдение)
- Danon MJ, Oh SJ, DiMauro S, et al. Lysosomal glycogen storage disease with normal acid maltase. Neurology. 1981;31(1):51-7. https://doi.org/10.1212/wnl.31.1.51
- Nishino I, Fu J, Tanji K, Yamada T, et al. Primary LAMP-2 deficiency causes X-linked vacuolar cardiomyopathy and myopathy (Danon disease). Nature. 2000;406(6798):906-10. https://doi.org/10.1038/35022604
- Tanaka Y, Guhde G, Suter A, et al. Accumulation of autophagic vacuoles and cardiomyopathy in LAMP-2-deficient mice. Nature. 2000;406(6798):902-6. https://doi.org/10.1038/35022595
- Roos JCP, Daniels MJ, Morris E, et al. Heterogeneity in a large pedigree with Danon disease: Implications for pathogenesis and management. Mol Genet Metab. 2018;123(2):177-183. https://doi.org/10.1016/j.ymgme.2017.06.008
- Boucek D, Jirikowic J, Taylor M. Natural history of Danon disease. Genet Med. 2011;13(6):563-8. https://doi.org/10.1097/GIM.0b013e31820ad795
- Cheng Z, Fang Q. Danon disease: focusing on heart. J Hum Genet. 2012;57(7):407-10. https://doi.org/10.1038/jhg.2012.72
- Vaykhanskaya TG, Sivitskaya LN, Danilenko NG i dr. Bolezn' Danona: redko vyyavlyaemoe sistemnoe zabolevanie s lamp2-kardiomiopatiey. Ros-sysky kardiologichesky zhurnal. 2017;10(150):93-99. In Russian
- Sugie K, Komaki H, Eura N, et al. A Nationwide Survey on Danon Disease in Japan. Int J Mol Sci. 2018;19(11):3507. https://doi.org/10.3390/ijms19113507
- Blagova OV, Nedostup AV, Kogan EA. Bolezni miokarda i perikarda. Ot sindromov k diagnozu i lecheniyu.- Moskva: Gyeotar-Mediya; 2019.- 884s. In Russian.
- Taylor MRG, Ku L, Slavov D et al. Familial Cardiomyopathy Registry. Danon disease presenting with dilated cardiomyopathy and a complex phenotype. J Hum Genet. 2007;52(10):830-835. https://doi.org/10.1007/s10038-007-0184-8
- Maron BJ. A phenocopy of sarcomeric hypertrophic cardiomyopathy: LAMP2 cardiomyopathy (Danon disease) from China. Eur Heart J. 2012;33(5):570-2. https://doi.org/10.1093/eurheartj/ehr438
- Hariri M, Millane G, Guimond MP, et al. Biogenesis of multilamellar bodies via autophagy. Mol Biol Cell. 2000;11(1):255-68. https://doi.org/10.1091/mbc.11.1.255
- Cheng Z, Fang Q. Danon disease: focusing on heart. J Hum Genet. 2012;57(7):407-10. https://doi.org/10.1038/jhg.2012.72


