Предикторы развития послеоперационных вентральных грыж и их профилактика в ургентной хирургии
Автор: Федосеев Андрей Владимирович, Инютин Александр Сергеевич, Лебедев Сергей Николаевич, Шкляр Вячеслав Сергеевич
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Клиническая медицина
Статья в выпуске: 2 (44), 2020 года.
Бесплатный доступ
Проблема прогнозирования и профилактики послеоперационных вентральных грыж является актуальной. Обследовано 450 больных на предмет предикторов грыжеобразования с определением степени его риска. Для оценки морфологии передней брюшной стенки 71 пациенту выполнено МРТ передней брюшной стенки. Выделены большие и малые предикторы грыжеобразования. Значимые в патогенезе грыжеобразования изменения тканей передней брюшной стенки, выявленные при МРТ, преобладали у лиц пожилого возраста, в особенности дефекты апоневроза, не определяемые физикально, что является высоким риском формирования послеоперационных вентральных грыж. С учетом степени риска послеоперационных вентральных грыж реализованы методы хирургической профилактики. В случае низкого риска лапарорафию необходимо проводить шахматно-укрепляющим швом, при высоком риске - превентивное протезирование, а при его невозможности - лапарорафию с использованием нити из сетчатого полипропиленового имплантата по разработанной методике.
Лапаротомия, ушивание апоневроза, послеоперационная вентральная грыжа, превентивное протезирование, сетчатая нить, мрт передней брюшной стенки
Короткий адрес: https://sciup.org/143172342
IDR: 143172342 | УДК: 617.55-089.84
Predictors of the development of postoperative ventral hernias and their prevention in urgent surgery
The problem of predicting and preventing postoperative ventral hernias is highly relevant. We examined 450 patients to identify predictors of hernia formation and determine its risk. Seventy-one patients have undergone MRI of the anterior abdominal wall to assess its morphology. We have identified minor and major predictors of hernia formation. Changes in the anterior abdominal wall tissues significant for the pathogenesis of herniation detected during MRI, prevailed in the elderly patients, especially aponeurosis defects that cannot be detected by physical examination, which implies a high risk of postoperative ventral hernias. We used methods of surgical prevention with the consideration of the risk of postoperative ventral hernias. Laparorrhaphy with the staggered strengthening suture is recommended for low-risk patients, whereas high-risk patients should undergo preventive grafting or laparorrhaphy using a polypropylene mesh implant according to the developed technique (if grafting is impossible).
Текст научной статьи Предикторы развития послеоперационных вентральных грыж и их профилактика в ургентной хирургии
В современной хирургии, несмотря на стремительное развитие лапароскопических методов лечения, срединный лапаро-томный доступ не уступает своих позиций, особенно в экстренной хирургии. Одним из осложнений операций, выполненных через указанный доступ, является послеоперационная вентральная грыжа (ПОВГ), ухудшающая качество жизни пациента, что требует повторной операции, приводящей к риску послеоперационных осложнений, а также влияющей на экономическую составляющую лечения данной патологии [7, 10]. По разным данным частота ПОВГ варьируется в широких пределах - от 2 до 33 % [2, 4, 7, 9]. ПОВГ многофакторная патология, вызываемая такими причинами, как ожирение, кахексия, пол, пожилой возраст, сахарный диабет, желтуха, аневризмы брюшной аорты, анемия, использование вазопрессорных препаратов, прием гормональных препаратов, курение, ХОБЛ, онкологические заболевания, доброкачественная гипертрофия предстательной железы, запоры и асцит [1, 3, 7] При этом вопрос прогнозирования ПОВГ остается открытым. Многие из факторов риска ПОВГ находятся вне контроля хирурга, в отличие от используемой техники лапарорафии, которая не меньше оказывает влияние на появление подобного осложнения, о чем свидетельствует ряд рандомизированных исследований. [6, 7, 8]. Поэтому важным является вопрос прогнозирования ПОВГ с выбором способа закрытия лапаротомной раны [2, 4, 5]. Немаловажен и факт наличия возможных дефектов белой линии живота без клинических проявлений грыжи при отсутствии в анамнезе срединной лапаротомии, что нужно учитывать при выборе метода лапарорафии и требует проведения предоперационного инструментального обследования тканей передней брюшной стенки.
Цель исследования: улучшение результатов лечения больных после срединной лапаротомии путём уменьшения частоты эвентраций и ПОВГ.
Материалы и методы
Обследовано 450 больных, прооперированных по поводу экстренной хирургической патологии через срединный лапаро-томный доступ. У данных пациентов в предоперационном и раннем послеоперационном периодах проанализировано порядка 45 потенциальных факторов риска формирования ПОВГ: вес, рост, индекс массы тела, наличие анатомо-функциональной недостаточности предней брюшной стенки, наличие признаков НДСТ с использованием критериев Смольновой Т.Ю. (2003), Т. Мил-ковска-Дмитровой и А. Каркашева (1987), наличие в анамнезе тяжёлого физического труда, занятие силовыми видами спорта, показатели красной крови, уровень билирубина, креатинина, глюкозы крови, содержание белка в сыворотке, сопутствующая патология, курение в анамнезе, основное заболевание, характер оперативного вмешательства и его длительность, наличие раневых инфекционных осложнений, наличие рубца в области оперативного доступа, способ закрытия лапаротомной раны, вид шовного материала, наличие перитонита, асцита, ношение бандажа в послеоперационном периоде. Через 1 год оценивались наличие дефектов апоневроза (физикально и по данным УЗИ), наличие грыжевого выпячивания: локализация, размер, отношение его к послеоперационному рубцу.
Для оценки связи между конституциональными, возрастными факторами и морфологическим строением передней брюшной стенки обследовали 71 пациента, обратившегося в лечебные учреждения для выполнения магнитно-резонансного исследования брюшной полости по различным, не связанным непосредственно с патологией передней брюшной стенки поводам. У лиц мужского пола распределение по возрасту составило: 11,7 % - молодые; 35,3 % - зрелые; 47 % - пожилые. Женщины распределились следующим образом: 24 % - молодые; 27,7 % - зрелые; 42,6 % - пожилые; 5,5 % - лица старческого возраста. Определяли скрытые дефекты апоневроза, жиро- вую инволюцию мышц, расширение пупочного кольца, диастаз прямых мышц.
На следующем этапе применены разработанные методы хирургической профилактики ПОВГ: способ ушивания лапаро-томной раны, заключающийся в наложении укрепляющего и шахматного швов (патент на изобретение № 2644846), методику превентивного протезирования передней брюшной стенки (патент на изобретение № 2670684) и способ ушивания лапаротом-ной раны с применением сетчатой нити (патент на изобретение № 2714439).
Лапарорафия шахматно-укрепляющим швом, заключающемся в наложении укрепляющих швов и непрерывного шва с расположением стежков в шахматном порядке (непрерывный шахматный шов) выполнена у 90 пациентов (рис. 1).
В контрольной группе, составившей 78 пациентов, белая линия живота ушивалась отдельными узловыми швами с применением полифиламентного нерассасывающе-гося шовного материала.
Обе группы были идентичны по полу (tn = 0,147; р = 0,087), по виду и частоте сопутствующих заболеваний (tст = 0,584; р = 0,092). Среди сопутствующей патологии у пациентов обеих групп в значительной степени преобладали заболевания сердечно-сосудистой системы, зарегистрированные у 50 % (24 чел.) лиц основной группы и у 47,6 % (30 чел.) пациентов - в контрольной. Эндокринная патология (сахарный диабет, гипотиреоз) обнаружена у 13 (27,1 %) больных в основной группе и у 13 (20,6 %) -в контрольной. Патология дыхательной системы встречалась реже: в 12,5 % и в 17,5 % случаев соответственно. Несколько сопут- ствующих заболеваний диагностировано у 7 (14,6 %) пациентов основной группы и у 10 (15,9 %) - группы контроля.
Показания к экстренному оперативному вмешательству через срединный доступ также значимых отличий не имели (t ст = -1,804; р = 0,168). Острая кишечная непроходимость в основной группе была диагностирована у 19 (39,6 %) пациентов, в группе контроля - в 25 (39,7 %), перфорация полого органа - у 17 (35,4 %) и у 20 пациентов (31,7 %), воспалительно-деструктивные заболевания органов брюшной полости - у 8 (16,7 %) и 13 (20,6 %), желчекаменная болезнь, холедохолитиаз 8 (16,7 %) и 13 (20,6 %). Герниолапаротомия по поводу ущемленной послеоперационной вентральной грыжи с резекцией тонкой кишки в основной группе выполнена в одном (2 %) случае, в группе контроля - в двух (3,2 %). Гемоперитонеум у пациентов в обеих группах диагностирован с одинаковой частотой: в основной группе в трех (6,3 %) случаях и в группе контроля - также в трех (4,8 %).
Выполнено 27 оперативных вмешательств у больных высокого риска послеоперационного грыжеобразования: 15 (основная группа) - с применением превентивного эндопротезирования, заключающегося в имплантации сетчатого имплантата шириной 3 см. и длиной, соответствующей длине лапаротомии, в преперитоне-альное пространство вдоль линии разреза срединного апоневроза и ушиванием последнего непрерывным швом с захватом сетчатого имплантата (10 больных) (рис. 2).
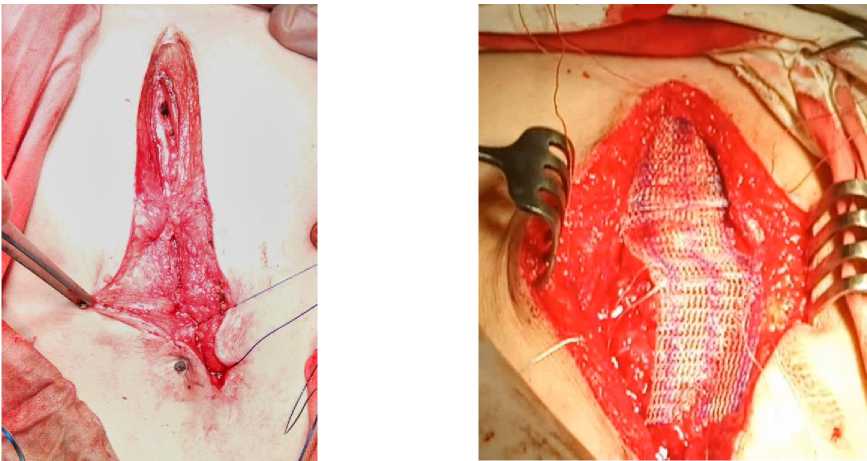
Рис. 1. Лапарорафия шахматно-укрепляющим швом
В случае невозможности реализации последнего, вследствии высокого анестезиологического риска (ASA > 4 МНОАР-89 > 5), технических трудностей, в качестве альтернативы реализовывался способ ушивания лапаротомной раны с применением сетчатой нити (5 больных). Способ основан на ушивании белой линии живота укрепляющими швами в местах наибольшего натяжения ее краев с последующим наложением непрерывного шва. В качестве материала для выполнения укрепляющих швов служит сетчатый эндопротез цилиндрической формы, получаемый путём растягивания за края полос сетчатого эндопротеза шириной 12 мм, длиной 15 см на максимально возможную длину, фиксирующегося в открытом ушке режущей, изогнутой на 1/2 или 3/8 окружности, хирургической иглы с диаметром не менее 1мм. и
Рис. 2. Методика превентивного протезирования передней брюшной стенки ушиванием белой линии живота таким образом, что первый вкол иглы делается, отступя 1см от линии разреза белой линии живота снаружи внутрь, а выкол на противоположной вколу стороне белой линии живота в косом направлении на 1,5 см от края раны и в 1,5 см относительно уровня вкола, следующий вкол иглы выполняется на противоположной стороне белой линии живота на 1,5 см от края последней и на том же уровне, что и первый выкол иглы, а вы-кол производится на противоположной вко-лу стороне белой линии живота в косом направлении на 1 см от края раны на уровне первого вкола. Свободные концы сетчатых нитей завязываются на два узла, при этом лишние концы отрезаются в 2–3 мм от второго узла и прошиваются проленовой нитью 2-0 (рис. 3–4).
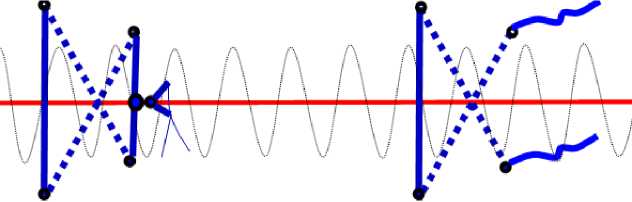
Рис. 3. Схема способа ушивания лапаротомной раны с применением сетчатой нити
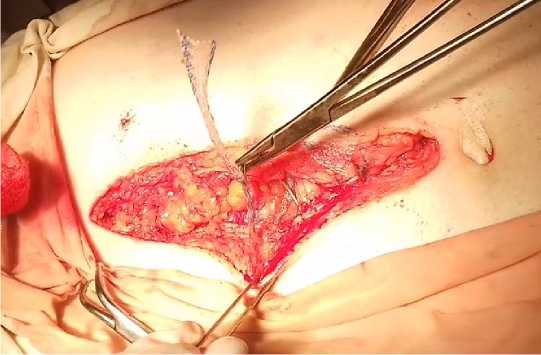
Рис. 4. Ушивание лапаротомной раны с применением сетчатой нити
В контрольной группе у 12 больных с высоким риском грыжеобразования лапа-рорафия проводилась отдельными узловыми швами.
Группы были сравнимы по типам и частоте применения той или иной разновидности срединной лапаротомии (tCT = 0,76; p < 0,05), полу (t ст = 0,147; р = 0,087), возрасту (tn = 0,68; p < 0,05), наличию сочетания нескольких факторов риска послеоперационного грыжеобразования. Показания к экстренному оперативному вмешательству через срединный доступ также значимых отличий не имели. Острая кишечная непроходимость в основной группе была диагностирована у пяти (39,6 %) пациентов, в группе контроля - у трех (39,7 %), перфорация полого органа - у трех (35,4 %) пациентов основной группы и у двух - контрольной (31,7 %), воспалительно-деструктивные заболевания органов брюшной полости - у пяти (16,7 %) и четырех (20,6 %) соответственно, желчекаменная болезнь, холедохо-литиаз у двух пациентов основной группы и трёх контрольной.
В послеоперационном периоде у всех больных во время физикального и ультразвукового исследования оценивалась частота раневых осложнений, таких как эвентрация, послеоперационнная вентральная грыжа.
При сравнении исследуемых групп применяли критерий Стьюдента (tcj). Для корреляционого анализа использовали линейную корреляцию Пирсона (r) и ранго- вую Спирмена (гсп). С целью проверки вероятности события использовали U-критерий Манна-Уитни. Достоверность результатов оценивали положительной при получении p < 0,05.
Результаты
Частота формирования ПОВГ после срединных лапаротомий через 12–14 месяцев наблюдения составила 19 % (85 случаев). С учетом факторов риска возникновения ПОВГ разработана схема определения показаний к превентивному эндопротезированию, основанная на расчете силы корреляционной связи методом Пирсона для каждого из значимых факторов. На основании полученных данных были выделены «большие предикторы», сила связи которых с изучаемым явлением составила 0,9–0,7 и «малые предикторы» - с силой связи от 0,7 до 0,5.
«Большими предикторами» являются возраст старше 60 лет, ожирение, верхнесрединный доступ, фибринозный, либо ограниченный гнойный перитонит, недифференцированная дисплазия соединительной ткани, возвращение к тяжёлому физическому труду.
«Малые предикторы»: возраст 44-59 лет, брахиморфный живот, повышенный уровень креатинина (110 мкмоль/л), повышенный уровень глюкозы крови (> 7 ммоль/л), анемия II-III ст., длительность операции более 120 мин. (табл. 1).
Таблица 1
Предикторы грыжеобразования
|
№ |
Признак |
Коэффициент корреляции(r) |
|
1 |
Возраст старше 60 лет |
0,847 |
|
2 |
Ожирение |
0,834 |
|
3 |
Верхнесрединный доступ |
0,765 |
|
4 |
Раннее возвращение к тяжелому физическому труду |
0,742 |
|
5 |
Фибринозный или ограниченный гнойный перитонит |
0,735 |
|
6 |
НДСТ |
0,718 |
|
7 |
Возраст 44–59 лет |
0,693 |
|
8 |
Брахиморфный живот |
0,652 |
|
9 |
Креатинин > 110мкм/л |
0,597 |
|
10 |
Глюкоза крови > 6 ммоль/л |
0,575 |
|
11 |
Анемия II–III степени. |
0,569 |
|
12 |
Длительность операции более 120 минут |
0,561 |
Комбинация данных признаков даёт частоту грыжеобразования в случае наличия двух «больших» предикторов в 65 % (p < 0,05), трёх «малых» – 75 % (p < 0,05), трёх «больших» – до 85 % (p < 0,05), в результате чего риск появления ПОВГ разделён на высокий (вероятность появления грыжи более 80 %) и низкий (менее 80 %).
После МРТ наиболее часто, у 51 (41,4 %) обследованных, диагностировалась жировая инволюция мышц передней брюшной стенки, диастаз белой линии живота определялся у 31 (25,2 %) больного, расширение пупочного кольца у 26 (21,1 %) пациентов, а дефекты апоневроза белой линии, не определяемые при физикальном обследовании, в 15 (12,2 %) случаях. Важно отметить, что сочетание указанных изменений преобладали у лиц пожилого возраста, что объясняет сильную зависимость возраста старше 60 лет и риска грыжеобразования после срединной лапаротомии. Немаловажен и факт обнаружения дефектов апоневроза, являющимися по своей сути основой для формирования грыжи, указывая на «слабость» соединительнотканных структур, что следует отнести к высокому риску грыжеобразования.
При сравнении способов ушивания в основной группе эвентраций не было, ПОВГ отмечены у четырех (4,4 %) пациентов. У трех (3,3 %) пациентов при ультразвуковом исследовании выявлены дефекты апоневроза без грыжевого мешка (рис. 5).
В контрольной группе выявлено четыре (5 %) эвентрации и семь ПОВГ (9 %) в течение года. Дефекты рубца обнаружены у шести (7,6 %) пациентов (рис. 6). Из 13 больных с дефектами и грыжами апоневроза контрольной группы высокий риск гры-жеобразования отмечен только в 46 % случаев (шесть больных). У семи больных ПОВГ риск грыжеобразования был низким.
У шести больных основной группы с дефектами апоневроза и ПОВГ высокий риск грыжеобразования был диагностирован в 85 % случаев. Причём шесть больных основной группы также имели высокий риск развития осложнений, но грыжевых выпячиваний и дефектов послеоперационного рубца апоневроза выявлено не было. Следует признать, что предлагаемый способ ушивания апоневроза в случае высокого риска грыже-образования имеет определенные ограничения. Альтернативным способом профилактики ПОВГ с высоким риском грыжеоб-разования представляется превентивное протезирование передней брюшной стенки.
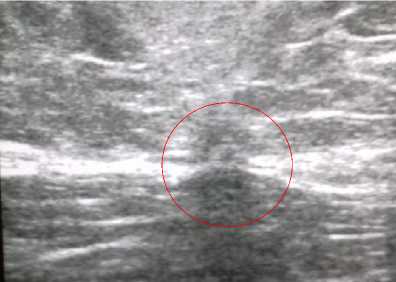
Рис. 5. Дефект рубца белой линии живота (УЗИ)
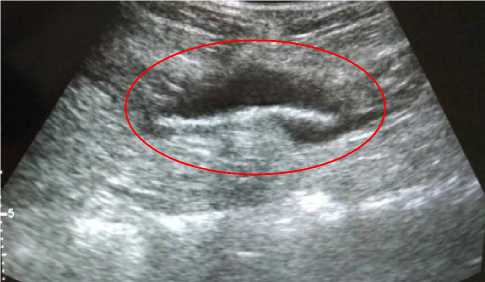
Рис. 6. Перипротезная серома (УЗИ)
При оценке характера раневого процесса по шкале ASEPSIS на седьмые сутки в основной группе «удовлетворительное» заживление лапаротомной раны отмечено у 79 (87,7 %) больных, «нарушенное» – у пяти (5,6 %), с признаками «минимального инфицирования» – у четырех (4,4 %), «умеренного инфицирования» – у двух (2,3 %), В контрольной группе «удовлетворительное заживление» диагностировано у 64 (82 %) больных, «нарушенное» – у шести (7,7 %), с признаками «минимального инфицирования» – у четырех (5,1 %), «умеренного инфицирования» – у двух (2,6 %), «тяжелой раневой инфекции» – у двух (2,6 %). Таким образом, в раннем послеоперационном периоде различий в течение раневого процесса при разных способах ушивания белой линии живота не выявлено (t Сt = –0,232; р = 0,251).
В группе высокого риска грыжеобразо-вания в случаях превентивного эндопротезирования передней брюшной стенки в течение 12–15 месяцев грыжевых выпячиваний, дефектов апоневроза выявлено не было. У пациентов, лапарорафия которым проводилась сетчатой нитью, грыжевых выпячиваний зафиксировано не было, но при УЗИ в одном случае диагностирован дефект апоневроза. В контрольной группе грыжи зафиксированы у 7 (58 %) человек. При превентивном протезировании серо- мы, потребовавшие дренирования под контролем ультразвука, диагностированы в двух случаях (1 типа по S. Morales-Conde 2012 г.). У четырех пациентов серомы были клинически не значимыми (0 тип по S. Morales-Conde 2012 г.) (рис. 6).
У двух пациентов с сетчатым швом и у трех с узловым узловых швов выявлены клинически незначимые серомы (0 тип по S. Morales-Conde 2012 г.). Частота формирования сером в основной группе была достоверно выше, чем в контрольной (p < 0,05), но на результате лечения это не сказалось.
Выводы
-
1. Для прогноза развития ПОВГ нужно учитывать несколько факторов их возникновения и в случае низкого риска применять шахматно-укрепляющий способ ушивания белой линии живота, при высоком риске – превентивное протезирование, а при его невозможности – лапарорафию с использованием нити из сетчатого полипропиленового имплантата по разработанной методике.
-
2. МРТ позволяет выявить морфологические изменения передней брюшной стенки, что нужно учитывать при закрытии передней брюшной стенки, применяя методики, способствующие формированию прочного рубца.
Список литературы Предикторы развития послеоперационных вентральных грыж и их профилактика в ургентной хирургии
- Lavreshin P.M., Gobedzhishvili V.K., Gobedzhishvili V.V. i dr. Prognozirovanie razvitiya pervichnyh posleoperacionnyh ventral'nyh gryzh // Sovremennye problemy nauki i obrazovaniya. - 2015. - № 3. URL: http://science-education.ru/ru/article/view?id=18369.
- Lebedev S.N., Fedoseev A.V., Inyutin A.S. i dr. Preventivnoe endoprotezirovanie pri sredinnyh laparotomiyah // Nauka molodyh (Eruditio Juvenium). - 2018. - T. 6. - № 2. - S. 211-217.
- Nacional'nye klinicheskie rekomendacii po gerniologii. Razdel "Posleoperacionnye ventral'nye gryzhi" Rossijskie klinicheskie rekomendacii po diagnostike, lecheniyu i profilaktike venoznyh tromboembolicheskih oslozhnenij 2017 god. Kratkoe izdanie. - M: Izdatel'stvo Rossijskogo Obshchestva Hirurgov, 2017. - 56 s.
- Fedoseev A.V., Murav'ev S.Yu., Budarev V.N. i dr. Nekotorye osobennosti beloj linii zhivota, kak predvestniki posleoperacionnoj gryzhi // Rossijskij mediko-biologicheskij vestnik imeni akademika I.P. Pavlova. - 2016. - № 1. - S. 109-115.
- Amjad S., Zia A., Syed M. A. et al. Incisional Hernia Post Laparotomy-Incidence and Risk Factors// Journal of Surgery. - 2018. - Vol. 6, № 1. - Р. 19-22.
- Deerenberg EB, Harlaar JJ, Steyerberg EW et al. Small bites versus large bites for closure of abdominal midline incisions (STITCH): a double-blind, multicentre, randomised controlled trial. Lancet. 2015. Epub. http://dx.doi. org/. DOI: 10.1016/S0140-6736(15)60459-7
- Cornish et al. Hughes Abdominal Repair Trial (HART) - Abdominal wall closure techniques to reduce the inci-dence of incisional hernias: study protocol for a randomized controlled trial Trials (2016) 17:454 DOI: 10.1186/s13063-016-1573-0
- Rahbari NN, Knebel P, Kieser M et al. Design and current status of CONTINT: continuous versus interrupted abdominal wall closure after emergency midline laparotomya randomized controlled multicenter trial [NCT00544583]. Trials. 2012;13:72.
- Skipworth JR, Khan Y, Motson RW et al. Incisional hernia rates following laparoscopic colorectal resection. Int J Surg. 2010;8(6):470-3.
- Van Ramshorst GH, Eker HH, Hop WC et al. Impact of incisional hernia on health-related quality of life and body image: a prospective cohort study. Am J Surg. 2012;204(2):144-50.


