Прерывистая гормонотерапия местнораспространенного рака простаты
Автор: Задерин В.П., Шевченко А.Н.
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Биологические науки
Статья в выпуске: 5-2 т.11, 2009 года.
Бесплатный доступ
Прерывистая гормонотерапия (ПГТ) местно-распространенного рака предстательной железы уменьшает побочные реакции гормонотерапии, повышая тем самым экологичность процесса медикаментозного воздействия на человека без ущерба для лечения опухоли. В исследование включено 19 больных раком простаты стадии Т3NXM0. Контролировали эффективность лечения уровнем ПСА и тестостерона крови, размерами простаты, качеством мочеиспускания, мониторингом функционального состояния сердечнососудистой системы и печени. Установлено, что время для достижения клинического и биохимического «здоровья» - 3-18 месяцев. Время прироста ПСА до уровня 15 нг/мл составило 9-17 месяцев. Длительность курса ПГТ - 6-25 мес., включая 35-78% времени без гормонотерапии. У 25% пациентов уровень тестостерона приходил к норме в период без гормонального лечения, что улучшало качество жизни.
Местнораспространенный рак простаты, прерывистая гормонотерапия
Короткий адрес: https://sciup.org/148198768
IDR: 148198768 | УДК: 612.018.2:615.7:611.637-006.6
Interrupted hormonotherapy of locally-advanced prostate cancer
Interrupted hormonetherapy (IHT) of locally-advanced prostate cancer reduces side-effects of hormonal therapy, thus increasing ecology of treatment process on humans, without prejudice to tumor treatment. The study included 19 patients with prostate cancer st. T3NXM0. Treatment efficacy was controlled by PSA level, blood testosterone level, sizes of prostate, quality of urination, monitoring of functional state of cardiovascular system and liver. It is es-tablished, that period for achieving clinical and biochemical "health" was equal to 3-18 months. Period of PSA in-crease to the level of 15 ng/ml was 9-17 months. The course of IHT continued during 6-25 months, including 35- 78% of time without treatment. In 25% of patients testosterone level came to norm during the period without hormo-nal treatment which improved quality of life.
Текст научной статьи Прерывистая гормонотерапия местнораспространенного рака простаты
посредством которой регулировался уровень тестостерона и простатоспецифического антигена (ПСА) и, в зависимости от их уровня, прекращалось или возобновлялось гормональное лечение. В [2] сообщили об успешном применении прерывистой гормонотерапии рака простаты. Средняя длительность времени, когда больной не получал гормональные препараты, составляла 38-50% от общего времени курса ПГТ. У 25% пациентов уровень тестостерона возвращался к норме в течение периода без гормонального лечения, что положительно сказывалось на качестве их жизни. На современном уровне знаний, стратегия гормонотерапии рака простаты должна строиться с учетом возможных побочных осложнений противоопухолевой терапии, степени допустимой тяжести осложнений, своевременности и эффективности профилактики и лечения возникших осложнений. Все эти условия не может выполнить схема непрерывной гормонотерапии рака простаты. Исходя из вышесказанного, метод прерывистой гормонотерапии можно отнести к разряду инновационной клинической технологии, позволяющей проводить специальную противоопухолевую терапию и, одновременно, соблюдать принцип – «не навреди».
Цель работы – улучшение результатов консервативного лечения больных местнораспространенным раком простаты стадии
Т3NXM0, имеющих хронические сопутствующие заболевания сердечно-сосудистой системы и печени.
Материал и методы. В исследование было включено 19 больных в возрасте от 56 до 82 лет, с верифицированным местно распространенным раком простаты стадии Т3NXM0, положительно реагирующих на гормонотерапию. Однако наличие сопутствующих заболеваний со стороны сердечнососудистой системы и печени (последствия инфаркта миокарда, кардиосклероз, гипертоническая болезнь, диабет, гепатит), осложняли проведение непрерывной гормонотерапии риском обострения заболеваний, что вынуждало врача временно прекращать гормонотерапию и лечить осложнения. Пациенты были разделены на две группы: 1 группа (10 человек) - больные, которых лечили методом НГТ в объеме максимальной андрогенной блокады + лучевая терапия на зону предстательной железы. Лучевое лечение рака простаты проводили больным в возрасте до 70 лет, в компенсированном состоянии заболеваний сердечнососудистой системы и печени. Режим наружной лучевой терапии: 2 Грея в день до суммарной дозы 60-65 Грей. Лучевую терапию больные перенесли в основном удовлетворительно. После лучевого лечения больным проводили НГТ в течение 6 месяцев и далее, при условии стабильного снижения ПСА менее 4 нг/мл, продолжали гормонотерапию в прерывистом режиме. Эффективность ПГТ контролировали ежемесячным исследованием ПСА крови в течение 6 месяцев, затем каждые 2-3 месяца («активное наблюдение»). Непрерывное гормональное лечение начинали при условии увеличения ПСА на 0,5 нг/мл или более ежемесячно в течение 3х месяцев или при стабильном показателе ПСА более 4 нг/мл. Опухоль становится ан-дрогеннезависимой когда, несмотря на проводимое лечение, значение ПСА остается более 4 нг/мл или происходит увеличение его значения на 4 нг/мл после каждого последующего анализа в течение 3 месяцев, несмотря на посткастрационный уровень тестостерона.
2 группа (9 человек) – больные, которым НГТ назначена в качестве основного варианта лечения (без лучевой терапии), с последующим переводом его в режим ПГТ. Первый месяц – лечение антиандрогенами:
прием препаратов Касодекс 150мг, 1табл. 1раз в день или Нилумид 150мг, 1табл. 1раз в день или Флутамид 250мг, 1табл. 3 раза в день или Андрокур-Депо, 1 инъекция внутримышечно, 1раз в 2недели. На 15 день после начала лечения делают инъекцию ЛГРГ (лютеинезирующий релизинг-гормон) или ГнРГ (гонадотропин релизинг-гормон) – препараты Золадекс, Простап, Люкрин. Контроль ПСА и тестостерона через 3 месяца. При стабильном снижении ПСА<4 нг/л лечение прерывают, продолжая контроль ПСА каждый месяц. При увеличении ПСА до первоначального уровня – возобновляют лечение по вышеописанной схеме (лечение антиандрогенами). Если ПСА не снизился и уровень тестостерона не приблизился к по-сткастрационному (медикаментозная кастрация) уровню, то продолжают лечение больного, как при гормонорезистентном раке простаты. В качестве дополнительной гормональной терапии мы применяли схему «проскар+касодекс», т.к. проскар блокирует внутрипростатический переход тестостерона в дигидротестостерон, а касодекс блокирует цитоплазматические рецепторы дигидротестостерона. Улучшение мочеиспускания достигали назначением препаратов Ом-ник или Дальфаз. При симптомах расстройства мочеиспускания, похожих на клинику нейрогенного мочевого пузыря, назначали Детрузитол. Если медикаментозная терапия не снижала уровень тестостерона или не было существенной динамики снижения ПСА, больным предлагают хирургическую кастрацию (выполнена двум больным). Контроль размеров и объема простаты позволяет судить об эффективности лечения и о вероятной причине дизурических расстройств у больного (раздражение шейки мочевого пузыря за счет давления опухоли). В случае угрозы острой задержки мочи больным выполняли трансуретральную резекцию (ТУР) простаты или эпицистостомию, что позволяло восстанавливать пассаж мочи, предотвращать тяжелые осложнения в верхних мочевых путях. В случае эффективного лечении рака простаты восстанавали мочеиспускание. Контролировали эффективность лечения по пяти основным показателям: уровень ПСА крови, уровень тестостерона, размеры предстательной железы, качество мочеиспускания, мониторинг функционального состояния сердечнососудистой системы и печени (электрокардиограмма, свертывающая система крови, липиды крови, мочевина, креатинин, билирубин, ферменты крови, и другие исследования по рекомендации и под контролем терапевта, кардиолога).
Результаты исследования. Исследование проводилось в течение 8 лет и в него были включены больные раком простаты, которые поступали на лечение в урологическое отделение РНИОИ в разные годы. Анализ 19 случаев ПГТ рака простаты показывает, что время для достижения клинического и биохимического «здоровья» составляет от 3 до 18 месяцев. Время прироста ПСА до уровня 15 нг/мл составило 9-17 месяцев. В течение периода «без лечения» больным необходимо каждые 3 мес. определять уровень ПСА и тестостерона. Если у пациента уровень ПСА до лечения был больше 20 нг/мл и в результате лечения снизился до показателей менее 4 нг/мл, но затем стал увеличиваться («биохимический рецидив»,то новый цикл гормонального лечения начинают при достижении уровня ПСА 10-20 нг/мл. При исходном уровне ПСА 10-20 нг/мл второй курс лечения начинают при увеличении ПСА 5-15 нг/мл. По нашим данным длительность курса ПГТ у пациентов была от 6 до 25 мес., при этом период без гормонотерапии составил 35-78% от общего времени лечения. У 22% пациентов уровень тестостерона приходит к норме в течение периода без гормонального лечения, что положительно сказывалось на качестве жизни (восстановление либидо). Время наблюдения за больными было от 18 до 105 месяцев. Под нашим постоянным наблюдением находилось 6 больных местнораспространенным раком простаты: 1 больной наблюдается 114 месяцев, 2 больных – 36 и 39 месяцев, 2 больных – 26 и 29 месяцев, 1 больной наблюдался в течение 48 месяцев, получал ПГТ и умер от сердечной недостаточности в возрасте 82 лет. 10 пациентов, начавших ПГТ под контролем нашей клиники продолжают лечение в онкодиспансерах по месту жительства. Судьба 3 больных неизвестна после 8-16 месяцев наблюдения. Следует отметить, что применение лучевой терапии в комплексе с гормонотерапией позволяет быстрее получать эффект восстановления уровня ПСА. Обращает на себя внимание тот факт, что качество жизни больных раком простаты положительно реагирующих на ПГТ составляет 70-80% процентов по шкале качества жизни Карнов-ского.
Клинический пример. Больной Г., 1939 года, и.б. №15573/н. При первичном обращении в РНИОИ, в декабре 2000 г., предъявлял жалобы на дизурию, ночные мочеиспускания до 5 раз. ТРУЗИ простаты: объем простаты 44,4 см3, размеры – 5,1х3,2х5,2 см. Остаточной мочи 45 мл. Пальцевое ректальное исследование выявило бугристую, деревянистой плотности простату, фиксированное парапростатическое пространство. Уровень ПСА крови – 8,85 нг/мл. Пункционная биопсия простаты – аденокарцинома, высокодифференцированная, Глиссон 8. Диагноз: рак предстательной железы Т2в – Т3а N0M0. Сопутствующие заболевания: постинфарктный кардиосклероз, ИБС, диабет 2 типа, ожирение 3 степени. 11.01.2001 года больному выполнена энуклеация яичек и через 3 дня начато ежедневное, в/венное введение эстрогенов (хонвана, суммарная доза 18 грамм). Лечение перенес удовлетворительно. Уровень ПСА после лечения снизился до 0,6 нг/мл, однако размеры простаты не уменьшились. Поэтому с 25.03. по 23.05. 2002 г. больному на область простаты проведена лучевая терапия (ДГТ) суммарной дозой 60 Гр. 27.06.2002 г. уровень ПСА – 0,21 нг/мл. УЗИ простаты: размеры 5,2х4,0х5,7 см, остаточной мочи 67 мл, сохраняются учащенные ночные мочеиспускания (до 5-6 раз). Больному была назначена гормонотерапия, противовоспалительная терапия и спазмолитики. В течение июля-декабря 2002 г. получал эстрадурин-депо по 60 мг в месяц и простамол. УЗИ простаты 16. 01.2003 г.: размеры 4х3,5х4 см с очагами кальцина-тов, остаточной мочи 35 мл. При пальцевом ректальном исследовании – простата очень плотная, гладкая, с очагами повышенной плотности. Мочится свободно, ночные мочеиспускания 1-2 раза, ПСА крови 0,06 нг/мл. В течение 20030-2007 гг. проводился контроль ПСА, уровень тестостерона, УЗИ простаты, мониторинг ЭКГ и субъективного самочувствия пациента. Уровень ПСА колебался от о,01 до 0,09 нг/мл (рис. 1). Размеры простаты – 4,8х3,0х4,0. Пациент социально активен, работает на прежней работе по своей специальности (радиоинженер), восстановилась половая функция без применения стимулирующих лекарственных препаратов, получает плановое профилактическое лечение сердечной недостаточности. В мае 2008 г., после перенесенного гриппа, стал отмечать вялую струю мочи и учащенные мочеиспускания ночью до 5 раз. УЗИ простаты- 5,0х4,0х4,0 см, остаточной мочи – 60 мл. ПСА 4,8 нг/мл. Пальцевое ректальное исследование определило увеличение размеров простаты по сравнению с данными от 16.01.2003 г.. Проведено лечение: андрокур + про-скар в течение 3 месяцев, с перерывом 1 месяц для лечения сердечной недостаточности, затем еще трехмесячный курс андрокур + проскар. В январе 2009 г. при обследовании: УЗИ простаты – 4,5х3,7х4,0, остаточной мочи 20 мл; ночью мочится 1-2 раза; ПСА 1,5 нг/мл. В общей сложности больной наблюдается нами в течение 114 месяцев, При этом только 22% времени больной получал гормональное лечение. Приведенный случай истории болезни пациента с местнораспространенным раком простаты показывает удовлетворительные результаты лучевого лечения в сочетании с прерывистой гормонотерапией, под динамическим контролем ПСА крови (рис. 1) и уровня тестостерона, УЗИ простаты и планового профилак тического лечения сердечной недостаточности.
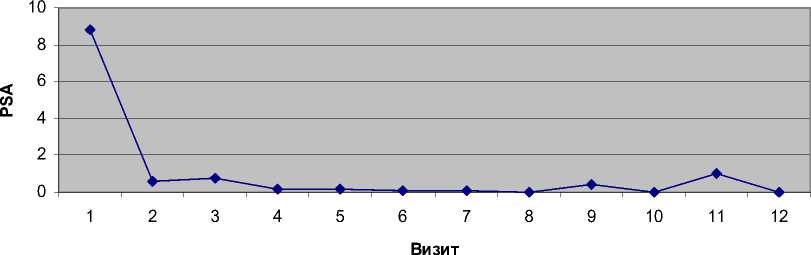
Рис. 1. График изменения уровня ПСА
Выводы: в процессе ПГТ местнораспространенного рака простаты критериями назначения и отмены приема гормональных препаратов должна быть динамика: клинических симптомов рака простаты, уровня ПСА и тестостерона, тяжесть осложнений гормонотерапии со стороны сердечнососудистой системы и печени. Процесс ПГТ динамичен, требует от больного своевременных визитов к врачу для контрольных осмотров и коррекции лечения. Важным преимуществом ПГТ является повышение качества жизни больных РПЖ за счет снижения побочных эффектов гормонотерапии.
Список литературы Прерывистая гормонотерапия местнораспространенного рака простаты
- Klotz, L.H. Intermittent endocrine therapy for advanced prostate cancer/L.H. Klotz, H.W. Herr, M.J. Morse, W.F. Whitmore//Cancer. -1 986. -58. -P. 2546-2550.
- Prapotnich, D. A 10 year clinical experience with intermittent hormonal therapy for prostate cancer/D. Prapotnich, K. Fizazi, B. Escudier// Eur. Urol. -2003. -43. -P. 233-240.


