Приближенный инженерный расчет кристаллизаторов-охладителей для молочного сахара в изогидрических условиях
Автор: Полянский К.К., Калашников Г.В., Муравьев А.С.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Процессы и аппараты пищевых производств
Статья в выпуске: 1 (75), 2018 года.
Бесплатный доступ
Ранее была предпринята попытка создания математической модели непрерывной кристаллизации лактозы в водных растворах при различных пересыщениях. Расчетный способ базировался на основе нового критерия метастабильности пересыщенных растворов. Критерий метастабильности раствора в данном случае представляет собой безразмерную величину от 0 до 1 и отражает роль зародышеобразования в любой момент времени. Другими словами, эта безразмерная величина, показывающая соотношение скоростей зародышеобразования и роста кристаллов. Нами эта величина определена путем математического моделирования с использованием модифицированной модели Гюнтера–Маца. Практическая значимость критерия заключается в установлении области кристаллизации (смешанная, нуклеации и роста) с учетом поверхности внесенной кристаллической фазы. Установлено, что при малой поверхности процесс кристаллизации протекает преимущественно в смешанной области, при отсутствии затравки (F=0), при превышении границы метастабильности идет в бласт нуклеации (Pg=0,1), при больших поверхностях кристаллов F. процесс протекает в области роста даже при высоких пересыщениях (Pg=0,9), т.е. он позволяет быстро определить необходимое количество затравки с целью интенсификации процесса кристаллизации. Он может быть применен для любого кристаллизуемого вещества, если имеются кинетические параметры процесса (константы скорости и кинетические порядки зародышеобразования и роста, растворимость и д.р.). Однако присутствие несахаров и соответствующей приборной базы вызывают большие осложнения по нахождению вышеуказанных параметров процесса рабочих растворов, поэтому остановились на упрощенном инженерном методе расчета.
Кристаллизатор-охладитель, молочный сахар, материальный и тепловой баланс, коэффициент пересыщения, доброкачественность сиропа
Короткий адрес: https://sciup.org/140229987
IDR: 140229987 | DOI: 10.20914/2310-1202-2018-1-37-42
Approximate engineering calculation of chill molds for milk sugar in isohydric conditions
Earlier, an attempt was made to create a mathematical model for the continuous crystallization of lactose in aqueous solutions at various supersaturations. The calculation method was based on a new criterion for the metastability of supersaturated solutions. The metastability criterion of the solution in this case is a dimensionless quantity from 0 to 1 and reflects the role of nucleation at any time. In other words, this dimensionless quantity, showing the ratio of the rates of nucleation and growth of crystals. We determined this value by mathematical modeling using the modified Gunther–Mat model. The practical significance of the criterion is the establishment of a crystallization region (mixed, nucleation and growth), taking into account the surface of the introduced crystalline phase. It is established that for a small surface, the crystallization process proceeds predominantly in the mixed region, in the absence of a seed (F = 0), when the metastability limit is exceeded, goes into the blast nucleation "*"(Pg = 0.1), with large surfaces of the crystals F. The process proceeds in the growth region even at high supersaturations (Pg = 0.9), i.e. it allows you to quickly determine the required amount of seed to intensify the crystallization process. It can be used for any crystallizable substance if kinetic parameters of the process are available (rate constants and kinetic orders of nucleation and growth, solubility, etc.). However, the presence of nonsugars and the corresponding instrument base cause great errors in finding the above parameters of the process of working solutions, therefore, we decided on a simplified engineering calculation method.
Текст научной статьи Приближенный инженерный расчет кристаллизаторов-охладителей для молочного сахара в изогидрических условиях
Известно широкое применение в производстве молочного сахара открытых кристаллизаторов с перемешивающими и охлаждающими устройствами [1, 2, 4–6, 10–13].
При расчетах таких кристаллизаторов используют: уравнение материального баланса; уравнение теплового баланса процесса кристаллизации молочного сахара [3].
Указанные расчеты необходимы для определения таких показателей, как доброкачественность сиропа сыворотки, коэффициент пересыщения, количество кристаллов молочного сахара (в массовом выражении), количество охлаждающей воды.
В реальных условиях, как правило, известны температура кристаллизуемого сиропа, его количество, процентное содержание молочного сахара и сухих веществ в нем, Конечная температура и содержание молочного сахара в конечном растворе задаются [4–7].
Материальный и тепловой баланс, определение расхода воды на кристаллизатор-охладитель
В кристаллизаторе периодического действия с водяной рубашкой и вибрационными дисками охлаждается V =2 м3 насыщенного раствора лактозы С 12 Н 22 О 11 от температуры t 1 н = 75 °С до температуры t 1 к = 20 °C. Начальная температура охлаждающей воды t 2 н = 5 °C. Требуется определить расход охлаждающей воды G и время кристаллизации т , если коэффициент теплопередачи К = 250 Вт/(м2 °C).
По кривой растворимости лактозы [5] определяем концентрацию насыщенного раствора С 12 Н 22 О 11 (массовая доля) при 75 °C, а 1 = 0,49 и при 20 С а 2 =0,161. Так как теплоемкость кристаллов С кр = 1,202 кДж/(кг °C), то по правилу аддитивности определим теплоемкость исходного раствора С 1 :
С = а С кр + ( 1 — а ) С в = 0,49 х 1,202 + (1)
+ ( 1 - 0,49 ) х 4,19 = 2,72 кДж/ ( кг o С )
где С в – теплоемкость воды, С в = 4,19 кДж/(кг°С).
Теплота кристаллизации q = 25,6 кДж/кг, плотность исходного раствора (наибольшая) р 1 = 1545,3 кг/м3.
Из уравнения теплового баланса определяем количество теплоты Q, которое необходимо отводить из раствора при его кристаллизации [8–10]:
Q = Vr С 1 ( t 1 н- 1 1 к ) + GK p q , (2)
Количество образуемых кристаллов G кр , выпадаемых в растворе, можно определить из уравнения материального баланса по сухим веществам:
g kp = а а - v Р 1 =
1 - а 2
0,49 - 0,161,.,.,. .....
--2 - 1545,3 = 1211,9 кг
1 - 0,161
Следовательно:
Q = 2 х 1545,3 х 2,72 х ( 75 - 20 ) +
+ 1211,9 х 25,6 = 493378,3 кДж ,
Определяем поверхность теплопередачи. Так как объем кристаллизуемого раствора задан, а тип оборудования известен, что конструктивно, определяем, например, для вертикального оборудования размеры.
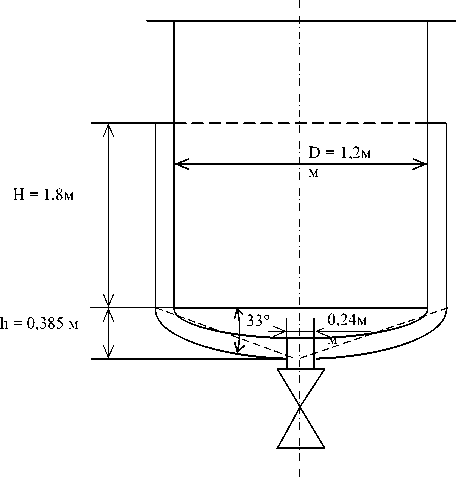
Рисунок 1. Определение размеров кристаллизатора-охладителя
Figure 1. Determination of the sizes of the crystallizer-cooler
При выбранных размерах полезный объем кристаллизатора:
n D 2 т т nD 2 h
Vкр. =--H +
4 43
3,14 - 1,2 2 3,14 - 1,2 2 0,385 , ._. 3
--1,8 +---= 2,1798 м , при этом теплопередающая поверхность оборудования:
и n D D V2
F=nDH+=
= 3,14 - 1,2 - 1,8 + 3,14 - 1,2 - 1,2 - ^2 = 8,37м2
, ,, , 2 2
Приняв температуру воды, выходящей из рубашки в окончательный момент охлаждения t 2 к = 15 °C, определяем:
Доброкачественность сиропа или раствора:
А = t t
—
—
t 2 н t 2 л
Отсюда температур:
20-5 .
=------= 3 и lgA = 0,4771 (7)
20 — 15
вычисляем среднюю разность
Др =50 - 100 = 78,12%.
Коэффициент пересыщения вычисляем по формуле:
К ф
Ки = ,
К ,
раствора
A t ‘ = ср
t 1 н
2,3lg t 1 н t 1 к
t 1 к
—
—
t2н t2н
•
А — 1
2,3 А lg A
75 — 20
3 — 1
2,3 • lg
75 — 5 2,3 • 3 • lg3
= 16,7173 ° С
н где Кф – количество молочного сахара в его растворе при данной температуре, %;Кн – количество молочного сахара в насыщенном растворе, %
Концентрация насыщеного раствора молочного сахара при 20 °С составляет 16,1%:
20 — 5
По найденным значениям F,A и A t ‘ определим время кристаллизации:
Ки =- 20- = 1,24 .
16,1
t = -Q
493378,3 - 103
Составляем материальный баланс кристаллизации. Для этого используем уравнение кристаллизации:
kF A 7 250 - 8,37 - 16,7173 = 14860,79 c « 4,12 ч
SK = 100 M + SK uu к м
Данное время обусловлено интенсификацией процесса изогидрической кристаллизации кристаллов лактозы при использовании низкочастотных гармонических колебаний [7, 12]
Находим расход воды:
kF
G =---
250 • 8,37
c 2 - ln A 4190 - 2,3 - lg3 = 0,4551 кг/с = 1638,39 кг/г,
где теплоемкость воды с 2 = 4190 Дж/(кг -° С)
Общий объем воды за время кристаллизации:
При составлении материального баланса принимаем, что в процессе кристаллизации объемное количество сиропа остается постоянным. С учетом содержания несахаров содержание сухих веществ в периоде окончания кристаллизации составит 26%.
Масса 1 л сиропа, содержащего 26% сухих веществ, равна 1,12 кг, а масса исходного сиропа – 1,3 кг.
Следовательно, объем исходного сиропа составляет 2600/1,3 = 2000 л. В свою очередь масса мелассы равна 2000 - 1,12 = 2240 кг. Определим количество кристаллов молочного сахара:
С обЩ = G X t = (11) = 0,4551 х 14860,79 = 6835,9 кг
Справедливость составления материального и теплового баланса и определения расхода охлаждающей воды проверяется следующим расчетом.
На кристаллизацию при температуре 75 ° C направляется 2600кг сиропа, содержащего 50% молочного сахара, 64% сухих веществ. В процессе кристаллизации температура сиропа снижается до 20 ° С.Содержание молочного сахара в конечном растворе 12%. Составим материальный и тепловой баланс кристаллизации, определим коэффициент пересыщения молочного сахара в сиропе. Вычислим доброкачественность сиропа или раствора.
В соответствии с формулой определяем доброкачественность сиропа или раствора:
2600 - 50 — 2240 - 12
М к =
= 1031,2 кг . (17)
К
Др = -^-100, К
где К и – концентрация молочного сахара в исходном растворе, %; К с.в . – общая концентрация сухих веществ в растворе лактозы, %.
Тепловой баланс процесса кристаллизации составляем по отдельным его показателям.
Тепловой баланс процесса кристаллизации для молочного сахара можно представить следующим уравнением:
u uu к g м мм c cc п . ,
Определим количество теплоты, приходящее с сиропом, по уравнению теплового баланса лактозы:
Q u = 2600 х 2,72 х 75 = 530400 кДж (19)
Количество теплоты, выделяемое за счет теплоты кристаллизации незначительно, поэтому в расчетах его можно не учитывать.
Количество теплоты, отводимое с конечным раствором, Q м определим по формуле:
О м = 2240 х 3,705 х 20 = 165984 кДж, (20)
где с м = 0,161 - 1,202 + (1 - 0,161)*4,19 = 3,705 кДж/(кг -° С).
Количество теплоты, отводимое с кристаллами молочного сахара:
QK = 1031,2 x 1,202 x 20 = 24748,8 кДж, (21)
3. Уравнение материального баланса кристаллизации молочного сахара имеет вид:
S u x K u = 100 x M k + 5 м x К м , (28)
где с кр – теплоемкость молочного сахара, с кр = 1,202 кДж /(кг -° С).
В расчете принимаем, что потери теплоты в окружающую среду составляют 10% от количества поступающей теплоты:
Qn = 0,1 x 530400 = 53040 кДж (22)
Следовательно, количество теплоты, отводимое без учета количества теплоты, направляемого с хладагентом, составляет:
165984 + 24748,8 + 53040 = 243772,8 кДж. (23)
Таким образом, с хладагентом должно отводится определенное количество теплоты:
Q = 530400 - 243772,8 = 286627,2 кДж.
Количество теплоты Q отводимое хладагентом можно вычислить по формуле:
Q = S , x ( tk — t H ) x С х , (24)
где S k – количество хладагента, кг; t k , t н – соответственно, конечная и начальная температура хладагента, ° С; С х - удельная теплоемкость хладагента, Дж /(кг -° С).
Определим количество охлаждающей воды, приняв t k = 150C, a t H = 5 ° С, при этом теплоемкость воды принимаем равной 4,19 кДж /(кг -° С):
S , = 286627,2 = 6840,73 к Г . (25)
(15 - 5) ■ 4,19
-
1. Доброкачественность сиропа (раствора) Д р , % характеризуется наличием примесей (сухих веществ) в сывороточном сиропе, которые снижают скорость кристаллизации и затрудняют получение кристаллов однородных по размерам и форме:
-
2. Степень пересыщения лактозы в сиропе К п (коэффициент пересыщения) определяется следующим образом:
К
Др = ■ЮС, (26)
К с . в .
где К н – количество молочного сахара в насыщенном растворе, %; К с.в. – концентрация сухих веществ в растворе, %.
К п = К ф , (27)
п Кн где Кф – количество молочного сахара в его растворе при данной температуре, %; Кн – количество молочного сахара в насыщенном растворе, %.
где S u – количество исходного раствора, кг; S м – количество конечного маточного раствора, кг; K u – концентрация молочного сахара в исходном растворе, %; К м – концентрация молочного сахара в конечном растворе, %; M k – количество
кристаллов молочного сахара, кг.
Из приведенного уравнения можно определить количество кристаллов молочного сахара М к , кг:
М к =
S u ■ K u
—
S m ■ K m
При этом принимается, что в процессе кристаллизации объемное количество сиропа
остается постоянным.
4. Уравнение теплового баланса процесса кристаллизации может быть представлено в виде:
Su x c u x t u + Mк x g k = Sм x C M x t M + (30) + Mc x C m x t M + M c x C c x tc + Q + Q h ,
где С м – удельная теплоемкость удельного раствора, Дж/(кг°С); t н – температура исходного раствора, °С; g к – удельная теплота кристалла;
С м – удельная теплота конечного раствора, Дж/(кг °С); t м – температура конечного раствора, С; t с – температура кристаллов молочного сахара,°С; Q – количество теплоты, отводимое хладагентом, Дж; Q н – количества тепла, теряемого в среду, Дж.
В практических целях необходимо знать количество хладагента (охлаждающей воды) S х кг для ведения процесса кристаллизации, величина которой определяется из следующей зависимости:
Sx
Q
( tk — tn ) ■ C , knx
где t k ,t n – конечная и начальная температура хладагента (воды),°С; С х –удельная теплоемкость хладагента, Дж/(кг °С); (Для воды С х =4,1864 кДж/(кг°С)).
Неизвестная величина Q , Дж для указанного выражения определяется в следующей последовательности исходя из уравнения теплового баланса:
а) Количество теплоты, приносимое с сиропом Q и , кДж:
Q = S xc xt , (32)
и и ии ,
где с и – теплоемкость исходного сиропа лактозы, ее принимают равной удельной теплоемкости сахарозы с, которая определяется по формуле:
с = 4,2 — 0,0239 x Ксв , кДж / ( кг x 0 С ), (33)
К с.в . – концентрация сухих веществ, %.
Исходя из этого:
Q u = S u x ( 4,2 - 0,0239 x ^c . в ) x tu , (34)
-
б) Количество теплоты, отводимое с конечным раствором Qм, кДж определяется следующим образом:
Q = S x c x t = ммм
= Sм x(4,2-0,0239xКс.в)xtM,
-
в) Количество теплоты, отводимое
с кристаллами молочного сахара:
Qk = Мк x cc x tc = Мк x 1,2 tc , где сс = 1,2 – теплоемкость молочного сахара, кДж/(кг°С).
-
г) Потери теплоты в окружающую среду Qп, кДж принимают равным 10% от Q п:
Q n = 0,1 S u x ( 4,2 - 0,0239 x К^ ) x tu , (37)
-
д) Количество теплоты, отводимое без учета количества теплоты, уходящего с хладо-носителем составит:
Q + Qi + Q = S (4,2 - 0,0239 x К x t t + м k п м , , с . в м
+ М к x 1,2 tc + 0,1 Su ( 4,2 - 0,0239 x Кс . в ) x tu =
= ( 4,2 - 0,0239 x Км )( S m x tM + 0,1 x S u x t u ) +
+ М к x tc x 1,2, кДж
Список литературы Приближенный инженерный расчет кристаллизаторов-охладителей для молочного сахара в изогидрических условиях
- Полянский К.К. Кристаллизация лактозы. Производство молочного сахара//Переработка молока. 2017. № 6. С. 32-38.
- Полянский К. К., Калашников Г. В. Тепловой расчет кристаллизатора-охладителя для молочного сахара//Деп. ВЦНИИТЭИ мясомолпрома. 1984. № 1. С. 96.
- Липатов Н.Н. Руководство к лабораторным и практическим занятиям по курсу оборудования предприятий молочной промышленности. М.: Пищевая промышленность, 1978. 287 с.
- Zhang L. et al. Development of an inverse heat conduction model and its application to determination of heat transfer coefficient during casting solidification//Heat and Mass Transfer. 2014. V. 50. №. 7. P. 945-955.
- Полянский К.К. Кристаллизация лактозы в производстве молочных продуктов. Воронеж: ВТИ, 1981. 328 с.
- Гаврилов Г.Б., Кравченко Э.Ф., Куренков А.С. Технологические аспекты кристаллизации лактозы//Молочная промышленность. 2017. № 5. С. 44-45
- Power G. et al. Design and optimization of a multistage continuous cooling mixed suspension, mixed product removal crystallizer//Chemical Engineering Science. 2015. V. 133. P. 125-139.
- Бредихин А.С., Червецов В.В. Гидродинамика процесса охлаждения молочной сыворотки при поточной кристаллизации лактозы//Вестник ВГУИТ. 2013. № 3. С. 36-40.
- Fialkova E.A. et al. Analysis of the cyclic operation effect of the air cooling and heating crystallizer on crystal growth rate//Dairy Farming Journal. 2015.
- Slavorosova E.V. et al. Experimental studies of the milk whey nano-filtrate curdling process with the accom-panying lactose crystallization//Dairy Farming Journal. 2016.
- Rjabova A.E., Kirsanov V.V., Strizhko M.N., Bredikhin A.S. et al. Lactose crystallization: current issues and promising Engineering solutions//Foods and Raw materials. 2013. V. 1. №. 1.
- Храмцов А.Г., Нестеренко П.Г., Евдокимов И.А., Рябцева С.А. и др. Альтернативные варианты промышленной переработки молочной сыворотки//Молочная промышленность. 2014. №. 11. С. 44-48.
- Santos C.A., Quaresma J.M.V., Garcia A. Determination of transient interfacial heat transfer coefficients in chill mold castings//Journal of Alloys and Compounds. 2001. V. 319. №. 1-2. P. 174-186.


