Прибор для исследования эндотоксикоза на основе биотестирования
Автор: Ваганов А.В.
Журнал: Научное приборостроение @nauchnoe-priborostroenie
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.13, 2003 года.
Бесплатный доступ
Рассматривается турбидиметрический фотометр, позволяющий проводить исследование эндотоксикоза с использованием инфузорий по сыворотке крови человека. Описывается конструкция прибора на уровне блок-схемы. Приводятся экспериментальные зависимости.
Короткий адрес: https://sciup.org/14264304
IDR: 14264304 | УДК: 615.
Bioassay device for investigation of endotoxicosis
A new turbidimetric photometer for endotoxicosis investigation is described. The device is based on the infusoria bioassay in human serum. The flow diagram of the device and experimental results are presented.
Текст научной статьи Прибор для исследования эндотоксикоза на основе биотестирования
Исследование эндотоксикоза (Э), возможность определения его на ранней стадии, контроль течения заболевания представляют собой актуальную задачу в наши дни.
В последнее время многие специалисты по изучению Э используют биологический контроль и как его разновидность — биотестирование [1]. При этом тест-организмом могут быть экспериментальные животные (кролики, мыши и т. д.), культуры клеток, получаемые из тканей человеческого или животного происхождения, или простейшие.
Использование простейших, например, инфузорий для диагностики Э имеет неоспоримые преимущества: легкость культивирования, относительная дешевизна эксперимента, стабильность характеристик тест-объекта, безопасность культуры для человека.
В настоящее время известны два типа тест-реакций инфузорий, используемые при исследовании Э: угнетение прироста и гибель [2].
Тест-реакция "гибель инфузорий" является наиболее экспрессной, так как анализу подвергается неразведеная центрифугированная сыворотка крови больных и здоровых людей (контрольная группа). Сыворотка и культура инфузорий берется в соотношении 1:1. Оценивается время от начала воздействия сыворотки крови на клетки инфузорий до гибели (прекращения движения) последних. Максимальное время проведения опыта не превосходит 20 минут, что наряду с принципиальной простотой проведения свидетельствует о перспективности данного способа исследования Э. Однако широкое внедрение его в медицинскую практику сдерживают сложности реализации (микроскопный счет, секундомер), субъективный фактор и т. д.
Существующий турбидиметрический измеритель концентрации инфузорий "Биотестер" не может быть применен для исследования Э, т. к. в нем не учтены оптические и физико-химические особенности сыворотки крови, отсутствует адаптация инфузорий к солевому составу сыворотки, используется слишком большой объем тестируемой пробы (2 мл), отсутствует термостатирование пробы при измерении, недостаточна обнаруживающая способность прибора к инфузориям малых размеров (например, Tetrahimena pyriforms).
Все вышеизложенное послужило основанием для создания прибора контроля токсичности сыворотки крови, который позволит автоматически производить оценку изменения концентрации живых (подвижных) инфузорий в исследуемой биожидкости.
ПРИНЦИП ИЗМЕРЕНИЯ
Для регистрации изменения концентрации живых инфузорий в исследуемой среде предпочтение отдано турбидиметрическому способу, т. к. взвесь инфузорий как крупных частиц в оптически "мягкой" среде имеет сжатую вперед индикатрису рассеяния. Поэтому, с одной стороны, взвесь рассеивает малый поток излучения под углом 90 градусов к оси источника излучения, с другой стороны, проходящий через частицу поток излучения уменьшает величину экстинкции взвеси. При нефелометрической схеме построения прибора необходимо использовать методы фотометрии малых потоков, что неизменно приводит к усложнению конструкции [3].
Взвесь инфузорий образует хаотически подвижную, рассеянную взвесь прозрачных эллипсоидальных тел размерами 30–300 мкм.
Для описания взаимодействия светового излучения с инфузориями лучше всего подходит модель геометрической оптики. Она применима, если р > 100, где р = 2пг / Л. Здесь r — диаметр частицы, Л — длина волны светового излучения. Существенной качественной особенностью ослабления света частицами с большим р = 2пг / Л (или большим радиусом r) является появление вместе с рассеянием света в малых углах эффекта дифракции Фраунгофера в параллельных лучах. Фронт плоской волны образует "тень" за частицей и при условии r << R (R — расстояние от частицы до приемника) дифракционную картину, такую же какую создает отверстие радиуса r.
При работе с сывороткой крови в оптическом диапазоне возникает увеличение поглощения и рассеяния светового излучения по сравнению с водной средой вследствие возможной большой концентрации липопротеидов в исследуемой биожидкости (визуально это оценивается по степени ее мутности), а также возможности гемолиза сыворотки (полного или частичного разрушения гемоглобина), из-за чего она приобретает красный цвет.
Возможным диапазоном для регистрации изменения концентрации подвижных инфузорий при исследовании токсичности сыворотки крови является ближний инфракрасный спектр (720 1100 нм), т. к. значение оптической плотности в нем минимально (рис. 1). Оптимальной длиной волны для проведения измерений считается X = 810 нм: поглощение окисигемоглобином (HbO 2 ) и дезоксигемоглобином (HbR) одинаково [4].
Сыворотка крови является оптически более сложной средой, чем водная. Компоненты с наибольшими размерами до 600 нм оказывают влияние в виде помехи на формирование информационного сигнала из-за перемещения их в кювете конвекционными потоками. Наиболее полно ослабление и рассеяние света элементами сыворотки крови описывает теория Ми, учитывающая вторичные волны, распространяющиеся от частицы-осциллятора, на которую воздействует фронт плоской волны излучения.
Исследуемая среда (взвесь инфузорий и сыворотка крови) может быть промоделирована взвесью малых подвижных частиц (инфузории) в среде очень малых частиц различной концентрации и размеров (элементы сыворотки крови).
Увеличенное значение вязкости сыворотки крови по сравнению с водной средой приводит к некоторому снижению начальной скорости перемещения простейших. Однако это не влияет на конечный результат измерения (время полной остановки всех инфузорий в пробе).
С целью уменьшения влияния солевого состава сыворотки крови (в частности, NaCl) на простейших, что может привести к росту погрешности измерения, в проводимых экспериментах в качестве тест-объекта используются инфузории, адаптированные к 0.7 % раствору NaCl.
Уменьшение объема тестируемой пробы с 2 до 0.3 мл позволило не только сократить расход
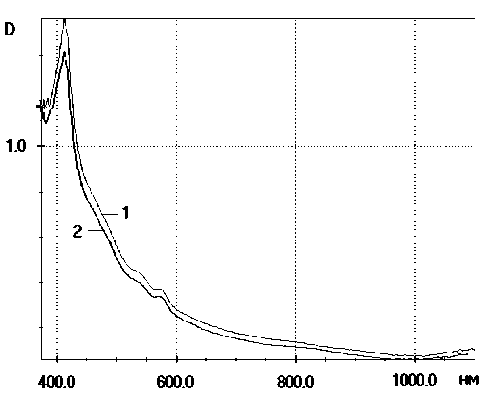
Рис. 1. Зависимость оптической плотности (D) от длины волны в исследуемом растворе (сыворотка крови + среда Лозин-Лозинского 1 : 1) на примере одной из сывороток (1). Та же сыворотка, но инактивированная — 2
биоматериала, но и сформулировать условия максимизации потока частиц (инфузорий) через контролируемый объем (датчик).
Для термостатирования кюветного модуля с исследуемой средой выбрана стандартная температура для медицинских исследований — 30 градусов.
Для работы с инфузориями малых размеров произведено повышение обнаруживающей способности прибора. По сравнению с "Биотестер" интенсивность импульсного излучения светодиода увеличена в 5 раз, общее усиление — в 2.5 раза.
ОПИСАНИЕ КОНСТРУКЦИИ ПРИБОРА
Оптоэлектронный датчик представлен на рис. 2. Оптическое излучение, создаваемое светодиодом СД, проходит через кювету с исследуемой пробой и проецируется на фотодиод ФД. Полученный сигнал изменения освещенности фотодиода преобразуется в электрический сигнал и усиливается фотоусилителем ФУ. Электрический сигнал на выходе датчика имеет переменную составляющую, т. к. учитываются как входящие в контролируемую зону, так и выходящие из нее инфузории из приграничных слоев е. Объем приграничных слоев можно вычислить по формуле
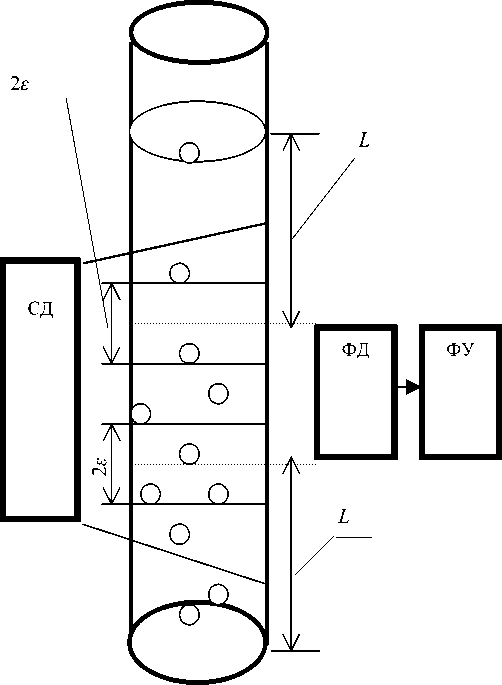
Рис. 2. Модель оптоэлектронного датчика.
СД — светодиод, ФД — фотодиод, ФУ — фотоусилитель, 2 е — высота приграничных слоев, L — расстояние от измерительного объема до границ сред
V = 2 Lf ■ е ■ d, где Lf — периметр датчика, е — толщина приграничных слоев, d — расстояние между светодиодом и фотодиодом.
Перемещаемые конвекционными потоками микрочастицы сыворотки крови создают сигнал помехи или сигнал-фон. Характер движения инфузорий дискретно-хаотичный, состоящий из прямолинейных перемещений со случайной сменой направлений. Поэтому для потока дискретно движущихся частиц через поверхность датчика (инфузории и микрочастицы сыворотки крови) подходит модель пуассоновских потоков. Полезный сигнал на выходе датчика имеет вид:
U ( t ) = n i ■ U о ■ f ( t - t i ) .
Здесь n i — число элементарных импульсов, возникающих за достаточно малый интервал времени 8 1 ; t i — случайный момент появления импульса, имеющего форму, описываемую функцией f ( t - t i )= | «при t < t , ;
[± 1, при t > t i .
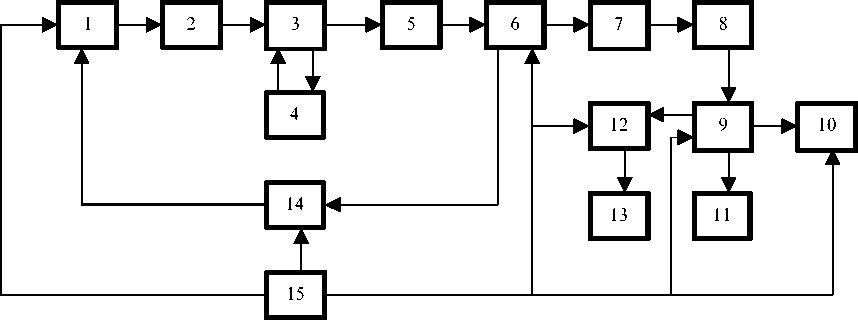
Рис. 3. Блок-схема измерителя токсичности сыворотки крови.
1 — усилитель, 2 — светодиод, 3 — кюветный модуль, 4 — блок термостабилизации, 5 — фотоусилитель, 6 — усилитель, 7 — фильтр, 8 — детектор, 9 — аналогово-цифровой преобразователь (АЦП), 10 — устройство для передачи измерительной информации в компьютер, 11 — блок индикации концентрации инфузорий, 12 — устройство отсчета времени, 13 — блок индикации минут, 14 — схема компенсации яркости светодиода, 15 — блок генератора
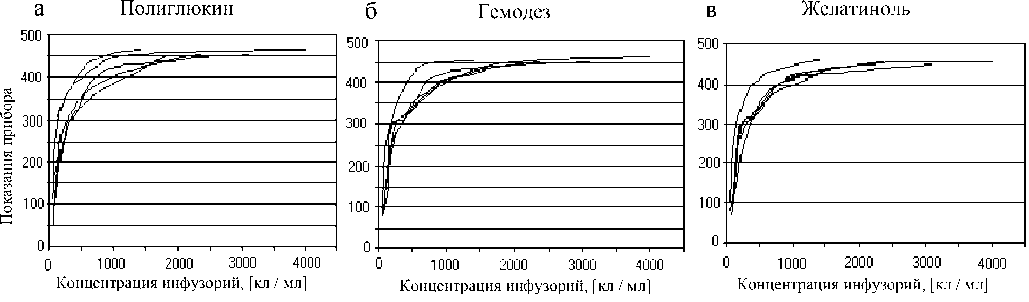
Рис. 4. Калибровочные кривые по заменителям сыворотки крови
Случайные величины n i и t i считаются независимыми.
Блок-схема измерителя представлена на рис. 3.
ПРАКТИЧЕСКИЕ РЕЗУЛЬТАТЫ
В ходе проведенных экспериментов построены калибровочные кривые (зависимость показаний прибора от концентрации живых инфузорий) с использованием заменителей сыворотки крови рис. 4. По этим кривым произведен выбор оптимальной рабочей концентрации взвеси инфузорий ( C ≈ 500 кл/мл), обоснованной относительно ли- нейной зависимостью показаний прибора от концентрации живых клеток в кювете. Выработан алгоритм проведения исследований.
Произведены пробные замеры, которые показали хорошую повторяемость результатов измерений (времени гибели), а также подтвердили корреляцию данного метода с методом оценки токсичности сыворотки крови по М.Я. Малаховой.
Список литературы Прибор для исследования эндотоксикоза на основе биотестирования
- Захаров И.С., Пожаров А.В. Биотехнические методы охраны окружающей среды: Учебн. пособие. СПб.: Изд-во СПбГЭТУ "ЛЭТИ", 2001. 80 с.
- Виноходов Д.О., Виноходов В.О., Гипан Л.И., Земляникина Т.А. Использование инфузорий в исследовании внутренних сред высших организмов//Архив ветеринарных наук. 1999. Т. 1, № 3. С. 551-557.
- Захаров И.С. Метод и аппаратура для измерений концентраций инфузорий в медико-экологических исследованиях. Автореф. дис. … канд. тех. наук. СПб., 1996. 16 с.
- Крепс Е.М. Оксигемометрия: техника, применение в физиологии и медицине. Л.: Изд-во Медгиз, 1959. 222 с.


