Применение ацетазоламида при лечении сердечной недостаточности: прошлое или будущее?
Автор: Серов В.А., Ширяевская Д.В., Ширяевский О.А., Ефремова Е.В.
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Обзоры
Статья в выпуске: 3, 2025 года.
Бесплатный доступ
Одним из нерешенных вопросов при лечении сердечной недостаточности является оптимизация назначения мочегонных препаратов. Предложено использовать комбинированную диуретическую терапию. Однако остается открытым вопрос: прием каких лекарственных средств наиболее целесообразен? В последние годы большое внимание привлекает ацетозоламид – ингибитор карбоангидразы. Цель – представить обзор клинических исследований и клинико-фармакологическое обоснование перспективы применения ацетозоламида у стационарных пациентов с острой сердечной недостаточностью. Материалы и методы. Проведен поиск в базах данных PubMed и eLIBRARY. Результаты. Приведены данные по фармакокинетике и фармакодинамике ацетозоламида, а также результаты недавно проведенных клинических исследований, касающихся применения комбинированной диуретической терапии при сердечной недостаточности. Показано, что особенности механизма действия ингибиторов карбоангидразы создают ряд преимуществ для их использования в схемах комбинированной диуретической терапии. Применение ацетозоламида статистически значимо увеличивало натрийурез, чаще приводило к исчезновению симптомов гипергидратации, уменьшало вероятность развития метаболического алколоза при лечении петлевыми диуретиками пациентов с острой сердечной недостаточностью. Побочные явления возникали редко и не носили тяжелого характера. В то же время как в краткосрочной, так и в долгосрочной перспективе не было выявлено снижения смертности. Выводы. Комбинированная диуретическая терапия приводит к выраженному уменьшению гипергидратации у пациентов с острой сердечной недостаточностью при удовлетворительном профиле безопасности. Ацетозоламид следует рассматривать как ценный вариант при необходимости быстрого устранения застойных явлений у пациентов с сердечной недостаточностью, а также у пациентов с метаболическими осложнениями, такими как алкалоз или гиперхлоремия, однако необходимы дополнительные клинические исследования для выработки оптимальной тактики назначения ингибиторов карбоангидразы.
Ацетозоламид, сердечная недостаточность, комбинированная диуретическая терапия
Короткий адрес: https://sciup.org/14133865
IDR: 14133865 | УДК: 616-085 | DOI: 10.34014/2227-1848-2025-3-41-59
Acetazolamide in heart failure: past-or future-oriented treatment?
Optimizing diuretic prescription for heart failure remains an unresolved issue. Combined diuretic therapy is known to be advisable. However, there is an unresolved question: what drugs should be used? Recently, much attention has been drawn to carbonic anhydrase inhibitor acetazolamide. The aim of the study is to present an overview of clinical studies and clinical and pharmacological rationale for acetazolamide prospects in hospitalized patients with acute heart failure. Materials and Methods. To gather information, search was conducted in the PubMed database and the eLIBRARY database. Results. The article presents data on the acetazolamide pharmacokinetics and pharmacodynamics. It also touches upon the results of recent clinical studies on combined diuretic therapy in heart failure. It is shown that the mechanism of action of carbonic anhydrase inhibitors has advantages for their use in combination diuretic therapy. Acetazolamide therapy statistically significantly increased natriuresis, more often led to the disappearance of hyperhydration symptoms, and reduced the likelihood of metabolic alkalosis while treating patients with acute heart failure with loop diuretics. Side effects were rare and not severe. At the same time, no decrease in short- and long-term mortality was observed. Conclusion. Combined diuretic therapy results in significant reductions in overhydratation in patients with acute heart failure under a satisfactory safety profile. Acetazolamide should be considered as a valuable option when fast diuretic effect is required in patients with heart failure, as well as in patients with metabolic complications such as alkalosis or hyperchloremia. However, more research and clinical studies are needed to develop optimal strategies for prescribing carbonic anhydrase inhibitors.
Текст научной статьи Применение ацетазоламида при лечении сердечной недостаточности: прошлое или будущее?
Введение. Последние десятилетия характеризуются появлением целого ряда новых классов лекарственных средств, существенно повлиявших на течение многих распространенных тяжелых заболеваний, таких как артериальная гипертензия, рак, сахарный диабет и т.д. Особенно заметен прогресс в медикаментозной терапии хронической сердечной недостаточности (ХСН). Назначение препаратов «фантастической четверки», которая включает ингибиторы рецепторов ангиотензина и неприлизина, бета-блокаторы, антагонисты минералокортикоидных рецепторов и ингибиторы натрий-глюкозного котранспортера 2-го типа (SGLT2), а также оптимизация их дозирования заметно улучшают прогноз у пациентов с ХСН со сниженной фракцией выброса [1, 2], снижают риск сердечно-сосудистой смерти и госпитализации по поводу ХСН [3–5]. Однако несмотря на очевидные успехи прогноз у пациентов с ХСН остается неблагоприятным: при ХСН I–II функционального класса (ФК) медиана времени дожития составляет 8,4 года (95 % ДИ 7,8–9,1), а при ХСН III–
IV ФК – 3,8 года (95 % ДИ 3,4–4,2) [6]. Согласно данным Американской кардиологической ассоциации, число госпитализаций по поводу сердечной недостаточности (СН) в США с 2013 по 2017 г. увеличилось на 26 % [7].
Использование новых лекарственных средств неизбежно увеличивает стоимость проводимого лечения, что часто является непосильным бременем как для бюджета отдельного пациента, так и для бюджета системы здравоохранения в целом. Это ведет к снижению комплаентности пациентов, невыполнению требований современных клинических рекомендаций. В то же время врачами часто недооценивается использование «старых» дешевых препаратов, которые могут иметь значительный лечебный потенциал, в ряде случаев еще недостаточно изученный.
Гипергидратация играет важную роль в патофизиологии СН, и противоотечное лечение представляет собой важную терапевтическую цель [8]. Снижение диуреза и натрийуреза, дисхлоремия являются одними из частых причин усугубления течения СН [9– 12]. В настоящее время основой начальной терапии, направленной на достижение адекватного диуреза/натрийуреза и эуволемии, является немедленное и повторное внутривенное введение петлевых диуретиков. Однако развитие резистентности к диуретикам является распространенным осложнением, затрудняющим лечение этого состояния [13]. Остаточные симптомы гипергидратации при выписке из стационара присутствуют у 31–48 % пациентов с СН, причем смертность у пациентов с гиперволемией достигает 50 % в течение года [14, 15].
Для преодоления резистентности используют раннюю комбинированную терапию диуретиками, что позволяет активировать раз- личные механизмы действия в разных сегментах нефрона [16].
Одним из эффективных препаратов является ингибитор карбоангидразы – ацетозола-мид, который стал использоваться в медицине с 1950-х гг. Однако до настоящего времени исследований, посвященных эффективности и безопасности применения ингибиторов карбоангидразы в кардиологии, проведено крайне мало.
Цель исследования. Представить обзор клинических исследований и клинико-фармакологическое обоснование перспективы применения ацетозоламида у стационарных пациентов с острой сердечной недостаточностью (ОСН).
Материалы и методы. В базах данных PubMed и eLIBRARY был проведен поиск с использованием терминов «ацетазоламид», «сердечная недостаточность», «острая сердечная недостаточность», «декомпенсированная сердечная недостаточность» (в названиях публикаций, аннотациях и ключевых словах).
Результаты. Всего в PubMed на 30 декабря 2024 г. ацетозоламид упоминается в 10 402 статьях, в т.ч. «ацетозоламид при сердечной недостаточности» – в 302; в eLIBRARY – в 98 и 12 публикациях соответственно. В PubMed первая статья о применении ацетозоламида датируется 1952 г., о его использовании при лечении сердечной недостаточности – 1953 г. В eLIBRARY сведения встречаются с 1998 г. Обращает на себя внимание тот факт, что после сорокалетнего (1970–2010 гг.) перерыва количество публикаций, посвященных применению ацетозоламида при сердечной недостаточности (рис. 1), значительно увеличилось. Прежде всего это связано с обнадеживающими результатами недавно проведенных исследований.
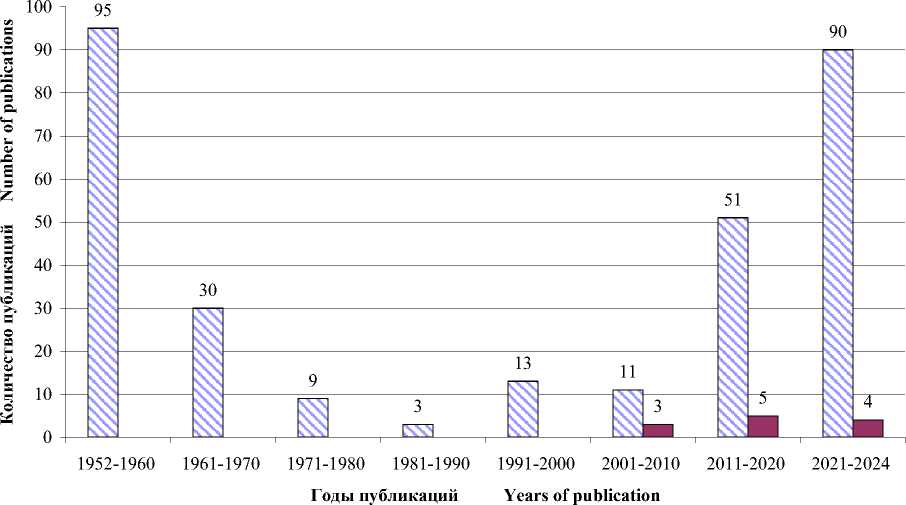
□ PubMed ■ eLIBRERY
Рис. 1. Динамика количества публикаций о применении ацетазоламида при сердечной недостаточности в базах данных PubMed и eLIBRARY
Fig. 1. Dynamics of publications on acetazolamide therapy in heart failure in PubMed and eLIBRARY
Фармакодинамика и фармакокинетика ацетазоламида
Ацетазоламид обладает высоким сродством к изоферментам карбоангидразы II и IV и блокирует ее активность на уровне проксимального отдела нефрона. Это ведет к уменьшению образования в клетках канальцев угольной кислоты. Увеличивается экскреция натрия с мочой в виде гидрокарбонатов, реакция мочи становится щелочной. Снижение поступления в кровь гидрокарбонатного иона становится причиной метаболического ацидоза. Канальцевая реабсорбция хлора не нарушается. В дистальных канальцах и собирательных трубках усиливается экскреция калия. В связи с развитием метаболического ацидоза при длительном применении ацетозо-ламида в канальцы поступает достаточное количество ионов водорода даже без участия карбоангидразы, что приводит к быстрому развитию толерантности, поэтому ингибиторы карбоангидразы эффективны только при лечении прерывистыми курсами [17].
После приема внутрь ацетозоламид быстро всасывается из желудочно-кишечного тракта, достигая максимальной концентрации в крови через 1–3 ч; определяемая концентрация в плазме сохраняется в течение 24 ч после приема препарата. Ацетазоламид более чем на 96 % связывается с белками плазмы, проникает через плацентарный барьер, а также, в небольших количествах, – в грудное молоко. Выведение из организма происходит за счет активной секреции в проксимальных каналь- цах почек. Препарат не накапливается в тканях. До 90 % ацетозоламида выводится почками в неизмененном виде за 24 ч [18].
Aцетозоламид используется при лечении многих состояний, например для снижения внутриглазного и внутричерепного давления, профилактики и лечения высотной болезни. В то же время в качестве диуретика практические врачи назначают его редко, что обусловлено слабым натрийуретическим действием и быстрым развитием толерантности. При этом часто не учитываются специфические достоинства препарата, в частности способность корректировать выраженный метаболический алкалоз, который возникает при лечении петлевыми диуретиками [19] и способствует снижению их эффективности [20].
Комбинированная диуретическая терапия при сердечной недостаточности
Несмотря на то что гипергидратация у пациентов с ОСН обычно устраняется с помощью петлевых диуретиков, значительная часть пациентов не получает оптимального лечения. Неадекватный ответ на диуретики и остаточная гипергидратация связаны с более высоким риском госпитализации, неблагоприятными исходами и увеличением стоимости лечения [21], при этом нет доказательств того, что их назначение снижает смертность. Тем не менее Европейское общество кардиологов (European Society of Cardiology) рекомендует назначать диуретики для достижения надлежащего баланса жидкости у пациентов, имеющих симптомы гипергидратации, как в хронической, так и в острой фазе сердечной недостаточности [22].
Для преодоления резистентности к петлевым диуретикам используют ряд стратегий, таких как экстракорпоральное удаление жидкости, введение низких доз дофамина и гипертонического раствора натрия хлорида [23]. Одним из эффективных методов является последовательная блокада всасывания натрия в канальцах нефрона с помощью диуретических лекарственных средств, влияющих на разные отрезки канальцев и применяющихся дополнительно к петлевым диуретикам, – комбинированная диуретическая терапия (КДТ). Од- нако убедительные доказательства эффективности и безопасности КДТ остаются ограниченными [24].
В 2023 г. были опубликованы результаты проведенного в Испании двойного слепого плацебо-контролируемого рандомизированного исследования CLOROTIC (Комбинация петлевых диуретиков с тиазидными диуретиками при декомпенсированной сердечной недостаточности) [25]. В рамках исследования 230 пациентов (из них 48 женщин, средний возраст – 83 года) с ОСН получали перорально гидрохлоротиазид или плацебо в течение 5 дней в дополнение к внутривенному введению фуросемида. Протокол применения петлевых диуретиков соответствовал протоколу применения низких доз в рамках исследования DOSE. Первичными конечными точками были изменения массы тела и одышки по оценке пациентов через 72 ч после рандомизации. Вторичные показатели включали реакцию на диуретики и смертность / повторную госпитализацию через 30 и 90 дней. Также оценивались показатели безопасности (изменения функции почек и/или электролитов). Через 72 ч у пациентов, получавших гидрохлоротиазид, наблюдалось более значительное (на 53 %, р=0,002) снижение веса по сравнению с теми, кто принимал плацебо. Кроме того, в группе, принимавшей гидрохлоротиазид, были больше суточный диурез (1775 против 1400 мл, р=0,05) и потеря веса на каждые 40 мг фуросемида (через 72 и 96 ч) (р=0,001), а также средняя экскреция натрия с мочой. Различий в показателях одышки, по мнению пациентов, не зафиксировано (площадь под кривой для визуальной аналоговой шкалы: 960 против 720; р=0,497). В то же время у пациентов, принимавших гидрохлоротиазид, чаще наблюдалось повышение уровня креатинина в сыворотке крови не менее чем на 26,5 мкмоль/л или снижение скорости клубочковой фильтрации (СКФ) не менее чем на 50 %: 46,5 % пациентов против 17,2 % в группе плацебо, р<0,001); гипокалиемия развивалась 44,7 % и 19,0 % случаев соответственно (р<0,001). Показатели повторной госпитализации и смертности в обеих группах были одинаковыми.
Ретроспективный анализ этого исследования продемонстрировал, что эффективность лечения не меняется в зависимости от исходной фракции выброса левого желудочка [26]. Также показатели диуретического ответа не отличались в зависимости от гендерной принадлежности пациентов, хотя у женщин чаще отмечалось ухудшение функции почек (ОШ 8,68; 95 % ДИ 3,41–24,63), чем у мужчин (ОШ 2,5; 95 % ДИ 0,99–4,87, p=0,027) [27].
Применение ацетозоламида при сердечной недостаточности
В 2022 г. были опубликованы результаты двойного слепого плацебо-контролируемого исследования ADVOR (Ацетазоламид при декомпенсированной сердечной недостаточности с перегрузкой объемом), проведенного в Бельгии [28]. В ходе исследования 519 пациентов с ОСН с клиническими признаками перегрузки объемом (т.е. отеками, плевральным выпотом или асцитом) и уровнем N-концевого про-B-типа натрийуретического пептида более 1000 пг/мл или уровнем B-типа натрийуретического пептида более 250 пг/мл, получающие пероральную поддерживающую терапию не менее 40 мг фуросемида или эквивалентную дозу других петлевых диуретиков (1 мг буметанида или 20 мг торасемида) в течение не менее 1 мес., были рандомизированы для получения либо внутривенного введения ацетозоламида, либо плацебо в дополнение к схеме внутривенного введения петлевых диуретиков (в дозе, в два раза превышающей пероральную домашнюю дозу). Максимальная доза фуросемида для внутривенного введения, разрешенная до рандомизации, составляла 80 мг. Из исследования были исключены пациенты, которые получали ацетозоламид или другие проксимальные канальцевые диуретики (например, ингибиторы SGLT2) в качестве поддерживающей терапии, имели систолическое артериальное давление менее 90 мм рт. ст. или СКФ менее 20 мл/мин/1,73 м2.
Первичной конечной точкой было достижение отсутствия признаков перегрузки объемом в течение 3 дней после рандомизации. Вторичные конечные точки включали совокупность смерти от любой причины или повторной госпитализации по поводу СН в течение 3 мес. наблюдения.
Первичная конечная точка чаще достигалась в группе ацетазоламида: у 108 из 256 пациентов (42,2 %) в группе ацетозоламида и у 79 из 259 (30,5 %) в группе плацебо (ОР 1,46; 95 % ДИ 1,17–1,82; р<0,001). Кроме того, в группе ацетозоламида уменьшалась длительность стационарного лечения (8,8 против 9,9 дня; р=0,016), был выше суммарный диурез и натрийурез. В тоже время не было выявлено различий в смертности от всех причин или повторной госпитализации из-за СН в последующие 90 дней: 29,7 % в группе ацетозо-ламида и 27,8 % в группе плацебо (ОР 1,07; 95 % ДИ 0,78–1,48).
Субанализ 462 пациентов из исследования ADVOR с полными данными о диурезе и концентрации натрия в моче показал, что прием ацетозоламида приводил к достоверному увеличению концентрации натрия в моче на 16 ммоль/л (на 19 %), повышению натрийуреза за первые 48 ч на 115 ммоль и более быстрому и полному купированию признаков объемной перегрузки, при этом эффект был значительным уже в первое утро обследования (р=0,022). Мужской пол, более высокое систолическое артериальное давление, лучшая СКФ и более высокий уровень натрия в сыворотке выступали другими независимыми предикторами, хотя оказывали менее выраженное влияние. Доза петлевых диуретиков не влияла на общий натрийурез. Не было выявлено взаимосвязи между натрийуретической реакцией и фракцией выброса или применением блокаторов ренин-ангиотензиновой системы. Сильный натрийуретический эффект был связан с более быстрой ликвидацией застойных явлений и сокращением продолжительности пребывания в стационаре. Многофакторный корреляционный анализ показал независимую связь повышения концентрации натрия в моче на каждые 10 ммоль/л со снижением риска смерти от всех причин или повторной госпитализации в связи с СН (ОР 0,92; 95 % ДИ 0,85–0,99) [29].
Более 80 % пациентов, включенных в исследование ADVOR, страдали хроническими заболеваниями почек. Проведенный анализ показал, что положительное влияние ацетозо-ламида на отечный синдром отмечалось по всему спектру СКФ; более того, влияние на диурез было более выражено у пациентов с исходно сниженной функцией почек [30]. Этот результат приобретает особое значение, учитывая высокую распространенность хронической болезни почек у пациентов с ХСН [31].
В редакционной статье журнала «Сердечная недостаточность» Американского кардиологического колледжа отмечено, что исследование ADVOR, несмотря на относительно небольшой размер выборки, явилось крупнейшим из когда-либо проводившихся рандомизированных исследований, касавшихся лечения диуретиками в стационаре. Применение ацетазоламида позволило добиться абсолютного улучшения показателя первичной конечной точки на 11,7 %. В то же время обращается внимание на ограничения этого исследования. Так, из исследования была исключена терапия ингибиторами SGLT2 [32]. Ингибиторы SGLT2 в настоящее время являются основой терапии ХСН при любой фракции выброса левого желудочка, причем их действие направлено на проксимальные канальцы почки, т.е. на тот же сегмент нефрона, на который нацелен ацетозо-ламид. Необходимо выяснить результат взаимодействия этих препаратов с ацетозолами-дом [33]. Ингибиторы SGLT2 обеспечивают устойчивые долгосрочные преимущества в отношении клинических исходов и состояния здоровья, которые проявляются уже на ранней стадии, в течение нескольких дней или недель после начала лечения. Поэтому, если пациенты еще не получали ингибиторы SGLT2 при поступлении, эти препараты следует рассматривать как раннюю дополнительную к приему петлевых диуретиков терапию, направленную на повышение эффективности лечения, с продолжением приема ингибиторов SGLT2 и после выписки из стационара [34]. Ингибиторы SGLT2 не рассматриваются исключительно как противоотечная терапия, и подходящие пациенты должны получать их независимо от состояния застойных явлений и нахождения в стационаре. В отличие от ацетозоламида, клинический эффект которого отмечается уже в первые 3 сут, ингибиторы SGLT2 увеличивают диурез и уменьшают симптомы застойных явлений только через значительно больший промежуток времени (15–90 дней), как на примере эм-паглифлозина было показано в исследованиях EMPULSE [35], EMPAG-HF [36] и EMPA-RSPONSE-AHF [37]. В связи с этим, по мнению M. Sabina et al., ацетозоламид следует рассматривать как ценный вариант при необходимости быстрого устранения застойных явлений у пациентов с СН, а также у пациентов с метаболическими осложнениями, такими как алкалоз или гиперхлоремия [13].
Средняя поддерживающая доза фуросемида при внутривенном введении в ADVOR была существенно ниже, чем в исследовании DOSE (Diuretic Optimal Strategy Evaluation in Acute Heart Failure) [38]: 120 мг против 320 мг соответственно. Большая эффективность аце-тозоламида при более высокой фоновой дозировке внутривенного петлевого диуретика не показана. Это связано с тем, что основным механизмом потенцирования эффекта при использовании данной комбинации является нейтрализация ацетозоламидом развития метаболического алкалоза на фоне введения фуросемида. Нельзя исключить, что при увеличении дозы петлевого диуретика этот компенсаторный эффект будет недостаточным, алкалоз будет развиваться и приведет к уменьшению суммарного диуретического эффекта. Для уточнения эффективности ацетозоламида при более высокой фоновой дозировке внутривенного петлевого диуретика требуются дополнительные клинические исследования с использованием более высоких доз фуросемида.
Отмечено, что несмотря на отсутствие статистической значимости, у пациентов, получавших ацетозоламид внутривенно, была более высокая частота смерти от всех причин (15,2 % против 12,0 %; ОР 1,28; 95 % ДИ 0,78– 2,05) и повторной госпитализации в связи с СН через 3 мес. (18,4 % против 17,4 %; ОР 1,07; 95 % ДИ 0,71–1,59). Через 3 мес. также наблюдалась значительно более высокая частота гипокалиемии в группе ацетозоламида (23,4 % против 14,7 %, р=0,02), что противоречит данным об отсутствии существенного влияния на гипокалиемию на этапе стационарного лечения. Все вышеперечисленное требует проведения дополнительных более масштабных и долгосрочных исследований [31].
В исследовании CANDI оценивалась эффективность и безопасность применения ацетазоламида при ОСН (средняя суточная доза – 125 мг, диапазон доз – 125–250 мг) по сравнению с хлорталидоном (средняя доза – 25 мг, диапазон – 25–25 мг) на фоне приема фуросемида (средняя доза – 120 мг, диапазон доз – 120–180 мг). Основной целью исследования было определение доли пациентов, у которых снижение веса составило не менее 1 кг в течение 24 ч после приема второго диуретика. В качестве других показателей были проанализированы диурез, натрийурез, а также изменения функции почек и уровня электролитов. В исследование были включены 55 пациентов: 26 (47,3 %) из них получали ацетазоламид, а 29 (52,7 %) – хлорталидон. Комбинированная терапия была начата на 7-й день госпитализации (ацетазоламид – на 7-й [4–11-й] день, хлорталидон – на 7-й [5–10-й] день; р=0,793). После корректировки на различные факторы эффект ацетозоламида по сравнению с хлор-талидоном был более значительным, и большая часть пациентов в группе ацетозоламида достигла желаемого снижения веса (62 % пациентов против 26 % в группе хлорталидона, р=0,02). Не было выявлено достоверных различий в показателях диуреза (эффект ацетазоламида +202,5 мл; 95 % ДИ -155,1–560,1; р=0,260) и натрийуреза (эффект ацетазоламида: +13,11 мэкв/л; 95 % ДИ -2,35–28,59; р=0,095) и в изменениях функции почек. Применение ацетозоламида было связано с большим снижением уровня рН и бикарбоната, что может предотвращать метаболический алкалоз и является значимым преимуществом перед тиазидными диуретиками [39].
В мета-анализ, проведенный B.A. Malik et al., было включено три рандомизированных клинических исследования (569 пациентов), в которых изучалась эффективность применения ацетозоламида при лечении СН [40]. У пациентов, получавших ацетозоламид, ликвидация гипергидротации достигалась значительно чаще по сравнению с пациентами, ран- домизированными в контрольную группу (ОР 1,34; 95 % ДИ 1,06–1,67), также был выше средний натрийурез и диурез. Не было обнаружено существенных различий между двумя группами в показателях смертности от всех причин и госпитализации из-за СН. Результаты данного мета-анализа практически не отличались от результатов исследования ADVOR, так как именно пациенты, включенные в это исследование, составляли основное количество анализируемых случаев.
В действующих клинических рекомендациях Министерства здравоохранения Российской Федерации по лечению ХСН [41] ацето-золамид предлагается назначать пациентам с ОСН и резистентными отеками на фоне внутривенного применения петлевых диуретиков в целях улучшения клинической симптоматики. Для поддерживающей терапии ацетозо-ламид не используется в связи с быстрым развитием резистентности. В то же время недавно проведенное рандомизированное исследование по оценке долгосрочной (в течение 12 мес.) эффективности ацетазоламида в терапии дыхания Чейна – Стокса у больных с ХСН и низкой фракцией выброса левого желудочка показало, что применение 250 мг ацетазоламида в сутки достоверно уменьшает выраженность дыхания Чейна – Стокса [42].
В метаанализе A.K. Siddiqi et al., включившем 5 исследований (684 пациента), ацетозо-ламид оценивался как дополнительное мочегонное средство у пациентов с ОСН со средним сроком наблюдения 3 мес. Было продемонстрировано значительное увеличение натрийуреза (MD 55,07; 95 % ДИ 35,1–77,04; р<0,00001), диуреза (MD 1,04; 95 % ДИ 0,10– 1,97; р=0,03) в группе ацетозоламида по сравнению с контрольной, но не было выявлено достоверной разницы в показателях асцита (ОР 0,56; 95 % ДИ 0,23–1,36; р=0,20), отеков (ОР 1,02; 95 % ДИ 0,52–2,0; р=0,95), хрипов при аускультации легких (ОР 0,82; 95 % ДИ 0,44–1,51; р=0,52), в частоте повышения давления в яремной вене (ОР 0,86; 95 % ДИ 0,63– 1,17; р=0,35). Авторами сделан вывод, что ацетозоламид в качестве дополнительного мочегонного средства значительно улучшает об- щие показатели эффективности противоотеч-ного лечения, но устраняет не все симптомы перегрузки объемом [43].
В настоящее время в России проводится открытое проспективное рандомизированное многоцентровое исследование (ОРИОН-А), в которое планируется включить 400 пациентов, поступивших в экстренном порядке с декомпенсацией ХСН II–IV ФК NYHA и находящихся на стационарном лечении. Цель исследования – изучить эффективность и безопасность применения ацетозоламида, назначаемого внутрь пациентам с декомпенсированной СН на госпитальном этапе в течение 72 ч с момента поступления, по сравнению со стандартной терапией [44]. Подобное, но менее крупное одноцентровое исследование в 2024 г. анонсировано иранскими исследователями [45].
Побочные эффекты ацетозоламида
Серьезные побочные эффекты, возникающие при лечении ацетозоламидом, редки и чаще всего связаны с наличием отягощающих факторов [46]. C.N. Schmickl et al. включили в свой мета-анализ 42 исследования побочных эффектов применения ацетозоламида (средняя суточная доза – 542 мг, 6,9 мг/кг) при острой/хронической горной болезни, нарушениях сна, дыхания и в офтальмологии в течение 3–7 дней [47]. Наиболее распространенными побочными эффектами были парестезии (51,4 %), нарушения вкуса (7,2 %), полиурия (13,5 %), утомляемость (10,6 %), тошнота (12,7 %), шум в ушах (11,0 %), диарея (10,6 %), одышка (8,8 %), гастроэзофагеальный рефлюкс (9,6 %), депрессия (7,6 %) и головокружение (6,4 %), при этом частота парестезий, нарушения слуха и утомляемости была тесно связана с величиной суточной дозы. Сообщалось о снижении либидо [48] и импотенции [49] у пациентов, получавших ацетозоламид по поводу глаукомы. Снижение либидо полностью прекратилось или заметно сократилось после отмены препарата во всех случаях. Гипокалиемия наблюдалась почти исключительно у пациентов, принимавших тиазидные диуретики и блокаторы рецепторов ангиотензина [50]. Следует отметить, что в большин- стве включенных в мета-анализ исследованиях пациенты применяли ацетозоламид более трех дней подряд, что не рекомендуется при лечении СН.
Побочные эффекты ацетозоламида при лечении СН изучены недостаточно. В одноцентровое наблюдательное проспективное исследование, проведенное во Франции в 2023– 2024 гг., было включено 58 пациентов, получавших стационарное лечение по поводу ОСН. Из них 28 пациентам назначен ацетозо-ламид (500 мг внутривенно ежедневно в течение 3 дней) одновременно с внутривенным введением фуросемида, а 30 больным – только внутривенное введение фуросемида. Пациенты, получавшие ацетозоламид, были моложе (средний возраст составил 78 и 85 лет соответственно, p=0,01) и реже страдали хроническими заболеваниями почек (средняя расчетная СКФ была равна 60 и 38 мл/мин/1,73 м2, p=0,02). Различий в частоте возникновения артериальной гипотензии, нарушений функции почек и тяжелой гипокалиемии выявлено не было. Ни в одной из групп не наблюдалось тяжелого метаболического ацидоза [51]. В исследовании ADVOR также не было обнаружено существенных различий в отношении таких нежелательных явлений, как тяжелый метаболический ацидоз, тяжелая гипокалиемия и артериальная гипотензия. Применение ацетазоламида или плацебо было прекращено по усмотрению врача из-за гипотонии (у 4 и 2 пациентов соответственно) или повышения уровня креатинина сыворотки (у 1 пациента в группе ацетазоламида) [28]. Применение аце-тозоламида было связано с более высокой частотой ухудшения функции почек (повышение уровня креатинина не менее чем на 0,3 мг/дл) в течение периода лечения (40,5 % против 18,9 %; р<0,001), но через 3 мес. разницы в уровне креатинина выявлено не было. Это ухудшение функции почек во время госпитализации не было связано с увеличением частоты госпитализаций по поводу СН или смертности и не влияло на комбинированную конечную точку. Более того, пропорционально более высокий натрийурез и диурез наблюдались у пациентов с более низкой функцией почек [30].
Обсуждение. Результаты приведенных в настоящем обзоре исследований показали, что КДТ может усиливать диурез, вызванный фуросемидом, и приводит к более выраженному уменьшению гипергидратации у пациентов с ОСН при удовлетворительном профиле безопасности. Таким образом, последовательная блокада в канальцах нефронов может быть начальной противоотечной стратегией, хотя остается неизвестным, приведут ли наблюдаемые благотворные эффекты к снижению числа повторных госпитализаций или смертности в долгосрочной перспективе [52].
Применение ацетозоламида для устранения застойных явлений в американских и европейских рекомендациях по диагностике и лечению СН относится к I классу доказательности [1, 7]. Наличие патофизиологических особенностей обусловливает ряд оснований для применения ацетозоламида в комбинации с петлевыми диуретиками для лечения СН. Во-первых, ацетозоламид увеличивает количество натрия, поступающего в петлю Генле, что усиливает натрийуретический эффект петлевых диуретиков [53]. Во-вторых, ингибирование реабсорбции натрия в проксимальном отделе почек приводит к увеличению доставки натрия и хлорида к клеткам плотного пятна, расположенным в конце петли Генле, что активирует тубулогломерулярную обратную связь подобно тому, как это делают ингибиторы SGLT2 [54]. Наконец, в исследованиях на животных было показано, что ацето-золамид предотвращает ишемически-репер-фузионное повреждение, способствуя расширению сосудов за счет индукции HIF-1α, усилению выработки оксида азота, снижению апоптоза клеток почек и, таким образом, оказывая нефропротективное действие [55]. Ацетазоламид способен уменьшать гипоксическую легочную вазоконстрикцию независимо от ингибирования карбоангидразы, что, возможно, связано с уменьшением опосредованного гипоксией образования активных форм кислорода в гладких мышцах легочных сосудов [56]. Положительное значение в лечении сердечно-сосудистых заболеваний может иметь улучшение реологических свойств крови (снижение агрегируемости и рост деформируемости эритроцитов) в условиях гиперкапнии при приеме ацетозоламида [57]. Особенно следует обратить внимание на способность ацетозоламида уменьшать образование и поступление в кровь гидрокарбонатного иона. В исследовании T. Misaka et al. было показано, что повышенный уровень HCO3- в крови (>26 ммоль/л) приводит к долгосрочным неблагоприятным исходам у пациентов с ХСН даже при нормальном уровне рН [58].
Заключение. Совершенствование подходов к лечению декомпенсированной ХСН является актуальной задачей. До тех пор, пока не будут проведены клинические исследования, в которых будут сравниваться различные схемы комбинированной терапии с внутривенным введением высоких доз петлевых диуретиков в острой фазе и последующей эффективной поддерживающей терапией после выписки из стационара, доказательства в пользу комбинированной терапии диуретиками будут оставаться недостаточными [59]. Отсутствие улучшения прогноза у пациентов с ХСН в исследовании ADVOR не должно разочаровывать, так как трудно предположить, что однократное трехдневное применение какого-либо лекарственного средства способно повлиять на среднесрочный и долгосрочный прогноз. Вероятно, требуются повторные курсы применения ацетозоламида для получения положительного результата. Необходимы дополнительные клинические исследования для выработки оптимальной тактики назначения ингибиторов карбоангидразы при лечении ХСН. Но уже сейчас можно сказать, что «старый» и слабый диуретик аце-тозоламид не должен быть забыт и имеет хорошие перспективы для терапии сердечной недостаточности.


