Применение аддитивных технологий при замещении огнестрельных дефектов костей конечностей
Автор: Давыдов Д.В., Брижань Л.К., Керимов А.А., Кукушко Е.А., Хоминец И.В., Найда Д.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4-1 т.17, 2022 года.
Бесплатный доступ
Применение 30-печати в современной травматологии и ортопедии рассматривается в качестве перспективного направления в решении проблем замещения дефектов костей различной локализации. Целью нашего исследования стало изучение возможности замещения огнестрельных дефектов костей конечностей на основе аддитивных технологий. За период с марта 2018 по апрель 2021 г. в Центре травматологии и ортопедии ФГБУ «Главный военный клинический госпиталь имени академика Н.Н. Бурденко» Министерства обороны РФ проведено лечение 23 пациентов, из них 19 (82,6%) мужчин и 4 (17,4%) женщины с огнестрельными дефектами костей конечностей. Ближайшие и среднесрочные результаты замещения огнестрельных дефектов костей конечностей индивидуальными металлическими имплантатами, изготовленными на 30-принтере, показали эффективность данной технологии. При помощи 30-печати возможно изготовление индивидуальных имплантатов любой конфигурации, что обеспечивает максимально полное анатомическое восстановление поврежденного сегмента и значительно облегчает последующую реабилитацию.
3d-моделирование, sd-печать, sd-имплантаты, аддитивные технологии, замещение дефектов костей, огнестрельные дефекты костей
Короткий адрес: https://sciup.org/140296608
IDR: 140296608 | DOI: 10.25881/20728255_2022_17_4_2_57
The use of additive technologies in the replacement of gunshot defects of a bones
3-d technologies in modern traumatology and orthopedics have firmly taken their step in replacing bone defects of various localizations. The aim of our study was to optimize the technology of replacing gunshot extremity defects with individual autografts based on the use of 3d computer modeling, their clinical testing, evaluation of the results of application, analysis of complication and development of measures for their prevention. For the period from March 2018 to April 2021 at the Center Traumatology and Orthopedics of the Federal State Institution "The Main Military Clinical Hospital named after academician N.N. Burdenko” Russian Defence Ministry, operated on 23 (100%) patients, including 19 (82,6 %) men and 4 (17,4%) women with gunshot defects or extremity bones. Tested and introduced into everyday activities on the basis o the Center Traumatology and Orthopedics, the used 3d substitution in the treatment gunshot defects or extremity bones, not previously used in the Russian Federation, showed good results in the early postoperative period. Replacement of bone defects with implants made of bone-substituting material it has proven itself as a reliable method. The use 3d technologies allows to model individual implants of any complexity, thereby most optimally approach the treatment of a particular patient, as anatomically as possible replace a gunshot bones defects and achieve early recovery functions of the damaged extremity.
Текст научной статьи Применение аддитивных технологий при замещении огнестрельных дефектов костей конечностей
Огнестрельные ранения конечностей имеют специфические особенности, к которым следует отнести первичное инфицирование, наличие зон первичного и вторичного некроза тканей, участков кости с сомнительной жизнеспособностью и пониженными регенераторными возможностями, формирование сложных по форме и величине дефектов костей [1; 2]. Для замещения дефектов используются несвободная костная пластика по Илизарову, свободная пересадка аутокости в изолированном варианте или в составе комплексов тканей на микрососудистых анастомозах [3; 4]. Серьезную проблему представляет замещение околосуставных и внутрисуставных дефектов, поскольку в таких случаях необходимо решить несколько сложных задач. Первая — подготовка реципиентского ложа и обеспечение оптимальных условий для интеграции трансплантата и (или) имплантата. Вторая — подбор и моделирование трансплантата и (или) имплантата по форме дефекта кости для обеспечения продуктивного контакта с реципиентским ложем. Третья — обеспечение стабильной фиксации системы кость-трансплантат (-имплантат) для последующей реабилитации пациента и восстановления функции поврежденной конечности [5].
Костные аутотрансплантаты считаются оптимальным материалом для замещения дефектов костной ткани, т.к. выполняют не только механическую, но и физиологическую функцию за счет наличия биологических компонентов (ССК, коллагеновый каркас, БАВ, минералы и др.), способствующих регенерации тканей [6]. Так же для стимуляции регенерации могут использоваться биологические способы в виде: обогащенной тромбоцитами аутоплазмы; тканеинженерных конструкций; концентратов стромальных клеток [5]. Однако использование аутотрансплантатов имеет ряд недостатков, таких как: травматизация донорского участка, ограниченный объем получаемого материала, невозможность в полной мере смоделировать трансплантат в соответствии с формой и контуром дефекта кости [7].
Новые возможности открывают методы замещения костных дефектов различной этиологии и локализации с применением индивидуальных имплантатов. Перспективной представляется технология компьютерного 3D-моделирования, применяющаяся в различных областях медицины: травматологии и ортопедии [8–10], нейрохирургии [11], челюстно-лицевой хирургии [12], онкологии [13]. Главным элементом данной технологии

является создание на основе результатов мультиспираль-ной компьютерной томографии (МСКТ) индивидуального имплантата, соответствующего по форме и размерам дефекту кости. Важным преимуществом 3D-имплантата является возможность воссоздания мелких деталей для замещения дефектов со сложной внутренней геометрией, что обеспечивает его плотное прилегание к воспринимающему ложу и увеличивает перспективы интеграции с окружающими тканями. Таким образом, индивидуальные 3D-имплантаты открывают новые перспективы в решении проблемы замещения костных дефектов [14].
Огнестрельные дефекты костей конечностей, представляют собой интересный, сложный и, в то же время, перспективный объект для применения имплантатов на основе 3D-моделирования. Проведенный обзор современной литературы, по ключевым словам, на русском и английском языке выявил дефицит информации по рассматриваемой проблеме, что определило актуальность темы и необходимость выполнения данного исследования.
Цель исследования — оптимизация технологии замещения огнестрельных дефектов костей конечностей индивидуальными имплантатами на основе компьютерного 3D-моделирования, их клиническая апробация и оценка результатов применения.
Материал и методы
За период с марта 2018 по апрель 2021 г. в Центре травматологии и ортопедии ФГБУ «Главный военный клинический госпиталь имени академика Н.Н. Бурденко» Министерства обороны РФ проведено лечение 23 пациентов с огнестрельными дефектами костей конечностей, из которых было 19 (82,6%) мужчин и 4 (17,4%) женщины. Возраст больных варьировал от 19 до 45 лет. Средний возраст пациентов был равен 28,9±0,5 лет, что свидетельствует о превалировании больных трудоспособного возраста. По локализации огнестрельные дефекты распределились следующим образом: плечо — 1 (4,35%), предплечье — 7 (30,4%), кисть — 1 (4,35%), бедро — 2 (8,7%), голень — 5 (21,7%), стопа — 7 (30,4%). Итого: верхняя конечность 9 (39,1%) , нижняя конечность 14 (60,9%).
Критерии включения: наличие огнестрельного дефекта кости; отсутствие клинико-лабораторных признаков инфекции реципиентской области.
Критерии исключения: наличие очагов хронической инфекции вне поврежденного сегмента конечности, наличие сахарного диабета.
Изготовление и производство индивидуальных 3D-имплантатов регламентировано статьей 38 Федерального закона «Об основах охраны здоровья граждан в Российской Федерации» от 21.11.2011 №323-ФЗ, Постановлением правительства РФ от 27.12.2012 г. №1416 «Об утверждении Правил государственной регистрации медицинских изделий», Письмом Федеральной службы по надзору в сфере здравоохранения от 21.07.2015 г. №04-21338/15. Стерилизация осуществлялась в соот- ветствии с Постановлением Главного государственного санитарного врача РФ от 18.05.2010 N 58 (ред. от 10.06.2016 г.) «Об утверждении СанПиН 2.1.3.2630-10 «Санитарно-эпидемиологические требования к организациям, осуществляющим медицинскую деятельность» (с изменениями на 27 октября 2020 г.).
Предварительная подготовка для изготовления индивидуального 3D-имплантата состоит из следующих этапов.
-
1. Выполнение мультиспиральной компьютерной томографии поврежденного сегмента с толщиной среза 1 мм и анализ исходных данных пациента на персональном компьютере при помощи программы ХХХ.
-
2. Создание рендера (наброска) металлоконструкции хирургом совместно с инженером.
-
3. Создание в программе 3D-модели имплантата инженером-проектировщиком.
-
4. Внесение корректировки в 3D-модель хирургом.
-
5. Изготовление полимерного прототипа имплантата и точной копии кости с дефектом.
-
6. Отработка техники хирургической операции на полимерной модели.
-
7. Окончательное изготовление имплантата.
Печать имплантатов осуществляли на 3D-принтере Concept Laser M2 (Германия, компания «Concept Laser»), который работает на основе технологии селективного лазерного спекания — SLM или Selective lasermelting. Суть производства заключается в нанесении слоя металлического порошка на рабочую плиту и последующем воздействии лазера на неё. Поверхность слой за слоем сканируется лучом лазера, в результате чего происходит плавление металлического порошка. При изготовлении 3D-моделей использовался сплав из титана, алюминия и ванадия (90% Ti — 6% Al — 4% V), который обладает улучшенным соотношением прочности и массы по отношению к другим сплавам. Материал превращается в однородную массу, которая создает слои 3D-изделия. Рабочая платформа, завершив свой цикл, опускается на глубину, равную толщине слоя. Процедура повторяется для каждого слоя изделия. Затем готовая 3D-конструкция отделяется от рабочей плиты и проходит финальную обработку.
Операции замещения дефекта кости выполняли под общей или проводниковой анестезией. Доступ к зоне дефекта осуществляли в зависимости от анатомии сегмента и особенностей местных посттравматических изменений. Обязательным условием замещения дефекта 3D-имплантатом была стабильная фиксация системы кость-имплантат. Вместо контакта имплантат-кость дополнительно вводился концентрат аспирата костного мозга пациента (BMAC) с целью обеспечения лучшей интеграции имплантата. Приготовление ВМАС осуществлялось по стандартизированному протоколу.
В раннем послеоперационном периоде (ближайшие результаты) оценивали состояние послеоперационной
раны, стабильность фиксации и точность расположения 3D-имплантата в зоне дефекта, выраженность болевого синдрома, наличие осложнений, продолжительность пребывания пациентов в стационаре.
Для контроля положения имплантата и его интеграции применяли рентгенографию и компьютерную томографию (КТ). Клинические результаты оценивали по шкалам-опросникам, срокам лечения, количеству и тяжести осложнений. Для оценки функционального результата лечения раненых с поражением верхней конечности применяли опросник DASH (Disabilities of the Arm, Shoulder and Hand, таблица 2.) [9]. Для оценки функциональных результатов лечения пострадавших с переломами костей нижней конечности — шкалу Neer-Grantham-Shelton (таблица 3) [10]. В данной шкале для характеристики пункта «движения в суставе» применили показатели движений в суставах в соответствии с таблицей 4 Постановления Правительства РФ от 04.07.2013 г. №565 «Об утверждении Положения о военно-врачебной экспертизе» [14]. Во всех случаях оценивали болевой синдром по визуально-аналоговой шкале (ВАШ) (табл. 1) в баллах от 1 до 100, через 2 и 6 месяцев после операции [15]. Срок наблюдения пациентов составил от 4 месяцев до 2 лет.
Результаты
У всех пациентов в полном объеме был реализован предоперационный план: имеющийся дефект замещен 3D-имплантатом со стабильной фиксацией в реципи-ентском ложе. Способ фиксации имплантата для каждого случая определялся индивидуально. В некоторых случаях фиксация достигалась при помощи винтов различной длины и диаметра, в других — дополнительно использовалась пластина для более стабильного удержания имплантата. Положение имплантата полностью повторяло замещенный костный дефект.
Средний объем кровопотери составил 230±60 мл. Длительность операции 95±25 мин. По результатам контрольных рентгенографий и компьютерной томографии остеоинтеграция наступила во всех случаях в сроки от 3 до 12 мес.
Результаты оценки интенсивности боли показали полное отсутствие болевого синдрома у 8 пациентов (34,8%) через 6 месяцев с момента операции (табл. 1). При этом отмечено, что болевой синдром более выражен после замещения суставных и околосуставных дефектов и имеет прямую связь с функциональной нагрузкой.
У раненых с дефектами костей нижних конечностей при оценке по шкале Neer-Grantham-Shelton (с модификациями) хорошие результаты получили в 10 (71,5%) случаях, удовлетворительные — в 4 (28,5%) случаях. Таким образом, исходы хирургического лечения оценили у 74% (17 пациентов) как хорошие и отличные, у 26% (6 пациентов) — удовлетворительные.
Поверхностные воспалительные явления и краевой некроз встретился у 1 пациента (4,3%). Данное ослож-
Табл. 1. Распределение пациентов по выраженности болевого синдрома в различные сроки после операции по ВАШ
|
Интенсивность боли, баллы |
Срок после операции/ общее количество пациентов |
|
|
2 месяца после операции |
6 месяцев после операции |
|
|
Отсутствует (0–5) |
2 (8,7%) |
8 (34,8%) |
|
Слабая (6–35) |
15 (65,2%) |
13 (56,5%) |
|
Умеренная (36–55) |
4 (17,4%) |
2 (8,7%) |
|
Выраженная (56–75) |
2 (8,7%) |
0 |
|
Очень сильная (76–100) |
0 |
0 |
|
ВСЕГО |
23 (100%) |
23 (100%) |
Табл. 2. Динамика улучшения функции травмированной верхней конечности по опроснику DASH
|
Сумма баллов |
Dash / общее количество пациентов |
|
|
2 месяца после операции |
6 месяцев после операции |
|
|
Хорошо (26–50 баллов) |
5 (55,6%) |
7 (77,8%) |
|
Удовлетворительно (51–75 баллов) |
2 (22,2%) |
2 (22,2%) |
|
Неудовлетворительно (76–100 баллов) |
2 (22,25) |
– |
|
ВСЕГО |
9 (100%) |
9 (100%) |
Табл. 3. Результаты лечения пострадавших с переломами костей нижней конечности по данным шкалы Neer-Grantham-Shelton (через 6 месяцев после операции)
Клиническое наблюдение
Пациентка Т. 38 лет, поступила через 1 месяц после травмы с диагнозом: Огнестрельное дробовое слепое ранение правого голеностопного сустава с оскольчатым переломом дистального метаэпифиза большеберцовой кости, многооскольчатым переломом таранной кости с дефектом общим объемом около 3 см3, с повреждением сухожилия задней большеберцовой мышцы (Рис. 1). После этапных хирургических обработок больной выполнена пластика дефекта мягких тканей внутренней поверхности правого голеностопного сустава несвободным суральным лоскутом правой голени (Рис. 2).

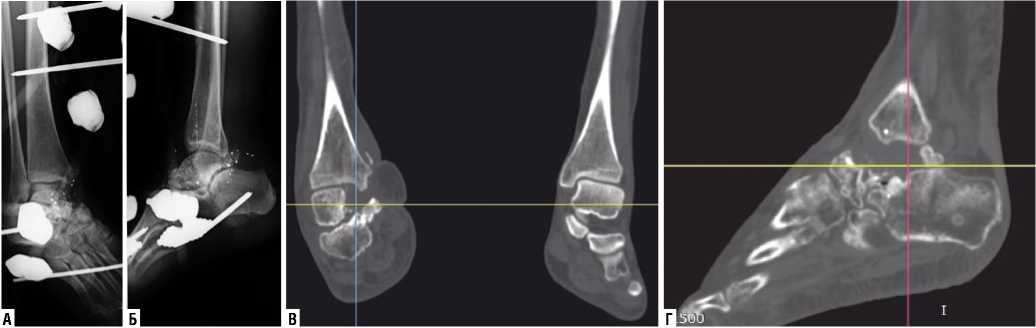
Рис. 1. Пациентка Т. 38 лет. Рентгенограммы правого голеностопного сустава: А — в прямой; Б — боковой проекции; В, Г — КТ голеностопных суставов в сравнении (показана зона дефекта таранной кости).
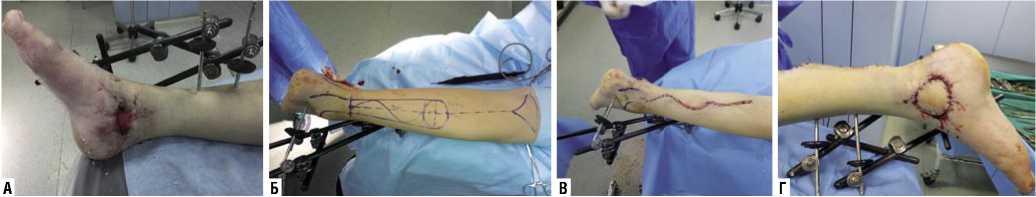
Рис. 2. Внешний вид голени и голеностопного сустава: А — зона кожного дефекта внутренней поверхности сустава; Б–Г — этапы пластики дефекта мягких тканей несвободным суральным лоскутом правой голени.
По заживлению операционных ран больной разрешена осевая нагрузка на правую нижнюю конечность, однако ввиду обширного дефекта таранной кости сформировалась патологическая варусная установка стопы, болевой синдром сохранялся (Рис. 3). С целью устранения деформации правой стопы, сохранения опороспособности правой нижней конечности, а также восстановления амплитуды движений в голеностопном суставе, выполнено эндопротезирование таранной кости (реконструктивно-пластическое замещение дефекта правой таранной кости с фиксацией тремя винтами) (Рис. 5). Индивидуальное изделие, по форме соответствующее правой таранной кости, было изготовлено по описанной выше методике (Рис. 4).
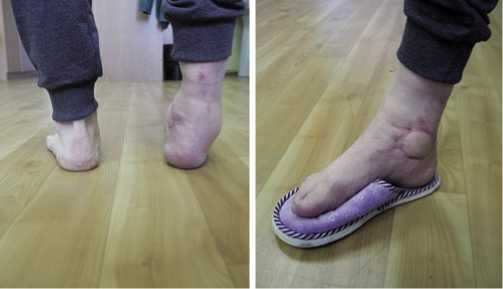
Рис. 3. Внешний вид голеностопного сустава после этапного лечения (варусная деформация правой стопы).

Рис. 4. Внешний вид имплантата (эндопротез таранной кости), изготовленного на 3D-принтере.

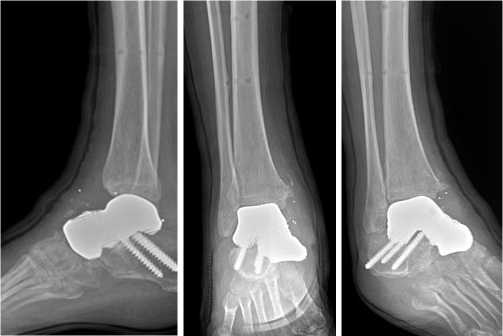
Рис. 5. Рентгенограммы правого голеностопного сустава в 3-х проекциях после реконструктивно-пластического замещения таранной кости протезом с фиксацией тремя винтами.
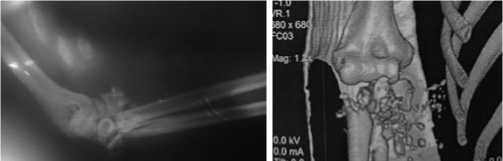
Рис. 6. Рентгенограмма и КТ правого локтевого сустава при поступлении.
В послеоперационном периоде проведено реабилитационное лечение, направленное на восстановление функции и опороспособности правой нижней конечности. Разработка движений в пассивном режиме начата после стихания болевого синдрома на 2 сутки после операции. Через 3 недели после операции начата дозированная нагрузка на правую ногу с постепенным увеличением до полной в течение последующих 8 недель. Через 4 недели после операции достигнута хорошая функция правого голеностопного сустава (подошвенное сгибание до 115 градусов, тыльное разгибание до 76 градусов).
Поздних инфекционных осложнений после операции не отмечено. Результат лечения через 6 месяцев после операции по шкале Neer-Grantham-Shelton оценен как хороший (35 баллов). Результат по шкале ВАШ составил 24 балла, что соответствует слабой интенсивности болевого синдрома. Объем движения в голеностопном суставе полный.
Клиническое наблюдение
Пациент Ш., 23 лет получил сквозное пулевое ранение верхней трети правого предплечья с внутрисуставным оскольчатым переломом и дефектом костной ткани проксимальных матаэпифизов правых локтевой и лучевой костей со смещением отломков с посттравматической невропатией правого локтевого и срединного нервов (Рис. 6).
Первым этапом выполнена ПХО ран, фиксация перелома в АВФ КСВП, дренированиеVAC-системой. В дальнейшем, выполнена установка антибактериального цементного спейсера. Демонтаж аппарата внешней фиксации произведен через 1,5 месяца (Рис. 7, 8).
После предоперационного планирования на основе компьютерных томограмм выполнено компьютерное моделирование индивидуального имплантата для замещения дефекта проксимального отдела локтевой кости и печать при помощи 3D-принтера (Рис. 9).
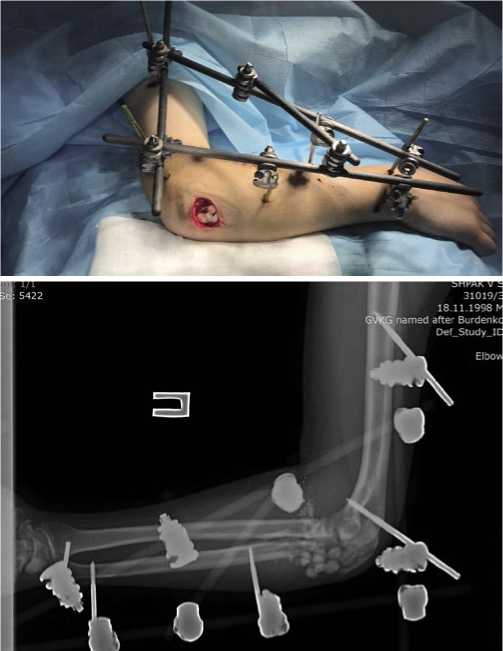
Рис. 7. Рентгенограммы правого локтевого сустава после уставновки анти-батериального спейсера и внешнией вид правой верхней конечности после операции.
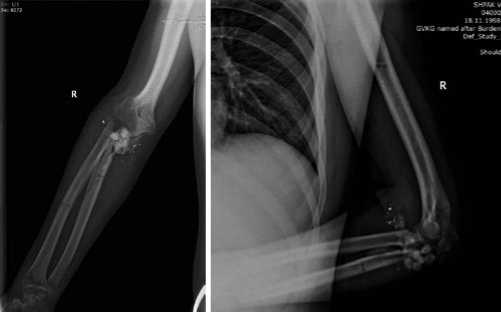
Рис. 8. Рентгенограммы после демонтажа АВФ.
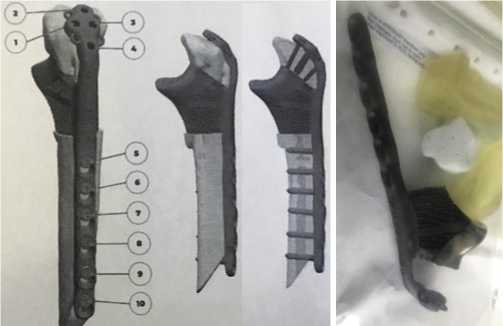
Рис. 9. 3D-модель имплантата и ее внешний вид.
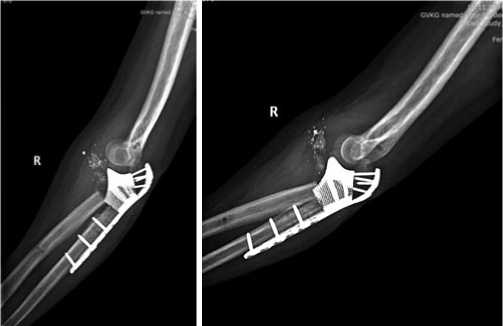
Рис. 10. Рентгенограммы правого локтевого сустава после операции.
Через пять месяцев с момента получения травмы пациенту выполнена реконструктивно-пластическая операция — удаление цементного спейсера, корригирующая остеотомия локтевой кости, открытая репозиция, артролиз, костная аутопластика, остеосинтез локтевой кости реконструктивной титановой конструкцией для замещения дефекта проксимального метаэпифиза локтевой кости индивидуального изготовления с введением ВМАС в месте контакта кость-имплантат (Рис. 10).
Функциональный результат через 4 недели после операции (Рис. 10). В дальнейшем, после проведенного курса лечебной физкультуры, через 8 недель после операции, достигнуто полное разгибание в локтевом суставе, активное сгибание до 70 градусов.
Обсуждение
Встречающиеся в мировой и отечественной литературе публикации, посвященные использованию 3D-печати при замещении дефектов костей различной локализации, характеризуются ограниченным количеством наблюдений и фактически являются демонстрацией первого опыта. В значительной мере эта характеристика применима и к данному исследованию. Новизна, пока еще ограниченная доступность и малая известность
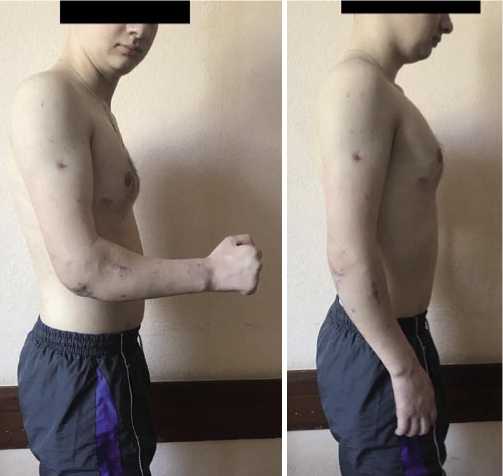
Рис. 11. Функциональный результат через 4 недели после операции.
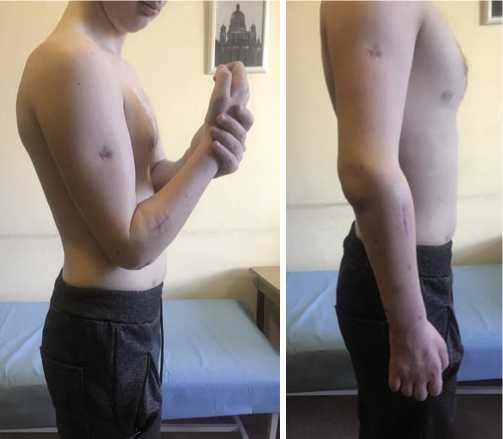
Рис. 12. Функциональный результат через 8 недель после операции.
технологии, повышенные требования к безопасности в плане развития осложнений являются объяснением относительно небольшого количества наблюдений в рассматриваемой группе. Извлеченный из проведенной работы практический опыт в значительной мере касается технических аспектов, позволяющих представить определенные рекомендации, которые, возможно, будут полезны заинтересованным специалистам при лечении таких раненых.
Прежде всего, необходимо рассматривать данную технологию как имплантацию массивного эндопротеза в условиях повышенного риска обострения инфекции после открытого изначально инфицированного перелома,
сопровождающегося дефектом кости и мягких тканей. Поэтому основным критерием отбора является отсутствие признаков местного воспаления. Это достигается адекватным первичным лечением с использованием максимально возможного арсенала современных средств иммобилизации и борьбы с инфекционными осложнениями. Наличие признаков воспаления должно рассматриваться как противопоказание к замещению дефекта 3D-имплантатом.
Реабилитация с целью восстановления функции конечности является непременным элементом, позволяющим рассчитывать на хороший результат. При этом следует учитывать объем первичного повреждения тканей сегмента, локализацию и величину дефекта кости, сохранность двигательных структур, характер нагрузки, методику фиксации имплантата и другие показатели. Психологическое состояние и мотивация также играют важную роль в получении положительного результата лечения.
Применяемое для изготовления изделий оборудование не является в буквальном смысле медицинским. Оно является универсальным, требующим профильной подготовки и привлечения, помимо травматологов-ортопедов, целого круга специалистов — рентгенологов, инженеров, программистов и других, участвующих в производственном процессе. Современное законодательство при соответствующем оформлении документации позволяет использовать подобные конструкции в медицине, что обеспечивает определенную свободу действий и внушает надежду на более широкое внедрение данной технологии.
Полученные положительные ближайшие результаты, отсутствие серьезных осложнений, восстановление функции и низкий болевой синдром являются обнадеживающим фактором и обоснованием продолжения исследований в этом направлении.
Заключение
Результаты исследования показали высокую эффективность использования 3D имплантатов для замещения огнестрельных дефектов костей различной локализации. Структура и остеокондуктивные свойства поверхности имплантатов в сочетании с использованием концентрата аспирата костного мозга обеспечили достаточную остеоинтеграцию с реципиентным ложем в короткие сроки с сохранением достигнутого результата в среднесрочной перспективе. Это обусловлено биосовместимостью титанового сплава, используемого для изготовления имплантата, его ячеистой структурой с наличием микропор оптимального размера, а также за счет обеспечения стабильной первичной фиксации.
Замещение дефектов костей имплантатами из костнозамещающего материала зарекомендовало себя как эффективный метод. Использование 3D-технологий позволяет моделировать индивидуальные имплантаты любой сложности, тем самым обеспечить оптимальный подход к лечению конкретного пациента, максимально анатомично заместить огнестрельный дефект костной ткани и достичь раннего восстановления функции поврежденной конечности.
Использование 3D-технологии при лечении пациентов со сложным дефектами костей различной локализации обеспечивает персонифицированный подход за счет максимально точного восстановления анатомии поврежденного сегмента.
Возможность получения хороших результатов обеспечивается комплексным многоэтапным лечением, в основе которого лежит качественное оказание первичной помощи, тщательное планирование операции и полноценная реабилитация. Собственно хирургическое вмешательство является важной составляющей частью этого комплексного лечения, но возможность получения хорошего результата обеспечивается всем комплексом перечисленных мер.
На современном этапе применение индивидуальных имплантатов на основе 3D-технологий требует дальнейшего изучения и оценки отдаленных результатов.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Применение аддитивных технологий при замещении огнестрельных дефектов костей конечностей
- Шаповалов В.М., Хоминец В.В., Брижань Л.К., и др. Современное состояние и совершенствование травматолого-ортопедической помощи раненым в конечности // Военно-медицинский журнал. — 2018. — Т.339. — №10. — С.20-27.
- Грицюк А.А., Нелин Н.И. Лечение комбинированных дефектов нижних конечностей после боевых травм // Травматология и ортопедия России. — 2006. — №2(40). — С.216.
- Артемьев А.А., Грицюк А.А., Нелин Н.И., и др. Клинико-рентгенологические особенности формирования дистракционного регенерата при удлинении голени по Илизарову // Кафедра травматологии и ортопедии. — 2018. — №3(33). — С.5-9. doi:10.17238/issn:2226-2016.2018.3.5-9.
- Борзунов Д.Ю., Моховиков Д.С., Колчин С.Н. и др. Комбинированное применение несвободной костной пластики по Илизарову и техники Masquelet при реабилитации пациентов с приобретенными костными дефектами и ложными суставами // Гений ортопедии. — 2020. — Т.26. — №4. — С.532-538. doi: 10.18019/1028-4427-2020-26-4-532-538.
- Крюков Е.В., Брижань Л.К., Хоминец В.В. Опыт клинического применения тканеинженерных конструкций в лечении протяженных дефектов костной ткани // Гений Ортопедии. — 2019. — Т.25. — №1. — С.49-57. doi: 10.18019/ 1028-4427-2019-25-1-49-57.
- Хоминец В.В., Щукин А.В., Михайлов С.В. и др. Особенности лечения раненых с огнестрельными переломами длинных костей конечностей методом последовательного внутреннего остеосинтеза // Политравма. — 2017. — №3. — С.12-22.
- Мураев А.А., Иванов С.Ю., Ивашкевич С.Г. и др. Органотипичные костные имплантаты — перспектива развития современных остеопластических материалов // Стоматология. — 2017. — Т.96. — №3. — С.36-39. doi: 10.17116/stomat 201796336-39.
- Патент РФ на изобретение № 2697790 C1, МПК G09B 23/28. Тихилов Р.М., Шубняков И.И., Денисов А.О. и др. Способ моделирования дефектов костной ткани для изучения рефиксации мягких тканей к пористым титановым имплантатам с использованием аддитивных технологий.
- Dhawan A, Kennedy PM, Rizk EB, Ozbolat IT. Three-dimensional Bioprinting for Bone and Cartilage Restoration in Orthopaedic Surgery. Journal of the American Academy of Orthopaedic Surgeons. 2019; 27(5): e215-e226. doi: 10.5435/JAAOS-D-17-00632.
- Попков А.В., Кононович Н.А., Горбач Е.Н. и др. Эффективность использования 3D-имплантатов с биоактивными свойствами для замещения обширных дефектов костей: экспериментальное исследование // Травматология и ортопедия России. — 2021. — Т.27. — №1. — С.37-52. doi:10.21823/2311-2905-2021-27-1-37-52.
- Иванов В.П., Ким А.В., Хачатрян В.А. 3D-печать в краниофациальной хирургии и нейрохирургии. Опыт ФГБУ «НМИЦ им. В.А.Алмазова» // Нейрохирургия и неврология детского возраста. — 2018. — №3. — С.28-39.
- Арапова И.А., Кучерова П.А. 3D-печать в челюстно-лицевой хирургии // Главный врач Юга России. — 2017. — Т.58. — С.13-17.
- Сушенцов Е.А., Мусаев Э.Р., Софронов Д.И. и др. Компьютерные технологии и 3D-принтинг в лечении больных с опухолями костей таза // Саркомы костей, мягких тканей и опухоли кожи. — 2018. — №1. — С.29-32.
- Kokkinis D, Schaffner M, Studart AR. Multimaterial magnetically assisted 3D printing of composite materials. Nat. Commun. 2015;6(8643): 1-10. doi: 10.1038.
- Няза К.В., Сенатов Ф.С., Анисимова Н.Ю., и др. Пористый каркас для замещения дефектов костной ткани, полученный методом 3d-печати. Российский биотерапевтический журнал. — 2016. — №15(1). — С.79.
- Тетерина А.Ю., Фетисова В.Э., Федотов А.Ю. и др. Биосовместимые биодеградируемые композиционные материалы в системе биополимеры-фосфаты кальция для замещения костно-хрящевых дефектов // Материаловедение. — 2020. — №8. — С.41-48. doi: 10.31044/1684-579X-2020-0-8-41-48.
- Atroshi I, Gummesson C, Andersson B, Dahlgren E, Johansson A. The disabilities of the arm, shoulder and hand (DASH) outcome questionnaire: reliability and validity of the Swedish version evaluated in 176 patients. Acta Orthop Scand. 2000; 71(6): 613-618. doi: 10.1080/000164700317362262.
- Neer CS 2nd, Grantham SA, Shelton ML. Supracondylar fracture of the adult femur. A study of one hundred and ten cases. J Bone Joint Surg Am. 1967; 49(4): 591-613.
- Постановление Правительства РФ от 04.07.2013 г. №565 (ред. от 01.06.2020) «Об утверждении Положения о военно-врачебной экспертизе».
- Hawker GA, Mian S, Kendzerska T, French M. Measures of adult pain: Visual Analog Scale for Pain (VAS Pain), Numeric Rating Scale for Pain (NRS Pain), McGill Pain Questionnaire (MPQ), Short-Form McGill Pain Questionnaire (SF-MPQ), Chronic Pain Grade Scale (CPGS), Short Form-36 Bodily Pain Scale (SF-36 BPS), and Measure of Intermittent and Constant Osteoarthritis Pain (ICOAP). Arthritis Care Res (Hoboken). 2011; 63(11): 240-252.


