Применение дозированной дермотензии для закрытия раневых дефектов мягких тканей голени гнойно-некротического и травматического происхождения
Автор: Пятаков С.Н., Завражнов А.А., Федосов С.Р., Шевченко А.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.7, 2012 года.
Бесплатный доступ
Целью исследования, в которое были включены 239 пациентов с раневыми дефектами мягких тканей голени, явилось улучшение результатов лечения больных с обширными гнойно-некротическими ранами мягких тканей голени различной этиологии на основе разработки и внедрения в клиническую практику усовершенствованной оригинальной методики дозированной дермотензии. Показано, что предложенная методика динамической дермотензии позволяет ускорить пластическое закрытие ран, сократить сроки пребывания больных в стационаре, улучшить непосредственные косметический и функциональный результаты лечения, а также создать перспективы дальнейших пластических реконструктивных операций.
Дермотензия, лечение ран, раневой дефект голени
Короткий адрес: https://sciup.org/140188106
IDR: 140188106 | УДК: 617.586-089.844:616.718-005.4
Текст научной статьи Применение дозированной дермотензии для закрытия раневых дефектов мягких тканей голени гнойно-некротического и травматического происхождения
Лечение раневых дефектов, возникающих в результате гнойно-некротической инфекции мягких тканей и механических повреждений, остается актуальной проблемой хирургии [2, 19]. Современный подход к лечению больных с мягкоткаными дефектами предусматривает раннее закрытие раневой поверхности, что невозможно без проведения адекватной первичной и/или вторичной хирургической обработки и выполнения кожно-пластических операций [3, 10]. При этом хирургическая обработка патологического очага может увеличивать раневой дефект, а кожная пластика в контаминированной ране сопровождаться большим количеством послеоперационных осложнений [16].
Среди огромного арсенала кожно-пластических операций для закрытия раневых дефектов наиболее часто используют пластику местными тканями, которая может выполняться одномоментно или методом дозированной дермотензии [9, 11, 12, 13]. При дефиците местных тканей используют пластику расщепленным кожным лоскутом, а при расположении раны в функционально значимой зоне применяют пластику перемещенным лоскутом на постоянной или временной питающей ножке и на микро-сосудистых анастомозах [1, 7, 14].
Выбор метода пластического закрытия обычно определяется возрастом больного, тяжестью состояния, наличием сопутствующих заболеваний, но, главным образом, локализацией и характером патологического процесса [5].
Наиболее сложную группу для лечения представляют больные с раневыми мягкоткаными дефектами на голени, возникающими после гнойно-некротического процесса или высокоэнергетической травмы. Сложность клинической ситуации определяется анатомическими особенностями данной области (малым резервом пластического материала и тонкими по толщине кожно-подкожно-фасциальными лоскутами), а также частым (в 12–15% случаев) наличием остита или остеомиелита берцовых костей [8]. Кроме того, первичное санирующее оперативное вмешательство, сопровождаемое иссечением некротических тканей и костными резекциями, может привести к грубой деформации раны с невозможностью ее закрытия местными тканями. Пластика раны лоскутом на сосудистой ножке может быть затруднена в условиях постоянной контаминации. Пластика свободно-расщепленным лоскутом является лишь временным решением проблемы и функционально не пригодной при сохранении опороспособности конечности. В этой связи перспективным является закрытие раневых дефектов с помощью использования всех возможностей дозированной дермотензии [4, 6, 15, 17, 18, 20].
Целью настоящего исследования явилось улучшение результатов лечения больных с обширными гнойно-некротическими ранами мягких тканей голени различной этиологии на основе разработки и внедрения в клиническую практику усовершенствованной методики дозированной дермотензии.
Материалы и методы
Проанализированы результаты лечения 239 больных с раневыми дефектами мягких тканей голени различной этиологии, переведенных с 2006 по 2011 гг. в Краснодарскую краевую клиническую больницу № 1 им. профессора С.В. Очаповского (ККБ № 1) из других лечебно-профилактических учреждений Краснодарского края. Среди них 137 больных имели посттравматические дефекты мягких тканей (Sср. = 160 ± 16 см2) и 102 больных – раневые дефекты после перенесенных гнойно-некротических процессов кожи, подкожной клетчатки и остеомиелита (Sср. = 182 ± 24 см2). Практически все больные ранее подверглись оперативному лечению в объеме первичной хирургической обработки – 59%, некрэктомии – 9%, открытой фасциотомии – 6% и вторичной хирургической обработке – 32% с сегментарной резекцией костей голени – 9%.
В условиях ККБ № 1 всем больным проводилось хирургическое лечение, направленное на удаление некротических тканей, стихание воспалительных явлений и кожно-пластическое закрытие ран. В период с 2006 по 2008 гг. 103 (95%) больным закрытие ран голени выполнялось только свободной аутодермопластикой расщепленным кожным лоскутом (группа 1). В период с 2008 по 2011 гг. у 90 (69%) больных применялась дозированная дермотензия с использованием авторских методик (группа 2). Обе группы пациентов были сопоставимы по возрасту, полу и объему повреждений покровных тканей (p ≥ 0,05).
Пластические операции производились только во второй фазе раневого процесса. С целью подготовки ран к закрытию больным выполнялись хирургические обработки (первичные или вторичные), которые во 2 группе сопровождались наложением вакуумных повязок (V.A.C.) по общепринятой методике (рис. 1).
Для оценки состояния тканей в зоне раневого дефекта, динамики течения раневого процесса и эффективности применяемого лечения использовались микробиологические, цитологические, планиметрические исследования, а так же проводилась оценка микроциркуляции в области раны путем измерения транскутанного напряжения кислорода в капиллярной крови кожи
(ТсРО2) с помощью оксимонитора и лазерной допплеровской флоурометрии.
Разработанная система для проведения дермотензии включала в себя аппарат внешней фиксации со спицами Киршнера, к которым закреплялись параллельные стержни с отверстиями (рисунок 2).
Между спицами и стержнями устанавливались упругие тарированные пружины диаметром 0,7–0,8 см и длиной 10–12 см, соединенные нитями со стержнями аппарата внешней фиксации и датчики силы натяжения нитей (тензодатчики). Датчики включались в состав системы (индикатора) мониторинга для обеспечения задания и контроля величины силы натяжения.
Дермотензия осуществлялась следующим образом: предварительно по длине раны (отступя 1–1,5 см от края) через всю толщу кожно-подкожно-фасциального лоскута в виде «змейки» проводили спицы Киршнера. При этом концы спиц выводили на кожу и загибали для предотвращения травматизации эпидермиса. Заранее оба силовыводящих элемента тензодатчика (Г-образной формы) снабжали толстыми лавсановыми нитями-тягами. Одну из нитей проводили при помощи шовной иглы с внутренней поверхности лоскута с захватом спицы Киршнера, чем достигали наименьшую травматизацию и ишемию мягких тканей во время тензии. Затем, в зависимости от локализации раневого дефекта на конечности, монтировали аппарат внешней фиксации на основе комплекта аппарата Илизарова. На штангах, полукольцах и кольцах аппарата, на высоте не менее 10 см укрепляли два и более параллельно расположенных стержня с отверстиями, к которым фиксировались стержни-спи-ценатяжители. К этим стержням крепили тензодачики и тарированные пружины, снабженные нитью. Количество датчиков, пружин, стержней-спиценатяжителей, спиц и длина нитей зависели от размеров, формы и расположения раневого дефекта. Вытяжение лоскутов проводили путем растяжения пружин на необходимую длину с поддержанием заданной степени натяжения, контролируемой с помощью датчика. Вся система обеспечивала непрерывное и «мягкое»
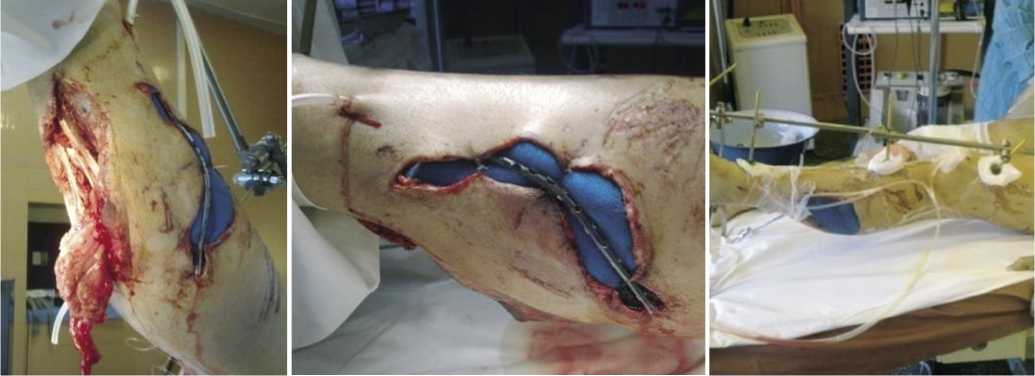
Рис. 1. Хирургическая обработка раны голени и наложение вакуумного дренирования

Пятаков С.Н., Завражнов А.А., Федосов С.Р., Шевченко А.В.
ПРИМЕНЕНИЕ ДОЗИРОВАННОЙ ДЕРМОТЕНЗИИ ДЛЯ ЗАКРЫТИЯ РАНЕВЫХ ДЕФЕКТОВ МЯГКИХ ТКАНЕЙ ГОЛЕНИ ГНОЙНО-НЕКРОТИЧЕСКОГО И ТРАВМАТИЧЕСКОГО ПРОИСХОЖДЕНИЯ

Рис. 2. Этапы выполнения методики дозированной дермотензии
растяжение кожно-подкожно-фасциального лоскута без перевязок раны, делая методику более комфортной для пациента, исключая многократное, в течение суток, подтягивание нитей «на глаз». Перевязки ран выполняли один раз в сутки, используя в зависимости от фазы раневого процесса мази на водорастворимой основе или специальные раневые покрытия. При необходимости, в ходе перевязок изменяли угол и направление тензии каждого кожно-подкожно-фасциального лоскута, достигая хорошей адаптации краев раны. После окончания тензиии на рану накладывали вторичные ранние швы (рис. 3).

Рис. 3. Наложение вторичных швов после окончания дермотензии
Результаты и обсуждение
При использовании методики дозированной дермотензии для закрытия раневых дефектов на голени решались следующие задачи:
-
1. Обеспечение контролируемой дермотензии в режиме постоянного времени в диапазоне величин 0,5–5,0 кг (5–50Н) с помощью калиброванного пружинного элемента и постоянного мониторинга за значениями;
-
2. Проведение постоянного и адекватного растяжения кожно-подкожно- фасциальных лоскутов без выполнения перевязок;
-
3. Использование методики как на ранах простой конфигурации (в виде эллипса или двух параллельных линий), так и на ранах неправильной формы;
-
4. Гашение колебательных движений (толчков и ударов, действующих на раму устройства) в различных участках раневой поверхности, что создает благоприятные условия для регенеративного процесса и устраняет «распиливающий» эффект нитей;
-
5. Обеспечение дермотензии, дозированной по силе натяжения кожно-подкожно-фасциального лоскута и регулирование угла его прилегания к раневой поверхности с целью достижение плотного соприкосновения стенок раны и создания наиболее благоприятных условий для перевязок;
-
6. Повышение уровня медико-социальной реабилитации за счет закрытия раны местными тканями (без применения других видов кожной пластики).
Особо следует отметить, что выполнение растяжения мягких тканей «на глаз» с помощью рутинного ручного натягивания нитей вызывает ишемизацию краев лоскутов и образование зон вторичного некроза, что создает условия для вторичного инфицирования и в конечном итоге приводит к еще большему дефициту пластического материала мягких тканей. В других случаях, тензия оказывается малоэффективной из-за быстрого провисания нитей.
Предложенная методика дермотензии решает эти задачи, сведя до минимума возможные недостатки. Постоянное вытяжение лоскута с контролем уровня допустимого натяжения в различных участках раневой поверхности позволяет максимально быстро закрыть тканевой дефект не вызывая нарушения кровоснабжения в вытягиваемых участках кожи, о чем свидетельствовали показатели транскутанного напряжения кислорода в капиллярной крови, измеренные в разных точках и в разные временные интервалы у наших больных (табл. 1).
Табл. 1. Показатель транскутанного напряжения кислорода (ТсРО2) в капиллярной крови вытягиваемых кожных лоскутов
|
Временной интервал |
Показатель ТсРО2 |
Достоверность различий |
|
До начала тензии |
67 ± 5 мм рт. ст. |
– |
|
Через 1 сутки |
54 ± 4 мм рт. ст. |
p ≥ 0,05 |
|
Через 3 суток |
60 ± 5 мм рт. ст |
p ≥ 0,05 |
|
Через 5 суток |
62 ± 3 мм рт. ст. |
p ≤ 0,05 |

Пятаков С.Н., Завражнов А.А., Федосов С.Р., Шевченко А.В.
ПРИМЕНЕНИЕ ДОЗИРОВАННОЙ ДЕРМОТЕНЗИИ ДЛЯ ЗАКРЫТИЯ РАНЕВЫХ ДЕФЕКТОВ МЯГКИХ ТКАНЕЙ ГОЛЕНИ ГНОЙНО-НЕКРОТИЧЕСКОГО И ТРАВМАТИЧЕСКОГО ПРОИСХОЖДЕНИЯ
Кожа в верхней трети голени являлась хорошим пластическим материалом для дермотензии по описанной методике (особенно при растяжении в поперечном направлении относительно оси конечности), что позволило полностью закрыть раневые дефекты площадью до 120 см2 в 74 (82%) случаях. При локализации дефекта кожи площадью более 80 см2 в нижней трети голени, дозированная дермотензия в 16 (18%) случаях дополнялась аутодермопластикой расщепленным кожным лоскутом.
Использование дермотензии при закрытии дефектов, образовавшихся после некротической формы рожистого воспаления (2 наблюдения), оказалось не эффективным в связи с высоким риском формирования зон вторичного некроза кожи, о чем свидетельствовали показатели ТсРО2 в капиллярной крови в местах предполагаемой тензии (менее 32 мм рт. ст.). В то же время раневые дефекты, возникшие после обширных, в том числе некротизирующих инфекций, после купирования инфекционного процесса в 88% случаев (у 14 из 16 пациентов) были закрыты местными тканями только с помощью дозированной дермотензии.
Наилучшие результаты дермотензии на голени были достигнуты при лечение ран травматического происхождения. Нам удалось только этой методикой устранить раневые дефекты у 52 (92%) больных. В 3 (6%) случаях пластика местными тканями была дополнена аутодермопластикой расщепленным кожным лоскутом.
Важным преимуществом непрерывного растяжения кожных лоскутов путем использования постоянных сил заданной величины явились более активная стимуляция ангиогенеза и увеличение эластических свойств кожи, что в конечном итоге приводило к увеличению площади и к ускорению закрытия раневого дефекта в сравнении с пластикой расщепленным кожным лоскутом. В группе 1 раны были закрыты за 25,1 ± 0,9 суток, в группе 2 – за 21,3 ± 1,1 суток (p < 0,05).
При анализе отдаленных результатов используемых видов закрытия раневых дефектов голени по Ванкуверской шкале состояния рубца (VPS) через 1 месяц после выписки из стационара всеми больными отмечены явные преимущества дозированной дерматензии по сравнению с пластикой расщепленным кожным лоскутом (р ≤ 0,01) – таблица 2. Немаловажно то, что площадь, занимаемая рубцом после дермотензии. была в 12–20 раз меньше, чем площадь функционально слабопригодной кожи при свободной аутодермопластике.
Таким образом, предложенная методика динамической дермотензии позволяет значительно ускорить пластическое закрытие ран, сократить сроки пребывания больных в стационаре, а также улучшить непосредственные косметический и функциональный результаты лечения, а также создать перспективы дальнейших пластических операций у больных с раневыми дефектами мягких тканей голени гнойно-некротического и травматического происхождения.
Табл. 2. Оценка состояния рубца через 1 месяц после выписки из стационара
|
Ванкуверская шкала оценки рубцов (VPS) |
Группа 1 |
Группа 2 |
|
Пигментация |
3 |
2 |
|
Высота рубца |
1 |
0 |
|
Пластичность |
0 |
3 |
|
Васкуляризация |
1 |
1 |
Список литературы Применение дозированной дермотензии для закрытия раневых дефектов мягких тканей голени гнойно-некротического и травматического происхождения
- Амирасланов Ю. А., Саркисов Д.С., Колокольникова Е.Г. и др. Пластика дефектов мягких тканей методом дозированного растяжения. Врач 1993; 2; 25-27.
- Амирасланов Ю.А., Митиш В.А., Борисов И.В. и др. Ранние реконструктивно-восстановительные операции при обширных травматических повреждениях голени, орсложненных гнойной инфекцией. Хирургия 1998;5: 36-39.
- Бобров М.И., Ежов Ю.И., Иванов А.М. Первичные и ранние кожно-пластические операции у травматолого-ортопедических больных с гнойной раневой инфекцией. Материалы научной конференции «Актуальные проблемы травматологии и ортопедии», проводимой в рамках международного форума «Человек и травма». Часть 7: Тез. докл. Нижний Новгород 2001; 136-138.
- Борткявичус Э.П., Рубикас Р.А. Устройство для сведения краев раны. Открытия. Изобретения 1989; 6: 20.
- Гостищев В.К., Липатов К.В., Комарова Е.А. и др. Дифференцированный подход к выбору кожно-пластических операций у больных с хирургической инфекцией. Хирургия 2009; 12: 19-24.
- Дамбаев Г.Ц., Монасевич Л.А., Кирш В.А. и др. Устройство для сближения краев раны. Открытия. Изобретения 1989; 5: 12.
- Ефименко Н.А., Рыбаков С.М., Грицюк А.А. и др. Пластическое замещение дефектов тканей конечностей (компьютерный анализ результатов лечения, моделирование и прогнозирование). Анналы пластической, реконструктивной и эстетической хирургии 2001; 3: 50-59.
- Зайцев А.Б. Реконструктивно-Восстановительное лечение больных с остеомиелитом голени. Автореф. Дисс. докт. мед. наук. Нижний Новгород; 2009; 23 с.
- Измайлов Г.А., Ахметзянов Ш.И., Измайлов С.Г. Устройство для сближения краев раны. Открытия. Изобретения 1983; 13: 27.
- Митиш В.А., Амиросланов Ю.Л. Пластические и реконструктивные операции в гнойной хирургии и травматологии. Хирургия 2000; 4: 41-44.
- Рамазанов Р.М. Экспериментально-клиническое обоснование способа лечения послеоперационных и рецидивных вентральных грыж с применением механического шва: Автореф. Дисс. Канд. мед. наук. Казань, 1983; 24 с.
- Соков Е.Л. Способ сближения краев раны. Хирургия 1988; 4: 130-131.
- Чертов Е.А., Жеребицкий А.В., Юсупов Ю.Н. Управляемое раскрытие ран аппаратом спицевой кожной фиксации как метод лечения анаэробной инфекции нижних конечностей. Вестн хир 1998; 2: 66-68.
- Abramson D.L., Gibstein L.A., Pribaz J.J. An inexpensive method of intraoperative skin stretching for closure of large cutaneous wounds. Ann Plast Surg 1997; 38: 540-542.
- Browne T. Closing a wide wound by using two stout spinal needles and three Allis forceps. Plast Reconstr Surg 1998; 101 (4): 1160-1161.
- Caruso D.M., King T.J., Tsujimura R.B., Weiland D.E., Schiller W.R. Primary closure of fasciotomy incisions with a skin-stretching device in patients with burn and trauma. J Burn Care Rehab 1997; 18 (2): 125-132.
- Harvey R.J., Litwak Ph., Ribich W.A., Dbowik J.M. Wound closing device. Патент США №4430998, МКИ А 61 В 17/08 1984.
- Hirshowitz B., Lindenbaum E., Har-shai Y. A skin-stretching device for the harnessing of viscoelastic properties of skin. Plast Reconstr Surg 1993; 92: 260-270.
- Narayanan K., Futrell J.W., Bentz M., Hurwitz D. Comparative clinical study of the sure-closure device with conventional wound closure techniques. Ann Plast Surg 1995; 35: 485-491.
- Sangwan S.S., Sharma V., Siwash R.C. Role of pin traction in wound closure. Orthopedics 1999; 22 (4): 419-422.


