Применение фибринового клея в лечении несостоятельности культи бронха после нижней лобэктомии справа (клиническое наблюдение)
Автор: Галлямов Э. А., Никулин А. В., Дидуев Г. И., Малофей А. М., Романихин А. И., Сурков А. И., Гвоздев А. А., Фетлам Д. Л.
Журнал: Хирургическая практика @spractice
Рубрика: Статьи
Статья в выпуске: 3 (51), 2022 года.
Бесплатный доступ
Несмотря на постоянно совершенствующуюся технику операций, применение современных шовных материалов и сшивающе-режущих аппаратов, проблема возникновения несостоятельности культи бронха остается нерешенной до сих пор. Для лечения несостоятельности культи бронха предложено множество способов, начиная от эндоскопической коагуляции слизистой и установки различного типа окклюдеров и заканчивая повторными хирургическими вмешательствами. Существует огромное количество публикаций, посвященных применению фибринового клея в различных областях медицины, например, в нейрохирургии, челюстно-лицевой хирургии, ортопедии, стоматологии и торакальной хирургии с успехом применяется фибриновый клей, в том числе и при развитии несостоятельности культи бронха. В данной статье приведено клиническое наблюдение применения фибринового клея в лечении несостоятельности культи бронха после нижней лобэктомии справа.
Фибриновый клей, несостоятельность культи бронха, бронхоплевральный свищ
Короткий адрес: https://sciup.org/142235705
IDR: 142235705 | УДК: 616.24-089.85 | DOI: 10.38181/2223-2427-2022-3-49-55
The use of fibrin glue in the treatment of bronchial stump failure after lower lobectomy on the right (a clinical case)
Despite the constantly improving technique of operations, the use of modern suture materials and stitching-cutting devices, the problem of the occurrence of the failure of the bronchial stump remains unresolved. Many methods have been proposed for the treatment of bronchial stump failure, ranging from endoscopic mucosal coagulation and the installation of various types of occluders and ending with repeated surgical interventions. There are a huge number of publications devoted to the use of fibrin glue in various fields of medicine, for example, in neurosurgery, maxillofacial surgery, orthopedics, dentistry and thoracic surgery, fibrin glue is successfully used, including in the development of bronchial stump failure. This article presents a clinical observation of the use of fibrin glue in the treatment of bronchial stump failure after lower lobectomy on the right.
Текст научной статьи Применение фибринового клея в лечении несостоятельности культи бронха после нижней лобэктомии справа (клиническое наблюдение)
Несостоятельность культи бронха с развитием бронхоплеврального свища (БПФ) является грозным осложнением «большой» торакальной хирургии. Несмотря на постоянно совершенствующуюся технику операций, применение современных шовных материалов и сшивающе-режущих аппаратов, проблема возникновения несостоятельности культи бронха остается нерешенной. По данным разных авторов частота развития бронхоплеврального свища после лобэктомии составляет от 0,3 до 3,8%, после пневмонэктомии от 4,5 до 40%. Летальность при развитии бронхоплеврального свища после пневмонэктомии пугающе высока от 18 до 71%, однако в случае развития бронхоплеврального свища после лобэктомии ситуация не так катастрофична [1, 2, 3, 4, 5–7].
Для лечения несостоятельности культи бронха предложено множество способов, начиная от эндоскопической коагуляции слизистой и установки различного типа окклюдеров и заканчивая повторными хирургическими вмешательствами. Заживление дефекта культи долевого бронха наблюдается в 26- 44%. Определяющее значение в прогнозе заживления имеет размер дефекта [5].
Считается, что при небольшом размере дефекта культи до 2мм эндоскопические методы с высокой долей вероятности обеспечивают закрытие дефекта, тем самым позволяя избежать повторной операции.[8]
В последние десятилетия в различных областях медицины, например в нейрохирургии, челюстно-лицевой хирургии,ортопедии,стоматологии и торакальной хирургии с успехом применяется фибриновый клей, в том числе и при развитии несостоятельности культи бронха[8]. Существует огромное количество публикаций, посвященных применению фибринового клея в лечении стриктур уретры,кишечных свищей,альвео-лярной недостаточности и т. д. Авторы показывают что с помощью фибринового клея можно не только ускорить сроки заживления , но и уменьшить количество гнойновоспалительных осложнений [9-11] В отечественной клинической практике использование аутологичного фибринового клея системы VivostatTM является ограниченным. Так, отдельные авторы сообщают об эффективности применения данной системы в колоректальной хирургии с целью профилактики несостоятельности колоректального анастомоза [12].
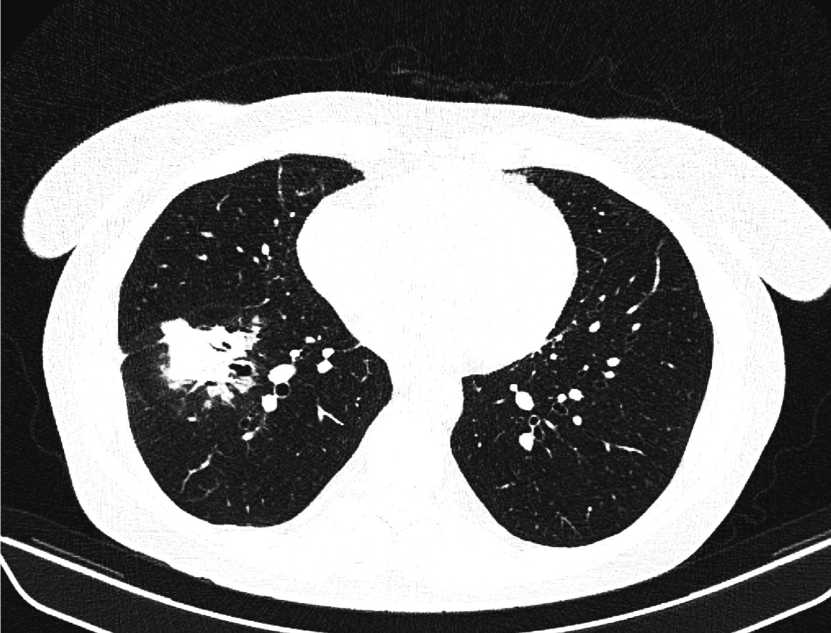
Рис. 1. КТ ОГК до операции (в нижней доле правого легкого определяется опухолевое образование) Fig. 1. CT of the chest before surgery (a tumor formation is determined in the lower lobe of the right lung)
Например, Hideki Kawai et al. сообщают о снижении частоты развития альвеолярной недостаточности после резекций легких без использования сшивающего аппарата (использовался гармонический скальпель) с 44 до 4,3%[13]. Другие японские авторы говорят об использовании ФК не только для профилактики альвеолярной недостаточности,но и для уменьшения объема кровопотери и лимфореи во время операций [14-16]
В основе действия ФК лежит способность потенцировать собственный репаративный потенциал организма за счет кратковременного всплеска провоспалительной активности и последующим нарастанием противовоспалительных и иммунорегуляторных цитокинов. Таким образом фибриновый клей представляет собой не только системный иммуномодулятор, содержащий в себе пластический материал, но и местный стимулятор репарации тканей [11].
Помимо этого фибриновый клей обладает рядом преимуществ перед клеями на основе цианокрилата за счет отличной биосовместимости и разлагаемости [17].
Клиническое наблюдение
Больная Я, 58 лет поступила в торакальное отделение ГКБ им И.В. Давыдовского с диагнозом подозрение на периферический рак с централизацией нижней доли правого легкого (рис. 1).
При обследовании данных за отдаленные метастазы выявлено не было, после предоперационной подготовки больной выполнена ВАТС нижняя лобэктомия справа с медиастинальной лимфодиссекцией. Гистологическое заключение: ацинарная аденокарцинома, рT2аN0M0 IB ст (TNM8). Ранний послеоперационный период протекал без осложнений, на четвертый день дренаж из правой плевральной полости удален. Больная выписана. Через 28 дней после операции больная обратилась к врачу с жалобами на чувство нехватки воздуха. При контрольной рентгенографии выявлен правосторонний пневмогидроторакс. Больная повторно госпитализирована. В этот же день выполнено дренирование правой плевральной полости. При этом отмечался сброс воздуха при небольшом покашливании. При контрольной бронхоскопии выявлена несостоятельность культи правого нижнедолевого бронха диаметром 3 мм (рис. 2).
Через 6 дней с момента поступления, 34 дня с момента операции после консервативной терапии произведена аппликация аутологичного фибринового клея. В качестве которого была использована собственная
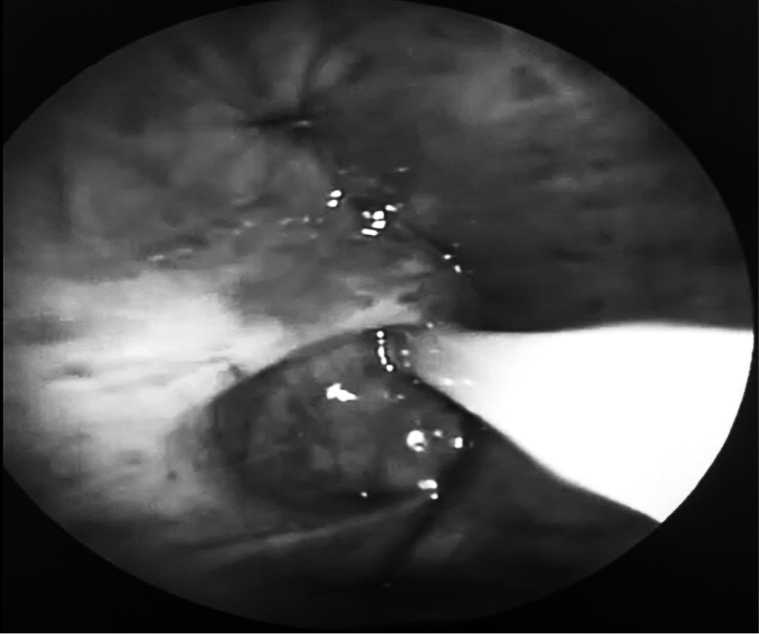
Рис. 2. Несостоятельность культи правого нижнедолевого бронха (в дефект введен катетер 3 мм) Fig. 2. Failure of the stump of the right lower lobe bronchus (a 3 mm catheter was inserted into the defect)
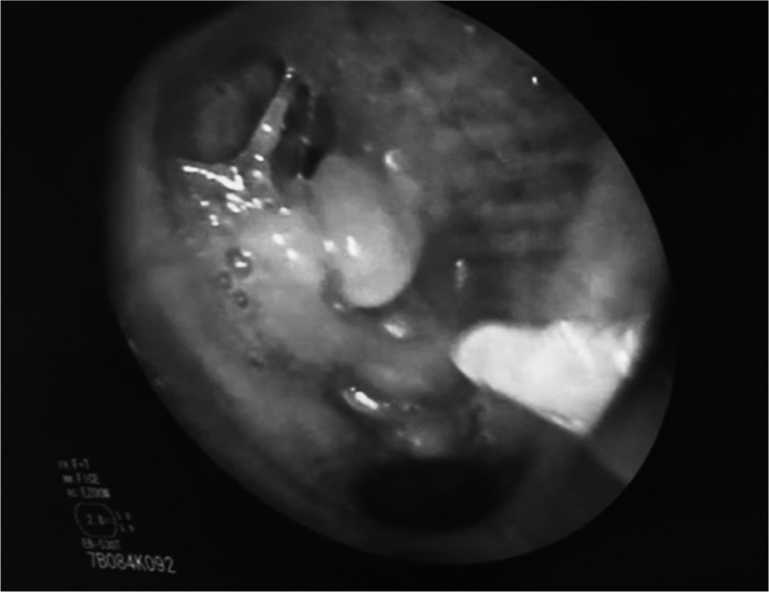
Рис. 3. Аппликация фибринового клея Fig. 3. Fibrin glue application
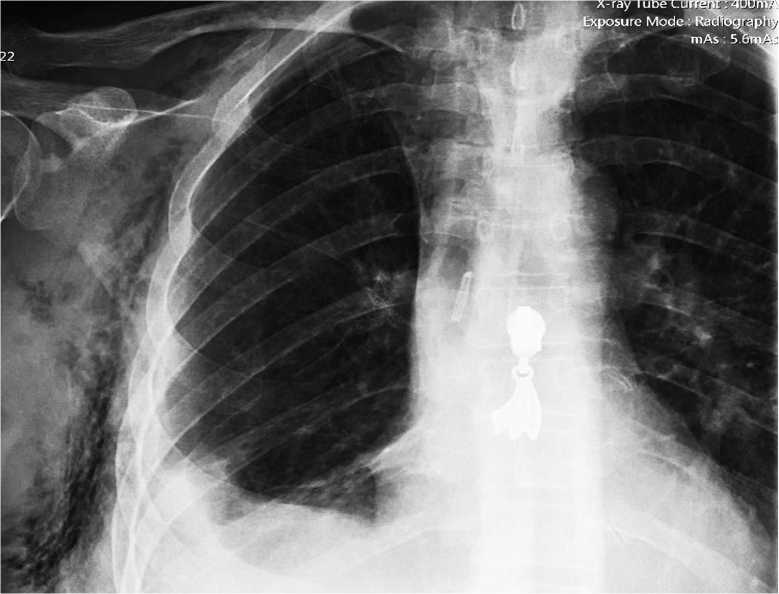
Рис. 4. Контрольная рентгенография перед выпиской Fig. 4. Control radiography before discharge плазма крови, сепарированная ex tempore на комплексе для приготовления фибринового клея и обогащенного тромбоцитами фибрина «Vivostat System». Из 120 мл собственной крови пациента после полного цикла работы комплекса получается от 5,5 до 6,5 мл готового фибринового клея. Полученный вариант криопреципитата был введен по тонкому зонду через канал бронхоскопа, дополнительно обтуратор не использовался (рис. 3).
Сразу же после аппликации прекратился сброс воздуха по дренажу. Дренаж удален на 3 сутки после аппликации фибринового клея после контрольной ренгтено-графии. Больная была выписана (рис. 4).
Контрольная бронхоскопия была выполнена через 2 недели после аппликации. Культя нижнедолевого бронха состоятельна (рис. 5).
Заключение
Возможности применения фибринового аутоклея на основе собственной плазмы больного требуют дальнейшего изучения, вместе с тем данные литературы свидетельствуют об успешном применении фибринового клея в различных областях медицины. Использование фибринового клея на основе собственной плазмы позволяет добавить ко всем достоинствам адгезива безусловные преимущества аутологичного препарата. В торакальной хирургии использование фибринового клея позволяет не только добиться лучшего гемостаза во время операции и уменьшить риск возникновения альвеолярной недостаточности в раннем послеоперационном периоде, но и может с успехом применяться в лечении такого грозного осложнения, как несостоятельность культи бронха после лобэктомии.
Список литературы Применение фибринового клея в лечении несостоятельности культи бронха после нижней лобэктомии справа (клиническое наблюдение)
- Caushi F, Qirjako G, Skenduli I, Xhemalaj D, Hafizi H, Bala S, Hatibi A, Mezini A. Is the flap reinforcement of the bronchial stump really necessary to prevent bronchial fistula? J Cardiothorac Surg. 2020 Sep 11;15(1):248. https://doi.org/10.1186/s13019-020-01290-0
- Fishman TJ, Salabei JK, Zadeh CM, Malhi MS, Asnake ZT, Bazikian Y. An atypical complicated left-sided bronchopleural fistula presenting more than seven months after lobectomy. Respir Med Case Rep. 2020 Apr 19;30:101056. https://doi.org/10.1016/j.rmcr.2020.101056
- Iwasaki M, Shimomura M, Ii T. Negative-pressure wound therapy in combination with bronchial occlusion to treat bronchopleural fistula: a case report. Surg Case Rep. 2021 Mar 2;7(1):61. https://doi.org/10.1186/s40792-021-01144-4
- Nachira D, Chiappetta M, Fuso L, Varone F, Leli I, Congedo MT, Margaritora S, Granone P. Analysis of risk factors in the development of bronchopleural fistula after major anatomic lung resection: experience of a single centre. ANZ J Surg. 2018 Apr;88(4):322-326. https://doi.org/10.1111/ans.13886
- Ualikhanov A, Batyrbekov K. Endoscopic closure of the fistula stump of the bronchus after pulmonectomy. Respir Med Case Rep. 2020 Oct 12;31:101249. https://doi.org/10.1016/j.rmcr.2020.101249
- Ucvet A, Gursoy S, Sirzai S, Erbaycu AE, Ozturk AA, Ceylan KC, Kaya SO. Bronchial closure methods and risks for bronchopleural fistula in pulmonary resections: how a surgeon may choose the optimum method? Interact Cardiovasc Thorac Surg. 2011 Apr;12(4):558-62. https://doi.org/10.1510/icvts.2010.251157
- Wang YQ, Zhuang W. Treat bronchopleural fistula after right lower lobectomy by extra right middle lobectomy-a neglected approach. Interact Cardiovasc Thorac Surg. 2020 Jul 1;31(1):63-70. https://doi.org/10.1093/icvts/ivaa050
- Imai K, Matsuzaki I, Minamiya Y, Saito H, Yoshida S, Hirayama K, Sawano T, Ogawa J. Postoperative bronchial stump fistula after lobectomy: response to occlusion with polyglycolic acid mesh and fibrin glue via bronchoscopy. Gen Thorac Cardiovasc Surg. 2011 Nov;59(11):771-4. https://doi.org/10.1007/s11748-010-0767-8
- Пушкарь Д.Ю., Живов А.В., Исмаилов М.Р., Багаудинов М.Р. Результаты использования фибринового клея при оперативном лечении стриктур уретры. Андрология и генитальная хирургия. 2013;14(1):49-53. https://doi.org/10.17650/2070-9781-2013-1-49-53
- Набиева Э.Р., Якупова Е.Р. Фибриновый клей как перспективный метод лечения при протезирующей герниопластике. Устойчивое развитие науки и образования. 2019. №. 3. С. 279-284
- Черноусов А.Ф., Хоробрых Т.В., Ищенко О.В., Васнев О.С. Применение фибринового клея как стимулятора репарации при лечении больных с несформированными кишечными свищами. Вестник хирургической гастроэнтерологии. 2009. № 3, С 21-28.
- Агапов М.А., Маркарьян Д.Р., Гарманова Т.Н., Казаченко Е.А., Цимайло И.В., Какоткин В.В. Применение системы vivostat® как метода профилактики несостоятельности анастомоза после низкой передней резекции прямой кишки. Клинический случай. Хирургическая практика. 2022;(2):84-92. https://doi.org/10.38181/2223-2427-2022-2-84-92.
- Kawai H. Fibrin Glue-Minocycline Combination as a Sustained Release for the Prevention of Postoperative Alveolar Air Leak in Thoracoscopic Lung Resections. Thorac Cardiovasc Surg. 2017 Aug;65(5):392-394. https://doi.org/10.1055/s-0037-1598622
- Kawai N, Kawaguchi T, Suzuki S, Yasukawa M, Tojo T, Taniguchi S. Low-voltage coagulation, polyglycolic acid sheets, and fibrin glue to control air leaks in lung surgery. Gen Thorac Cardiovasc Surg. 2017 Dec;65(12):705-709. https://doi.org/10.1007/s11748-017-0829-2
- Kawamoto N, Okita R, Hayashi M, Okada M, Ito K, Ikeda E, Inokawa H. Suspected fibrin glue-induced acute eosinophilic pneumonia after pulmonary resection: A case report. Thorac Cancer. 2021 Jul;12(14):2126-2129. https://doi.org/10.1111/1759-7714.14040
- Kawashima M, Kohno T, Fujimori S, Kimura N, Suzuki S, Yoshimura R, Yuhara S, Kohno A, Wakatabe M, Makino S. Feasibility of autologous fibrin glue in general thoracic surgery. J Thorac Dis. 2020 Mar;12(3):484-492. https://doi.org/10.21037/jtd.2020.01.01
- Petter-Puchner AH, Simunek M, Redl H, Puchner KU, Van Griensven M. A comparison of a cyanoacrylate [corrected] glue (Glubran) vs. fibrin sealant (Tisseel) in experimental models of partial pulmonary resection and lung incision [corrected] in rabbits. J Invest Surg. 2010 Feb;23(1):40-7. https://doi.org/10.3109/08941930903469383


