Применение инновационного отечественного контрастного средства на основе гадолиния для МР-диагностики злокачественных новообразований в эксперименте
Автор: Чернов Владимир Иванович, Тицкая Анна Александровна, Синилкин Иван Геннадьевич, Зельчан Роман Владимирович, Григорьев Евгений Геннадьевич, Фролова Ирина Григорьевна, Нам И.Ф.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 4 (70), 2015 года.
Бесплатный доступ
В представленном исследовании продемонстрирована функциональная пригодность и специфическая активность отечественного инновационного контрастного средства на основе гадолиния для магнитно-резонансной томографии в эксперименте. В ходе эксперимента было показано, что исследуемое контрастное средство активно накапливается в органах и тканях лабораторных животных. На моделях опухолевого поражения у лабораторных животных было продемонстрировано активное накопление контрастного средства на основе гадолиния в опухолевом узле и длительное сохранение препарата в нем.
Мрт, онкология, инновационное контрастное средство на основе гадолиния
Короткий адрес: https://sciup.org/14056777
IDR: 14056777 | УДК: 616-006.04-073.75:
The use of innovative domestic contrast agent gadolinium-based for MR-cancer diagnosis in experiment
The present study of the functional suitability and specific activity of the contrast agent gadolinium-based for magnetic resonance imaging demonstrated that the investigated contrast agent intensively accumulates in organs and anatomical structures of the experimental animals. In the model of tumor lesions in animals, study have shown that investigational contrast agent accumulates in the tumor tissue and retained there in for a long enough time.
Текст научной статьи Применение инновационного отечественного контрастного средства на основе гадолиния для МР-диагностики злокачественных новообразований в эксперименте
Современные технологии магнитно-резонансной томографии (МРТ) неразрывно связаны с использованием магнитно-резонансных контрастнодиагностических средств (МРКС), которые не только многократно увеличивают чувствительность и специфичность диагностики, но и являются неотъемлемой частью самой диагностической процедуры. В европейских странах контрасты при МРТ используются в 70–80 % случаев, в России этот показатель составляет 9 %, что прежде всего связано с экономическими причинами и отсутствием отечественных контрастных средств. Исследование опухолей без введения МРКС обладает низкой информативностью. Так, по данным ВОЗ, при проведении МРТ без контраста частота ошибочных диагнозов может достигать 40 %. Наиболее часто используемым в практике МРТ парамагнитным металлом является ион гадолиния (Gd+3), который имеет семь неспаренных электронов [1–6]. Решение проблемы создания отечественного контрастного лекарственного средства на основе гадолиния для магнитно-резонансной диагностики позволит обеспечить отечественное здравоохранение эффективным более дешевым импортозамещающим препаратом.
В связи с изложенным целью исследования явилась экспериментальная оценка возможности использования для магнитно-резонансной диагностики злокачественных новообразований отече- ственного контрастного средства «Пентагаскан» на основе комплекса гадолиния.
Материалы и методы
Исследуемое контрастное средство на основе гадолиния («Пентагаскан» ООО «МедКон-трастСинтез»). Препарат представляет собой гадолиний динатриевую соль диэтилентриамин-N,N,N´,N´´,N´´, - пентауксусной кислоты в виде раствора для инфузий (табл. 1).
Первый этап исследования заключался в сравнительной оценке функциональной пригодности нового МР-контраста («Пентагаскан») у 30 интактных белых крыс-самцов линии «Вистар» массой 300–350 г. Препаратом сравнения являлся «Магневист», в эту группу включено 30 интактных белых крыс-самцов линии «Вистар» аналогичной массы. Вначале МР-томография проводилась всем животным в нативном режиме, без введения парамагнетиков. Затем животные были распределены на две группы в зависимости от используемого контрастного средства.
Затем была проведена оценка эффективности применения «Пентагаскана» на животных с экспериментальной опухолью. В качестве биологической модели опухоли использовались перевиваемые злокачественные новообразования мышей – карциномы легких Льюис, использовался солидный вариант карциномы Льюис (Банк клеточных линий РОНЦ
Таблица 1
Сведения об исследуемом препарате
Всех животных содержали на стандартном рационе вивария со свободным доступом к воде, в соответствии с Правилами Европейской конвенции по защите позвоночных животных, используемых для экспериментальных и иных научных целей.
Исследование интактных крыс выполнялось спустя 5 мин после введения контрастного средства в бедренную вену в дозе 0,2 мл. Аналогичные исследования мышей с перевитой опухолью проводилось через 1, 5 и 9 мин после инъекции контраста «Пентагаскан» в объеме 0,1 мл через инфраорбитальный синус.
В целях обеспечения полной неподвижности на протяжении всего исследования экспериментальные животные наркотизировались путем внутримышечной инфузии 5 % раствора кетамина. При выполнении исследования объективно каких-либо побочных эффектов не было выявлено, и выход из наркоза был с полным восстановлением активности животного.
Животных располагали на поддоне в естественном положении. Центр поддона с крысой помещался в изоцентр тоннеля магнита, исполь- зовалась головная 16-канальная высокочастотная катушка Head Matrix. Оценку контрастирующего эффекта препарата осуществляли визуально и полуколичественно. Изображения были получены при следующих параметрах сканирования: Т1-SE последовательность – TR=550 мс, TE=17 мс, FоV – 181×270 мм, матрица – 292×512, толщина среза – 5 мм, шаг – 1,5 мм; последовательность с жироподавлением T1-TSE fatsat – TR=677 мс, TE=11 мс, FOV – 135×270 мм, матрица – 512×192, толщина среза – 3 мм, шаг – 0,3 мм.
Статистическую обработку полученных данных проводили с использованием прикладного программного пакета IBM SPSS statistics 20.0. Проводился описательный и сравнительный анализ. Проверку на нормальность распределения количественных признаков проводили с помощью W-теста Шапиро – Уилка. Описательный анализ включал определение среднего арифметического значения (X), ошибки среднего значения (m), а также расчет квартилей (Me, Q1-Q3) для не нормально и не симметрично распределенных параметров. Сравнительный анализ основывался на определении достоверности разницы показателей по t-критерию Стьюдента для нормально распределенных и по Z-критерию Манна – Уитни для не нормально распределенных параметров, для сравнения зависимых данных использовался критерий Уилкоксона.
Результаты исследования и обсуждение
При визуальной оценке изображений как в группе животных с введением исследуемого лекарственного средства («Пентагаскан»), так и в группе сравнения («Магневист») отмечалось усиление МР-сигнала на постконтрастных сканах в режиме Т1-взвешанного изображения. Определялось накопление контрастов в кортикальном слое почечной паренхимы и видимых сосудах объекта. На отсроченных сканах визуализировалось гомогенное накопление контраста в почках,
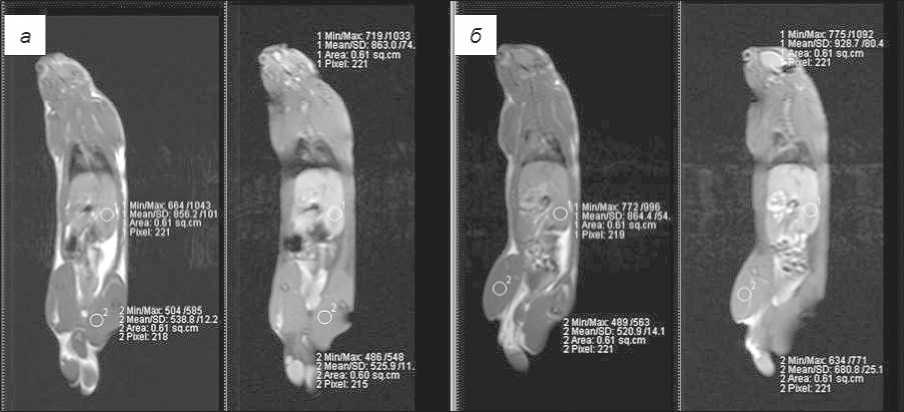
Рис. 1. Распределение исследуемого лекарственного средства («Пентагаскан») в организме интактных животных. После введения контраста в режимах T1-SE (а) и T1-TSEfatsat (б) отмечается его накопление в паренхиме почек, печени, мочевом пузыре
печени, селезенке. Определялось накопление парамагнетиков в мочевом пузыре в виде усиления МР-сигнала (рис. 1, 2).
Показатели интенсивности МР-сигнала измерялись встроенным в программное обеспечение модулем, с помощью выделения ROI (зоны интереса) в виде круга одинаковой площади, охватывающего корковое и мозговое вещество почки. Учитывая толщину среза, в зоне интереса находился объем, равный 0,60–0,61 см2.
В качестве референсной зоны использовалась мышечная ткань грызуна (область бедренного мышечного массива). Также была измерена интенсивность накопившейся контрастированной мочи. Полученные показатели интенсивности МР-сигнала в соответствующих участках тела представлены в табл. 2. Полученные результаты исследования специфической активности исследуемого лекарственного средства («Пентагаскан»)
у интактных животных свидетельствуют о том, что контрастирующая способность этого препарата практически не отличается от средства сравнения («Магневист»). Отсутствие достоверных различий контрастирующих способностей экспериментального лекарственного средства («Пентагаскан») и контрольных образцов («Магневист») подтверждается не только визуально, но и расчетом показателей интенсивности МР-сигнала в различных режимах сканирования.
С целью определения оптимальных временных промежутков для проведения исследования после внутривенного контрастного усиления с использованием лекарственного средства на основе гадолиния («Пентагаскан») была выполнена серия экспериментов. При этом визуально оценивались интенсивность и характер накопления контрастного средства в опухолевой ткани в различные временные промежутки: через 1, 5 и
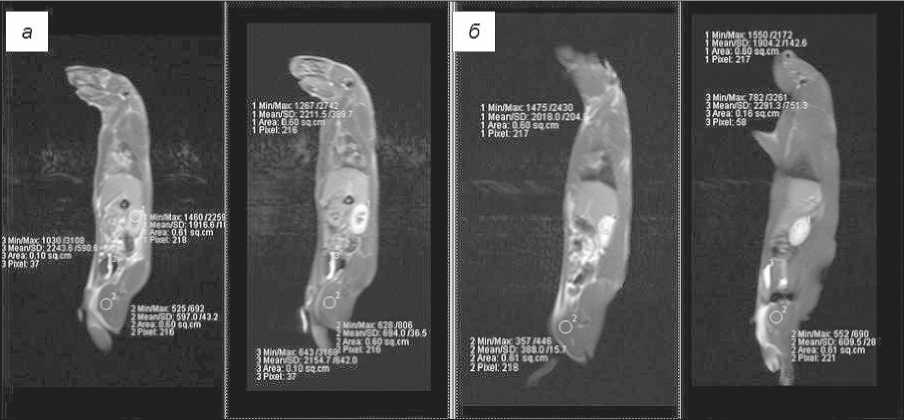
Рис. 2. Распределение средства сравнения («Магневист») в организме интактных животных. После введения контраста в режимах T1-SE (а) и T1-TSEfatsat (б) отмечается его накопление в паренхиме почек, печени, мочевом пузыре
Таблица 2
Интенсивность МР-сигнала
|
Режим исследования |
Значение измеренной интенсивности в выделенных зонах интереса (значение/станд.отклон.) |
||||
|
До введения |
После введения контраста |
Контрастированная моча в мочевом пузыре |
|||
|
почка |
мышца |
почка |
мышца |
||
|
Пентагаскан Т1-SE |
825,7/14,8 |
530,3/5,1 |
1902,3/28,7 |
565,8/10,3 |
2192,9/9,5 |
|
Магневист Т1-SE |
864,4/54 |
520,9/14 |
2018,0/204 |
388,0/15 |
2142,0/446 |
|
Пентагаскан T1-TSE fatsat |
879,8/40,1 |
580,6/83,1 |
2111,1/181 |
665,5/54,3 |
2188,2/34,4 |
|
Магневист T1-TSE fatsat |
928,7/80 |
680,8/25 |
1904,2/143 |
609,5/28 |
2291,3/751 |
Таблица 3
Показатели интенсивности МР-сигнала у экспериментальных животных в нативную фазу исследования и после контрастного усиления
|
Средние значения измеренной интенсивности в выделенных зонах интереса (значение/станд.отклон.) |
|||
|
Почка |
Опухоль |
||
|
Нативная фаза |
Контрастное усиление |
Нативная фаза |
Контрастное усиление |
|
931,0/23,2 |
1929,0/16,9 |
561,9/11,2 |
1039,7/8,9 |
9 мин после внутривенного введения контраста. Временные промежутки выбраны с учетом интенсивности обменных процессов экспериментальных животных.
После обработки полученных данных было отмечено, что в раннюю фазу исследования экспериментальное лекарственное средство («Пен-тагаскан») интенсивно накапливается в паренхиме почек. При этом накопление парамагнетика в опухолевой ткани наблюдается уже в раннюю фазу сканирования и сохраняется в ней долгое время. Интенсивность накопления препарата в опухоли оставалась на одном уровне в разные фазы исследования (рис. 3).
Для подтверждения факта контрастного усиления при использовании лекарственного средства («Пентагаскан») были рассчитаны количественные параметры МР-сигнала в нативную фазу исследования и после внутривенного введения контраста. Для этого измеряли уровень МР-сигнала в области опухолевого узла и в проекции почки до и после внутривенного контрастирования. Средние значения показателей интенсивности МР-сигнала в области опухолевого узла и в проекции почки представлены в табл. 3.
Заключение
Выполненные эксперименты по изучению специфической активности лекарственного средства на основе гадолиния у экспериментальных животных со злокачественными новообразованиями позволяют сделать следующие выводы:
– готовая лекарственная форма контрастного лекарственного средства на основе гадолиния («Пентагаскан») для магнитно-резонансной томографии интенсивно накапливается в органах, элиминирующих препарат, а также в опухолевой ткани, имеющей высокие показатели метаболизма, что достоверно фиксируется при любой стандартной Т1-взвешенной последовательности;
– исследуемое контрастное средство на основе гадолиния («Пентагаскан») интенсивно накапливается и сохраняется на протяжении долгого времени в патологической опухолевой ткани, что позволяет
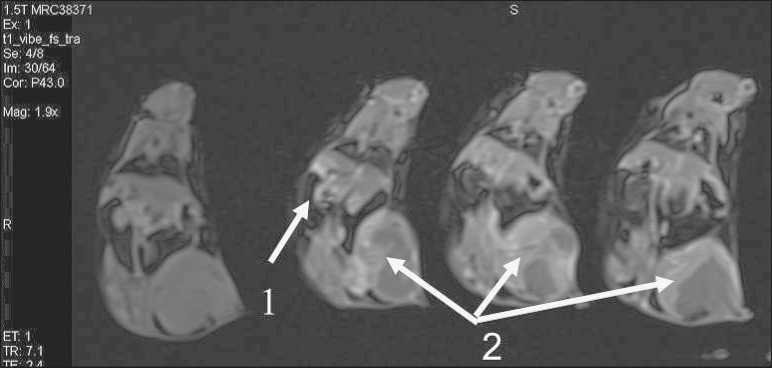
Рис. 3. МР-томограммы животных в режиме Т1-VIBE FS (слева – направо): мышь без применения контрастного усиления; через 1; 5 и 9 мин после введения контраста. Отмечено более интенсивное накопление парамагнетика паренхимой почек в раннюю фазу сканирования (1). Неоднородное (за счет признаков некроза в центральных отделах опухоли) накопление контраста опухолью (2)
проводить исследование с большим количеством импульсных последовательностей и плоскостей сканирования;
– готовая лекарственная форма контрастного лекарственного средства для магнитно-резонансной томографии («Пентагаскан») интенсивно накапливается в структуре опухоли экспериментальных животных. Прирост значений интенсивности МР-сигнала по отношению к нативной фазе сканирования составляет до 184 %. Это, в свою очередь,
Список литературы Применение инновационного отечественного контрастного средства на основе гадолиния для МР-диагностики злокачественных новообразований в эксперименте
- Brasch R.C., Weinmann H-J., Wesbey G.E. Contrast-Enhanced NMR Imaging: Animal Studies Using Gadolinium-DTPA complex//AJR. 1984. Vol. 142 (3). P. 625-630.
- Carr D.H., Brown J., Bydder G.M., Weinmann H.J., Speck U., Thomas D.J., Young I.R. Intravenous chelated gadolinium as a contrast agent in NMR imaging of cerebral tumours//Lancet. 1984. Vol. 1 (8375). P. 484-486.
- Laniado M., Weinmann H.J., Schörner W., Felix R., Speck U. First use of GdDTPA/dimeglumine in man//Physiol. Chem. Phys. Med. NMR. 1984. Vol. 16 (2). Р.157-165.
- Weinmann H.J., Brasch R.C., Press W.R., Wesbey G.E. Characteristics of gadolinium-DTPA complex: a potential NMR contrast agent//AJR. 1984. Vol. 142 (3). P. 619-624.
- Weinmann H.J., Ebert W., Misselwitz B., Schmitt-Willich H. Tissuespecific MR contrast agents//Eur. J. Radiol. 2003. Vol. 46 (1). P. 33-44.
- Weinmann H.J., Laniado M., Mützel W. Pharmacokinetics of Gd-DTPA/dimeglumine after intravenous injection into healthy volunteers//Physiol. Chem. Phys. Med. NMR. 1984. Vol. 16 (2). P. 167-172.


