Применение интраоперационного фильтрационного плазмафереза в условиях искусственного кровообращения у пациентов с инфекционным эндокардитом
Автор: Музычин А.Л., Хавандеев М.Л., Мошкин С.В., Залюбовская Л.В., Гительзон Е.А., Файбушевич А.Г.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.19, 2024 года.
Бесплатный доступ
Обоснование: Применение различных эфферентных методов зарекомендовало себя с положительной стороны в комплексе лечения пациентов с кардиохирургической патологией. В работе представлен способ проведения фильтрационного плазмафереза в процессе оперативного вмешательства в условиях искусственного кровообращения (ИК) у пациентов с инфекционным эндокардитом (ИЭ).Цель: Оценить эффективность разработанного метода интраоперационного плазмафереза в условиях ИК у пациентов с ИЭ.Материалы и методы: В материалах исследования описывается способ интеграции плазмофильтра непосредственно в контур аппарата ИК без применения дополнительного оборудования для проведения плазмафереза. Исследование настоящего метода проводилось на базе отделения кардио - и рентгенэндоваскулярной хирургии ГБУ ДНР «РКБ имени М.И. Калинина», г. Донецк в период с 2014 по 2024 гг. В исследовании приняли участие 96 пациентов, которые были разделены на две группы (52 и 44 пациента соответственно). В Группе I выполнялась процедура интраоперационного плазмафереза. В Группе II процедура плазмафереза не выполнялась. Пациентам выполнены следующие оперативные вмешательства: протезирование аортального клапана (ПАК) - 28 (29,17%), протезирование митрального клапана (ПМК) - 30 (31,25%), протезирование трикуспидального клапана (ПТК) - 33 (34,38%), протезирование аортального и митрального клапанов - 5 (5,2%).
Инфекционный эндокардит, плазмаферез, искусственное кровообращение
Короткий адрес: https://sciup.org/140307879
IDR: 140307879 | DOI: 10.25881/20728255_2024_19_3_38
Intraoperative filtration plasmapheresis during cardiopulmonary bypass in patients with infective endocarditis
Rationale: The use of various efferent methods has proven positive in the complex treatment of patients with cardiac surgical pathology. The article presents a method for performing filtration plasmapheresis during during cardiopulmonary bypass surgery in patients with infective endocarditis.Objective: To evaluate the effectiveness of the developed method of intraoperative plasmapheresis during cardiopulmonary bypass in patients with infective endocarditis.Methods: The study materials describe a method for integrating a plasma filter directly into the circuit of a heart - lung machine without the use of additional equipment for plasmapheresis. The study of this method was carried out on the basis of the Department of Cardio - and X - ray Vascular Surgery of the State Budgetary Institution of the DPR “Republic Clinical Hospital named after M.I. Kalinin”, Donetsk in the period from 2014 to 2024. The study involved 96 patients who were divided into two groups (52 and 44 patients, respectively). In Group I, the procedure of intraoperative plasmapheresis was performed. In Group II, the plasmapheresis procedure was not performed. Patients underwent the following surgical interventions: aortic valve replacement (AVR) - 28 (29.17%), mitral valve replacement (MVR) - 30 (31.25%), tricuspid valve replacement (TVR) - 33 (34.38%), replacement of aortic and mitral valves - 5 (5.2%).Conclusion: Intraoperative plasmapheresis helps improve exit from cardiopulmonary bypass by independently restoring the rhythm without the use of defibrillation and reducing the need for the use of adrenergic agonists to normalize blood pressure.The use of the method demonstrates an improvement in the course of the postoperative period, manifested in a decrease in cardiotonic support, early normalization of body temperature and laboratory parameters, namely: the absolute number of leukocytes, relative to the content of band and segmented leukocytes, erythrocyte sedimentation rate, C - reactive protein and leukocyte intoxication index
Текст научной статьи Применение интраоперационного фильтрационного плазмафереза в условиях искусственного кровообращения у пациентов с инфекционным эндокардитом
Плазмаферез (ПА) является эстракорпоральным методом терапии и представляет из себя процесс удаления части плазмы крови пациента гравитационным или фильтрационным способом. Официальное использование термина ПА впервые было предложено американским врачом J.J. Abel в 1914 г. [1]. С тех пор данный эфферентный метод вошел в медицинскую практику, и в том или ином виде применяется по сегодняшний день. Несомненно, как сама методика, так и принципы ее проведения за всю более чем столетнюю историю претерпели немало изменений [2]. Это позволило опытным путем выработать общие современные подходы как к проведению самой процедуры, так и к выбору оборудования и расходных материалов для проведения ПА, которые широко представлены производителями всего мира. Тем не менее модификации данного метода находят свою актуальность и в современных условиях. Поиск способов улучшения и адаптации классических подходов к проведению ПА позволяет расширить традиционные границы применения данного метода.
Актуальность
ПА успешно применяется в стационарных и амбулаторных условиях, является частью комплексного лечения многих заболеваний и синдромов [2–4]. Экстракорпоральная гемокоррекция в кардиологической и кардиохирургической практике применяется часто, и позволяет снизить риски послеоперационных септических осложнений, системного воспалительного ответа, полиорганной недостаточности. ПА применяется при ИБС, лечении аритмий и синдрома дилатационной кардиомиопатии [5–9]. Применение экстракорпоральной терапии вызывает доказанное замедление прогрессирования атеросклероза, снижает риск развития рестенозов в послеоперационном периоде реваскуляризации миокарда, что связывают с уменьшением уровня липопротеидов. У пациентов с кардиальной патологией после курса ПА в комплексе основного лечения отмечается снижение титров антикардиальных антител и значимый прирост фракции выброса [10–12].
При анализе опыта применения ПА в современной практике амбулаторий и стационаров установлено, что проведение данной процедуры требует наличия специализированного оборудования и подготовки специалиста [13; 14]. Аппарат для ПА, одноразовые расходные материалы в виде плазмофильтра и комплекта магистралей, катетеры, инфузионные растворы и антикоагулянт – необходимый минимум для проведения ПА.
В отделениях кардиохирургии ПА проводится часто, однако подобные процедуры выполняются либо в дооперационном, либо послеоперационном периоде. В свою очередь, использование таких методов гемоконцентрации и гемокоррекции как ультрафильтрация (УФ) и модифицированная ультрафильтрация (МУФ) в отделениях кардиохирургии, выполняющих оперативные вмешательства в условиях ИК, является рутинной интраоперационной практикой.
Цель
Оценить эффективность разработанного метода интраоперационного ПА в условиях ИК у пациентов с ИЭ.
Материалы и методы
Исследование проводилось на базе отделения кар-дио – и рентгенэндоваскулярной хирургии ГБУ ДНР «РКБ имени М.И.Калинина», г. Донецк. В период с 2014 по 2024 гг. прооперировано 96 пациентов (50 мужчин и 46 женщин) в возрасте от 26 до 68 лет по поводу ИЭ. Средний возраст составил 39,3±7,9 лет. Пациенты поступали в отделение с результатами данных ЭхоКГ, коронарографии (у пациентов старше 45 лет), КТ органов грудной клетки, функции внешнего дыхания, УЗИ органов брюшной полости и сосудов шеи, эзофагофиброгастродуоденоскопии. При госпитализации пациентам выполняли стандартный набор анализов крови: группа крови и резус фактор, общий клинический анализ крови, биохимический анализ крови (мочевина, креатинин, глюкоза, билирубин и его фракции, АЛТ, АСТ, электролиты), коагулограмма, общий клинический анализ мочи.
Описание метода
Предложенный метод дает техническую возможность для проведения плазмафереза в интраоперационном периоде кардиохирургических операций в условиях ИК без применения специализированного оборудования для ПА. Модификация традиционного контура аппарата ИК расширяет возможности использования эфферентных методов и позволяет производить интраоперационную гемокоррекцию в условиях ИК.
За основу взят способ проведения мембранного аппаратного ПА, выполняемого на оборудовании «АПФ1-Гемофер» или «Гемофеникс» с применением стандартного набора магистралей и плазмофильтра ПФМ-800 или ПФМ-01-ТТ РОСА, стандартный протокол перфузии в условиях ИК, а также принципы проведения интраоперационных процедур УФ и МУФ.
Как известно, в основе работы аппаратуры для мембранного ПА лежит принцип фильтрации крови пациента, приводимой в движение насосом. Роликовый или перистальтический насос создает движение жидкости в магистрали вращением. Аппарат, оснащенный шаговым двигателем, совершает поступательные движения и производит сжатие фрагмента магистрали, а система обратных клапанов обеспечивает движение жидкости в нужном направлении. Данная процедура, как правило, проводится по принципу забора и возврата в одну и ту же вену. Кровь из катетерезированной вены под действием насоса, приводимого в движение шаговым двигателем, по магистралям через систему однонаправленных клапанов поступает в плазмофильтр. Структура фильтра ПФМ-800

Музычин А.Л., Хавандеев М.Л., Мошкин С.В. и др.
ПРИМЕНЕНИЕ ИНТРАОПЕРАЦИОННОГО ФИЛЬТРАЦИОННОГО ПЛАЗМАФЕРЕЗА В УСЛОВИЯХ ИСКУССТВЕННОГО КРОВООБРАЩЕНИЯ У ПАЦИЕНТОВ С ИНФЕКЦИОННЫМ ЭНДОКАРДИТОМ
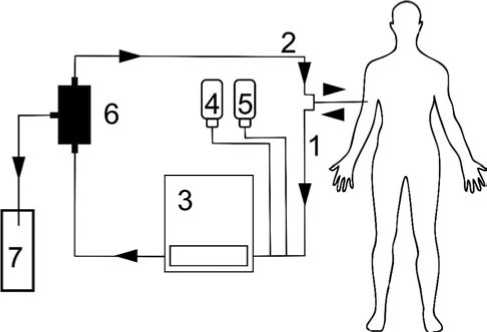
Рис. 1. Принципиальная схема работы аппарата ПА. 1 – магистраль забора крови; 2 – магистраль возврата крови; 3 – аппарат ПА с шаговым двигателем; 4 – антикоагулянт; 5 – раствор натрия хлорида 0,9%; 6 – плазмофильтр; 7 – емкость для эксфузата.
или ПФМ-01-ТТ РОСА, в основе которой лежит трековая мембрана, позволяет разделять протекающую через него кровь на плазму и сгущенную клеточную эритромассу по действием трансмембранного давления. В процессе процедуры ПА регулируется поступление в систему антикоагулянта и раствора натрия хлорида 0,9% для предотвращения тромбирования контура, поддержания необходимых реологических свойств крови и водного баланса пациента. После фильтрации кровь возвращается пациенту. Принципиальная схема работы аппарата ПА приведена на рис. 1.
Суть предлагаемого метода заключается в интеграции плазмофильтра в контур аппарата ИК. Внедрение данного метода в практику расширяет возможности применения ПА в его классическом виде и может быть предметом выбора для специалиста, как дополнительный инструмент гемокоррекции. С одной стороны, метод включает в себя все преимущества ПА, с другой – позволяет в условиях ИК снижать объем цирклирующей крови, проявляя свойства гемоконцентрации. Интраоперационный ПА не заменяет ультрафильтрацию, однако данная процедура имеет схожие технические особенности и принципы проведения.
В условиях ИК для проведения мембранного ПА дополнительного оборудования не требуется. Современный аппарат ИК оснащен всеми необходимыми датчиками давления в магистралях, скорости потока и температуры. Системы защиты включают в себя контроль наличия воздуха в магистралях и датчик контроля уровня жидкости в кардиотомном резервуаре. АИК и анестезиологическая мониторинговая система предоставляют широкий спектр данных. Высокая интраоперационная частота контроля лабораторных показателей позволяют практически постоянно анализировать состояние пациента и выполнять необходимую коррекцию. Конструкция оксигенатора рассчитана на подключение рециркуляционных и деаэрационных шунтов, гемофильтра, прочего оборудования.
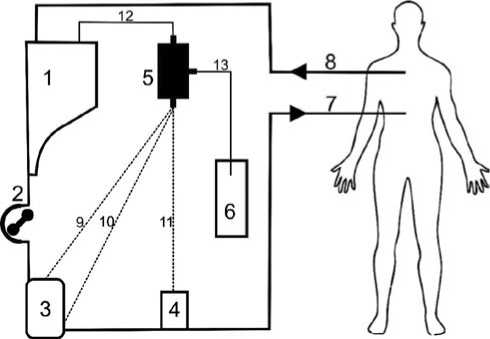
Рис. 2. Варианты интеграции плазмофильтра в контур ИК. 1 – кардиотом-ный резервуар; 2 – основной насос АИК; 3 – оксигенатор; 4 – артериальный фильтр; 5 – плазмофильтр; 6 – емкость для эксфузата;
7 – артериальная магистраль контура ИК; 8 – венозная магистраль контура ИК; 9–11 – варианты подключения приводящей магистрали плазмофильтра; 12 – отводящая магистраль плазмофильтра; 13 – магистраль эксфузата.
Все в комплексе – дает техническую возможность для выполнения интраоперационного ПА.
Интегрирование плазмофильтра в контур ИК не представляет сложности, сравнимо с удобством применения гемоконцентратора и может быть выполнено как в момент сборки контура ИК до начала оперативного вмешательства, так и в любой момент работы АИК. Аппаратура, применяемая для проведения ИК позволяет использовать весь спектр датчиков, применяемых в процедурах классического аппаратного ПА (фото).
Для обеспечения процедуры ПА потребуется: непосредственно плазмофильтр и емкость для эксфузата. В зависимости от особенностей конструкции оксигенатора, способов его расположения и удобства проведения процедуры ПА – возможны различные варианты интеграции плазмофильтра в контур ИК. Общие принципы модификации контура ИК для проведения ПА идентичны принципам УФ. Варианты принципиальной схемы подключения приведены на рис. 2.
Пример интеграции плазмофильтра в контур ИК приведен на рис. 3.
Несмотря на то, что основной принцип работы и функции плазмофильтра в процедурах классического и интраоперационного ПА сохраняется, существует ряд особенностей.
В случае интеграции плазмофильтра в контур ИК, контроль давления на входе в него не требуется, так как показатели давления, фиксируемые в артериальной магистрали и всех шунтах оксигенатора сопоставимы по значению. Давление перфузата на выходе из плазмофиль-тра в данной системе возможно отслеживать датчиком давления аппарата ИК, однако это имеет второстепенное значение. Дополнительные антикоагулянты не применяются, поскольку ИК проводится в условиях тотальной
Музычин А.Л., Хавандеев М.Л., Мошкин С.В. и др. ПРИМЕНЕНИЕ ИНТРАОПЕРАЦИОННОГО ФИЛЬТРАЦИОННОГО ПЛАЗМАФЕРЕЗА В УСЛОВИЯХ ИСКУССТВЕННОГО КРОВООБРАЩЕНИЯ У ПАЦИЕНТОВ С ИНФЕКЦИОННЫМ ЭНДОКАРДИТОМ

Рис. 3. Пример интеграции плазмофильтра в контур ИК.
гепаринизации. Скорость фильтрации поддерживается работой основного насоса. Приводящая магистраль фильтра представляет из себя шунт от основного потока крови. Отводящая – производит сброс в кардиотомный резервуар контура ИК. В связи с этим, контроль воздуха в магистралях плазмофильтра не требуется. Стандартная регулировка окклюзии роликовых моторов до начала ИК минимизирует механическое воздействие на эритроциты.
Проведение интраоперационного плазмафереза в условиях ИК
Мы начинали процедуру интраоперационного плазмафереза за 10 минут до предполагаемого снятия зажима с аорты и продолжали до момента достижения требуемого объема полученного эксфузата плазмы. Старт процедуры обеспечивается открытием приводящей магистрали плазмофильта. В результате работы основного роликового насоса, обеспечивающего перфузию, часть крови, проходящей через плазмофильтр, подвергается фильтрации, после чего возвращается по отводящей магистрали в кардиотомный резервуар. Эксфузат удаляется в емкость. Производится контроль скорости фильтрации, объема эксфузата, стандартных параметров ИК.
Объем удаляемой плазмы и режим плазмафереза определяется общими клиническими рекомендациями и подбирается исходя из конкретной клинической и интраоперационной ситуации. Средний объем удаляемой плазмы у пациентов в группе 1 составил 10,7±3,9 мл/кг массы тела.
Результаты и обсуждение
Пациентам выполнены следующие оперативные вмешательства: протезирование аортального клапана (ПАК) – 28 (29,17%), протезирование митрального кла-
Табл. 1. Распределение пациентов по виду оперативного вмешательства в группе I
|
Вид оперативного вмешательства |
Кол-во пациентов |
Процент от общего количества пациентов с ИЭ |
|
Протезирование аортального клапана |
12 |
12,5 |
|
Протезирование митрального клапана |
17 |
17,7 |
|
Протезирование трикуспидального клапана |
20 |
20,9 |
|
Протезирование аортального и митрального клапанов |
3 |
3,1 |
Табл. 2. Распределение пациентов по виду оперативного вмешательства в группе II
В рамках настоящего исследования пациенты были разделены на две группы: в группе I (n = 52) пациентам выполняли интраоперационный ПА, а в группe II (n = 44) – процедуру интраоперационного плазмафереза не проводили. Данные представлены в табл. 1 и табл. 2.
Для инфузионной терапии всем пациентам проводили катетеризацию одной из внутренней яремных или подключичных вен. Артериальное давление во время операций с ИК измеряли инвазивно посредством катетеризации лучевой или бедренной артерии. Операции выполняли в условиях комбинированной общей анестезии с ИВЛ.
Все оперативные вмешательства выполнены в условиях ИК по стандартной схеме: срединная стернотомия, перикардиотомия, подключение аппарата ИК, антеградная фармакохолодовая кардиоплегия раствором «Кустодиол», наложение зажима на аорту. Далее иссекали пораженный клапан, выполняли его протезирование, деаэрацию, герметизацию, снятие зажима с аорты и восстанавливали сердечную деятельность. После нормализации гемодинамики подшивали временные электроды к правому желудочку, дренировали перикард и ретростер-нальное пространство, выполняли тщательный гемостаз, стернометаллоостеосинтез стальной проволокой и послойное ушивание раны.
На этапе премедикации корректировалась оптимальная ЧСС на уровне 80–90 ударов в минуту, посредством дозирования атропина сульфата, внутривенно вводилось: мидазолам – 50 мкг/кг массы тела, фентанил – 1–2 мкг/кг массы тела. Индукция в анестетезию проводилась тиопенталом натрия – 3 мг/кг массы тела либо
Музычин А.Л., Хавандеев М.Л., Мошкин С.В. и др.
ПРИМЕНЕНИЕ ИНТРАОПЕРАЦИОННОГО ФИЛЬТРАЦИОННОГО ПЛАЗМАФЕРЕЗА В УСЛОВИЯХ ИСКУССТВЕННОГО КРОВООБРАЩЕНИЯ У ПАЦИЕНТОВ С ИНФЕКЦИОННЫМ ЭНДОКАРДИТОМ пропофолом – 2 мг/кг массы тела. С целью релаксации, перед интубацией трахеи, использовался рокурония бромид – 0,6 мг/кг массы тела. В качестве базисного наркоза использовался севофлюран, из рассчёта 1–1,2 МАК, проводилась непрерывная инфузия фентанила – 0,1–0,3 мг/час. Релаксация поддерживалась дробным введением рокуро-ния бромида 0.15 мг/кг массы тела либо его непрерывной инфузией – 0,3 мг/кг/час. Гемодинамическая поддержка осуществлялась непрерывной инфузией норадреналина, допамина, адреналина, добутамина в различных комбинациях и расчетных дозировках, либо изолированно, в зависимости от исходных функциональных параметров сердечной деятельности, а также интраоперационных факторов, воздействующих на сердечную сократимость. Перфузия проводилась с использованием аппаратов ИК Terumo System I (Япония), Stockert S5 (Германия). Оксигенаторы Medtronic Affinity NT (США), Euroset Skipper, Euroset Skipper AF (Италия). Комплекты магистралей к оксигенаторам в модификации custom pack или standard pack с последующей адаптацией по длине в контур ИК. В исследовании применялся мембранный плазмофильтр ПФМ 800 с площадью фильтрации 800 см2 (Россия).
Первичный объем заполнения (ПОЗ), оксигенатора и магистралей во всех группах пациентов по составу и объему идентичный, и включал в себя: натрия хлорид 0,9% – 1000,0 мл, Натрия гидрокарбонат 5% – 100,0 мл, Маннит 15% – 200,0 мл. Гепарин из расчёта 500 ЕД на 100 мл ПОЗ. Растворы, применяемые дополнительно во время перфузии по необходимости: натрия гидрокарбонат 5%, калия хдорид – 7,5%, Гелофу-зин, натрия хлорид 0,9%. Объемная скорость перфузии рассчитывалась исходя из площади поверхности тела пациента и перфузионного индекса 2,5 л/мин/м2. ИК проводилось в условиях умеренной гипотермии (t – 34 °C).
Средние значения длительности ИК и пережатия аорты в группах приведены в табл. 3.
После окончания операции больных переводили в отделение интенсивной терапии. Протокол лечения больных в отделении интенсивной терапии, помимо проведения респираторной поддержки, включал коррекцию показателей гемодинамики (введение инотропных средств, вазопрессоров и вазодилататоров, инфузионных сред), электролитных расстройств, антибиотикотерапию, гемотрансфузию при необходимости и профилактику стрессовых язв. На 2-е сутки послеоперационного периода пациентов переводили в отделение кардиохирургии для дальнейшего лечения и наблюдения.
Пациентам регулярно проводили термометрию. Температура тела в послеоперационном периоде достоверно отличалась в группах. В диаграмме 1 представлены данные средних значений температуры тела с 1-х по 3-е сутки после оперативного вмешательства в группах 1 и 2.
Больным регулярно выполнялись лабораторные методы исследования для достижения целевого уровня МНО, контроля уровня гемоглобина, коррекции электролитных нарушений (при необходимости). В общем кли-
Табл. 3. Распределение пациентов по длительности ИК и пережатия аорты в группах
|
Вид оперативного вмешательства |
Группа I Время ИК среднее |
Группа II Время ИК среднее |
Группа I Время пережатия аорты среднее |
Группа II Время пережатия аорты среднее |
|
Протезирование аортального клапана |
42,6±7,3 |
40,4±6,9 |
35,7±9,2 |
33,8±8,9 |
|
Протезирование митрального клапана |
49,1±11,3 |
48,3±10,2 |
37,2±7,7 |
36,5±8,7 |
|
Протезирование трикуспидального клапана |
49,3±10,8 |
43,3±10,1 |
34,5±8,1 |
32,4±7,9 |
|
Протезирование аортального и митрального клапанов |
79,2±11,3 |
83,1±11,7 |
73,4±10,7 |
75,1±12,1 |
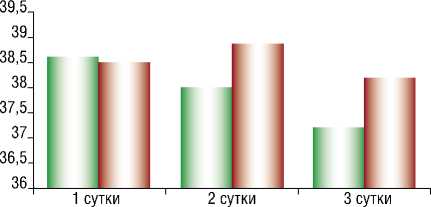
I Температура тела, °C Группа 1
■ Температура тела, °C Группа 2
Диаграмма 1.
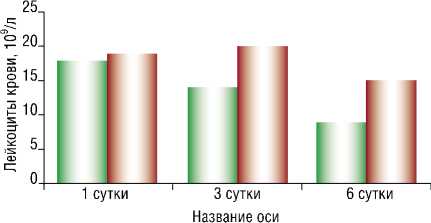
I II Группа! ■ ■ Группа2
Диаграмма 2.
ническом анализе крови также отмечалась достоверная разница между показателями уровня лейкоцитов в группах. Данные наблюдений за 6 суток представлены в виде диаграммы 2.
Мы можем отметить, что в группе 1 показатели СОЭ, абсолютное количество лейкоцитов, процентное содержание юных, палочкоядерных, сегментоядерных нейтрофилов, лейкоцитарный индекс интоксикации статистически ниже по сравнению с группой 2.
Нормализация температуры тела в раннем послеоперационном периоде у пациентов в группе 1 наступала в более ранние сроки по сраввнению с группой 2.
Музычин А.Л., Хавандеев М.Л., Мошкин С.В. и др. ПРИМЕНЕНИЕ ИНТРАОПЕРАЦИОННОГО ФИЛЬТРАЦИОННОГО ПЛАЗМАФЕРЕЗА В УСЛОВИЯХ ИСКУССТВЕННОГО КРОВООБРАЩЕНИЯ У ПАЦИЕНТОВ С ИНФЕКЦИОННЫМ ЭНДОКАРДИТОМ
В ходе исследования установлено, что в группе 1 самостоятельное восстановление сердечного ритма после снятия зажима с аорты наблюдалось в 81,6% случаев, что на 13,7% превышает данный показатель во 2 группе пациентов (67,9%).
Кардиотоническая поддержка в раннем послеоперационном периоде применялась у пациентов 1 группы в 58%, а в группе 2 – в 76% случаев.
Выводы
Применение метода итраоперационного фильтрационного ПА в условиях ИК технически осуществимо, не представляет сложности и не требует приобретения дополнительного оборудования.
В условиях ИК данный метод сохраняет все преимущества ПА, а также позволяет осуществлять волемическую коррекцию и гемоконцентрацию.
Интраоперационный ПА способствует улучшению выхода из ИК путем самостоятельного восстановлению ритма без применения дефибрилляции и снижения потребности в применении адреномиметиков для нормализации артериального давления.
Применение метода интраоперационного ПА демонстрирует улучшение протекания послеоперационного периода, проявляющегося в снижении кардиотонической поддержки, ранней нормализации температуры тела и лабораторных показателей, а именно: абсолютного количества лейкоцитов, относительно содержания палочкоядерных и сегментоядерных лейкоцитов, скорости оседания эритроцитов, С – реактивного белка и лейкоцитарного индекса интоксикации.
Список литературы Применение интраоперационного фильтрационного плазмафереза в условиях искусственного кровообращения у пациентов с инфекционным эндокардитом
- Abel JJ, Rowntree LG, Turner BB. Plasma removal with return of corpuscles (plasmapheresis). J. Pharmacol. Exp. Ther. 1914; 5: 625–627.
- Калинин Н.Н., Варламова С.В. Гемаферез в клинической практике // Альманах клинической медицины. – 2009. – №20. – С.3–9.
- Клиническое применение экстракорпоральных методов лечения / Под ред. Калинина Н.Н. – М.: Трекпортехнолоджи, 2006.
- Воинов В.А. Эфферентная терапия. Мембранный плазмаферез. – М.: Медицина, 2002.
- Куликова В.А., Недоступ А.В., Благова О.В. и др. Эффективность лечения аритмий и синдрома дилатационной кардиомиопатии иммунно – воспалительного генеза с помощью плазмафереза // Российский кардиологический журнал. – 2018. – №12. – С.32–43.
- Мальчевский Ю.Е., Рагимов А.А., Каспаров Э.В. Некоторые клинико – лабораторные показатели при различных режимах плазмафереза у больных стабильной стенокардией напряжения III–IV функционального класса. // Здоровье в XXI веке. – 2018 – Т.20. – №2. – С.55–59.
- Соловьева И.Н., Михайлов Ю.Е., Андрианова М.Ю. Дискретный плазмаферез при ишемической болезни сердца // Терапевтический архив. – 2014. – Т.86. – №8. – C.13–17.
- Шевченко Ю.Л. Хирургическое лечение инфекционного эндокардита и основы гнойно-септической кардиохирургии. – 2-е изд. – М.: Династия, 2020. – 448 с.
- Шевченко Ю.Л. Хирургическое лечение эндокардита: 35-летний опыт // Анналы хирургии. – 2016. – Т.21. – №1-2. – С.42-51.
- Тишко В.В., Тыренко В.В., Козлов К.Л. и др. Мультидисциплинарный подход к ведению пациентов высокого риска после повторных реваскуляризаций миокарда // Клиническая геронтология. – 2014. – №9–10. – С.40–44.
- Erqou S, et al. Lipoprotein(a) concentration and the risk of coronary heart disease, stroke, and nonvascular mortality. Jama. 2009; 302(4): 412–423.
- Куликова В.А., Недоступ А.В., Благова О.В. и др. Эффективность лечения дилатационной кардиомиопатии иммуновоспалительного генеза с помощью плазмафереза // Клин. и эксперимент. хир. Журн. им. акад. Б.В. Петровского. – 2019. – Т.7. – №1. – С.6–16.
- Ворыханов А.В. Ресурсное обеспечение деятельности отделения экстракорпоральных методов лечения // Современные проблемы здравоохранения и медицинской статистики. – 2015. – №3. – С.9–17.
- Соловьева И.Н., Полякова Ю.В., Марченко Т.В. Организация экстракорпоральной помощи в многопрофильной медицинской организации // Менеджер здравоохранения. – 2020. – №2. – С.2 –26.


