Применение ксеноперикарда в сочетании с NPWT (negative pressure wound therapy) в лечении распространенной эмпиемы плевры с бронхоплевральным свищом (клиническое наблюдение)
Автор: Галлямов Э. А., Сурков А. И., Никулин А. В., Дидуев Г. И., Малофей А. М., Романихин А. И.
Журнал: Хирургическая практика @spractice
Рубрика: Статьи
Статья в выпуске: 2 (50), 2022 года.
Бесплатный доступ
Развитие бронхоплеврального свища (БПС) на фоне распространенной эмпиемы плевры, как следствие перенесенной пневмонии тяжелого течения, является грозным осложнением. Наиболее значимым препятствием в хирургическом лечении данной группы пациентов являются: выраженный коморбидный фон, низкие функциональные показатели больных, высокие требования к хирургической технике при выполнении реконструктивно-пластических вмешательств при БПС. Предложено множество хирургических методов лечения бронхоплевральных свищей. Первые из них заключались в ушивании дефекта. Однако доступ через инфицированную плевральную полость приводит к прорезыванию швов и рецидиву свища, несмотря на то, что некоторые авторы предложили сочетать эти операции с различными вариантами миопластики, торакопластики, удалением фиброзной капсулы эмпиемы. Неудовлетворительные функциональные и косметические исходы при выполнении указанных оперативных вмешательств послужили поводом для развития эндоскопических, малоинвазивных хирургических вмешательств. Современные технологии позволяют проводить временную эндоскопическую бронхоокклюзию, которая останавливает сброс воздуха из дефекта. Однако вместе с этим она "выключает" часть легочной ткани из газообмена. Длительная бронхиальная окклюзия приводит к развитию пневмонии с исходом в деструкцию легочной ткани. Нашим коллективом авторов лечение бронхоплеврального свища с помощью ксеноперикарда в сочетании с терапией отрицательным давлением. Данное направление представляется нам весьма перспективным, и в настоящей работе мы хотели бы поделиться первым опытом.
Бронхоплевральный свищ, эмпиема плевры, коморбидный фон, ксеноперикард
Короткий адрес: https://sciup.org/142235294
IDR: 142235294 | УДК: 616.25-002.3 | DOI: 10.38181/2223-2427-2022-2-75-83
Xenopericard combined with NPWT (negative pressure wound therapy) in the treatment of advanced pleural empyema with bronchopleural fistula (clinical follow-up)
The development of bronchopleural fistula (BPS) against the background of advanced pleural empyema, as a result of severe pneumonia, is a formidable complication. The most significant obstacle in the surgical treatment of this group of patients is: a pronounced comorbid background, low functional indicators of patients, high requirements for surgical technique when performing reconstructive plastic interventions in BPS. Multiple surgical methods for treating bronchopleural fistulas are suggested. The first of these were to suture the defect. However, access through the infected pleural cavity leads to suture eruption and recurrence of the fistula, despite the fact that some authors have proposed combining these operations with various variants of myoplasty, thoracoplasty, removal of the fibrous capsule of empyema. Unsatisfactory functional and cosmetic outcomes during these surgical interventions led to the development of endoscopic, minimally invasive surgical interventions. Modern technologies allow temporary endoscopic bronchiococclusion, which stops the release of air from the defect. However, at the same time, she "turns off " part of the lung tissue from the gas exchange. Prolonged bronchial occlusion leads to the development of pneumonia with an outcome in the destruction of lung tissue. Our team of authors treatment of bronchopleural fistula with xenopericardium in combination with negative pressure therapy. This area seems to us very promising, and in this work we would like to share our first experience.
Текст научной статьи Применение ксеноперикарда в сочетании с NPWT (negative pressure wound therapy) в лечении распространенной эмпиемы плевры с бронхоплевральным свищом (клиническое наблюдение)
Бронхоплевральный свищ (БПС) представляет собой патологическое сообщение между трахеобронхиальным деревом и плевральной полостью. Наиболее часто причиной БПС является инфекционная деструкция паренхимы легкого. БПС может быть потенциально катастрофическим осложнением после пневмонэктомии или другой резекции легкого. Отдельно стоит выделить несостоятельность культи бронха после выполнения анатомических резекций легких, как причину БПС, которая является грозным, потенциально жизнеугрожающим осложнением хирургического лечения.
Эмпиема плевры – это воспаление плевральных листков, сопровождающееся образованием гнойного экссудата в плевральной полости. Заболеваемость постоянно увеличивается с девяностых годов прошлого столетия [1]. Несмотря на оптимальное медикаментозное лечение, развитие данной патологии по-прежнему связано со значительной смертностью. Плевральный выпот, который возникает примерно у 40% пациентов с пневмонией, успешно лечится консервативно с помощью соответствующей антибиотикотерапии. Однако в 10% случаев происходит формирование эмпиемы плевры [2].
По течению, эмпиему плевры разделяют на острую (длительность заболевания — до 8 нед.) и хроническую (длительность — более 8 нед.). Лечение пациентов с хронической эмпиемой плевры, с бронхоплевральным свищом в настоящее время является актуальной проблемой в торакальной хирургии. Закрытие БПС у данной группы пациентов является сложной задачей. Основная роль в лечении пациентов с хронической ЭП и БПС принадлежит хирургическим методам, в задачи которых входит закрытие бронхоплеврального сообщения, а также ликвидация остаточной плевральной полости.При выполнении данных задач доступен широкий спектр лечебных мероприятий: торакоцентез, дренирование полости эмпиемы, внутриплевральное введение антибактериальных, фибринолитических средств, хирургическая санация полости эмпиемы. Эффективность рутинного использования фибринолоитических средств, однако, низка и не может быть рекомендована для рутинного применения [3,4,5,6].
Хирургическая санация полости эмпиемы при наличии БПС не позволяет во всех случаях получить ожидаемый эффект от лечения [7,8,9]. Когда малоинвазивные методы санации ОПП не приносят результата или ЭП перешла в хроническую стадию единственным радикальным способом многие хирурги считают санацию полости эмпиемы через торакостому с последующей торакопластикой. В случае длительно сохраняющейся полости эмпиемы, особенно при наличии БПС, до настоящего времени широко применяется наложение торакостомы с последующим открытым ведением полости эмпиемы [10,11,12,13]. Травматичность, неудовлетворительный косметический и функциональный исход данного метода лечения явились причиной поиска более эффективных методов лечения данной проблемы.
На данный момент, широкое распространение в гнойной и торакальной хирургии получила терапия ран отрицательным давлением (NPWT). Данный метод ускоряет заживление ран, стимулирует репарационные процессы, улучшает расправление остаточной легочной ткани и сужает полость раны, в том числе полость эмпиемы [14]. Применение NPWT-терапии, как метод лечения при эмпиеме плевры с БПС требует дальнейшего изучения [15].
В случае же наличия БПС в плевральной полости не создается отрицательное давление в следствии постоянного сброса воздуха. Таким образом для использования NPWT терапии возникает необходимость закрытия бпс. С этой целью нами применен как пластический материал ксеноперикард (“Кардиоплант”). Данный материал изготавливается на основе децеллюляризированного вы-сокоочищенного перикарда домашних животных. Сырье для изготовления изделия проходит сложную многоступенчатую химико-биологическую обработку согласно запатентованной технологии с использованием анти-кальциевых матрикс-сберегающих методик. Благодаря этому из биоткани полностью удаляются все носители антигенности – клеточные элементы и гликозаминогликаны межклеточного матрикса. Структурная архитектоника фибриллярных белков остается нетронутой. Это позволяет заплате выступить в роли матрицы для заселения клеток реципиента, трансформироваться в собственные здоровые ткани и метаболизироваться по законам природных процессов.Заплата абсолютно биосовместима. [23].
Наиболее широко ксеноперикард в настоящее время применяется в реконструктивно-пластической хирургии: для закрытия дефектов межпредсердной и межжелудочковой перегородок, создания искусственных клапанов сердца, протезирования сосудов, протезирования и пластики клапанов сердца, околосердечных тканей, биопротезирования и пластики магистральных сосудов [16, 17, 18, 19, 20, 21, 22]; в хирургии грыж брюшной стенки, диафрагмальных грыж, закрытии ран в условиях абдоминального компартмент-синдрома, для протезирования желчных протоков, укрытия паренхиматозных органов при их резекции [14]; в урологии и гинекологии для пластики мочевыводящих путей, укрепления мышц тазового дна, урослингов, закрытия культи почки; в травматологии и ортопедии при протезировании сухожилий, укреплении связочного аппарата суставов.
Клиническое наблюдение
Пациент Х. 40лет, проходил длительное стационарное лечение в терапевтическом отделении по поводу вирус ассоциированной COVID-19 двусторонней полисегментар-ной пневмонии. Течение заболевания осложнилось деструкцией легочной ткани, развитием правосторонней эмпиемой плевры с бронхоплевральным свищем. Учитывая распространенный характер эмпиемы, стойкий БПС принято решение о переводе пациента в профильное отделение торакальной хирургии ГКБ им. Давыдовского.
Ввиду невозможности расправления правого легкого на фоне активной вакуум-аспирации, необходимости адекватной санации правой плевральной полости – принято решение о необходимости проведения оперативного лечения. В качестве доступа выбрана ВАТС.
Интраоперационно: полость эмпиемы располагается от купола гемиторакса до диафрагмы, в дне полости до 100 мл гнойного экссудата. Париетальная и висцеральная плевра по всему объему остаточной полости с признаками острого воспаления, рубцово изменена, гипереми-рована, контактно кровоточива, сосудистый рисунок не прослеживается.На поверхности париетальной и висцеральной плевры по всему объему остаточной полости имеется гнойно-фибринозный налет (2-3 фаза воспалительного процесса). Легочная ткань плотной консистенции за счет воспаления, тускло серого цвета. В проекции S 9, 10 определяются полости деструкции легочной паренхимы размерами 0.2х0.2 см, из которых поступает воздух. Выполнена санация полости эмпиемы, частичная декортикация легкого. Интраоперационно выполнена ФБС: в правый нижнедолевой бронх установлен резиновый блокатор Medlung №12. Бронхо-блокация эффективна, патологический сброс воздуха из областей деструкции при водной пробе прекращен.
В течении 3х суток после окклюзии правого нижнедолевого бронха отмечалось нарастание ДН,падение
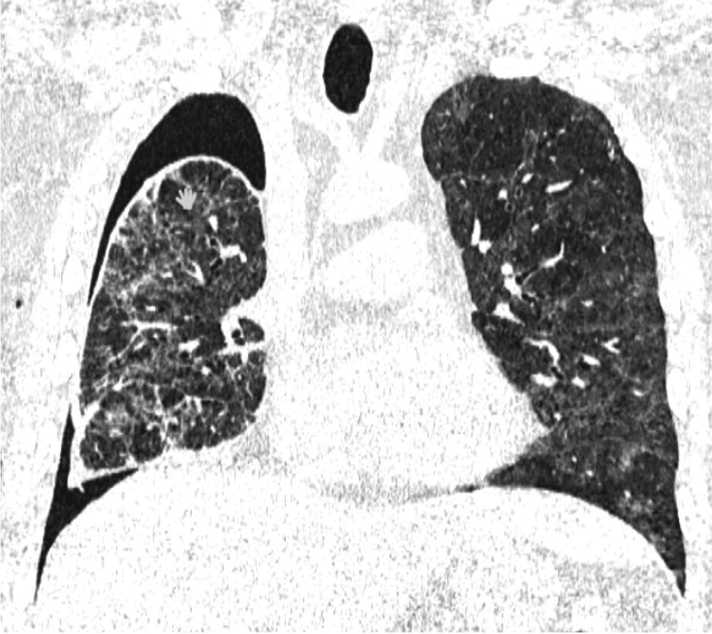
Рис. 1. Неполное расправление правого легкого после дренирования правой плевральной полости по поводу правосторонней распространенной пара-пневмонической эмпиемы плевры с БПС
Fig. 1. Incomplete expansion of the right lung after drainage of the right pleural cavity due to right-sided widespread parapneumonic pleural empyema with BPS
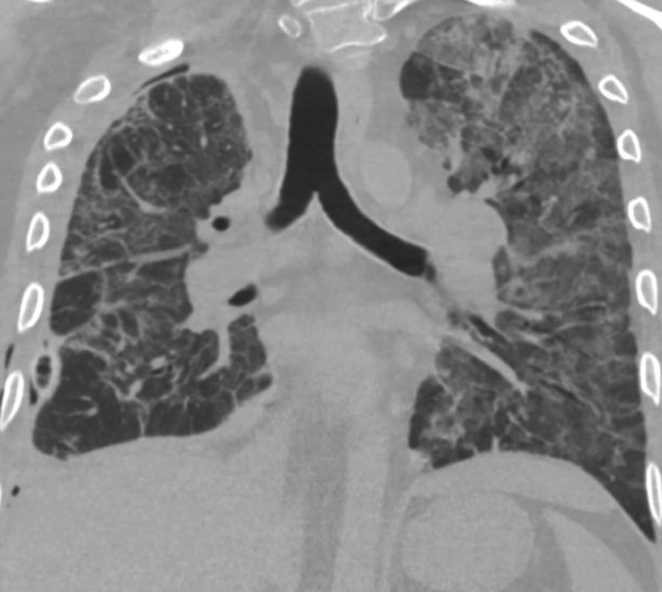
Рис. 2. Компьютерная томография органов грудной клетки после выполненного 1 этапа оперативного лечения Fig. 2. Computed tomography of the chest after the first stage of surgical treatment
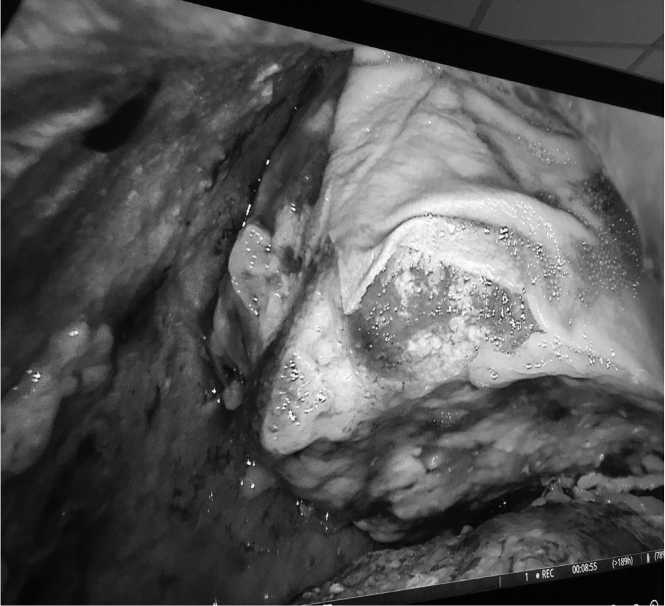
Рис. 3. Ксеноперикард, уложенный на дефекты легочной ткани
Fig. 3. Xenopericardium laid on lung tissue defects
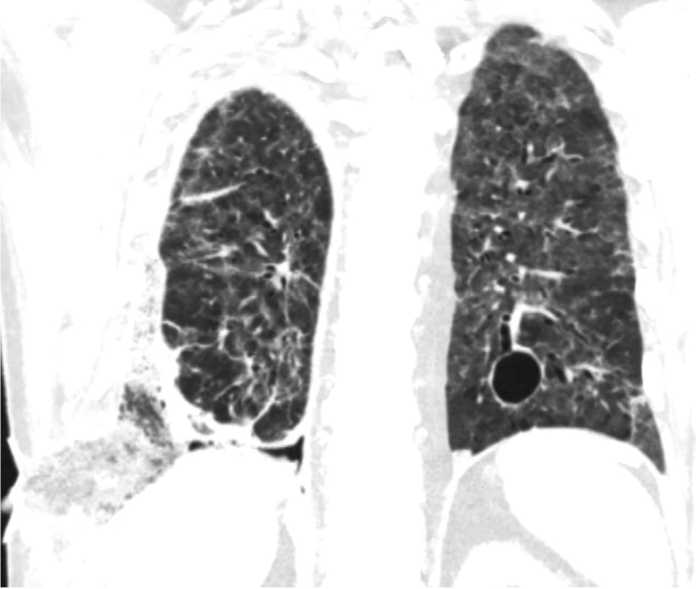
Рис. 4. Контрольный КТ снимок ОГК с монтированной NPWT- системой, с ксеноперикардом, уложенным на дефекты легочной ткани Fig. 4. Control CT scan of the chest with a mounted NPWT system, with xenopericardium placed on lung tissue defects
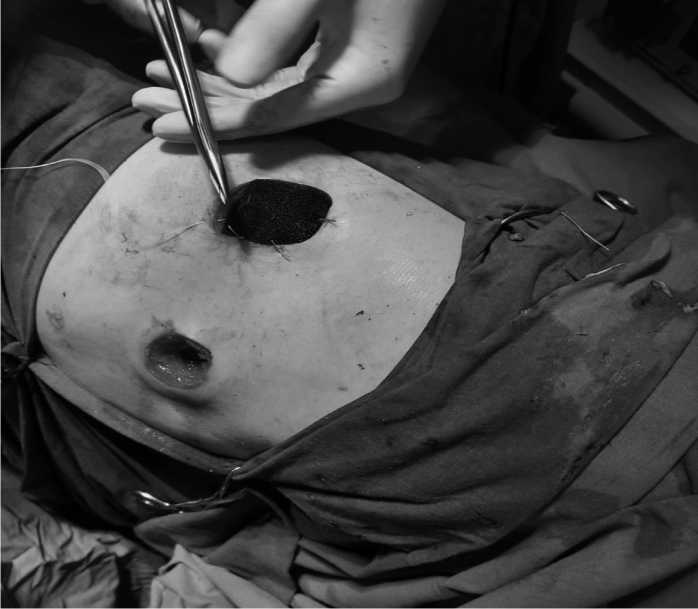
Рис. 5. Этапная смена NPWT-системы через миниторакостому
Fig. 5. Staged change of the NPWT system through a mini-thoracostomy
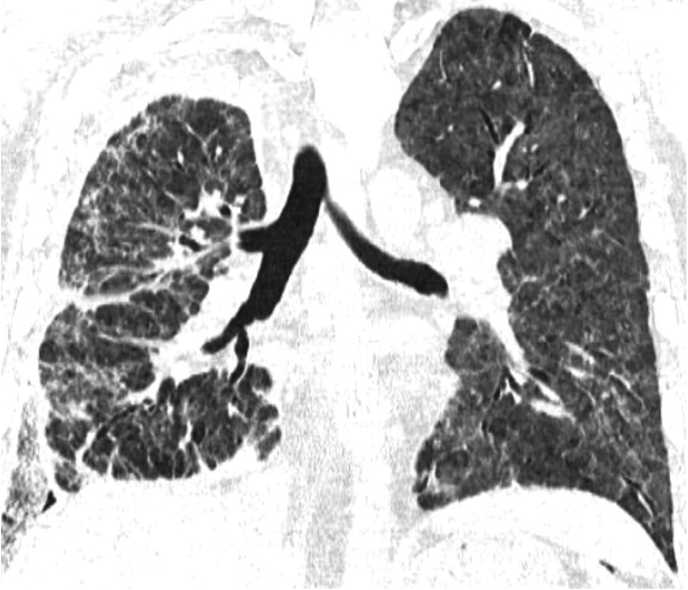
Рис. 6. Торакостома, тампонированная салфетками с антисептиком Fig. 6. Thoracostoma tamponed with antiseptic wipes
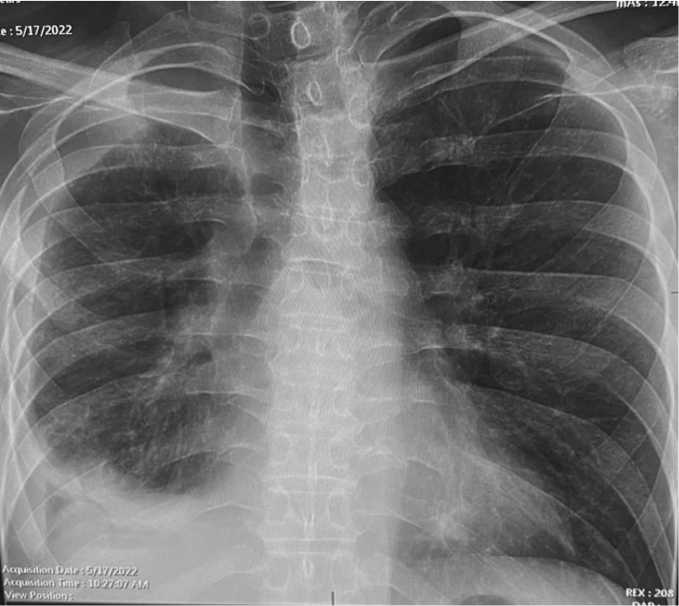
Рис. 7. Контрольный рентген ОГК через 4 недели после удаления дренажа из плевральной полости Fig. 7. Control X-ray of the chest 4 weeks after removal of the drainage from the pleural cavity spO2 до 75%, несмотря на неинвазивную вентиляцию легких. Выполнена повторная фибробронхоскопия, извлечения эндобронхиального окклюдера. Сброс воздуха по дренажу возобновился, на контрольных снимках легкое коллабировано.
Учитывая недостаточную эффективность стандартных методов лечения, было принято решение о необходимости выполнения повторного хирургического лечения.Цель повторной операции – окклюзия БПС. После последовательного изучения отечественной и зарубежной литературы, беря во внимание особенности течения заболевания у конкретного пациента,в качестве пластического материала для закрытия БПС выбран ксеноперикард. В дополнение к нему для редукции объема полости эмпиемы – монтаж NPWT- системы интраплеврально.
В качестве доступа выбрана миниторакостомия с резекцией заднего отрезка VIII ребра. Внутриплеврально в проекцию бронхоплеврального свища уложен ксеноперикард. Для его фиксации была использована мелкопористая губка (Vivano Tec Pro Unit). Выполнен интраплевральный монтаж NPWT- системы в постоянном режиме -100 мм рт. ст. Вакуум стойкий.
Вакуумная терапия проводилась в течении 15 дней, смена губки каждые 5суток под торакоскопическим контролем. Дополнительно выполнялось периодическое наложение пневмоперитонеума в объеме до 2,5 литров воздуха (1 раз в 4 дня). На контрольной торакоскопии (15сутки от момента закрытия свища ксеноперикардом) ксеноперикард надежно фиксирован к месту свища. NPWT- система демонтирована. Остаточная полость минимальных размеров.
После затухания воспалительного процесса в области торакостомной раны, учитывая отсутствие необходимости санации полости эмпиемы через нее, принято решение о пластическом ее закрытии на 28 сутки после операции.
Учитывая минимальную остаточную плевральную полость,высокий риск рецидива гнойных осложнений, на амбулаторный этап дренаж оставлен. Пациент выписан с дренажом на 38 сутки послеоперационного периода.
Заключение
Возможности применения ксеноперикарда для ликвидации бронхоплеврального свища является перспективным методом в лечении пациентов с эмпиемой плевры с БПС, хотя, и требуют дальнейшего изучения. особенно при невозможности проведения реконструк- тивно пластической операции у пациентов с низкими функциональными резервами.
Список литературы Применение ксеноперикарда в сочетании с NPWT (negative pressure wound therapy) в лечении распространенной эмпиемы плевры с бронхоплевральным свищом (клиническое наблюдение)
- Ahmed RA, Marrie TJ, Huang JQ. Thoracic empyema in patients with community-acquired pneumonia. Am J Med 2006; 119: 877–883. https://doi.org/10.1016/j.amjmed.2006.03.042
- Light RW. Management of parapneumonic effusions. Arch Intern Med 1981; 141: 1339–1341.
- Zahid I, Nagendran M, Routledge T, Scarci M. Comparison of video-assisted thoracoscopic surgery and open surgery in the management of primary empyema. Curr Opin Pulm Med. 2011 Jul;17(4):255-9. https://doi.org/10.1097/MCP.0b013e3283473ffe
- Maskell NA, Davies CW, Nunn AJ, Hedley EL, Gleeson FV, Miller R, Gabe R, Rees GL, Peto TE, Woodhead MA, Lane DJ, Darbyshire JH, Davies RJ; First Multicenter Intrapleural Sepsis Trial (MIST1) Group. U.K. Controlled trial of intrapleural streptokinase for pleural infection. N Engl J Med. 2005 Mar 3;352(9):865-74. https://doi.org/10.1056/NEJMoa042473
- Cameron R, Davies HR. Intra-pleural fibrinolytic therapy versus conservative management in the treatment of adult parapneumonic effusions and empyema. Cochrane Database Syst Rev 2008; 2: CD002312.
- Lois M, Noppen M. Bronchopleural fistulas: an overview of the problem with special focus on endoscopic management. Chest. 2005. № 128(6). Р. 3955-3965.
- Кесаев О.Ш. Хирургическое лечение бронхоплевральных осложнений после пневмонэктомий. Дис… кандидата мед. наук. Москва. 2014. С. 183. [Kesaev O.Sh. Surgical treatment of bronchopleural complications after pneumonectomies’. Dis... candidate honey. sciences. Moscow. 2014. S. 183. (In Russian)]
- de Perrot M, Licker M, Robert J, Spiliopoulos A. Incidence, risk factors and management of bronchopleural fistulae after pneumonectomy. Scand Cardiovasc J. 1999;33(3):171-4. https://doi.org/10.1080/14017439950141812
- Groetzner J, Holzer M, Stockhausen D, Tchashin I, Altmayer M, Graba M, Bieselt R. Intrathoracic application of vacuum wound therapy following thoracic surgery. Thorac Cardiovasc Surg. 2009 Oct;57(7):417-20. https://doi.org/10.1055/s-0029-1185907
- Вишневский А.А., Ромашов Ю.В., Акылбеков И.К., Сафаров Б.Д. Хирургическое лечение послеоперационных бронхоплевральных осложнений у больных раком легкого. Рак легкого. – Москва. 1992. С.119-122. [Vishnevsky A.A., Romashov Yu.V., Akylbekov I.K., Safarov B.D. Surgical treatment of postoperative bronchopleural complications in patients with lung cancer. Lung cancer. Moscow. 1992. S. 119-122. (In Russian)]
- Мухин Е.П., Джунусбеков А.Д., Мукушев Н.Р. Операции на главных бронхах при пострезекционных эмпиемах плевры. Рак легкого. Москва. 1992. С. 149-152. [Mukhin E.P., Dzhunusbekov AD, Mukushev N.R. Operations on the main bronchi in postrejection pleural empyems. Lung cancer. – Moscow. 1992. S. 149-152. (In Russian)]
- Порханов В.А., Коровин А.Я., Карпов Д.М., Князев Л.П. Повторные операции при бронхиальных свищах после пневмонэктомий. Актуальные вопросы хирургии легких на современном этапе: тезисы докладов IX Украинской научно практической конференции по грудной хирургии. Киев. 1990. С. 112-113. [Porkhanov V.A., Korovin A.Ya., Karpov D.M., Knyazev L.P. Repeated operations in bronchial fistulas after pneumonectomies’. Topical issues of 97 lung surgery at the present stage: abstracts of the reports of the IX Ukrainian Scientific Practical Conference on Thoracic Surgery. Kyiv. 1990. S. 112-113. (In Russian)]
- Haraguchi S, Koizumi K, Hioki M, Hirata T, Hirai K, Mikami I, Kubokura H, Enomoto Y, Kinoshita H, Shimizu K. Analysis of risk factors for postpneumonectomy bronchopleural fistulas in patients with lung cancer. J Nippon Med Sch. 2006 Dec;73(6):314-9. https://doi.org/10.1272/jnms.73.314
- Aru GM, Jew NB, Tribble CG, Merrill WH. Intrathoracic vacuum-assisted management of persistent and infected pleural spaces. Ann Thorac Surg. 2010;90:266–270. https://doi.org/10.1016/j.athoracsur.2010.04.092
- Palmen M, van Breugel HN, Geskes GG, van Belle A, Swennen JM, Drijkoningen AH, et al. Open window thoracostomy treatment of empyema is accelerated by vacuum-assisted closure. Ann Thorac Surg. 2009;88:1131–1136. https://doi.org/10.1016/j.athoracsur.2009.06.030
- Иванов А.С., Иванов В.А., Балоян Г.М., Евсеев Е.П., Шехтер А.Б., Милованова З.П. Ксенопластика в реконструктивной хирургии сердца и сосудов. Результаты 20-летнего использования пластических материалов на основе ксеноперикарда. Биопротезы в сердечно-сосудистой хирургии. Материалы Всероссийской конференции с международным участием. Кемерово, 21-23 июня, 2001. С.41-43. [Ivanov A.S., Ivanov V.A., Baloyan GM, Evseev EP, Shekhter AB, Milovanova Z.P. Xenoplasty in reconstructive heart and vascular surgery. Results of 20-year use of xenopericardial plastic materials. Bioprostheses in cardiovascular surgery. Materials of the All-Russian Conference with international participation. Kemerovo, June 21-23, 2001 S.41-43. (In Russian)]
- Карпенко А.А., Кужугет Р.А., Стародубцев В.Б., Игнатенко П.В., Ким И.Н., Горбатых В.Н. Непосредственные и отдаленные результаты различных методов реконструкции каротидной бифуркации. Патология кровообращения и кардиохирургия №1-2013, стр.21-24. [Karpenko A.A., Kuzhuget R.A., Starodubtsev V.B., Ignatenko P.V., Kim I.N., Gorbatykh V.N. Immediate and long-term results of various methods of reconstruction of carotid bifurcation. Circulatory pathology and cardiac surgery. No. 1-2013, pp. 21-24. (In Russian)]
- Милованова З.П., Иванов А.С., Черепенин Л.П., Дземешкевич С.Л., Балоян Г.М. 11-летний опыт применения ксеноперикарда в хирургии сердца. Тезисы докладов и сообщений II Всероссийского съезда сердечно-сосудистых хирургов, Санкт-Петербург, Ч. II. 1993. С. 159-160. [Z.P. Milovanova, A.S. Ivanov, L.P. Cherepenin, S.L. Dzemeshkevich, G.M. Baloyan, 11 years experience with xenopericardium in heart surgery. Theses of reports and messages of the II All-Russian Congress of Cardiovascular Surgeons, St. Petersburg, Part II. 1993. S. 159-160. (In Russian)]
- Столяров М. С. «Клинико-функциональная оценка пластики сонных артерий заплатой из ксеноперикарда, обработанного диэпоксисоединениями, при каротидной эндартерэктомии». Автореф. дисс. кан. мед. наук. Новосибирск., 2008. [Stolyarov M. S. "Clinical and functional assessment of carotid artery plasticity with a patch of xenopericardium treated with diepoxy compounds in carotid endarterectomy." Autoref. diss. kan. honey. sciences. Novosibirsk., 2008. (In Russian)]
- Fung Zui Hong Sean. Long-term results of xenopericardial conduit implantation in surgical correction of ascending aortic aneurysm. Diss. cand. honey. sciences M.. 2012
- Mueller C, Dave H, Prêtre R. Surgical repair of aorto-ventricular tunnel. Multimed Man Cardiothorac Surg. 2012 Jan 1;2012:mms006. https://doi.org/10.1093/mmcts/mms006
- Nonaka M, Iwakura A, Yamanaka K. Technique to treat extensive abscesses in double valve replacement for prosthetic valve endocarditis. J Heart Valve Dis. 2013 Jul;22(4):575-7.
- Пластина ксеноперикардиальная «Кардиоплант». — Текст : электронный // Cardioplant: [сайт]. — URL: https://cardioplant.ru/cardiovascularsurgery/plastinaxeno (дата обращения: 10.05.2022).


