Применение неадекватной регионарной химиотерапии у больных с раком головки поджелудочной железы
Автор: Тавобилов М.М., Карпов А.А., Шабунин А.В.
Журнал: Московский хирургический журнал @mossj
Статья в выпуске: 4 (50), 2016 года.
Бесплатный доступ
Введение. Основываясь на данных о первично-диссеминированном характере опухолевого процесса при протоковой аденокарциноме головки поджелудочной железы, в современную клиническую практику внедряются современные методы неоадъювантной регионарной химиотерапии (НРХТ). Материалы и методы. В условиях Городской клинической больницы им. С.П. Боткина проведено проспективное клиническое исследование, в котором пациентам с протоковой аденокарциномой головки поджелудочной железы перед выполнением радикального хирургического лечения проводится НРХТ в двух методиках. Результаты. За период с июля 2014 года по июль 2016 года было выполнено НРХТ была проведена 33 больным, 19 из которых в усовершенствованном режиме. Выводы. Проведенное нами исследование показало, что применение усовершенствованной методики масляной химиоэмболизации позволяет сократить время самой процедуры и её себестоимость, при этом, не влияя на её эффективность.
Рак поджелудочной железы, неоадъювантная регионарная химиотерапия, панкреатодуоденальная резекция
Короткий адрес: https://sciup.org/142211275
IDR: 142211275
Текст научной статьи Применение неадекватной регионарной химиотерапии у больных с раком головки поджелудочной железы
Background. Neoadjuvant regional chemotherapy (NRCT) is a novel treatment option in pancreatic head cancer treatment.
Methods. In Botkin Hospital between 2014-2016 were treated 33 patients with pancreatic head cancer with neoadjuvant regional chemotherapy addition.
Results. In first group (14 patients) laparotomy was made in 13-54 days after NRCT, in the second (19 patients) – in 3-5 days. 9 pancreatic resections were made in first group, 16- in the second. Complications ratio in both groups were similar. Efficacy and procedure cost were evaluated.
Conclusion. Our modification of NRCT method could lower cost of procedure without losing the efficacy.
Введение.
Рак поджелудочной железы - один из наиболее сложных в плане диагностики и лечения онкологических заболеваний. Отличительной особенностью его является увеличение заболеваемости и низкая продолжительность жизни этих пациентов. В 2014 году диагностировано до 200 000 больных раком поджелудочной железы во всем мире, две трети из которых зафиксированы в развитых странах [1]. Рак поджелудочной железы является четвертой наиболее частой причиной онкологически-ассоциированной смерти больных у мужчин (после рака легкого, простаты, колоректального рака) и у женщин (рак легкого, молочной железы, колоректальный рак)[2].
В современном представлении – рак головки поджелудочной железы – это системная болезнь, которая, к сожалению, выявляется далеко не всегда в ранней стадии своего развития. Так при размере опухоли поджелудочной железы до 1 см, риск наличия метастатических очагов составляет 28%, при опухоли 2 см – 73%, а при размере 3 см – уже 94% [3]. Обоснованием комплексного лечения больных резекта-бельным раком поджелудочной железы с неоадъювантной химиотерапией являются данные о биологических особенностях метастазирования, которые относят протоковый рак поджелудочной железы к первично-генерализованному заболеванию [4]. Все это обуславливает необходимость поиска методов диагностики и способов лечения, которые позволят и улучшить диагностику опухоли и усовершенствовать лечебный алгоритм. Улучшение, усовершенствование и последующее внедрение новых способов лечения на разных этапах позволит замедлить распространение опухолевого поражения, снизит возникновение местных рецидивов у больных, которые перенесли радикальное оперативное вмешательство – панкреатогастродуоденальную резекцию. Необходимо при этом отметить, что радикальное оперативное вмешательство на момент постановки диагноза, возможно выполнить лишь у 15-20% пациентов, а пятилетняя выживаемость составляет около 10% [5].
В неоадъювантном режиме для локального воздействия на опухолевую ткань химиопрепаратов в практику была внедрена масляная химиоэмболизация артерий поджелудочной железы [6]. В исследованиях, проведенных на базе ЦНИРРИ (Санкт-Петербург) убедительно показана возможность преодоления устойчивости рака поджелудочной железы к химиопрепаратам при повышении их концентрации и увеличении экспозиции воздействия. В представленной авторами работе обосновывается целесообразность неоадъювантной масляной химиоэмболизации в качестве одного из этапов лечения рака поджелудочной железы [7, 8].
Основываясь на представленных литературных данных, нами было продолжено исследование метода неоадъювантной регионарной химиотерапии (НРХТ). Наше исследование состояло из двух частей. В первой части нами усовершенствована методика выполнения неоадъювантной химиоэмболизации. Вторая часть исследования посвящена определению оптимальных сроков выполнения радикального оперативного вмешательства после НРХТ.
Материал и методы
За период с июля 2014 года по июль 2016 года НРХТ выполнена 33 больным. Среди них преобладали лица мужского пола - 21:12 пациентов. Средний возраст больных составил 61,6±0,9 (41-77) лет. Показанием для выполнения неоадъювантной химиоэмболизации служило наличие у пациента верифицированной резектабельной либо погранично-резектабельной протоковой аденокарциномы головки поджелудочной железы. Диагноз ставился на основании данных ультразвуковых и лучевых методов визуализации. Во всех случаях с целью получения морфологического заключения выполнялось эндосонографическое исследование с тонкоигольной пункцией. После обсуждения на мультидисциплинарном онкологическом консилиуме, в отделении рентгенхирургических способов лечения проводилась процедура масляной неоадъювантной химиоэмболизации. Всем больным проводилась регионарная терапия по стандартной схеме с использованием 1,0 - 50 мл оригинального препарата «Гемзар» (Eli Lilly Vostok S.A., Швейцария) в разведении в 10 мл масляного контрастного вещества «Lipiodol Ultra Fluid» (Guebert, Франция).
В нашем исследовании принимали участие две группы больных. В первой группе НРХТ была выполнена по стандартной методике, во второй – по усовершенствованной методике.
Стандартная процедура неоадъювантной химиоэмболизации артерий поджелудочной железы осуществляется через трансфеморальный сосудистый доступ. Первым этапом проводится диагностическая ангиография чревного ствола и верхней брыжеечной артерии с возвратной портографией. Это позволяет оценить анатомические особенности кровоснабжения поджелудочной железы и опухоли, а также определить степень вовлеченности магистральных сосудов в опухолевый процесс. Далее выполняется селективная катетеризация гастродуоденальной артерии с помощью микрокатетера по предварительно заведенному проводнику. С целью эмболизации всех сосудов питающих опухоль, а также предотвращения нецелевой эмболизации, используется перераспределительная техника эмболизации, для чего в правую желудочно-сальниковую артерию, дистальнее отхождения всех артерий кровоснабжающих опухоль, устанавливаются спирали в количестве 2-3 штук. После достижения редукции кровотока по правой желудочносальниковой артерии вводится химиоэмболизат.
Усовершенствование методики химиоэмболизации, заключается в том, что после выполнения ангиографии чревного ствола, диагностический катетер устанавливается в проксимальном отделе гастродуоденальной артерии по предварительно заведенному проводнику. После этого в правую желудочно-сальниковую артерию заводится проводник, по которому дистальнее места отхождения артерий кровоснабжающих опухоль устанавливается и раздувается баллонный катетер, диаметр которого, соответствует диаметру артерии в данном сегменте, после чего через диагностический катетер проводится контрольная ангиография гастродуоденальной артерии. При прекращении кровотока по правой желудочно-сальниковой артерии через диагностический катетер вводится химиоэмболизат, в случае если кровоток сохраняется, производится замена баллонного катетера на баллонный катетер большего диаметра, с последующим его раздутием и проведением контрольной ангиографии. После окончания процедуры баллонный катетер сдувается и удаляется вместе с проводником и диагностическим катетером.
Эффективность обеих вариантов НРХТ определялась нами при контрольной СКТ брюшной полости, которая выполнялась с третьих по шестые сутки после процедуры.
В ходе дальнейшего исследования нами проводилось изучение оптимальных сроков выполнения радикального оперативного вмешательства после проведённой ранее НРХТ. С этой целью нами были изучены результаты радикального оперативного вмешательства – панкреатогастродуоденаль-ной резекции, которая была выполнена в различные сроки после НРХТ. В связи с отсутствием отличий клинического эффекта обеих методик НРХТ – вариант выполнения НРХТ (стандартный либо усовершенствованный) в данном разделе исследования нами не учитывался.
На первом этапе данного исследования оперативное вмешательство было выполнено в сроки от 13 до 54 суток после НРХТ (в среднем 32,4 дня). Оперированы 14 больных, из них радикально – 9, у пяти пациентов интраоперационно выявлены признаки местнораспространённого нере-зектабельного опухолевого процесса. Двух больных не оперировали, т.к. в ходе предоперационного скрининга были выявлены признаки метастатического поражения печени
В дальнейшем нами были изменены сроки выполнения радикального вмешательства. Панкреатогастродуоденаль-ная резекция выполнялась на 3-5 сутки после артериальной химиоэмболизации. Данные пациенты составили вторую группу, их было девятнадцать.
В 16 случаях выполнена радикальная операция, в трёх случаях интраоперационно были выявлены признаки местнораспространённого нерезектабельного опухолевого процесса. Этим пациентам был сформирован терминолатеральный гепатикоеюноанастомоз и позадиободочный гастроэнтероанастомоз на «короткой» петле тонкой кишки.
Патоморфологическая стадия заболевания у всех радикально оперированных больных была T3N1M0, во всех случаях гистологически опухоль представлена умереннодифференцированной протоковой аденокарциномой.
Послеоперационная тактика ведения больных, перенесших радикальное оперативное вмешательство после НРХТ не отличалась от стандартной. Оценены специфические осложнения, такие как панкреатическая фистула различных классов, гастростаз и кровотечения с использованием классификации ISGPS, и общие по градации Clavien-Dindo.
Результаты
В группе больных, которым НРХТ была выполнена по стандартной методике, она была успешна у всех пациентов. Продолжительность вмешательства составила в среднем 63±0,7 минуты (от 51 до 72 минут), лучевая нагрузка -0,78 мЗв (от 0,51 до 0,92 мЗв). При этом была рассчитана средняя себестоимость данного варианта вмешательства. Она составила 119 350 рублей.
Во второй группе (13 больных) процедура была осуществлена в усовершенствованном варианте, она также была успешно выполнена у всех пациентов. Продолжительность вмешательства составила в среднем 36±0,8 минут (от 32 до 41 минуты), лучевая нагрузка - 0,41 мЗв (от 0,32 до 0,58 мЗв). Средняя себестоимость вмешательства в данном варианте составила 34 100 рублей.
В послеоперационном периоде всем пациентам выполнялся контроль клинического и биохимического анализов крови. В двух случаях был отмечен постэмболизационный синдром (при стандартной методике), проявлявшийся как умеренным абдоминальным болевым синдромом, так и транзиторным повышением уровня панкреатической амилазы сыворотки крови. На фоне проведения консервативной терапии явления болевого синдрома и гиперамила-земии были купированы в течении первых двух суток от начала клинических проявлений.
С целью оценки степени насыщения химиоэмболиза-том опухолевой ткани, регионарных лимфатических узлов и ткани печени всем пациентам на 3-6 сутки после НРХТ выполнялась компьютерная томография органов брюшной полости в нативном режиме. Во всех случаях было выявлено наличие контраста в проекции головки поджелудочной железы. В непораженной ткани поджелудочной железы химиоэмболизат не определялся, что подтверждает селективность выполненной химиоэмболизации. В 10 случаях отмечено контрастирование ткани печени, что свидетельствовало о частичном попадании химиопрепарата в портальное сосудистое русло, которое не проявлялось клиническими либо лабораторными изменениями. В результатах компьютерной томографии брюшной полости у больных в обеих исследованных группах каких-либо отличий выявлено не было.
В ходе изучения оптимальных сроков выполнения радикальной операции в первой группе пациентов (поздние сроки выполнения ПДР) панкреатическая фистула была отмечена у 6 пациентов (класс «А» по ISGPS у 2 больных, класс «В» у 2 и класс «С» у двух пациентов). Послеоперационное геморрагическое осложнение класса «А» было у двух больных (по одному класс «А» и «В»). Гастростаз выявлен у четырех пациентов, из них у двух он был класса «А» и у двух класса «В».
Оценивая осложнения согласно классификации Clavien-Dindo, мы в итоге получили следующие результаты. Осложнения первой степени отмечены у 2, второй степени у 3 пациентов. Все они не потребовали значительных изменений в стандартной схеме послеоперационного ведения. Третьей степени осложнение выявлено у двух пациента, были выполнены дренирования жидкостных скоплений под контролем УЗИ. Осложнений четвертой и пятой степени отмечено не было.
В последующем во всех случаях радикального оперативного вмешательства, было проведено гистологическое исследование удаленного макропрепарата. Макропрепараты были представлены органокомплексом: резецированной головкой поджелудочной железы, частью желудка и отрезком тонкой кишки.
После проведения параллельных срезов в аксиальной плоскости по отношению к железе, опухолевый узел во всех случаях был неправильной формы, белесоватого цвета, каменистой плотности. Его размер варьировал от 2 см до 4,5 см. Также во всех исследованных случаях на разрезах тканей поджелудочной железы просматривались очаги некроза, в виде желтоватых замазкообразных участков, как в опухолевом узле, так и в стенке ДПК, а также в прилежащей сохранной паренхиме поджелудочной железы и перипанкре-атической жировой клетчатке (рис. 1). Участки некроза были неправильной формы, локализовались преимущественно ближе к передней поверхности железы по ходу введения химиопрепарата. Следует отметить, что в одном случае стенка ДПК и удаленная часть поджелудочной железы были темносинюшного цвета с массивными очагами распада.
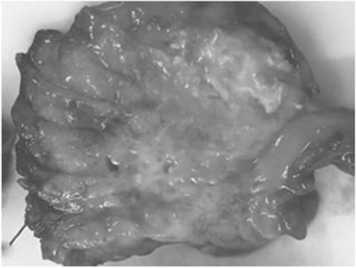
Рис. 1. Макропрепарат, резецированная головка поджелудочной железы. При аксиальном разрезе макропрепарата - очаг некроза
При микроскопическом исследовании во всех 9 случаях опухоль представлена классическим вариантом умереннодифференцированной протоковой аденокарциномы с участками анапластического компонента. Объем анапластического компонента разнился и составлял от 5% до 15% опухолевой ткани, но во всех случаях не являлся преобладающим.
Во всех случаях после НРХТ в проекции некрозов отмечались кистозно-расширенные частично разрушенные опухолевые железистые структуры с некротическим детритом в просветах (рис. 2). В данных участках десмопластическая строма была разрушена, за счет выраженной смешанной лейкоцитарной инфильтрации с преобладанием гранулоцитов (рис. 3.). Часть опухолевых желез буквально «плавала» в воспалительном инфильтрате. Воспалительная инфильтрация распространялась на мышечную оболочку ДПК, по ходу опухолевой инвазии в стенку ДПК (рис. 4). Инвазия опухоли в стенку ДПК обнаружена в 5-ти случаях: в четырех до слизистого слоя и в 1-ом до мышечного слоя. В одном случае отмечался асептический некроз мышечной оболочки ДПК, в виде гомогенизированных гладкомышечных волокон с пикнотичными ядрами. В одном из 6-ти случаев, в прилежащей парапанкреатической клетчатке обнаружены стеатонекрозы, как результат острого краевого панкреатита после НРХТ (рис. 5)
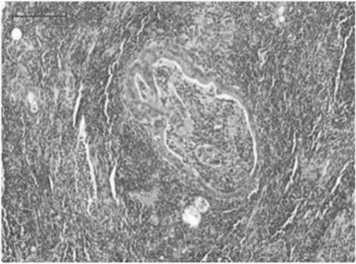
Рис. 2. ПАК, в просвете опухолевой железы некротический детрит. В строме выраженное воспаление. Опухоль «плавает» в воспалительном инфильтрате. Окр.: гематоксилином и эозином. Ув. ×200
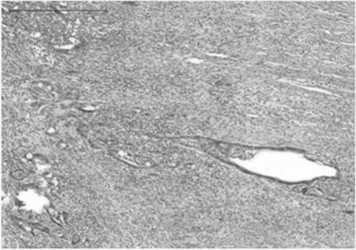
Рис. 3. ПАК. Разрушение десмопластической стромы в опухоли, инфильтрация нейтрофилами. Окр.: гематоксилином и эозином.
Ув. ×200
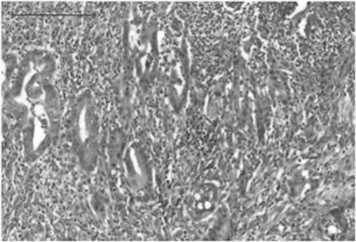
Рис. 4. ПАК. Инвазия в стенку ДПК. В мышечной оболочке ДПК диффузная воспалительная инфильтрация, распространяющаяся со стороны поджелудочной железы. При большем увеличении инфильтрация представлена преимущественно нейтрофилами.
Окр.: гематоксилином и эозином. Ув. ×200 ; ×400
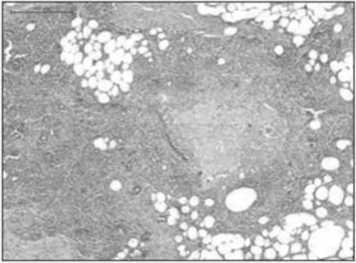
Рис. 5. Стеатонекроз в парапанкреатической жировой клетчатке. Ув. ×200
Необходимо отметить, что у больных с протоковой аденокарциномой поджелудочной железы, опухолевые узлы которых не подвергались НРХТ, как правило, неопластические железистые структуры неправильной формы; изменения в строме опухоли, сопровождаются выраженной десмопластической реакцией; воспалительная инфильтрация минимальна или отсутствует, при этом характер инфильтрации – лимфоцитарный; некрозы чрезвычайно редки, встречаются только в больших по своему размеру опухолевых узлах и возникают, как правило, в результате нарушения питания опухолевой ткани.
В шести случаях, после НРХТ, обращало на себя внимание усиление митотической активности опухоли, не характерное для данного варианта рака поджелудочной железы без предварительного введения химиоэмболизата (рис. 6). При ИГХ реакции индекс Ki-67 был в пределах от 70-90%.
При ИГХ типировании лейкоцитарная инфильтрация была полиморфна, помимо гранулоцитов, представлена как В - , так и Т-лимфоцитами, но характер их распределения в строме отличался. Лимфоидная инфильтрация, сопровождающая инвазию опухоли в стенку ДПК, а также в зоне некрозов преимущественно представлена Т-лимфоцитами с небольшим преобладанием CD8+ над CD4+ . B – лимфо-
циты (СD79α+) представлены в лимфоидных узелковых скоплениях, без формирования центра размножения, на границы опухоли и неизмененной паренхимы железы, в участках проявления обструктивного панкреатита.
По ходу введения химиоэмболизата были обнаружены в просвете артериального сосуда мышечного типа тромбы с началом организации (рис. 7).
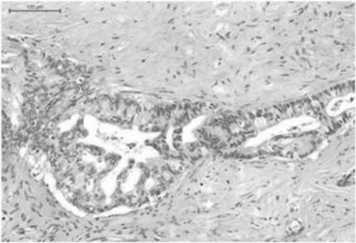
Рис 6. Выраженная митотическая активность. Окр.: гематоксилином и эозином. Ув. ×400
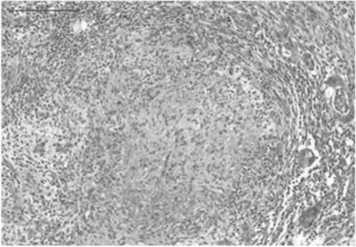
Рис. 7. ПАК. В просвете артериального сосуда мышечноэластического типа организованный тромб. Мышечная оболочка сосуда с выраженной воспалительной инфильтрацией.
Окр.: гематоксилином и эозином. Ув. ×400
Распространение опухоли в парапанкреатические мягкие ткани обнаружено только в одном случае. Интрапан-креатическая периневральная инвазия обнаружена во всех случаях. Экстрапанкреатическая периневральная инвазия обнаружена в 7 случаях. Поражение регионарных лимфатических узлов обнаружены во всех 9 случаях, при этом метастазировал дифференцированный компонент опухоли.
При окраске суданом III в ткани самой поджелудочной железы, ткани опухоли и прилежащей непосредственно к головке поджелудочной железы стенке ДПК позитивно окрашенные липиды были не обнаружены. При этом, обращало на себя внимание большое скопление позитивно-окрашенных капель жира в ткани регионарных лимфатических узлов. Это говорит о том, что при данных сроках выполнения радикальной операции химиоэмболизат практически полностью уходит из вышеперечисленных органов и тканей, а остаётся только в регионарных лимфатических узлах.
Учитывая полученные выраженные воспалительные изменения (морфологическая картина панкреонекроза и парапанкреонекроза) гистологические изменения ткани головки поджелудочной железы и парапанкреатической клетчатки, было принято решение об изменении сроков выполнения радикальной операции после НРХТ, как уже было сказано выше, данные пациенты составили вторую группу.
В послеоперационном периоде у этой группы пациентов также были оценены специфические осложнения. Панкреатическая фистула была отмечена у 5 пациентов (класс «А» по ISGPS у 2 больных, класс «В» у 2 и класс «С» у одного пациента). Послеоперационное геморрагическое осложнение класса «А» было у одного больного. Гастростаз выявлен у трёх пациентов, из них у двух он был класса «А».
Оценивая осложнения согласно классификации Clavien-Dindo, мы в итоге получили следующие результаты. Осложнения первой степени отмечены у 3, второй степени 2 пациентов. Все они не потребовали значительных изменений в стандартной схеме послеоперационного ведения. Осложнение третьей степени выявлено у одного больного, потребовались повторные миниинвазивные оперативные вмешательства (дренирования острых жидкостных скоплений под контролем УЗИ). Осложнений четвертой и пятой степени отмечено не было. В ходе последующего морфологического изучения макроскопически во всех 16 случаях в резецированном органокомплексе отсутствовали некротические изменения, обнаруженные у больных первой группы. При раскрытии через антиампулярное ребро во всех случаях зона большого и малого сосочков не изменена, в большинстве случаев на слизистой ДПК обнаружены изъязвление и втяжение стенки. При проведении параллельных срезов в аксиальной плоскости железы опухолевый узел был неправильной формы, белесоватого цвета, каменистой плотности размерами от 2 см до 5,2 см.
При гистологическом исследовании опухоль представлена высоко- и умеренно-дифференцированными формами, по 2/16 и 14/16 случаев соответственно. В 5-ти случаях наряду с дифференцированным компонентом обнаружен анапластический компонент. Во всех случаях имело место интра-панкреатическая периневральная инвазия. Инфильтрация стенки ДПК выявлена в 14-ти случаях, распространение в па-рапанкреатические ткани в 5 случаях. Поражение регионарных лимфатических узлов обнаружено в 15 из 19 случаях.
При окраске суданом III выявлены позитивно-окрашенные капли жира в толще опухоли, лимфатических щелях. В регионарных лимфатических узлах количество позитивно-окрашенных капель было меньше, по сравнению с первой группой наблюдения.
Обсуждение
НРХТ является перспективным методом комбинированного лечения больных с протоковой аденокарциномой головки поджелудочной железы. Как любая методика, она
имеет свои достоинства и недостатки. Основными недостатками данного вмешательства являются его высокая себестоимость, большая продолжительность процедуры и высокая лучевая нагрузка на пациента, что обусловлено необходимостью использования микрокатетеров и спиралей.
Необходимо отметить, что усовершенствованный вариант масляной химиоэмболизации позволяет в среднем снизить на 42,9% продолжительность всего вмешательства, на 47,4% лучевую нагрузку на пациента и на 71,4% себестоимость вмешательства.
При этом эффективность усовершенствованной методики, за счет длительной экспозиции рентгеноконтрастного химиоэмболизата в опухоли с одновременным распределением его по лимфатическим коллекторам и воротной системе печени подтверждено нами данными СКТ брюшной полости и последующим гистологическим исследованием.
Такая фармакокинетика химиоэмболизата после его селективного введения в артерии поджелудочной железы позволяет оказать воздействие химиопрепарата не только на первичный очаг, но и на регионарные лимфо- и гематогенные метастазы.
В свою очередь, необходимо отметить, что сократив сроки выполнения радикального оперативного вмешательства после НРХТ, удалось добиться более благоприятных условий для выполнения радикального оперативного вмешательства. Этому послужило меньшая степень выраженности воспалительного процесса как непосредственно в самой паренхиме железы, так и в парапанкреатической клетчатке, развившиеся в результате краевого панкреонекроза. При этом выявленные морфологические изменения в структуре самой опухоли – терапевтический патоморфоз - от воздействия на её химиопрепарата были идентичны у пациентов, вне зависимости от сроков выполнения радикального оперативного вмешательства. Результаты радикальных операций по количеству общих и специфических осложнений были лучше у пациентов, которым радикальное оперативное вмешательство выполнялось в более ранние сроки.
Заключение
Проведенное нами исследование показало, что применение усовершенствованной методики масляной химиоэмболизации позволяет сократить время самой процедуры и её себестоимость, при этом, не влияя на её эффективность.
Выполнение радикального оперативного вмешательства в течение первой недели после НРХТ, позволяет уменьшить количество ранних общих и специфических послеоперационных осложнений. Это обусловлено меньшей степенью выраженности воспалительно-некротических изменений ткани поджелудочной железы и перипанкреатической клетчатки. Необходимо при этом отметить, что степень выраженности терапевтического патоморфоза в данной группе больных не отличалась от той, которая была обнаружена у больных, оперированных в более поздние сроки после выполненной им масляной химиоэмболизации.
Список литературы Применение неадекватной регионарной химиотерапии у больных с раком головки поджелудочной железы
- Kamisawa T, Wood LD, Itoi T, Takaori K. Pancreatic cancer. Lancet. 2016 Jan 29. pii: S0140-6736(16)00141-0 DOI: 10.1016/S0140-6736(16)00141-0
- Кубышкин В.А., Вишневский В.А. Рак поджелудочной железы -М.: Медпрактика. -2003. -375 с.
- Lygidakis N.J., Sgourakis G., Georgia D. et al. Regional targeting chemo-immunotherapy in patients undergoing pancreatic resection in an advanced stage of their disease: a prospective randomized study//Ann. Surg. -2002. -Vol. 236,№6.-P. 806-813.
- Bramhall S.R., Allum W.H., Jones A.G. et al. Treatment and survival in 13.560 patients with pancreatic cancer and incidence of the disease in the West Midlands: An epidemiological study//Br. J. Surg. -1995. -Vol. 82. -P 111-115.
- Sohn T.A., Yeo C.J., Cameron J.L. et al. Resected adenocarcinomas of the pancreas -616 patients: Results, outcome, and prognostic indicators//J. Gastrointest. Surg. -2000. -Vol. 4. -P 567-579.
- Beger H.G., Gansauge F., Biichler M.W., Link K.H. Intraarterial adjuvant chemotherapy after pancreaticoduodenectomy for pancreatic cancer: Significant reduction in occurrence of liver metastasis.//World J. Surg. -1999. -Vol.23.-P946-949.
- Гранов А.М. Обоснование к внутрипортальному введению масляного рентгеноконтрастного вещества при портогепатографии//JI. -1970. -автореф. дисс.. докт.мед.наук. -36 с.
- Гранов Д.А., Таразов П.Г. Рентгеноэндоваскулярные вмешательства в лечении злокачественных опухолей печени -СПб.: ИКФ «Фолиант». -2002.-288 с.


