Применение нестероидного противовоспалительного препарата нимесулид в ревматологической практике
Автор: Матчанов С.Х.
Журнал: Juvenis scientia @jscientia
Рубрика: Медицинские науки
Статья в выпуске: 2, 2016 года.
Бесплатный доступ
Целью настоящего исследования явился сравнительный анализ действия нестероидных противовоспалительных препаратов диклофенака («Диклоберла») и нимесулида («Нимесила»). Отмечены их положительные качества, побочные реакции и осложнения терапии. Проанализированы особенности нестероидного противовоспалительного препарата (НПВП) нового типа - нимесулида, селективно ингибирующего циклооксигеназу-2. Препарат создан на основе новых представлений о механизме действия НПВП на воспалительный процесс.
Ревматология, нестероидные противовоспалительные препараты, побочные эффекты, простагландины, циклооксигеназа, нимесулид
Короткий адрес: https://sciup.org/14110213
IDR: 14110213
Application of nonsteroidal antiinfalammation drug nimesulid in rheumatological practice
The aim of the study was to analyze the effects of nonsteroidal anti-inflammatory drugs (NSAID) - diclofenac (“Dicloberl”) and nimesulid (“Nimesil”). Their favorable qualities, side effects and complications of therapy are noted. Features of the new type of NSAID, nimesulid, which selectively inhibits the enzyme cyclooxygenase-2, are described. This agent was created based on the recently described mechanisms of NSAIDs action on the inflammatory process.
Текст научной статьи Применение нестероидного противовоспалительного препарата нимесулид в ревматологической практике
Нестероидные противовоспалительные препараты (НПВП) представляют собой класс лекарственных средств, терапевтическая активность которых связана с предотвращением развития или снижением интенсивности воспаления. В настоящее время существует не менее 50 различающихся по химической структуре лекарственных форм, классифицируемых как НПВП [1-6]. Они являются одними из наиболее часто используемых в клинической практике лекарственных средств. Наиболее широко НПВП применяются в ревматологической практике [3, 7].
Известно, что длительный прием НПВП оказывает неблагоприятное воздействие на слизистую желудочно-кишечного тракта (ЖКТ), которые в целом встречаются примерно у 2540% больных, а в 5% случаев представляют серьезную угрозу для жизни пациентов. Поэтому в последние годы большое внимание уделяется проблеме безопасности применения НПВП [1, 8-10].
В 1994 г. J. Vane сформулировал гипотезу, согласно которой противовоспалительное, анальгетическое и жаропонижающее действие НПВП связано с их способностью ингибировать циклооксигеназу-2 (ЦОГ-2), в то время как наиболее часто встречающиеся побочные эффекты (поражение ЖКТ, почек, нарушение агрегации тромбоцитов) – с подавлением активности ЦОГ-1. В то же время, на основании расшифровки локализации и генетической регуляции и особенно структуры ЦОГ-1 и ЦОГ-2, созданы теоретические предпосылки для создания нового класса НПВП со способностью селективно ингибировать ЦОГ-2, применение которого позволит повы- сить безопасность лечения ревматических заболеваний [2-4, 7, 9, 11, 12].
В последние годы синтезированы несколько веществ с подобными фармакологическими свойствами, которые обладают высокой противовоспалительной и минимальной ульцеро-генной активностью. Среди них нимесулид зарекомендовал себя как весьма эффективный и малотоксичный НПВП [5, 8].
Форма выпуска препарата «Нимесил» – гранулы для приготовления суспензий для приема внутрь, в пакетиках по 2 г, содержащих 100 мг активного вещества – нимесулида. Ниме-сулид (4-нитро-2-феноксиметансульфонанилид) является селективным ингибитором ЦОГ-2.
Материал и методы исследования
Нами была изучена эффективность «Нимесила» у 45 больных, с достоверно установленным диагнозом по критериям института ревматологии Российской академии медицинских наук. Для исследования подобраны больные с отягощенным желудочно-кишечным анамнезом. Больные распределялись следующим образом: 10 больных ревматоидным артритом, 10 больных реактивным артритом, 10 больных анкилозирующим спондилоартритом и 15 больных псориатическим артритом.
Контрольную группу составили по 10 больных с каждой нозологической единицей. Больные контрольной группы в качестве нестероидного противовоспалительного препарата принимали диклофенак («Диклоберл») в дозе 100 мг в сутки.
Все больные для базисной терапии принимали таблетки делагил в дозе 250 мг в сутки.
Исследование проводилось на базе Республиканского ревматологического центра СКАЛ, а также в ревматологическом отделении клиники II ТашГосМИ.
Клинически у всех больных оценивались следующие показатели: боль в суставах (в баллах), суставной индекс Ричи (в баллах), количество воспаленных суставов, сила сжатия кистей (в мм. рт. ст.), тест Ли (в баллах). Больным анкилозирующим спондилоартритом дополнительно определяли симптомы Форестье, «нитки», Шобера, Отто, Томаера, Кушелевского.
Помимо этого, оценивались данные лабораторно-инструментальных методов исследования: общего анализа крови, общего анализа мочи, уровни C-реактивного белка и ревматоидного фактора, данные магнитно-резонансной томографии суставов.
Всем больным кроме клинико-инструментального и лабораторного обследования, проводили определение фенотипа гаптоглобина (Нр) методом дискового электрофореза в полиакриламидном геле по Devis в модификации Н.А. Осиной [12].
Определение распределения фенотипов Нр показало, что среди больных с острым течением реактивного артрита значительно чаще встречались лица с фенотипом Нр 2-1, а при хроническом варианте отмечалась высокая частота фенотипа Нр 2-2. Высокая частота фенотипа Нр 2-2 наблюдалась также у больных анкилозирующим спондилоартритом.
Особое место при оценке результатов исследования занимала эзофагогастродуоденоскопия (ЭГДС), которая проводилась до и после лечения. ЭГДС позволила объективно контролировать действие препарата на ЖКТ.
Больные, получавшие стационарное лечение в ревматологическом отделении, продолжали амбулаторное лечение в течение одного месяца в ревматологическом центре СКАЛ. Таким образом, сроки лечения больных составили 40-45 дней. Комплекс клинико-лабораторных и инструментальных исследований проводился до и после лечения.
Препарат «Нимесил» назначали 2 раза в день, по 100 мг активного вещества (нимесулид).
Больные контрольной группы вместо «Нимесила» получали диклофенак («Диклоберл») в таблетках по 100 мг в сутки.
Статистический анализ проводили с помощью пакета прикладных программ Statistica 8.0 (StatSoft Inc., США). Результаты представлены в виде средних значений и средних квадратических отклонений (М±SD) для количественных признаков. В процессе статистической обработки данных применяли методы описательной статистики, для сравнения двух независимых групп – критерий Манна–Уитни, для оценки значимости изменений показателей – критерий Уилкоксона. Различия считали достоверными при р<0,05.
Результаты
В таблице 1 приводятся результаты проведенного лечения у больных ревматоидным артритом.
Таблица 1
Динамика клинико-лабораторных показателей у больных ревматоидным артритом
|
Показатели |
Нимесулид |
Диклофенак |
||
|
До лечения |
После лечения |
До лечения |
После лечения |
|
|
Утренняя скованность (мин.) |
188,5±15,6 |
66,1±8,2* |
186,4±14,9 |
61,5±9,1* |
|
Индекс Ричи (баллы) |
21,3±1,2 |
7,8±0,9* |
22,1±1,1 |
8,1±0,8* |
|
Число воспаленных суставов |
6,2±0,4 |
1,1±0,2* |
6,1±0,3 |
1,4±0,2* |
|
Тест Ли (баллы) |
12,3±1,1 |
6,3±0,7* |
12,9±1,2 |
5,6±0,6* |
|
СОЭ (мм/ч) |
34,6±2,8 |
18,6±1,9* |
32,9±2,9 |
17,9±1,6* |
|
Боль в эпигастрии |
4,8±0,6 |
4,6±0,4 |
4,7±0,8 |
8,1±0,7* |
|
Изжога |
6,2±0,8 |
6,3±0,3 |
6,6±0,7 |
7,2±0,9 |
Примечание: * – статистическая значимость различий показателей до и после лечения.
Из данных, приведенных в таблице, видно, что препарат нимесулид по своей эффективности сравним с диклофенаком. В то же время у больных, принимавших диклофенак, отмечено увеличение частоты побочных реакций со стороны ЖКТ, таких как, боль в эпигастрии и изжога с 4,7±0,8 до 8,1±0,7 и 6,6±0,7 до 7,2±0,9 соответственно. Результаты ЭГДС также показали отрицательную динамику у больных, принимавших диклофенак, – обострение язвенной болезни двенадцатиперстной кишки у 7,5% больных, у 5% больных – появление эрозий в двенадцатиперстной кишке.
Аналогичный анализ был проведен в группе больных реактивным артритом. Эти пациенты в качестве антибактериальной терапии получали тетрациклин по 2 грамма в сутки. Результаты приведены на рисунке 1.
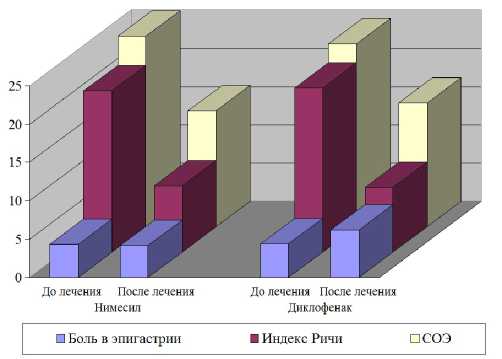
Рис. 1. Динамика клинико-лабораторных показателей у больных реактивным артритом
Представленные данные демонстрируют, что у больных, принимавших нимесулид, после лечения частота боли в эпигастрии не имела тенденции к увеличению. В то же время у больных, получавших диклофенак, после лечения боли в эпигастральной области отмечались более часто. Данные ЭГДС подтвердили субъективные жалобы со стороны органов ЖКТ.
Аналогичные данные получены у больных анкилозирующим спондилоартритом и псориатическим артритом.
Заключение
Результаты проведенного исследования позволяют обсудить один из сложных вопросов терапии ревматологических больных – соотношение пользы и риска применения НПВП, т.е. степень эффективности и безопасности в отношении развития побочных явлений со стороны ЖКТ. Можно утверждать, что полученные данные свидетельствуют о возможности использования «Нимесила» в широкой клинической практике. Доказанная высокая противовоспалительная активность «Нимесила», проявившаяся в уменьшении болевого синдрома со стороны суставов, и отсутствие значимого неблагоприятного влияния на ЖКТ позволяют сделать заключение, что препарат может быть применен в лечении различных ревматологических заболеваниях, даже при наличии желудочно-кишечных заболеваний (хронический гастрит, язвенная болезнь в фазе ремиссии).
Таким образом, применение нимесулида, селективного ингибитора ЦОГ-2, в широкой ревматологической практике позволяет повысить эффективность лечения и снизить риск развития побочных реакций со стороны ЖКТ.
Список литературы Применение нестероидного противовоспалительного препарата нимесулид в ревматологической практике
- Бунчук Н.В. Нестероидные противовоспалительные средства в лечении ревматоидного артрита/Бунчук Н.В.//Клин. фармакология и тер. -1993. -Т.З. -№1. -С.42-43
- Насонова В.А., Сигидин Я.А. Патогенетическая терапия ревматических заболеваний. М. 1985
- Насонов Е.Л. Нестероидные противовоспалительные средства. М. 2000: 143 с
- Насонова В.А., Бунчук Н.В. Ревматические болезни. Под ред. В.А. Насоновой, Н.В. Бунчука. -М.: Медицина. 1997: 520 с
- Vane J. Towards a better aspirin//Nature.-1994.-Vol. 367.-P. 215-216
- Geise J., Mc Donald J.J., Hauser S.D. et al. A Single Amino Acid Difference between Cyclooxygenase-1 (COX-1) and -2 (COX-2) Reverses the Selectivity of COX-2 Specific Inhibitors//J. Biol. Chem. -1996. -Vol. 271. -P. 15810-15814
- Kurumban R. G., Sievens AM, Gierse J. K. et al. Structural basis for selective inhnbition of cyclooxygenase-2 by anli -inflammatory agents//Nature. -1996. -Vol. 384. -P. 644-648
- Клиническая ревматология: рук. для практ. врачей/ред. В. И. Мазуров. -СПб.: Фолиант, 2001. -416 с.
- Clements P. J., Paulus H. E. Textbook of Rheumatology/Eds V.N. Kelli et al. -Philadelphia, 1993. -Vol. 1. -P. 700-730
- Hardin J.G., Longenecker G.L. Handbook of Drug Therapy in Rheumatiс Disease: Pharmacology and Clinical Aspect. -Boston, 1992
- Vane J.R., Botting R.M. Selective COX-2 Inhibitors. Pharmacology, Clinical Effects and Therapeutic Potential/Eds J. Vane J., Botting. -Boston, 1997. -P. 1-17
- Осина Н. А. Унификация результатов электрофореза белков сыворотки крови в полиакриламидном геле//Лаб.дело.-1982.-№ 8.-С.463-466


