Применение перфорированного низкотемпературного термопластика при лечении гнойных заболеваний кисти
Автор: Крайнюков П.Е., Кокорин В.В., Колодкин Б.Б., Сафонов О.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 2 т.12, 2017 года.
Бесплатный доступ
Представлен опыт лечения 43 больных с гнойными заболеваниями кисти. По нозологической форме 39 случаев - флегмоны кисти, 4 - случая костного панариция. Всем больным проведено оперативное лечение, применена функциональная иммобилизация кисти перфорированным термопластиком (поликапролактоном), что позволило создать оптимальные условия для заживления послеоперационных ран, избежать осложнений, уменьшить сроки пребывания в стационаре и обеспечить максимально быструю реабилитацию. Во всех наблюдениях достигнут хороший результат.
Гнойные заболевания кисти, флегмона, хирургическая инфекция, хирургическое лечение, иммобилизация, поликапролактон, термопластик
Короткий адрес: https://sciup.org/140188674
IDR: 140188674 | УДК: 617.576:616-002.3:615.832.9
Use of low-temperature perforated thermoplastic at treatment of purulent hand diseases
Experience in treatment of 43 patients with purulent diseases of the hand was analysed. Nosology was presented by 39 cases of brush phlegmon and 4 cases of felon. All patients underwent surgery with functional immobilization of brush by perforated thermoplastic (polycaprolactone), thereby creating optimal conditions for the healing of surgical wounds. Method of immobilization permits to avoid complications in the treatment of patients with purulent hand diseases, to reduce the length of stay, to create optimal conditions for wound toilet, the fastest recovery and rehabilitation. All cases had a good outcome.
Текст научной статьи Применение перфорированного низкотемпературного термопластика при лечении гнойных заболеваний кисти
Известно, что воспаление, как патофизиологическое явление, отражает специфическое взаимодействие между микро- и макроорганизмом. Однако в современной трактовке патогенеза гнойного воспаления (включая панариций и флегмону кисти) предпочтение отдается этиологическому (микробному) фактору. Отсюда и односторонняя этиологическая ориентация современных методов лечения очаговой гнойной инфекции. Наблюдаемые в очаге воспаления патологофизиологические изменения объясняются исключительно биохимическими качествами патогенных микроорганизмов; при этом явно недооценивается значение тканевой среды, в которой они проявляются. Этиологический фактор имеет активизирующее значение в развитии воспаления только в начальном периоде его формирования; в последующем динамика происходящих изменений обусловливается структурой и составом пораженных тканей [6, 7, 10].
В ликвидации воспалительного процесса большое значение в настоящее время придается медикаментозной терапии с использованием комплекса химиопрепаратов, физических методов воздействия на гнойную рану [12, 13].
Комплексный подход в лечении гнойных заболеваний кисти, складывается из последовательных и преемственных этапов лечения: диагностического, аналитического, оперативного, послеоперационного, реабилитационного. Залогом успеха в лечении гнойных заболеваний кисти остается своевременное и адекватное оперативное вмешательство, при этом правильный доступ к гнойному очагу определяет благоприятный исход [11, 14].
Оценивая системный подход к лечению гнойных заболеваний кисти, мы обратили внимание на редкое использование, а чаще – неиспользование иммобилизации поврежденного гнойным процессом сегмента конечности. Большинство хирургов сдержанно относятся к иммобилизации в лечении гнойных заболеваний кисти и применяют ее только при выраженном воспалении и отеке, явлениях лимфангита. При положительной динамике в первые дни лонгету снимают, чтобы начать раннюю реабилитацию, памятуя о том, что восстановление функции пальцев кисти после неподвижности физически и психологически проходит более длительно. В связи с этим ограничиваются марлевым бинтованием кисти или не используют иммобилизацию вовсе [1, 2, 5] Напротив, другие специалисты считают отсутствие иммобилизации наиболее часто допускаемой ошибкой при лечении панариция и флегмоны кисти, в то время как оперированная кисть во всех случаях нуждается в обездвиживании в среднем на 4–5 суток, т.е. на весь острый период течения раневого процесса. Целесообразность покоя оправдана созданием субъективных, более комфортных условий лечения, важностью поддержания производственной и социальной активности пациента на период болезни. По установленным данным, иммобилизация кисти при гнойно-воспалительных заболеваниях кисти обеспечивается примерно у 40% нуждающихся в ней пациентов [9].
На наш взгляд, соблюдение принципов и правил иммобилизации является важным элементом в лечении и всегда должно сопровождать оперативное вмешательство на кисти. Иммобилизация необходима не только для создания покоя пораженной кисти, но и для предупреж-

дения порочного положения пальцев в послеоперационном периоде, уменьшения болевой реакции, улучшения периферического кровообращения, защиты органа от неблагоприятных внешних воздействий, улучшения иммуно-биологического статуса воспаленных тканей.
Иммобилизация конечностей, в настоящее время, в основном применяется при лечении травм, поражений и их последствий, при этом используют различные средства – гипсовые повязки, синтетические полимеры, а в последнее время – матерчатые и биокомпозитные ортезы [3, 4]. Основываясь на успешном опыте применения современных материалов в травматологии и ортопедии, нами разработан и применен способ функциональной иммобилизации низкомолекулярным перфорированным термопластиком поликапролактоном в лечении гнойных заболеваний кисти.
Характеристика примененной технологии
Принцип действия иммобилизации основан на свойстве поликапролактона (полимера ε -капролактона – биоразлагаемого полиэфира с низкой температурой плавления) становиться пластичным при разогревании в диапазоне температур от 70° до 100° С (рис. 1). Ослабление связей между цепочками молекул материала позволяет придать изделию любую форму. По мере остывания до 35–40° С, прочность между молекулами восстанавливается, возвращая прежнюю жесткость вновь созданному ортезу.
Особенностями технологии являются:
-
1) высокая скорость иммобилизации;
-
2) скорость разогревания и затвердевания материала может варьировать от нескольких секунд до минут, в зависимости от температуры воды, используемой для размягчения термопластика. В горячей воде разогретый материал может находиться несколько часов без потери эксплуатационных свойств;
-
3) полиуретановое покрытие (рис. 2) исключает прилипание материала к рукам врача и коже пациента, склеивание листов между собой;
-
4) пластическая память формы поликапролактона, при повторном разогревании обеспечивает листу его первоначальный вид, что позволяет выполнять многократное моделирование повязки даже после ее полного затвердевания, в соответствии с клинической ситуацией;
-
5) высокая прочность изделия не теряется даже при растяжении листа до 15% от первоначального размера, а выполнение ортезирования непосредственно на пациенте позволяет достичь идеальной конгруэнтности повязки и поверхности сегмента конечности;
-
6) термопластик не требует специальных условий его хранения, заводских мощностей, специального инструментария или станков для изготовления иммобилизирующей повязки;
-
7) сегменты конечностей в ортезах доступны рентгенографическому и/или ультразвуковому исследованию,
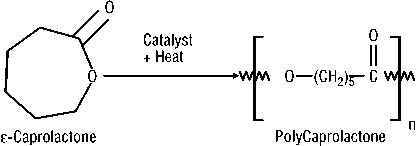
Рис. 1. Процесс полимеризации термопластика (Цит. по «Низкотемпературный термопластик Передовые технологии индивидуального ортезирования». СПб.: РосИмп, 2014)

Рис. 2. Внешний вид листов перфороированного термопластика толщиной от 0,8 до 5 мм. Сторона изделия, прилегающая к коже, покрыта полиуретаном поскольку и поликапролактон, и полиуретан проницаемы для рентгеновских лучей и УЗ-волн;
-
8) наложение непосредственно на кожу без использования подкладочного материала, позволяет проводить повторные перевязки, не снимая иммобилизацию.
Совмещение свойств поликапролактона и полиуретана в сочетании с перфорацией дает:
-
• исключительно малая масса (около 100–200 грамм) с толщиной стенки 3 мм;
-
• значительную прочность, гипоаллергенность и биосовместимость с тканями пациента;
-
• обеспечивает вентиляцию кожного покрова за счет воздушной прослойки в ячейках полиуретана и через вентиляционные отверстия перфорации. Достаточные воздухо- и влагообмен обеспечивают предотвращение мацераций кожного покрова.
Материал легко подвергается гигиенической обработке, позволяет проводить перевязки, туалет раны, не снимая повязки. Высокая прочность, малый вес, моделирование повязки и ее эстетичный вид, позволяют пациенту вести обычный образ жизни, выполнять свою работу, водить автомобиль и т.д., сохраняют его социальную адаптацию. Снятие повязки выполняется практически моментально, без специального оборудования и меди-
цинских инструментов и может быть временным (например, для выполнения физиотерапевтических процедур, лечебной физкультуры) или окончательным [5, 7].
Материалы и методы
В отделениях гнойной хирургии ведомственных многопрофильных стационаров проведено лечение 43 больных с гнойными заболеваниями кисти. Большая часть – 31 человек (72%) это мужчины до 40 лет, занимающиеся физическим трудом, что явилось первопричиной микротравматизации, а несвоевременное обращение и в некоторых случаях нерациональное лечение – привели к распространению гнойно-воспалительного процесса кисти. Женщины составили всего 7 случаев (28%), трав-матизация была вызвана: средствами бытового предназначения (иглы, маникюрные приборы и пр.), укусами животных, производственными травмами. Данные о распределении пациентов по нозологии и полу представлены в табл. 1.
К диагностике и лечению гнойных заболеваний кисти применяли выработанный ранее стандартизированный комплексный подход. Внимание уделяли этиологическому фактору возникновения гнойного про-
Табл. 1. Распределение пациентов с гнойно-воспалительными заболеваниями кисти по нозологии и полу
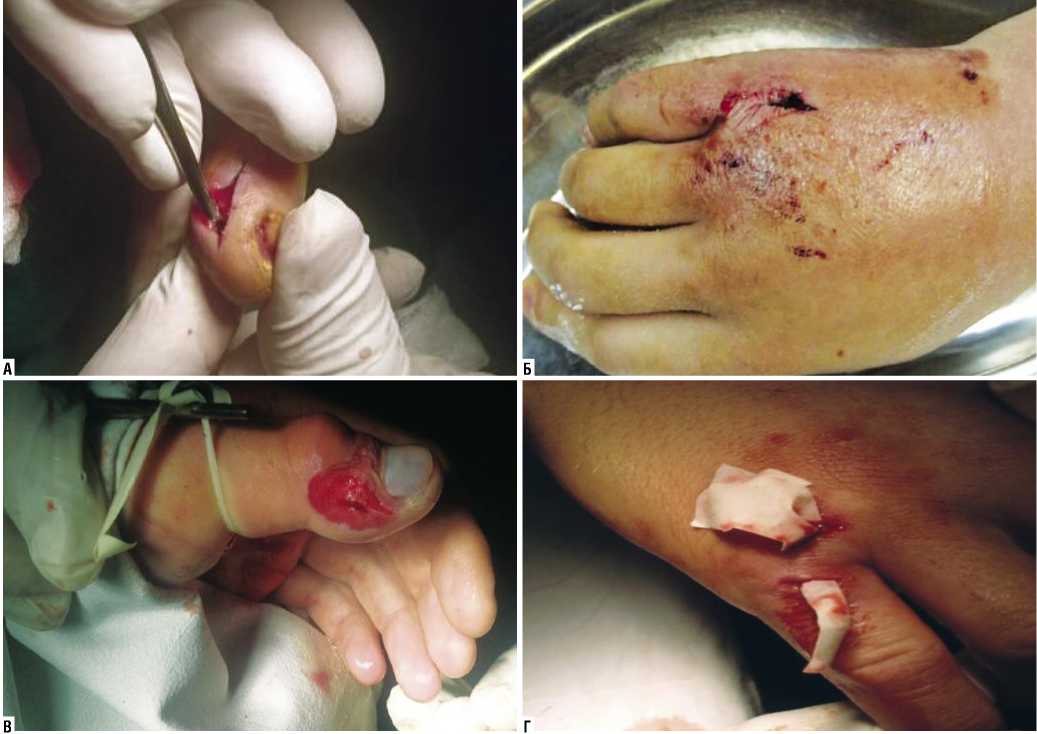
Рис. 3. Лепестковые разрезы. А – больной Д., 35 лет: костный панариций 2-го пальца правой кисти; Б – больной Г., 40 лет: U-образная флегмона правой кисти; В – больной С., 20 лет: подкожный панариций 1-го пальца левой кисти; Г – больной Ф., 23 года: флегмона правой кисти

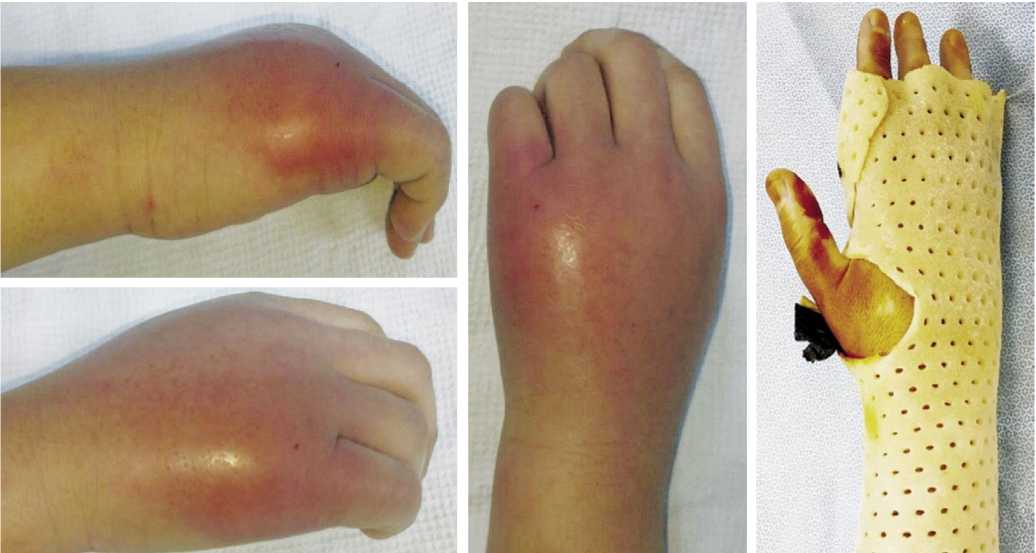
Рис. 4. Больной М. 42 лет. U-образная флегмона правой кисти. Послеоперационная иммобилизация термопластиком
аспирации. Рану обильно промывали антисептическими растворами. Дренирование проводили по общим принципам. Накладывали повязку с водорастворимой мазью. Перевязки с обработкой ран антисептиками проводили до их полного заживления.
На заключительном этапе операции выполняли функциональную иммобилизацию кисти перфорированным низкотемпературным термопластиком (поликапролактоном), оставляя доступ к ране и дренажам для проведения последующей санации (рис. 4). Наложение и моделирование термопластика выполняли, в некоторых случаях непосредственно на кожу, в некоторых – поверх асептической повязки. Кисти придавали функционально выгодное положение. С первых часов назначали антибиотики широкого спектра действия, чувствительные к грамотрицательной и нозокомиальной флоре [6]. Во всех случаях выполняли посевы отделяемого на микрофлору и чувствительность к антибиотикам. Антибактериальную терапию меняли на тропную, в зависимости от полученных результатов.
В тех случаях, когда иммобилизацию из термопластика накладывали непосредственно на кожу, все необходимые манипуляции выполняли, не снимая иммобилизующую повязку с кисти. В случаях, когда термопластик накладывали поверх повязки, иммобилизация, имея свои конструктивные особенности, легко позволяла снять и одеть ее, сохранив кисть в заданном положении (рис. 5). По нашему мнению, это позволяет снизить частоту развития послеоперационных ретракционных осложнений кисти (контрактур, анкилозов, фиброзов и т.д.), при этом промывание ран антисептическими растворами в
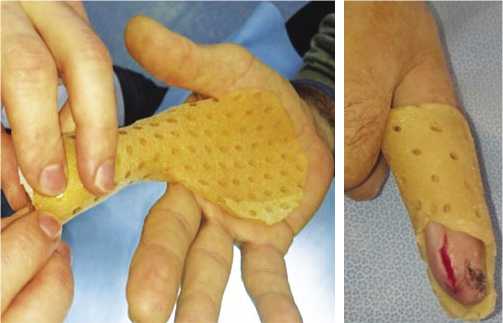
Рис. 5. Больной П. 58 лет. Костный панариций 2-го пальца правой кисти, 4-е сутки после операции, иммобилизация термопластиком необходимом количестве не меняет физических свойств термопластика, сохраняются упругость, жесткость, вес, память формы. Перфорированные отверстия позволяют своевременно эвакуировать скопление любого отделяемого, обеспечивают доступ воздуха и препятствуют возникновению кожных проявлений (вторичного воспаления, мацерации, опрелостей).
Длительность раневого процесса, в среднем, составила 7–9 суток до закрытия раны. В этот период со стороны мягких тканей формировалась демаркационная зона. По мере очищения, рана заполнялась грануляционной тканью, объем гнойной полости уменьшался, дренажи удаляли (рис. 6 ).

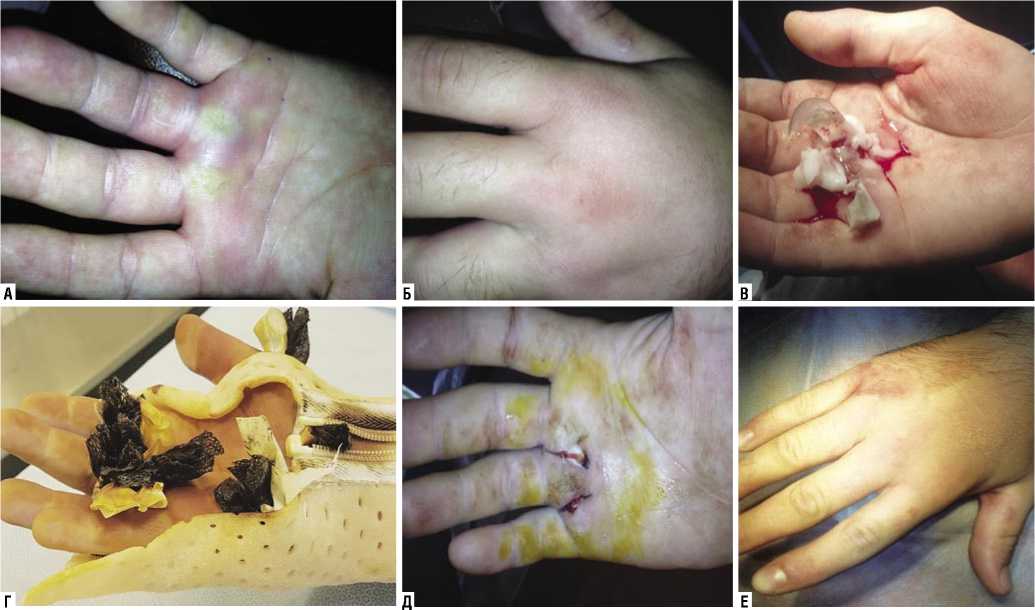
Рис. 6. Больной К., 21 год. Флегмона правой кисти. А, Б – при поступлении; В – вскрытие, дренирование; Г – иммобилизация термопластиком, Д, Е – 6-е сутки после операции
После стихания воспалительных явлений в ране – отека, экссудации – термопластическая повязка, благодаря легкости, прочности и мобильности позволяет начать раннюю функциональную реабилитацию, что также положительно влияет на исход лечения.
Таким образом, особенности этого материала заключаются в том, что иммобилизация осуществляется быстро и удобно, с фиксацией конечности в функционально выгодном положении; термопластик не прилипает к рукам врача, кожному и волосяному покрову пациента, позволяет проводить необходимые манипуляции в послеоперационном периоде без снятия и повторного наложения, рентгенконтрастен, обеспечивает перфузию воздуха, гипоаллергенен, не вызывает кожно-воспалительных явлений, обладает гидрофобностью, способствует сохранению мышечного тонуса, улучшению кровоснабжения и, как следствие, более быстрому снятию отека и болевого синдрома, сокращению сроков нетрудоспособности и более быстрому выздоровлению пациентов; также к достоинствам можно отнести его легкость и эстетический эффект.
Приводим клинические наблюдения
Больной Д., 64 лет, поступил в ЦВКГ им. П.В. Ман-дрыка с диагнозом: Костный панариций второго пальца левой кисти. Повредил палец на даче металлической стружкой, лечился самостоятельно. За медицинской помощью обратился в медицинское учреждение по месту жительства спустя трое суток с момента травмы, после появления отека, пульсирующих ночных болей во втором пальце правой кисти. Выполнено вскрытие, дренирование гнойника. Медикаментозное лечение по стандартной схеме. Рана зажила вторичным натяжением, выписан с выздоровлением. Спустя два месяца c момента травмы обратился с жалобами на вновь возникший отек второго пальца, ограничение движений в межфаланговых суставах, постоянные ноющие боли во втором пальце средней интенсивности. Осмотрен, выполнена R-графия, диагностирован костный панариций. Лепестковый разрез, дренирование гнойника, секвестрэктомия. Проведена комплексная терапия по разработанной методике с использованием функциональной иммобилизации перфорированным термпо-ластиком. Выписан с выздоровлением на 10-е сутки, приступил к работе (рис. 7).
Больная В., 21 год, поступила в ЦВКГ им. П.В. Ман-дрыка с диагнозом: остеомиелит ногтевых фаланг 3-го, 4-го пальцев правой кисти, инфицированные вяло-гранулирующие раны 3-го, 4-го пальцев правой кисти (рис. 8).
Травму получила на производстве при попадании в станок правой кисти. Неотложная помощь оказана в медсанчасти, выполнена ПХО, профилактика столбняка (АСС, ПСС). Проводилась антибактериальная терапия, перевязки. Послеоперационный период осложнился инфицированием раневых поверхностей.
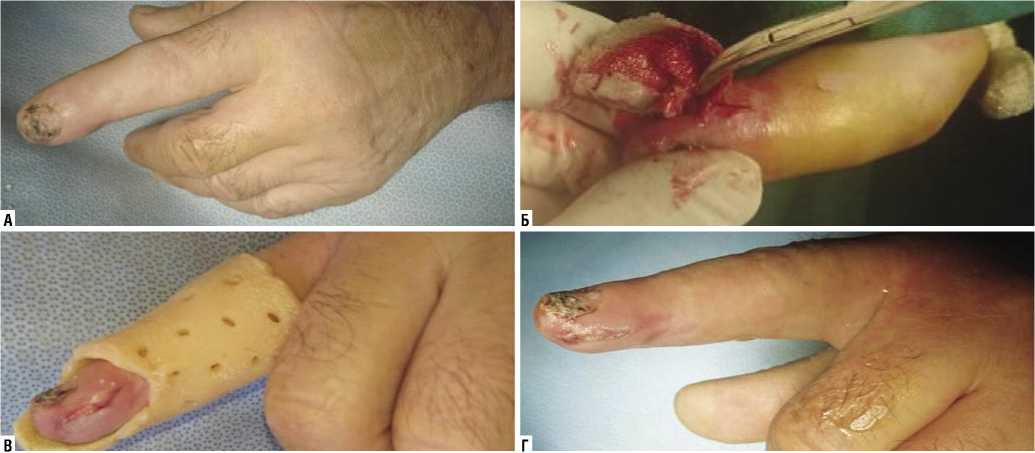
Рис. 7. А – внешний вид 2-го пальца при поступлении; Б – хирургическая обработка раны, лепестковый разрез; В – сутки после операции, гранулирующаяся рана, иммобилизация перфорированным термопластиком; Г – 7-е сутки после операции, заживление вторичным натяжением
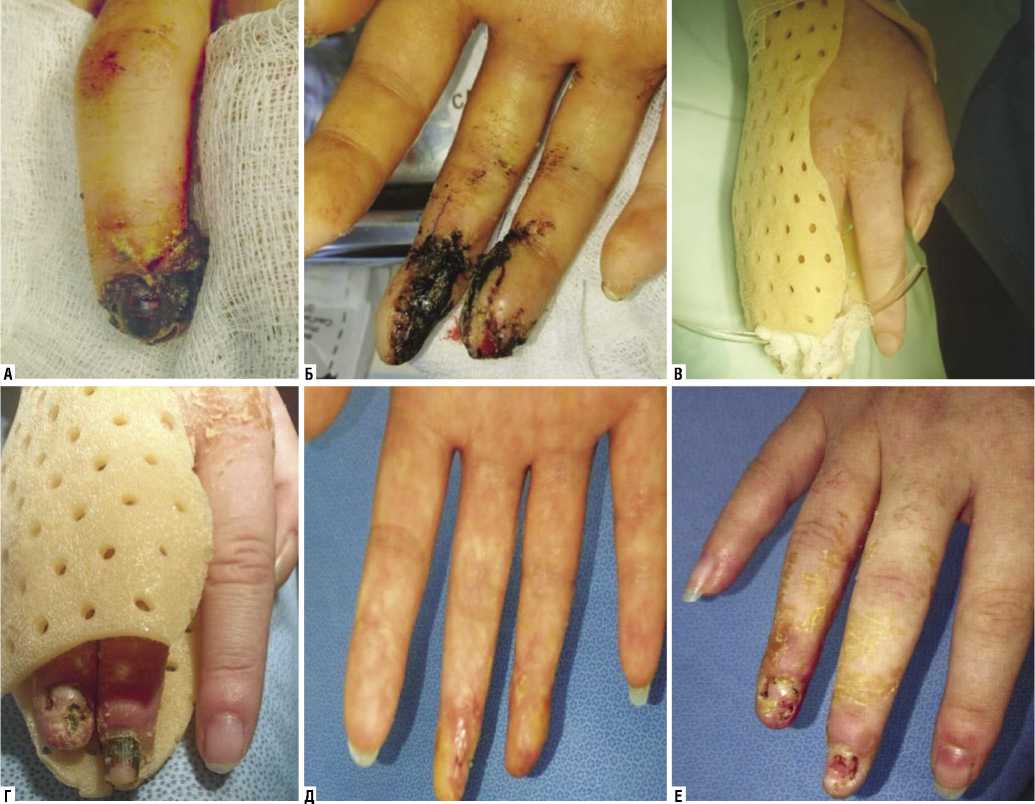
Рис. 8. А, Б – внешний вид пальцев кисти при поступлении; В, Г – проведение туалета ран иммобилизированной кисти; Д, Е – исход лечения, вторичное заживление ран пальцев кисти
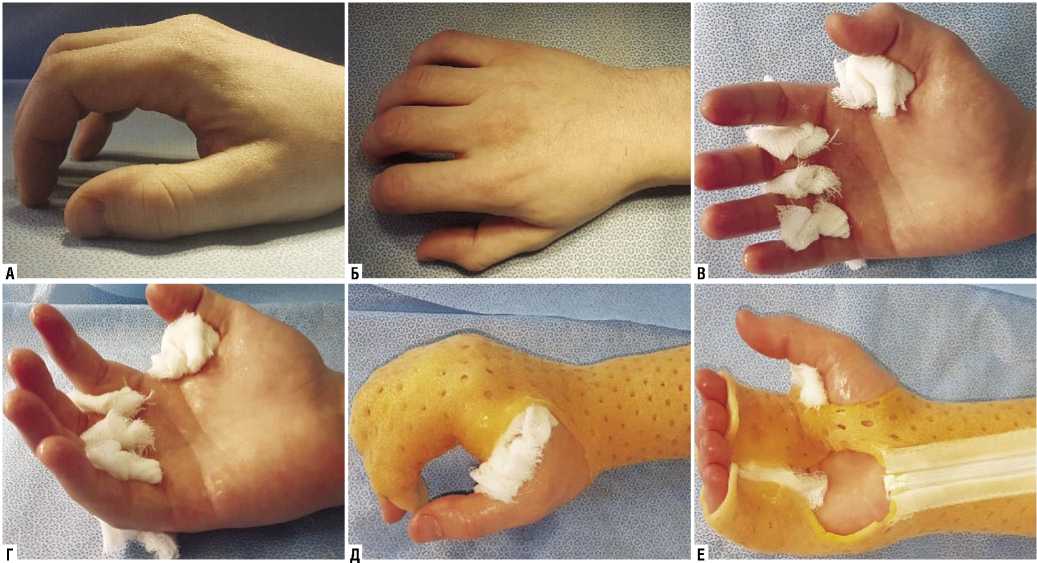
Рис. 9. А, Б – физиологическое положение кисти; В, Г – межпястные салфетки; Д, Е – положение кисти в повязке Турбокаст, возможность свободного доступа при санации
Дальнейшее лечение проводилось в ЦВКГ им. П.В Мандрыка. Выполнена R-графия кисти, диагностированы секвестры ногтевых фаланг обоих пальцев кисти. Проведена повторная хирургическая обработка ран, секвестрэтомия. Комплексное лечение по принятой схеме: местные и системные противовоспалительные, антибактериальные препараты, средства, улучшающие регионарное кровообращение и микроциркуляцию, иммуномодуляторы, лимфотропная и корригирующая терапия. Функциональная иммобилизация перфорированным термопластиком в течение 6 недель.
На фоне проводимого лечения раны очистились, заживлены вторичным натяжением. Функция кисти восстановлена, приступила к работе.
Обсуждение
Иммобилизация кисти в лечении гнойных заболеваний кисти остается на сегодняшний день спорным вопросом, различие взглядов обусловлено не только отсутствием широкого распространения и использования современных синтетических материалов, но и уверенностью ряда авторов в бессмысленности иммобилизации при лечении гнойных заболеваний кисти. Полученные нами результаты показывают иное – знание и соблюдение принципов иммобилизации и фиксации кисти дают преимущества в лечении и восстановлении функции кисти пациента. В разработанной системе комплексного подхода лечения данной патологии соблюдение этих принципов считается нами обязательным.
Принципы иммобилизации и фиксации кисти:
-
1) иммобилизация проводится после обработки кожи кисти и выполнения необходимых лечебных мероприятий;
-
2) кисти придают функционально выгодное положение (рис. 9 А, Б);
-
3) во избежание сморщивания межпястных связок пальцы раздвигают салфетками, ось пальцев направляют к шиловидному отростку лучевой кости (рис. 9 В, Г);
-
4) независимо от анатомической локализации воспалительного очага, обеспечение покоя необходимо для всей кисти, так как пальцы руки анатомически и функционально взаимосвязаны;
-
5) при тяжелых повреждениях и гнойных заболеваниях кисти иммобилизуют запястье, предплечье и локоть;
-
6) иммобилизация не должна препятствовать проведению регулярной санации ран, физиотерапевтическим процедурам, лечебной физкультуре (рис. 9 Д, Е);
-
7) иммобилизация продолжается пока не стихнет воспалительный процесс и дает возможность ранней активной разработки движений пальцев и кисти, способствует полноценному восстановлению функции кисти.
-
9. Усольцева Е.В., Машкара К.И. Хирургия заболеваний и повреждений кисти. – 3-е изд.,.- Л.: Медицина, 1986. – 352 с.
-
10. Фишман Л.Г. Клиника и диагностика заболеваний пальцев и кисти. – 1963.
– 391 с.
-
11. Lucas S. Mc Donald, Mary F. Bavaro, Eric P. Hofmeister, Leo T. Kroonen / Hand infections / J Hand Surg Vol 36A, August 2011, P. 1403–1412.
-
12. Meredith Osterman, Reid Draeger, Peter Stern, / Acute Hand infections
-
/ J Hand Surg Am. r Vol. 39, August 2014 P. 1628–1635.
-
-
13. Orrin I. Franko, MD, Reid A. Abrams, MD, Hand Infections, Orthopedic Clinics of North America, Volume 44, Issue 4, October 2013, P. 625–634.
-
14. Turker et al., Hand infections: a retrospective analysis. 2014, PeerJ 2:
Заключение
Иммобилизация является одним из этапов комплексного лечения гнойных заболеваний и повреждений кисти, и сочетается с другими лечебными мероприятиями, чаще всего с лечебной гимнастикой и физиотерапией.
Неправильно наложенные, обременительные иммобилизующие повязки на кисти и пальцах не только осложняют течение патологического процесса, но нередко являются причиной некроза мягких тканей, требующего длительного лечения, и стойких контрактур.
e513; DOI10.7717/peerj.513.
При иммобилизации нужно учитывать, что на кисти нет мощного массива мышц, поэтому не следует накладывать тяжелых, многослойных, обременительных повязок.
Иммобилизирующие повязки всегда индивидуальны, должны быть заранее продуманы и подготовлены с целью обеспечения свободного доступа к ране для ее санации и, в то же, время – надежной фиксации пораженной кисти.
Таким образом, способ функциональной иммобилизации перфорированным термопластиком позволил избежать развития осложнений в лечении пациентов с данной патологией, уменьшить сроки пребывания в стационаре, создать оптимальные условия для проведения санации ран, способствуя максимально быстрой реабилитации, не причиняя неудобств, возникающих при других способах иммобилизации.
Список литературы Применение перфорированного низкотемпературного термопластика при лечении гнойных заболеваний кисти
- Абаев Ю.К. Хирургическая повязка. -Минск: Беларусь, 2005. -150 с.
- Аничков И.П., Волкова К.Г., Гаршин В.Г. Морфология заживления ран. -М.: Медгиз, 1951. -123 с.
- Баиндурашвили А.Г., Афоничев К.А., Попов И.В. и др./Опыт применения синтетических иммобилизирующих бинтов Rhena cast и Rhena therm в детской ортопедии//Человек и здоровье. -СПб., 2006. -С. 66.
- Канюков В.Н., Стрекаловская А.Д., Килькинов В.И., Базарова Н.В./Материалы для современной медицины.-Оренбург: ГОУ ОГУ, 2004. -113 с.
- Киселев В.В. Практические и организационные аспекты хирургического лечения больных с инфекционными поражениями кисти//Здоровье. Медицинская экология. Наука. -2014. -№ 1(55). С. 16-18.
- Крайнюков П.Е., Матвеев С.А. Хирургия гнойных заболеваний кисти/-М.: Планета, 2016. -272 с.
- Мелешевич А.В. Панариций и флегмона кисти. -Гродно: ГрГУ, 2002. -185 с.
- Низкотемпературный термопластик. Передовые технологии индивидуального ортезирования. Альбом клинических наблюдений СПб.: РосИмп, 2014. -32 с.
- Усольцева Е.В., Машкара К.И. Хирургия заболеваний и повреждений кисти. -3-е изд.,.-Л.: Медицина, 1986. -352 с.
- Фишман Л.Г. Клиника и диагностика заболеваний пальцев и кисти. -1963. -391 с.
- Lucas S. Mc Donald, Mary F. Bavaro, Eric P. Hofmeister, Leo T. Kroonen/Hand infections/J Hand Surg Vol. 36A, August 2011, P. 1403-1412.
- Meredith Osterman, Reid Draeger, Peter Stern,/Acute Hand infections/J Hand Surg Am. r Vol. 39, August 2014 P. 1628-1635.
- Orrin I. Franko, MD, Reid A. Abrams, MD, Hand Infections, Orthopedic Clinics of North America, Volume 44, Issue 4, October 2013, P. 625-634.
- Turker et al., Hand infections: a retrospective analysis. 2014, PeerJ 2: e513; D0I10.7717/peerj.513.


