Применение препаратов аутологичной плазмы крови в лечении адгезивного капсулита плечевого сустава
Автор: Целищева Е.Ю., Лычагин А.В., Явлиева Р.Х., Гончарук Ю.Р., Ромадин Д.В., Калинский Е.Б.
Журнал: Кафедра травматологии и ортопедии @jkto
Статья в выпуске: 2 (44), 2021 года.
Бесплатный доступ
Основа терапии адгезивного капсулита - консервативное лечение. Его эффективность доказана во всем мире и достигает 90%. Терапия адгезивного капсулита направлена на устранение боли и воспаления суставной капсулы, что позволяет увеличить амплитуду движений и мышечную силу, а также улучшить качество жизни пациента. В настоящее время развитие клеточных технологий добавило в арсенал консервативной терапии адгезивного капсулита плечевого сустава внутрисуставные инъекции аутологичной плазмы богатой тромбоцитами (PRP). Будучи естественным биологическим стимулятором, плазма содержит множество факторов роста, выделяемых тромбоцитами, и поэтому действует на различные факторы регенеративного процесса. Материалы и методы: 42 пациента в возрасте от 47 до 60 лет с клинически и инструментально подтвержденным адгезивным капсулитом плечевого сустава, были пролечены внутрисуставными инъекциями аутологичной плазмы в Клинике травматологии, ортопедии и патологии суставов Университетской клинической больницы №1 Первого МГМУ им. И.М. Сеченова. Результаты: применение аутологичной плазмы крови в лечении адгезивного капсулита плечевого сустава позволило ослабить болевой синдром и увеличить амплитуду активных движений в суставе на разных стадиях заболевания. Богатая тромбоцитами плазма позволила снизить использование обезболивающих и противовоспалительных препаратов (p <0,05). Заключение: в комплексном лечении адгезивного капсулита плечевого сустава аутологичная плазма купирует болевой синдром, способствует восстановлению амплитуды движений, снижает лекарственную нагрузку.
Адгезивный капсулит, плазма богатая тромбоцитами, боль в плече.
Короткий адрес: https://sciup.org/142227540
IDR: 142227540 | УДК: 617.3 | DOI: 10.17238/issn2226-2016.2021.2.5-11
Application of autological blood plasma preparations in treatment of adhesive capsulites
The basis of adhesive capsulitis therapy is conservative treatment. Its effectiveness has been proven all over the world and reaches 90%. Adhesive capsulitis therapy is aimed at eliminating pain and inflammation of the joint capsule, which allows to increase the range of motion and muscle strength, as well as improve the patient's quality of life. Currently, the development of cellular technologies has added intra-articular injections of autologous platelet-rich plasma (PRP) to the arsenal of conservative therapy for adhesive capsulitis. As a natural biological stimulant, plasma contains many growth factors secreted by platelets, and therefore acts on various factors in the regenerative process. Materials and methods: 42 patients aged 47 to 60 years with clinically and instrumentally confirmed adhesive capsulitis were treated with intra-articular injections of autologous plasma at the Clinic of Traumatology, Orthopedics and Joint Pathology of the University Clinical Hospital No. 1 of the Sechenov University. Results: the use of autologous blood plasma in the treatment of adhesive capsulitis made it possible to weaken the pain syndrome and increase the amplitude of active movements in the joint at different stages of the disease. Platelet-rich plasma reduced the use of painkillers and anti-inflammatory drugs (p <0.05). Conclusion: in the complex treatment of adhesive capsulitis, autologous plasma relieves pain, helps to restore the range of motion, and reduces the drug load.
Текст научной статьи Применение препаратов аутологичной плазмы крови в лечении адгезивного капсулита плечевого сустава
Существует несколько теорий развития болевого синдрома в плечевом суставе, ограничения амплитуды движений и поражения околосуставных мягких тканей. Боль в области плеча встречается преимущественно у людей трудоспособного возраста (5-26%). Адгезивный капсулит (AК) – патология, характеризующаяся болевым синдромом и уплотнением суставной капсулы, приводящей к ограничению диапазона движений. Отведение конечности усиливает боль, вызывает спазм мышц ротаторной манжеты и вовлекает лопатку в суставные движения. Длительный и выраженный болевой синдром, помимо ограничения повседневной активности, отрицательно сказывается на сне и отдыхе пациента [1, 2]. Адгезивный капсулит ухудшает качество жизни и снижает трудоспособность. Нарушение трудоспособности определяет медицинскую и социально-экономическую значимость заболевания с учетом возраста пациентов.
Адгезивный капсулит плечевого сустава может развиться вследствие предшествующей патологии, иммобилизации пояса верхних конечностей, а также без провоцирующего фактора. Заболевания сердечно-сосудистой системы, плевры, поддиафрагмальных органов или диафрагмальные грыжи также могут вызывать отраженную боль в плече [3]. Важной теорией развития адгезивного капсулита является миофасциальная дисфункция мышц плечевого сустава с развитием триггерных зон – патологические изменения в мышцах смещают лопатку и плечевую кость [2, 3]. Заболевание протекает поэтапно с характерной для каждой стадии клинической картиной и возможностью частичного восстановления функции плеча.
Предлагается несколько гипотез, объясняющих преобладание женщин среди пациентов. Одна из них предложена в 1915 году М. Н. Лапинским и связана с развитием отраженной боли при патологии яичников. Согласно другой теории, развитие капсулита плечевого сустава связано с периодом менопаузы, при которой происходит снижение уровня эстрогенов, влияющее не только на минеральный обмен, но и на состояние мышечной ткани и капсульно-связочного аппарата [4].
Основная цель лечения адгезивного капсулита – устранение воспалительного процесса, уменьшение боли, улучшение качества жизни и функциональных параметров: силы мышц и амплитуды движений в плече. АК обычно требует комбинированного лечения и включает как лекарственную терапию (НПВП, глюкокортикоиды, инъекционная лекарственная терапия триггерных точек), так и немедикаментозную терапию – механотерапию в пассивном режиме (CPM-терапия), кинезиотейпиро-вание, физиотерапию и лечебную физкультуру. Консервативная терапия применяется во всем мире и эффективна в 90% случаев. В 10% случаев неэффективного лечения требуется хирургическое вмешательство [5, 6, 7].
Однако, дискуссии о вариантах консервативного лечения все еще продолжаются. Некоторые авторы рекомендуют использовать внутрисуставные инъекции глюкокортикоидов в качестве противовоспалительного и обезболивающего компонента [8, 9]. Другие авторы отдают предпочтение внутрисуставным блокадам анестетиками.
В настоящее время среди клеточных технологий применение богатой тромбоцитами плазмы (platelet rich plasma, PRP) является перспективным и безопасным методом регулирования как противовоспалительных, так и регенеративных механизмов [10, 11]. PRP содержит различные биологически активные факторы (продукты образования тромбов, факторы роста тромбоцитов, адгезивные молекулы и цитокины) и, следовательно, стимулирует репаративные и анаболические процессы в поврежденных тканях, восстанавливает обменные процессы, активирует местный иммунитет, улучшает метаболизм клеток и тканевое дыхание, оказывает противовоспалительный эффект [11].
PRP-терапия уже использовалась при лечении адгезивного капсулита плечевого сустава. Однако нет единого мнения о том, какая методика введения плазмы является наиболее оптимальной при лечении заболевания [2, 3, 11]. Таким образом, тема остается актуальной из-за отсутствия единой тактики лечения.
Цель исследования: оценить клиническую эффективность внутрисуставного применения аутологичной плазмы богатой тромбоцитами (PRP) в комплексном лечении адгезивного капсулита плечевого сустава на разных стадиях заболевания.
Материалы и методы
На кафедре травматологии, ортопедии и патологии суставов Первого МГМУ им. И.М. Сеченова Минздрава России было проведено проспективное рандомизированное исследование. Обследованы и пролечены 42 пациента в возрасте от 47 до 60 лет (средний возраст 51,2 ± 1,3 года) с диагностированным адгезивным капсулитом плечевого сустава. Среди них 38 женщин (90,47%) и 4 мужчин (9,5%). Все пациенты подписали форму информированного согласия на участие в исследование.
Пациенты были разделены на 2 группы (AК1 и AК2) в зависимости от стадии заболевания на момент обследования: 24 пациента в первой стадии заболевания и 18 во второй.
Каждый пациент прошел стандартное ортопедическое обследование [1, 12]. Всем пациентам была выполнена стандартная рентгенография и магнитно-резонансная томография (МРТ) плеча. Стандартная рентгенография использовалась для исключения переломов, вывихов и деформирующего остеоартроза. На высокочастотной МРТ 1,5 Тл на Т2-взвешенном изображении с подавлением сигнала жировой ткани TSE PD SPAIR, мы оценили степень утолщения и структуру капсулы, сухожильно-связочного аппарата и суставной губы плечевого сустава. МРТ плечевого сустава проводилась с помощью специальной поверхностной радиочастотной катушки. Срезы получали в трех плоскостях: корональной, сагиттальной и аксиальной [13, 14].
Степень болевого синдрома оценивали по визуальной аналоговой шкале (ВАШ) от 1 до 100, где 0 - отсутствие боли, а 100 -невыносимая боль. Качество жизни и функцию плеча оценивали с помощью ортопедического опросника (DASH) и простого плечевого теста (SST).
Основной раздел опросника DASH (шкала неспособностей/ симптомов) состоит из 30 пунктов-вопросов, связанных с состоянием функции кисти за последнюю неделю. При этом 21 из них выявляют степень трудности выполнения различных физических действий по причине ограничения функции плеча или кисти; 6 пунктов отражают тяжесть ряда симптомов, 3 оценивают социально-ролевые функции [15, 16].
SST – это шкала самооценки, которая оценивает функциональное состояние поврежденного плеча. Каждый вопрос посвящен функции плеча и особенностям выполняемой физической активности. Результаты оценивали до лечения, через неделю, 1 месяц и 3 месяца.
Протокол включал 3 инъекции PRP-LP с двухнедельным интервалом.
В комплекс лечения входили также физиотерапия (лазеротерапия на аппарате магнито-инфракрасной терапии и магнитотерапия переменным магнитным полем через 5 дней после инъекции с 3-дневным перерывом после каждой последующей инъекции), CPM-терапия (через 4 дня после первой инъекции, через 3 дня после второй инъекции) и дальнейшее восстановление мышечной силы с увеличением амплитуды активных движений через 3 дня после третьей инъекции. Больные продолжали заниматься лечебной гимнастикой более 3 месяцев.
Данное исследование было проведено в соответствии с этическими стандартами, изложенными в Хельсинкской Декларации в пересмотре от 2013 года.
Процедура подготовки плазмы богатой тромбоцитами
Плазма, богатая тромбоцитами, была приготовлена из крови пациента с использованием утвержденного медицинского устройства (RegenBCT, Regen Lab, Швейцария) и обработана в соответствии с протоколом производителя. Было взято 8 мл крови пациента в стерильную вакуумную пробирку, содержащую разделяющий гель и антикоагулянт цитрат натрия. Сразу после взятия крови пробирку помещали в центрифугу. Центрифугирование проводили при центробежной силе 1500 g (что соответствует скорости 3100 оборотов в минуту в нашей модели центрифуги) в течение 5 минут. Во время центрифугирования разделяющий гель становится жидким и вставляется между компонентами крови на уровне своей удельной плотности. В конце центрифугирования разделяющий гель восстанавливает свою первоначальную консистенцию и образует физический барьер, который изолирует тромбоциты и плазму в верхней части пробирки и удерживает эритроциты в нижней части. Полученная PRP представляет собой стандартизированную PRP с низким содержанием лейкоцитов (LP-PRP).
Статистическая обработка данных
Обработка проводилась с использованием пакета статистического анализа данных Statistica 8.0 для Windows (StatSoft Inc., США). Нормальность распределения оценивалась по критерию Колмогорова-Смирнова. Непрерывные значения с нормальным распределением представлены как M ± SD, где M - среднее значение выборки, SD - стандартное отклонение. Для сравнительного анализа количественных показателей исследования использовались непараметрические критерии, ранговый критерий Мэнни-Уитни (простой тест плеча и тест DASH). Мы использовали критерий Стьюдента для сравнения зависимых групп (до и после исследования амплитуды движения) по качественным показателям. Относительные (%) и абсолютные частоты использовались для описания качественных характеристик. Корреляционный анализ проводился с использованием критерия хи-квадрат.
Для статистической обработки использовались стандартные статистические пакеты: Statistica 10.0 и IBM SPSS Statistics 22.0.
Полученные результаты
В первой группе (AК1) все пациенты отрицали наличие острой травмы поврежденного сустава. У 9 пациентов (24,2%) аналогичная патология наблюдалась в контралатеральном суставе в течение 1-5 лет до настоящего заболевания. При осмотре поврежденное плечо приподнято, мышцы пояса верхней конечности укорочены, дельтовидная мышца гипотрофирова-на. Активные движения верхней конечности вызывают острую боль в проекции сустава и окружающих мышцах, пассивные движения – умеренную. Максимальная выраженность болевого синдрома наблюдалась в крайних точках диапазона движений. Пациенты отмечали, что боль в суставах сохраняется ночью и усиливается в положении лежа на спине с опорой на пораженный сустав. Амплитуда активных и пассивных движений верхней конечности ограничена одинаково, равна 50-80 градусов ретракции, 85 ± 5 градусов сгибания или 15-20 градусов дефицита сгибания, 32 ± 3 градуса внешней ротации и 37 ± 4 градуса внутренней ротации. При пальпации выявляется отек тканей области плеча, диффузная болезненность в проекции плечевой капсулы, локальная болезненность в надостной, подостной, трапециевидной и подлопаточной мышцах. На МРТ утолщение суставной капсулы до 4,4 ± 0,2 мм и отек суставной капсулы 88% ± 3% в области подмышечной ямки (Рисунок 1). Рентгенография не показала травматических изменений, признаков остеоартрита или свободных инородных тел.
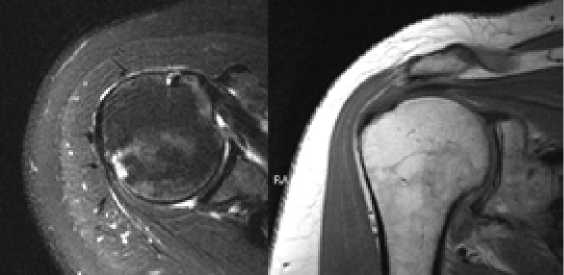
Рисунок 1. Адгезивный капсулит плечевого сустава (МРТ).
Во второй группе (AК2) клиническое обследование выявило гипотрофию дельтовидной и надостной мышц. Активные и пассивные движения вызывали боль, в покое боли отсутствовали. Объем движений в плече-лопаточном комплексе существенно ограничен: ретракция плеча до 40-50 ± 7 градусов, сгибание 4050 ± 5 градусов, разгибание 10 ± 5, внешняя ротация до 20 градусов и 0-5 ± 3 градусов внутренняя ротация. При пальпации в области плеча отмечалась диффузная боль. На МРТ утолщение суставной капсулы до 3,5 ± 0,3 мм и отек суставной капсулы 7683% в области подмышечной ямки. Рентгенография не показала травматических изменений, признаков остеоартрита или свободных инородных тел.
В результате подготовки было получено около 4-5 мл PRP- LP. Полученную плазму (PLT 343,28 ± 89,37 · 103 / мм3) вводили в сустав через задний доступ без предварительной анестезии.
В группе AК1 болевой синдром снизился с 80-90 до 45 по ВАШ в течение 7 дней. В группе АК2 к концу 1-й недели наблюдалось усиление болей на фоне повышенной физической нагрузки в начале терапии СРМ. Острый болевой синдром купировался медикаментозным лечением с последующим продолжением PRP-терапии с положительным результатом. В группе АК2 к концу второй недели было достигнуто достоверное снижение болевого синдрома (40 баллов по ВАШ) (Рисунок 2).
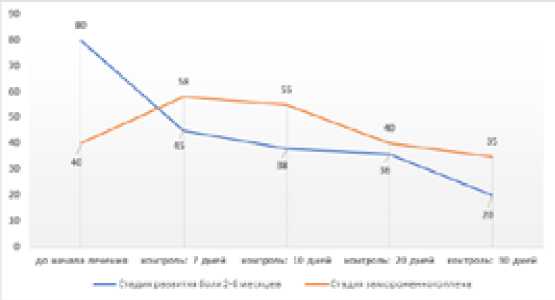
Рисунок 2. Изменение интенсивности болевого синдрома по шкале VAS.
К концу первого месяца лечение позволило значительно увеличить амплитуду движений у всех пациентов независимо от стадии заболевания (Рисунок 3). Положительные сдвиги с увеличением амплитуды движений плеча сохранялись в течение 3 месяцев (Таблица 1).
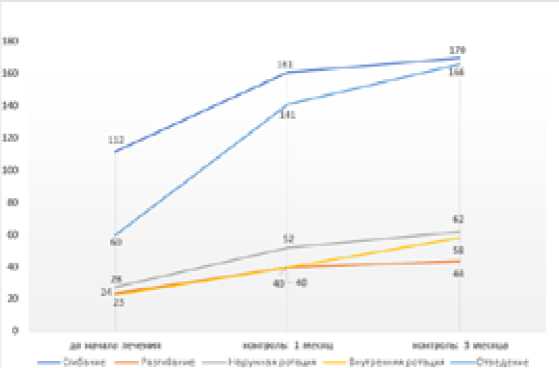
Рисунок 3. Динамика изменений амплитуды движений в плече
При анализе данных получено достоверное (p <0,05) положительное изменение всех показателей амплитуды движения плеча. Сгибание было 112,9 (± 41,8) градусов до лечения и 170,9 (± 15,9) через три месяца после лечения. Разгибание сустава составляло 24,8 (± 9,01) градуса до лечения и 44,7 (± 1,3) градуса через 3 месяца после лечения. До лечения внешняя ротация составляла 28,2 (± 15,7) градусов и внутренняя ротация 23,6 (±
11,8) градуса, через 3 месяца после лечения были достигнуты показатели 62,7 (± 17,6) и 58,5 (± 21,4) соответственно. Отведение плеча в плече-лопаточном комплексе составляло 60,0 (± 14,4) градусов до лечения и 166,2 (± 26,5) градусов через 3 месяца после лечения.
Таблица 1
Амплитуда движений в плече
|
Тип движений |
До лечения |
Спустя 1 месяц |
Спустя 3 месяца |
|
Сгибание |
112.9 (±41.8) |
161.2 (±23.2) |
170.9 (±15.9) |
|
Разгибание |
24.8 (±9.01) |
40.3 (±2.8) |
44.7 (±1.3) |
|
Наружная ротация |
28.2 (±15.7) |
52.0 (±15.8) |
62.7 (±17.6) |
|
Внутренняя ротация |
23.6 (±11.8) |
40.5 (±14.4) |
58.5 (±21.4) |
|
Отведение |
60.0 (±14.4) |
141.2 (±31.01) |
166.2 (±26.5) |
Пациенты обеих групп показали достоверное улучшение функции плеча в результате проведенного лечения. Эффект, достигнутый в течение 1 месяца, сохранялся после 3 месяцев наблюдения. Согласно результатам простого теста плеча (SST) и шкалы DASH улучшение функции плеча наблюдалось на протяжении всего наблюдения (Рисунок 4, 5).
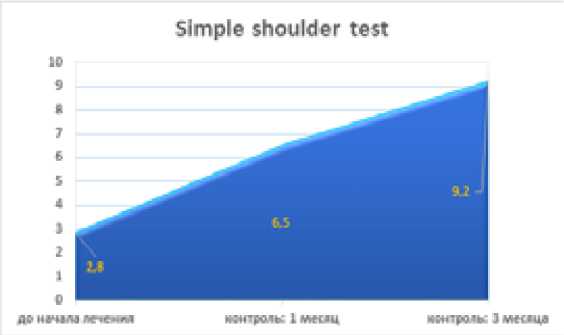
Рисунок 4. Динамика изменений результатов опроса по шкале Simple shoulder test на разных этапах лечения
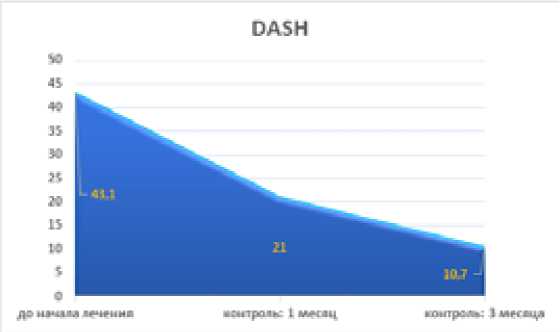
Рисунок 5. Динамика изменений результатов опроса по шкале DASH на разных этапах лечения.
По результатам простого плечевого теста показатели в группах до лечения (2,8 ± 1,8) достоверно (p <0,05) отличаются от показателей через 1 месяц (6,5 ± 2,5) и 3 месяца (9,2 ± 1,7) после лечения.
Мы также получили значительную разницу (p <0,005) результатов шкалы DASH. По шкале DASH результат до лечения составил 43,1 (± 19,5) балла, 21 (± 9,3) через один месяц и 10,7 (± 5,8) баллов через три месяца лечения.
Согласно полученным результатам, отмечается положительная динамика по вышеуказанным шкалам вне зависимости от сроков лечения.
Клинический случай
Больная Т., 62 лет из группы АК1. Жаловалась на боли в левом плече. Болевой синдром постепенно нарастал в течение 5 месяцев. Боль сохранялась ночью. Усиление болей привело к ограничению амплитуды движений верхней конечности. Самостоятельное лечение пациентки безрезультатно. При поступлении: болевой синдром 80 мм по ВАШ. При осмотре: отведение 40 градусов, наружная ротация 5 градусов, внутренняя - 10 градусов. Сгибание 165 гр., разгибание 25 гр. (Рисунок 6).
^< ^:
Рисунок 6. Пациент Т. до лечения
Пациентке проведено комплексное лечение. Инъекция PRP выполнялась по протоколу 3 раза с интервалом между инъекциями 2 недели. Дополнительной медикаментозной терапии не проводилось.
После первой инъекции интенсивность боли снизилась до 50 мм по ВАШ. К концу 2-й недели показатель снизился до 35 мм.
Через 1 месяц боль составила 10-15 мм, по ночам полностью исчезла. Отведение, сгибание и разгибание в суставе полностью восстановились. Однако, наружная ротация по-прежнему была ограничена 35 градусами с 10-градусным дефицитом внутренней ротации (Рисунок 7). Пациент отметил восстановление полной амплитуды движений через 3 месяца.

Рисунок 7. Пациент Т. после лечения.
Обсуждение
На сегодняшний день остается открытым вопрос этиологии адгезивного капсулита плечевого сустава. Все специалисты сходятся во мнении, что к 40 годам развиваются прогрессирующие дегенеративные и дистрофические изменения сухожилий, хронический болевой синдром, мышечный спазм, рефлекторное снижение амплитуды движений. Изменения развиваются постепенно в течение длительного времени, в связи с этим своевременное начало лечения невозможно.
Современное лечение адгезивного капсулита комплексное и включает в себя как лекарственные, так и нелекарственные методы лечения. Препаратами выбора являются НПВП и глю- кокортикоиды при стойком или выраженном болевом синдроме. Те же группы препаратов можно использовать для местного применения, внутрисуставного введения и блокады периферических нервов [12, 17]. Для уменьшения болевого синдрома в триггерных точках измененных мышц также можно использовать антигомотоксические препараты, для улучшения фос-форно-кальциевого обмена хрящевой ткани – препараты замедленного действия (SYSADOA). Немедикаментозное лечение представлено экстракорпоральной ударно-волновой, ультразвуковой и лазерной терапией, магнитотерапией с переменным магнитным полем. Оперативное лечение требуется при неэффективности консервативной терапии или при выраженных анатомических изменения плечевого сустава.
PRP-терапия набирает популярность во всем мире в лечении острых и хронических заболеваний опорно-двигательного аппарата. Накоплен большой клинический опыт применения PRP в комплексном лечении артрозов, тендинитов, острых и хронических патологий мышц и сухожилий [10, 18]. Преимущества метода - полная биосовместимость, отсутствие риска трансмиссивных инфекций, продолжительный эффект, отсутствие негативного воздействия на желудочно-кишечный тракт и ткани в области инъекции.
Плазма богатая тромбоцитами ускоряет регенерацию тканей за счет увеличения выработки коллагена и высвобождения противовоспалительных факторов, биологически активных молекул альфа-гранул тромбоцитов и факторов роста [11, 19] (табл.2). Многие исследователи подтверждают эффективность PRP при лечении патологии опорно-двигательного аппарата [12, 20]. Метод позволяет в ряде случаев отсрочить или предотвратить операцию.
Таблица 2
Тромбоцитарные факторы роста и их роль в организме
|
Фактор роста |
Функция |
|
Фактор роста фибробластов (FGF) |
Стимуляция роста сосудов, увеличение количества фибробластов |
|
Фактор эпидермального роста (EGF) |
Запуск процесса обновления и деления клеток |
|
Фактор роста эндотелия сосудов (VEGF) |
Воздействие на сосудистую проницаемость стенки и улучшение кровоснабжения к тканям |
|
Фактор роста тромбоцитов (PDGF) |
Важная роль в процессе выживания клеток и регенерации |
|
Инсулиноподобный фактор роста 1 (IGF) |
Рост клеток, дифференцировка и миграция |
|
Трансформирующий фактор роста бета (TGF-β) |
Уменьшение воспалительных поражений, стимуляция синтеза коллагена, подавление апоптоза |
PRP классифицируется по концентрации тромбоцитов и лейкоцитов в конечном продукте. Критерий концентрации тромбоцитов остается спорным [21, 22] из-за отсутствия точных данных о корреляции между концентрацией тромбоцитов в PRP и клиническим исходом [19, 23]. Некоторые авторы связывают различное действие факторов роста на клеточные рецепторы с отсутствием стимулирующего эффекта при низком количестве тромбоцитов в PRP и подавлением регенерации при концентрациях, превышающих 1000x103 мкл. Второй показатель – концентрация лейкоцитов. Высокая концентрация лейкоцитов увеличивает уровень провоспалительных медиаторов, стимулирующих воспаление. Некоторые фракции, включая лимфоциты и моноциты, положительно влияют на факторы роста, взаимодействуя со многими биологически активными молекулами [11]. В нашем исследовании пациентам вводили плазму с низким содержанием лейкоцитов (LP-PRP), содержащую 343,28 ± 89,37 · 103 тромбоцитов / мм3. Результаты показывают, что нет необ- ходимости в высокой концентрации тромбоцитов для получения терапевтического эффекта, однако имеет значение низкий уровень лейкоцитов.
Многие авторы отмечают положительные результаты PRP-терапии и безопасность этого биологического метода при лечении адгезивного капсулита плечевого сустава [11, 24]. Однако, в исследованиях не рассматривалась возможность PRP-терапии на разных стадиях заболевания.
Вывод
Применение плазмы богатой тромбоцитами у пациентов с первой стадией адгезивного капсулита плечевого сустава обеспечивает выраженное снижение болевого синдрома и незначительное восстановление амплитуды движений.
Введение LP-PRP на второй стадии заболевания также снижает воспаление и болевой синдром, позволяя активно восстанавливать амплитуду движений.
PRP-терапия позволяет снизить лекарственную нагрузку и может быть терапией выбора у пациентов с заболеваниями желудочно-кишечного тракта.
Финансирование: исследование не имело спонсорской поддержки.
Funding: the study had no sponsorship.
Список литературы Применение препаратов аутологичной плазмы крови в лечении адгезивного капсулита плечевого сустава
- P. J. Rundquist, D. D. Anderson, C. A. Guanche, Paula M. Ludewig, Shoulder Kinematics in Subjects With Frozen Shoulder. J. Arch Phys Med Rehabil, vol. 84, pp. 1473–1479, 2003. https://doi.org/10.1016/s0003-9993(03)00359-9
- C. M. Robinson, K. T. Seah, Y. H. Chee, P. Hindle, I. R. Murray. Frozen shoulder. J. Bone Joint Surg Br., vol. 94, no. 1, pp. 1–9, 2012. https://doi. org/10.1302/0301-620X.94B1.27093
- E. Itoi, G. Arce, G. I. Bain, R. L. Diercks, D. Guttmann, A. B. Imhoff, A. D. Mazzocca,
- H. Sugaya, Y.-S Yoo, Shoulder Stiffness: Current Concepts and Concerns. Book - Springer, pp. 21-41, 2015. https://doi.org/10.1016/j.arthro. 2016.03.024
- D. R. Leblanc, M. Schneider, P. Angele, G. Vollmer, D. Docheva. The effect of estrogen on tendon and ligament metabolism and function. J. Steroid Biochem Mol Biol, no. 172, pp. 106– 116, 2017. https://doi.org/10.1016/j.jsbmb. 2017.06.008
- M. J. Codsi. The painful shoulder: when to inject and when to refer. Clin. J. Med, vol. 74, no. 7, pp. 473-478, 2007. https://doi.org/10.3949/ccjm.74.7.473
- C. H. Cho, K. C. Bae, D. H. Kim. Treatment strategy for frozen shoulder. J. Clin. Orthop. Surg., vol. 11, no. 3, pp. 249-257, 2019. https://doi.org/10.4055/cios.2019.11.3.249
- M. I. Ibrahim, A. J. Jonson, R. Pivec, et al. Treatment of adhesive capsulitis of the shoulder with a static progressive stretch device: a prospective, randomized study. J. Long Eff Med Implants, vol. 22, no. 4, pp. 281–291, 2012. https://doi.org/10.1615/jlongtermeffmedimplants.2013007061
- B. K. Coombes, L. Bisset, B. Vicenzino. Efficacy and safety of corticosteroid injections and other injections for management of tendinopathy: a systematic review of randomised controlled trials. Lancet journal, vol. 376, no. 9754, pp. 1751–1767, 2010.
- Y. K. Shashank, S. Venkataraman, S. Neha,. Comparative efficacy of platelet rich plasma injection, corticosteroid injection and ultrasonic therapy in the treatment of periarthritis shoulder. J. Clin Diagn Res., vol. 11, no. 5, pp. 15–18, 2017. https://doi.org/10.1016/S0140-6736(10)61160-9
- I. Andia, M. Abate. Platelet-rich plasma: combination therapies for the musculoskeletal system. Front Med, vol. 12, no. 32, pp. 139-152, 2018. https:// doi.org/10.1007/s11684-017-0551-6
- A. Turzi, & Regen Lab team Biobridge foundation editions. PRP standardization & cells therapies, by Editions Favre SA, Lausanne, Switzerland, 2018, 5 с.
- R. C. Manske, T. S. Ellenbecker. Current concepts in shoulder examination of the overhead athlete. J. Sports Phys Ther, vol. 8, no. 5, pp. 554–578, 2013.
- C. B. Chung, L. S. Steinbach. MRI of the upper extremity: shoulder, elbou, wrist and hand. Book, Philadelphia: Wolters Kluwer Health, Lippincott Williams & Wilkins,728 p., 2010.
- M. Shahabpour, R. Sutter, J. Kramer. MRI of the shoulder. Book, English edition – Breitenseher Publisher. – Jan. 2018.
- W. W. Downie, P. A. Leatham, V. M. Rhind, M. E. Pickup, V. Wright. The visual analogue scale in the assessment of grip strength. J. Ann Rheum Dis., vol. 37, no. 4, pp. 382- 384, 1978. https://doi.org/10.1136/ard.37.4.382
- F. Franchignoni, S. Vercelli, A. Giordano, F. Sartorio, E. Bravini, G. Ferriero. Minimal clinically important difference of the disabilities of the arm, shoulder and hand outcome measure (DASH) and its shortened version (QuickDASH). J. Orthop Sports Phys Ther, vol. 44, no. 1, pp. 30-9, 2014. https:// doi.org/10.2519/jospt.2014.4893
- L. E. Warmington. Frozen shoulder – an effective method of treatment. Australian Journal of Physiotherapy, vol. 16, no. 3, pp. 124–130, 1970. https:// doi.org/10.1016/S0004-9514(14)61097-7
- G. S. Habib, R. Abu–Ahmad. Lack of effect of corticosteroid injection at the shoulder joint on blood glucose levels in diabetic patients. Clin Rheumatol, vol. 26, no. 4, pp. 566-568, 2006. https://doi.org/10.1007/s10067-006-0353-8
- H. B. Y. Chan, P. Y. Pua, C. H. How. Physical therapy in the management of frozen shoulder. Singapore Med J., vol. 58, no. 12, pp. 685-689, 2017. https://doi.org/10.11622/smedj.2017107
- K. Setayesh, A. Villarreal, A. Gottschalk, J. M. Tokish, W. Choate . Treatment of Muscle Injuries with Platelet-Rich Plasma: a Review of the Literature. J. Curr Rev Musculoskelet Med, vol. 11, no. 4, pp. 635–642, 2018. https://doi. org/10.1007/s12178-018-9526-8
- J. Chahla, M. E. Cinque, N. S. Piuzzi et al. A Call for Standardization in Platelet- Rich Plasma Preparation Protocols and Composition Reporting. The Journal of Bone & Joint Surgery, vol. 99, no. 20, pp. 1769–1779, 2017. https://doi. org/10.2106/JBJS.16.01374
- H. Nasir, J. Herman, B. Mohit,. An evidence-based evaluation on the use of platelet rich plasma in orthopedics – a review of the literature. SICOT J., no. 3, pp. 57, 2017. https://doi.org/10.1051/sicotj/2017036
- H. Aslani, S. T. Nourbakhsh, Z. Zafarani, M. Ahmadi-Bani, et al. Platelet-Rich Plasma for Frozen Shoulder: A Case Report. The Archives of Bone & Joint Surgery, vol. 4, no. 1, pp. 90- 93, 2016.


