Применение тиоктовой кислоты у женщин с синдромом поликистозных яичников и нормальной массой тела
Автор: Иванова Л.А., Король И.В., Коваленко Ю.С., Ружицкая Л.В., Танин И.Ю.
Журнал: Международный журнал гуманитарных и естественных наук @intjournal
Рубрика: Медицинские науки
Статья в выпуске: 10-1 (73), 2022 года.
Бесплатный доступ
Гиперинсулинемия является одной из основных причин развития синдрома поликистозных яичников (СПКЯ). Целью работы было оценить влияние тиоктовой кислоты на уровень базального и стимулированного инсулина плазмы крови, индекс HOMA-IR, объем яичников у женщин с СПКЯ и нормальной массой тела. 27 женщин с СПКЯ и нормальной массой тела были распределены на 2 группы. В течение 1 года пациентки основной группы (n=16) получали высокобелковую диету на 2100 калорий в сочетании с тиоктовой кислотой (300 мг 2 раза в сутки или 600 мг за 30 минут до завтрака). Антропометрическое обследование, определение уровня базального и стимулированного инсулина плазмы крови в ходе перорального глюкозотолерантного теста (ПГТТ), эстрадиол крови, расчет индекса инсулинорезистентности (HOMA-IR), объем яичников, толщину эндометрия по данным ультразвукового исследования проводили исходно и через 1 год лечения. В результате терапии тиоктовой кислотой (300 мг 2 раза в сутки или 600 мг за 30 минут до завтрака) в сочетании с высокобелковой диетой на 2100 калорий в основной группе существенно снизились средние уровни базального (на 30,8%, p
Тиоктовая кислота, гиперинсулинемия, синдром поликистозных яичников, нормальная масса тела
Короткий адрес: https://sciup.org/170197237
IDR: 170197237 | DOI: 10.24412/2500-1000-2022-10-1-90-96
Application of thyroid acid in women with polycistic ovary syndrome and normal body mass
Hyperinsulinemia is one of the main causes of the development of the polycystic ovary syndrome (PCOS). The aim of the work was to evaluate the effect of thioctic acid on basal and stimulated insulin plasma levels, HOMA-IR index, ovarian volume in women with PCOS and normal body weight. 27 women with PCOS and normal body weight were divided into 2 groups. Within 1 year, the patients of the main group (n = 16) received a high-protein diet for 2,100 kcal, combined with thioctic acid (300 mg twice a day or 600 mg 30 minutes before breakfast). Anthropometric examination, determination of basal and stimulated plasma insulin during oral glucose tolerance test (OGTT), insulin resistance calculation index (HOMA-IR), estradiol, the volume of the ovaries, endometrial thickness by ultrasound was performed at baseline and after 1 year of treatment. As a result of therapy thioctic acid (300 mg, 2 times a day, or 600 mg for 30 minutes before breakfast) in combination with a high-protein diet for 2100 kcal main group significantly decreased average levels of basal (to 30,8%, p
Текст научной статьи Применение тиоктовой кислоты у женщин с синдромом поликистозных яичников и нормальной массой тела
Убедительно доказано, что гиперинсу-линемия является одной из главных причин развития СПКЯ [1-3]. Женщины с СПКЯ подвержены повышенному риску развития метаболического синдрома. Инсулиновые сенситайзеры (метформин) в настоящее время успешно применяются для лечения у девочек-подростков с СПКЯ, способствуя нормализации уровня менструального цикла и снижению массы тела [4]. В ходе ряда исследований продемонстрировано, что применение тиоктовой кислоты у лиц с ожирением и/или избы- точной массой тела уменьшает как базальную, так и стимулированную гиперинсу-линемию, что приводит к снижению ИР, улучшению показателей липидного и углеводного обмена, уменьшению массы тела [2, 5-9]. Однако имеется мало данных о влиянии тиоктовой кислоты на эти показатели при исходно нормальной массе тела.
Доказано, что тиоктовая (а-липоевая) кислота повышает биодоступность глюкозы в инсулинзависимых и инсулиннезави-симых тканях. Она взаимодействует с рецепторами вентро-медиального ядра гипо- таламуса через подавление гипоталамической активности аденозинмонофосфат-киназы, что приводит к анорексигенному эффекту и повышению скорости термогенеза [1]. Тиоктовая кислота повышает продукцию и активность тирозинкиназы инсулиновых рецепторов, за счет чего увеличивается чувствительность к инсулину в жировой и мышечной тканях, снижается скорость глюконеогенеза в печени. Альфа-липоевая кислота может функционировать как частичный агонист PPAR-гамма ядер-ных рецепторов. В конечном итоге повышается активность переносчиков глюкозы GLUT–1 и GLUT–4, снижается экспрессия гена лептина, уменьшается уровень фактора некроза опухоли альфа, что в совокупности уменьшает ИР [10].
Учитывая гепатопротекторные свойства тиоктовой кислоты (снижение глюконеогенеза, торможение накопления липидов в печени), способность повышать уровень глобулинов, связывающих половые гормоны, она может являться препаратом выбора у пациенток с СПКЯ в сочетании с неалкогольной жировой болезнью печени [11].
Цель: оценить влияние тиоктовой кислоты на уровень базального и стимулированного инсулина плазмы крови, индекс HOMA-IR, объем яичников у женщин с СПКЯ и нормальной массой тела.
Материалы и методы исследования. В проспективное контролируемое рандомизированное исследование были включены 27 женщин с СПКЯ и нормальной массой тела в возрасте от 18 до 31 года (средний возраст 21,46±1,19 лет). Рандомизацию больных в основную и контрольную группы осуществляли путем использования таблицы случайных чисел.
Критериями включения в исследование были: наличие СПКЯ, индекс массы тела (ИМТ) ≥ 18,5 и <25 кг/м2, подписание добровольного информированного согласия на участие в исследовании. Критериями исключения были: возраст больных младше 18 лет, беременность, прием оральных контрацептивов в течение 3 месяцев до начала исследования, тяжелые соматические заболевания, злоупотребление алко- голем и (или) наркотиками, отказ пациента от исследования, ИМТ ≥ 25 кг/м2.
Исследование проводилось на базе МБУЗ Краснодарская городская клиническая больница скорой медицинской помощи. Пациенты были обследованы до и через 12 месяцев после назначенного лечения.
Пациенткам обеих групп назначалась диета на 2100 калорий, которая включала 3 основных приема пищи с высоким содержанием белка и обязательным приемом молочного жира (ежедневно 200 граммов творога 9% жирности, 20 граммов сливочного масла 82,5% жирности, молоко или кефир 2,5-3,5% жирности 150-200 мл в сутки, 50-100 г мяса в готовом виде в основном говядины или крольчатины), 50100 г бобовых (горох, фасоль) при хорошей переносимости. Легкоусвояемые углеводы в чистом виде исключались из рациона. Трудноусвояемые углеводы в виде каш, приготовленных на молоке или сливках, составляли не более 50% калорийности суточного рациона. Обязательным был прием свежих овощей и фруктов не менее 500 г в сутки. Пациенткам основной группы была добавлена тиоктовая кислота (300 мг, 2 таблетки утром за 30 минут до завтрака или по 300 мг 2 раза в сутки в течение 1 года).
Оценивались показатели базального и постпрандиального инсулина плазмы крови, индекса HOMA-IR, объем яичников. А также оценивалась продолжительность и регулярность овариально-менструального цикла, появление доминантного фолликула.
Основную группу составили пациентки (n=16), получавшие высокобелковую диету на 2100 калорий в сочетании с тиокто-вой кислотой (300 мг, 2 таблетки утром за 30 минут до завтрака или по 300 мг 2 раза в сутки в течение 1 года). В контрольную группу вошли пациентки (n=11), которые находились только на высокобелковой диете на 2100 калорий в течение всего периода исследования. Диагностику СПКЯ проводили согласно рекомендациям, предложенным в 2003 году Объединенным конгрессом Европейского общества репродукции человека и Американского об- щества репродуктивной медицины в Роттердаме.
Исходно и через 1 год лечения пациенткам проводили антропометрическое обследование (измерение роста, веса, окружности талии, рассчитывали индекс массы тела по формуле Кетле (масса тела (кг)/рост2 (см)), лабораторные исследования (базальный и стимулированный инсулин плазмы крови в ходе ПГТТ); эстрадиол крови, рассчитывали индекс инсули-норезистентности (HOMA-IR), трансвагинальное ультразвуковое исследование гениталий на 2-й–5-й день менструального цикла.
Глюкозу плазмы венозной крови (референсный интервал (РИ) 3,9-5,9 ммоль/л) определяли глюкозооксидазным методом с помощью реагентов «SentinelDiagnostics» (Италия) на анализаторе «Konelab» («ThermoFisherScientific», Финляндия). Инсулин плазмы крови (РИ 3,0-25,0 мкЕд/мл) исследовали посредством имму-ноферментного метода реактивами ELECSYS Insulin аппаратом «Roche Diagnostics Cobas e 411» («Roche», Швейцария). ИР определяли по формуле: HOMA IR = Глюкоза натощак (ммоль/л) х Инсулин натощак (мкЕд/мл)/ 22,5, где показатель ≥2,7 соответствовал ИР.
Этический комитет при ФГБОУ ВО КубГМУ Минздрава России от 20 января 2017 г. (протокол №47) постановил, что документы к работе представлены полностью, содержат необходимую информацию и не противоречат этическим нормам; добровольное информированное согласие отвечает принципам защиты прав испытуемых; права пациентов, планируемых для включения в исследование, не нарушены.
Результаты, полученные в ходе исследования, обрабатывали с помощью пакета программы Statistica 6.0. Возможность использования методов параметрической статистики подтверждали тестом Колмогорова-Смирнова. Сравнение полученных результатов, представленных в виде средних величин ± ошибка средней (M±m) в связанных совокупностях, проводили с помощью Т-критерия Уилкоксона. Достоверными считали полученные значения при р<0,05.
Результаты. Исходные демографические, клинические и лабораторные показатели в сравнивавшихся группах оказались сопоставимыми. Не отмечалось существенных межгрупповых различий по полу, возрасту, ИМТ. В этой связи представлялось возможным объяснить изменения показателей в динамике наблюдения и лечения влиянием терапии.
У женщин с СПКЯ имели место различные нарушения овариальноменструального цикла: олигоопсоменорея (n=4; 14,8%); аменорея (n=2; 7,4%); альго-дисменорея (n=2; 7,4%); ановуляторные циклы (n=22; 81,5%). У всех исследованных женщин имела место исходная гипе-ринсулинемия: базальная (n=7; 25,9%), постпрандиальная (n=8; 29,6%) или их сочетание (n=12; 44,4%).
При анализе показателей базального и постпрандиального инсулина плазмы крови через 1 год соблюдения высокобелковой диеты на 2100 калорий и приема тиок-товой кислоты выявлена существенная положительная динамика по сравнению с исходными данными (табл. 1).
Таблица 1. Динамика показателей углеводного обмена у больных с синдромом поликистозных яичников исходно и через 12 месяцев лечения тиоктовой кислотой
|
Показатель |
Основная группа исходно, (n=16) |
Контроль исходно, (n=11) |
Основная группа после лечения, (n=16) |
Контроль послеле-чения, (n=11) |
|
Глюкоза базальная, ммоль/л |
4,55±0,20 |
4,29±0,11 |
4,81±0,17 |
4,31±0,17 |
|
Глюкоза стимули-рованная, ммоль/л |
5,43±0,34 |
5,73±0,34 |
5,9±0,31 |
5,45±0,42 |
|
Инсулин базальный, мкЕд/мл |
33,59±5,91 |
32,16±4,88 |
23,3±4,121 |
33,07±4,65 |
|
Инсулин стимули-рованный, мкЕд/мл |
178,8±36,7 |
172,2±28,9 |
90,5±17,432 |
165,4±30,1 |
|
HOMA IR |
6,62±1,23 |
6,73±1,69 |
4,12±1,043 |
6,25±0,98 |
Так, в основной группе среднее значение базального инсулина снизилось на 30,8% (Т критерий Уилкоксона=26, p<0,05), а стимулированного инсулина на 49,4% (Т критерий Уилкоксона=0, p<0,05).
В контрольной группе существенных изменений данных показателей не наблюдалось. Полученные данные представлены на рисунке 1.
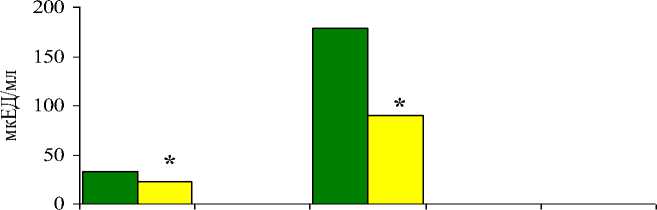
Базальный Стимулир.
инсулин Инсулин
До лечения Через 1 год лечения
Рис. 1. Динамика уровней базального и постпрандиального инсулина плазмы крови у женщин через 1 год лечения тиоктовой кислотой (600 мг/сутки) и высокобелковой диетой на 2100 калорий
Примечание: * - p<0,05, в сравнении с исходными показателями
В основной группе в результате приема тиоктовой кислоты получено существенное снижение индекса HOMA-IR на 37,8% (Т критерий Уилкоксона=22,5, p<0,05) в отличие от контрольной группы, где достоверных изменений среднего значения индекса инсулинорезистентности выявлено не было (рис. 2).
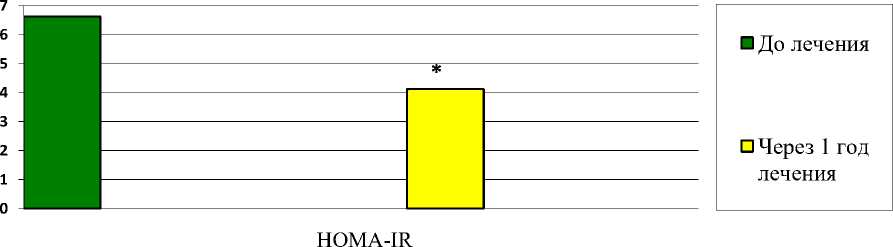
Рис. 2. Динамика уровня индекса HOMA-IR у женщин с синдромом поликистозных яичников через 1 год лечения тиоктовой кислотой (600 мг/сутки) и высокобелковой диетой на 2100 калорий
Примечание: * - p<0,05, в сравнении с исходными показателями
Через год после лечения в основной группе получено статистически значимое уменьшение среднего объема правого яичника на 30,2% и среднего объема левого яичника на 26,3% (Т критерий Уилкоксо- на=0, p<0,01 в обоих случаях). В группе контроля подобные положительные результаты через год диетотерапии отсутствовали. Полученные данные представлены на рисунке 3.
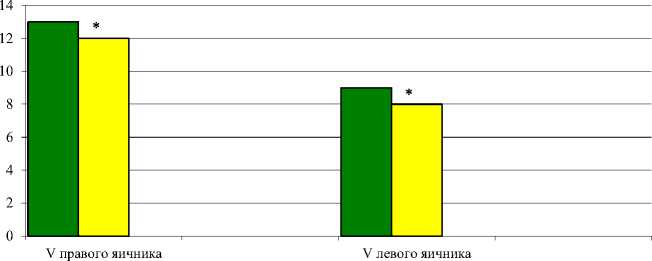
Рис. 3. Динамика среднего значения объема правого и левого яичников у больных с синдромом поликистозных яичников через 1 год лечения тиоктовой кислотой (600 мг/сутки) и высокобелковой диетой на 2100 калорий (по данным ультразвукового исследования)
-
□ До лечения
-
□ Через 1 год лечения
Лечение тиоктовой кислотой в сочетании с диетой на 2100 калорий у женщин с нормальной массой тела улучшило менструальную функцию и благоприятно повлияло на средний объем яичника. В основной группе у всех женщин нормализовалась продолжительность и урегулировалась частота овариально-менструального цикла. У трех пациенток (n=3; 18,8%) появился доминантный фолликул.
Данные таблицы 2 подтвердили наше предположение, что лечение препаратом тиоктовой кислоты на фоне диеты на 2100 калорий у лиц с СПКЯ и нормальной массой тела может приводить одновременно к увеличению толщины эндометрия, уровня эстрадиола плазмы крови, нормализации объема яичников на фоне увеличения веса тела исследуемых в пределах нормальных значений. Нежелательные явления не были выявлены.
Таблица 2. Динамика показателей ультразвукового исследования гениталий, средних показателей эстрадиола и массы тела у пациенток с синдромом поликистозных яичников через 12 месяцев лечения тиоктовой кислотой
|
Показатель |
Основная группа исходно, (n=15) |
Контроль исходно, (n=11) |
Основная группа после лечения, (n=15) |
Контроль после лечения, (n=11) |
|
Объем правого яичника, см3 |
13,42±0,81 |
12,9±0,65 |
9,37±0,91 |
13,22±0,9 |
|
Объем левого яичника, см3 |
12,02±0,75 |
12,66±0,42 |
8,85±0,652 |
12,45±0,33 |
|
Доминантный фолликул, % (n) |
6,25 (1) |
9 (1) |
25 (4) |
9 (1) |
|
Толщина эндометрия, мм |
5,72±1,18 |
5,61±1,27 |
5,9±1,42 |
5,88±1,34 |
|
Эстрадиол, пмоль/л |
152,62±51,3 |
150,23±47,8 |
370,76±71,153 |
154,2±50,2 |
|
Вес, кг |
21,94±0,68 |
21,52±0,7 |
22,94±0,704 |
21,78±0,19 |
Обсуждение. В нашей работе пациентки с нормальным весом имели высокие уровни базального и стимулированного инсулина, которые существенно снижались на фоне приема препаратов тиокто-вой кислоты. Проводимое лечение способствовало нормализации овариальноменструального цикла и появлению доминантного фолликула, что безусловно по- ложительно скажется как на предупреждении развития нарушений углеводного обмена и атеросклероза, так и на планировании будущей беременности.
До настоящего времени отсутствуют исследования по влиянию тиоктовой кислоты на ИР и гиперинсулинемию у женщин с СПКЯ и нормальной массой тела. В то время как именно гиперинсулинемия играет ключевую роль в стимуляции секреции андрогенов яичниками при этой патологии. Доказано, что ожирение и СПКЯ оказывают синергичное влияние на степень и тяжесть ИР и последующей гипе-ринсулинемии. Выявлено, что чувствительность к инсулину различается в зависимости от менструальной функции [12]. Так, у женщин с СПКЯ, нормальной массой тела и олигоменореей чаще отмечалась инсулинорезистентность, чем у женщин с регулярным циклом. По данным Conway и соавт. у 30% женщин без ожирения и СПКЯ инсулинорезистентность выражена незначительно [13]. Однако в исследовании Falcone и соавт. в 63% случаев женщины с нормальным весом имели ИР [14].
Заключение. Согласно полученным нами результатам лечение тиоктовой кислотой в сочетании с высокобелковой дие- той на 2100 калорий у пациенток с СПКЯ и нормальной массой тела способствует уменьшению уровней базального и стиму- лированного инсулина плазмы крови, индекса HOMA-IR, достоверного уменьшения среднего объема яичников, появлению овуляторных циклов подобно лечению ти-октовой кислотой пациенток с ожирением и СПКЯ [2, 5, 6]. Для пациенток с нормальной массой тела и СПКЯ немаловаж- ным моментом в увеличении уровня эстрадиола и толщины эндометрия, снижении ИР является увеличение массы тела в пределах нормальных значений. ИР у таких женщин связана с наличием центрального ожирения. По-видимому, для подтверждения этого факта у женщин с СПКЯ и нормальной массой тела необходимо не только рассчитывать ИМТ, но и измерять окружность талии в динамике.
Список литературы Применение тиоктовой кислоты у женщин с синдромом поликистозных яичников и нормальной массой тела
- Никольская В.А., Постольник Н.А., Меметова З.Н. Гиперинсулинемия, влияние на метаболические процессы в организме // Международный научно-исследовательский журнал. - 2014. - №5. - С. 390-394.
- Ivanova L.A. Thioctic acid and hormonal replacement treatment in men and women with 2 type diabetes and obesity. Journal of Clinical Lipidology: Abstracts. - 2007. - Vol. 1 (5). -P. 499.
- Holte J. Polycystic ovary syndrome and insulin resistance: thrifty genes struggling with overfeeding and sedentary life style // J. Endocrinol. Invest. - 1998. - Vol. 21. - P. 589-601.
- Palomba S. Role of metformin in patients with polycystic ovary syndrome: the state of the art // Minerva Ginecol. - 2008. - Vol. 60 (1). - P. 77.
- Ivanova L.A. Influence of Thioctic Acid on the Hyperinsulinemia and Ovarium Volume in Female Patients with Polycystic Ovary Syndrome // Open Journal of Endocrine and Metabolic Diseases. - 2015. - Vol. 5 (4). - P. 37-40.
- Ivanova L.A. Influence of Thioctic Acid on Polycystic Ovary Syndrome. 16th international congress of endocrinology-ICE/ENDO, June 21-24, 2014 Chicago, Illinois.
- Чернышева Е.Н., Панова Т.Н., Донская М.Г. Процессы перекисного окисления липи-дов и преждевременное старение при метаболическом синдроме // Кубанский научный медицинский вестник. - 2013. - №1. - С. 30-35.
- Андреева Ю.В. Гиперинсулинемия и инсулиновая резистентность (краткий литературный обзор) // Вестник новых медицинских технологий. - 2012. - №2 (XIX). - С. 6-7.
- Басов А.А., Мелконян К.И., Сторожук А.П. Влияние препаратов липоевой кислоты на показатели прооксидантно-антиоксидантной системы крови при сахарном диабете и гипотиреозе // Современные проблемы науки и образования. - 2013. - №6. - С. 15-18.
- McCarty M.F., Barroso-Aranda J., Contreras F. The rejuvenatory impact of lipoic acid on mitochondrial function in aging rats may reflect induction and activation of PPAR-gamma coac-tivator-1alpha // Medical Hypotheses. - 2009. - Vol. 72 (1). - P. 29-33.
- Подымова С.Д. Современные возможности клинического применения альфа-липоевой кислоты у больных хроническими заболеваниями печени // Фармацевтический вестник. - 2005. - № 11. - С. 37-38.
- Robinson S., Kiddy D., Gelding S.V. et al. The relationship of insulin insensitivity to menstrual pattern in women with hyperandrogenism and polycystic ovaries // Clin Endocrinol. -1993. - Vol. 39 (3). - P. 351-355.
- Conway G.S., Honour J.W., Jacobs H.S. Heterogeneity of the polycystic ovary syndrome. Clinical, endocrine and ultrasound features in 556 patients // Clin Endocrinol. - 1989. -Vol. 30 (4). - P. 459-470.
- Falcone T., Finegood Dt., Fantus G., et al. Androgen response to endogenous insulin secretion during frequently sampled intravenous glucose tolerance test in normal and hyperandro-genic women // J Clin Endocrinol Metabol. - 1990. - Vol. 71. - P. 1653-1657.


