Применение трехмерного моделирования в реконструктивной хирургии пищеводно-желудочного перехода
Автор: Хоробрых Т.В., Агаджанов В.Г., Кадиров Д.Д., Романовский А.А., Салихов Р.Е., Галяутдинов А.Ф.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические случаи
Статья в выпуске: 3 (93), 2025 года.
Бесплатный доступ
Введение. Хирургические вмешательства в области кардиоэзофагеальной зоны представляют собой сложные манипуляции, которые часто сопровождаются ятрогенными осложнениями. Это обусловлено спецификой анатомического строения данной зоны. В связи с этим, существует необходимость в более точных и безопасных методах планирования операций. Современные технологии, такие как трёхмерное моделирование, позволяют создать персонализированную модель данной области, что даёт возможность хирургу детально изучить анатомические особенности пациента. Это способствует более точной навигации во время операции и снижает вероятность возникновения осложнений. Цель исследования. Продемонстрировать эффективность применения трехмерного моделирования пищеводно-желудочного перехода при рецидивной грыже пищеводного отверстия диафрагмы. Материалы и методы исследования. Проведен анализ МСКТ больного рецидивной грыжей пищеводного отверстия диафрагмы с оценкой анатомических особенностей кардиоэзофагеальной зоны. Построенная на основании этого 3D модель области пищеводно-желудочного перехода с измененной анатомией предоставлена хирургам для планирования предстоящей операции. Полученные данные в последующем сопоставлены с интраоперационной картиной. Результаты. Пациенту с рецидивной грыжей пищеводного отверстия диафрагмы выполнено оперативное вмешательство с предварительным трехмерным моделированием. Интра- и постоперационные осложнения отсутствовали. Учитывая гладкое течение послеоперационного периода, пациент выписан на 5-е сутки после хирургического вмешательства. Заключение. Применение 3D моделирования у пациента с рецидивной грыжей пищеводного отверстия диафрагмы улучшило интраоперационную навигацию, что позволило избежать осложнений.
3D моделирование, компьютерная томография, рецидивная грыжа пищеводного отверстия диафрагмы
Короткий адрес: https://sciup.org/142245642
IDR: 142245642 | УДК: 617-089.844 | DOI: 10.17238/2072-3180-2025-3-158-164
3D modeling in reconstructive surgery of esophageal-gastric junction
Introduction. Surgical interventions in the gastroesophageal junction are complex manipulations that are often accompanied by iatrogenic complications. This is due to the specific anatomical structure of this area. Therefore, more accurate and secure methods for planning operations are required. Modern technologies, such as three-dimensional modelling, make it possible to create a personalized model of this area, which allows the surgeon to study the anatomical features of the patient in detail. This helps navigate more accurately during surgery and reduces the likelihood of complications. Purpose of the study. To demonstrate the effectiveness of using 3D modelling of the gastroesophageal junction area when performing surgical intervention for recurrent hiatal hernia. Materials and methods. The patient's MSCT was analysed by assessing the anatomical features of the area of interest. Based on this, a 3D model of the gastroesophageal junction area with an altered anatomy was provided to surgeons for planning the upcoming operation. The obtained data were subsequently compared with the intraoperative findings. Results. A patient with recurrent hiatal hernia underwent surgery with preliminary 3D modeling. No intra- or postoperative complications were observed. Considering the smooth course of the postoperative period, the patient was discharged in satisfactory condition on the 5th day after surgery. Conclusion. The use of 3D modeling in a patient with recurrent hiatal hernia enhanced intraoperative navigation, thereby preventing complications.
Текст научной статьи Применение трехмерного моделирования в реконструктивной хирургии пищеводно-желудочного перехода
Одним из наиболее перспективных направлений является использование компьютерного 3D моделирования, которое открывает новые горизонты в предоперационном планировании и реконструктивной хирургии [1–4]. В частности, это касается хирургического лечения грыж пищеводного отверстия диафрагмы (ГПОД), которые представляют собой сложные патологии, требующие тщательной подготовки и глубокого понимания анатомических особенностей пациента [5].
Анатомические особенности могут значительно различаться среди пациентов, что, в свою очередь, определяет важность предоперационного планирования [6, 7]. В этом контексте 3D моделирование позволяет создать точные трёхмерные модели анатомических структур, что способ-о ствует лучшему пониманию индивидуальных особенностей каждого пациента и, как следствие, более эффективному планированию хирургического вмешательства, особенно в условиях измененной анатомии, периэзофагита, спаечных процессов, укороченного пищевода.
Цель исследования. Продемонстрировать эффективность применения трехмерного моделирования пищеводно-желудочного перехода при рецидивной грыже пищеводного отверстия диафрагмы.
Материалы и методы
Пациент Д., 48 лет, госпитализирован в Университетскую клиническую больницу № 4 (УКБ № 4) в марте 2024 г. Предъявлял жалобы на тяжесть в эпигастрии после еды, дискомфорт за грудиной, изжогу при физических нагрузках и наклоне туловища, а также на тошноту и общее недомогание. Индекс массы тела – 30,2 кг/м2, физический статус по классификации Американского общества анестезиологов (American Society of Anesthesiologists, ASA) – II.
Пациент в течение трех лет принимал спазмолитические препараты и ингибиторы протонной помпы без очевидного стойкого эффекта.
В 2023 г. пациент был оперирован по поводу тотальной ГПОД 3-го типа по классификации Американского общества желудочно-кишечных и эндоскопических хирургов (Society of American Gastrointestinal and Endoscopic Surgeons, SAGES), выполнена лапароскопическая фундопликация по Ниссену. После перенесенного оперативного вмешательства был достигнут кратковременный регресс клинической симптоматики. С течением времени стал отмечать боли в эпигастральной области после приема твёрдой пищи, начали появляться признаки дисфагии с последующим неуклонным прогрессированием. С начала 2024 г. рацион питания пациента состоял только из жидкой пищи. При амбулаторном обследовании по месту жительства пациенту было рекомендовано консервативное лечение.
В условиях стационара УКБ № 4 проведено комплексное обследование пациента. Оценка предоперационного статуса пациента с помощью опросников продемонстрировала крайне неудовлетворительные результаты: GSRS (англ. Gastrointestinal Symptom Rating Scale, Шкала оценки желудочно-кишечных симптомов) – 51 балл, GERDQ (англ. Gastroesophageal Reflux Disease, Гастроэзофагеальная рефлюксная болезнь) – 11 баллов.
По данным эзофагогастродуоденоскопии (ЭГДС) Z-линия на расстоянии 30.0 см по меткам эндоскопа, смещена выше уровня ножек диафрагмы на 7.0 см. Кардия плотно не смыкается.
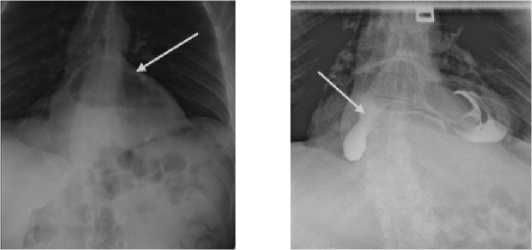
Рис. 1 (а, б). Рентгеноскопия с водорастворимым контрастированием. Желудок (стрелка) определяется в проекции наддиафрагмальных отделов и имеет каскадную форму
Fig. 1 (a, b). Fluoroscopy with water-soluble contrast. The stomach (arrow) is visualized in the projection of the supradiaphragmatic regions and has a cascade-shaped configuration
Для наглядного представления особенностей интересующей анатомической области, совместно со специалистами лучевой диагностики, по данным МСКТ выполнено 3D моделирование. При предварительном виртуальном планировании информация обрабатывалась при помощи соответствующего программного обеспечения (Inobitec Medical Imaging Software), инобитек DICOM-просмотрщик PRO (лицензионный) (рис. 3).
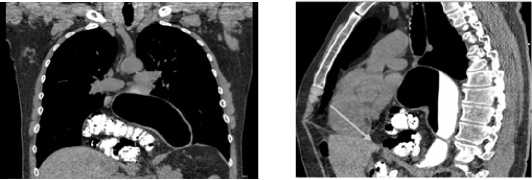
Fig. 2 (a, b). MSCT of the chest and abdomen with intravenous and per os contrast, direct and lateral projections. The stomach, the hepatic flexure, and part of the transverse colon are located in the thoracic cavity. The arrow indicates the conventional level of the diaphragm
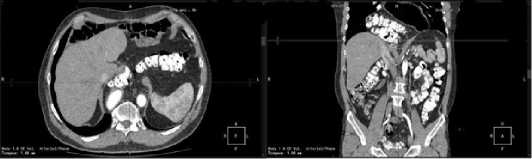
Рис. 3. Этап сегментации и выполнения компьютерного моделирования. Синий цвет – желудок над диафрагмой, зеленый – поперечная ободочная кишка, красный – артерии, голубой – двенадцатиперстная кишка
Fig. 3. Segmentation and computer modeling stage. Blue – stomach above the diaphragm, green – transverse colon, red – arteries, light blue – duodenum
С целью повышения наглядности, с помощью наложения маски был создан контур, соответствующий положению диафрагмы. Для каждой наложенной маски были созданы поверхности сегментаций, что повысило наглядность полученных трехмерных моделей. Полученные данные в последующем сопоставлены с интраоперационной картиной (рис. 4).
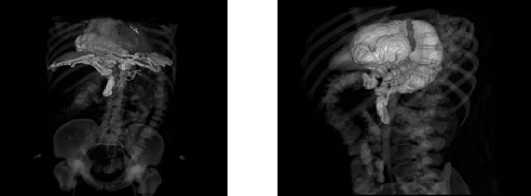
Рис. 4 (а, б). 3D моделирование. На рис. 4а: синий цвет – желудок над диафрагмой, зеленый – поперечная ободочная кишка над диафрагмой, оранжевый – диафрагма, красный – артерии, голубой – двенадцатиперстная кишка. На рис. 4б (в грыжевом мешке): желтый цвет – желудок над диафрагмой, фиолетовый – пищевод Fig. 4 (a, b). 3D modeling. Fig. 4a: blue – supradiaphragmatic stomach, green – supradiaphragmatic transverse colon, orange – diaphragm, Red – arteries, light blue – duodenum. Fig. 4b (within the hernia sac): yellow – stomach above the diaphragm, purple – esophagus
Полученные данные анамнеза, клинической картины, инструментальных методов исследования свидетельствовали о крайне низком качестве жизни (согласно опросникам, GSRS и GERDQ) ввиду наличия стойких симптомов патологического рефлюкса.
Исходя из проведенного обследования, пациенту установлен диагноз: Рецидивная грыжа пищеводного отверстия диафрагмы. Рефлюкс эзофагит. Лапароскопическая фундопликация по Ниссену от 2023 г. Осложнение: пептическая стриктура нижнегрудного отдела пищевода, эрозивный рефлюкс-эзофагит.
Проведённое лечение и его результат, последующая оценка состояния пациента и контрольные обследования
В мае 2024 года пациенту выполнена операция в объеме лапароскопической рефундопликации по методике А.Ф. Черноусова.
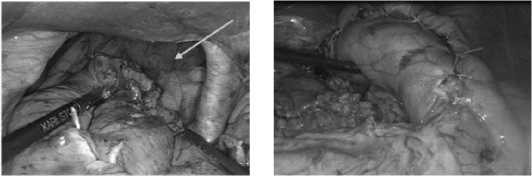
Рис. 5. Интраоперационное фото. На рис. 5а: расширенное до
10 см пищеводное отверстие диафрагмы (стрелка). На рис.
5б: ремоделированная фундопликационная манжета
Fig. 5. Intraoperative photograph. Fig. 5a: the esophageal hiatus of the diaphragm is dilated to 10 cm (arrow). Fig. 5b: the remodeled fundoplication wrap
В качестве заключительного этапа оперативного вмешательства произведена задняя крурорафия Z-образными швами с помощью нерассасывающегося синтетического шовного материала для ушивания ПОД до диаметра пищевода без его ущемления.
Интраоперационные манипуляции, выполняемые хирургом, с возможностью обращения к 3D модели обеспечивали ориентацию «на месте» и идентификацию критических анатомических ориентиров.
Продолжительность операции составила 170 мин. Интраоперационная кровопотеря – 100 мл. Интраоперационные осложнения отсутствовали.
Послеоперационный период без осложнений, пациент выписан на 5-е сутки после операции под амбулаторное наблюдение по месту жительства.
Обсуждение
В данном клиническом случае, содержимое грыжевого мешка, расположение органов и структур относительно друг друга полностью соответствовали дооперационной трехмерной модели.
Вероятность рецидива после операции, выполненной по поводу гастроэзофагеальной рефлюксной болезни (ГЭРБ) различна. Рецидив ГЭРБ и ГПОД является одним из наиболее распространенных осложнений после антирефлюксной хирургии, с частотой встречаемости от 4 % до 24 % [10]. Рецидивы классифицируются как симптоматические и рентгенологические. Рентгенологические рецидивы могут достигать 59 %, но в большинстве случаев они бессимптомны и не требуют повторной операции [11]. Только около 5–8 % пациентов с рецидивом нуждаются в повторном хирургическом вмешательстве из-за выраженных симптомов [12].
Согласно данным литературы наибольшие сложности при реконструктивных операциях представляет собой измененная анатомия пищеводно-желудочного перехода вследствие длительно существующей грыжи ПОД, явлений периэзофагита, укорочение пищевода и адгезивного процесса между элементами грыжевого мешка [13]. Развитие предоперационного 3D-моделирования, позволяющее представлять анатомическую информацию в интерактивной и визуально понятной форме, открывает перспективные горизонты для улучшения результатов реконструктивных операций на пищеводно-желудочном переходе [14]. Тем не менее в литературе до сих пор имеется мало данных о ее роли в хирургии ГПОД.
Доказана клиническая значимость трехмерной реконструкции хиатальных грыж для практикующих врачей, как ценного инструмента, упрощающего понимание сложных анатомических взаимосвязей при данном заболевании, а также планировании операций в анатомическом аспекте [14–16].
В описанном клиническом случае сопоставление интраоперационной картины с компьютерной моделью позволило нам интерпретировать взаимоотношение органов и структур в условиях измененной хирургической анатомии и избежать травмы соседних органов или значимых анатомических структур, во многом за счет возможности выбора инструмента в каждой конкретной зоне оперирования. В первую очередь, речь идет об альтернативе использования хирургической энергии, холодному инструменту и наоборот.
Конечно, методика требует более детального исследования на статистически значимом материале, а наши заключения по данному клиническому случаю являются лишь предварительными.
На сегодняшний день 3D реконструкция постепенно находит всё большее применение в различных областях хирургии, причём использование искусственного интеллекта позволяет сделать данный метод визуализации более доступным для освоения широким кругом специалистов [14, 17].
Заключение
Использование трехмерной модели для реконструкции кардиоэзофагельного перехода может позволить улучшить результаты хирургического лечения, за счет уменьшения интраоперационных осложнений. Основное преимущество данной технологии заключается в детальном понимании индивидуальных анатомических особенностей, планировании операции, придерживаясь принципов безопасной хирургии.
Интеграция анатомических данных в 3D-модели, создаваемые на этапе предоперационного планирования, потенциально может расширить возможности реконструктивной хирургии пищеводно-желудочного перехода за счет более точного и персонализированного подхода.


