Применение вакуум-терапии и эпидермального фактора роста в комплексном лечении стерномедиастинита
Автор: Левчук А.Л., Катков А.А., Гудымович В.Г., Бозиев З.Н., Федотов П.А., Зайниддинов Ф.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Клинические наблюдения
Статья в выпуске: 2 т.20, 2025 года.
Бесплатный доступ
Представлено клиническое наблюдение успешного лечения больной гнойным стерномедиастинитом, развившимся в ближайшем послеоперационном периоде после кардиохирургического вмешательства. Ранняя диагностика этого грозного осложнения осуществлялась с выполнением мультиспиральной компьютерной томографии с 3D-реконструкцией. В комплексном лечении стерномедиастинита использованы: этапные хирургические обработки раны с вакуум-терапией и местным применением эпидермального фактора роста. Достигнуто клиническое выздоровление с сохранением удовлетворительного качества жизни пациентки.
Послеоперационный стерномедиастинит, вакуум-терапия, эпидермальный фактор роста
Короткий адрес: https://sciup.org/140309995
IDR: 140309995 | DOI: 10.25881/20728255_2025_20_2_141
Application of vacuum therapy and epidermal growth factor in the complex treatment of sternomediastinitis
A clinical case of successful treatment of a patient with purulent sternomediastinitis that developed in the immediate postoperative period after performing cardiac surgery is presented. Early diagnosis of this formidable complication was carried out by performing multispiral computed tomography with 3D reconstruction. In the complex treatment of sternomediastinitis, the main role was played by stage-by-stage surgical treatment of wounds using vacuum therapy and topical application of epidermal growth factor. A clinical recovery has been achieved while maintaining a high level of quality of life for the patient.
Текст научной статьи Применение вакуум-терапии и эпидермального фактора роста в комплексном лечении стерномедиастинита
В России ежегодно выполняется около 60 тыс. операций на сердце [1]. Гнойно-септические осложнения со стороны передней грудной стенки после операций с трансстернальным доступом по-прежнему остаются на достаточно высоком уровне и встречаются до 4% наблюдений [2]. Учитывая, что в мире выполняется более 1 млн. операций на сердце и органах средостения из трансстернального доступа, то фактически гнойный стерномедиастинит ежегодно развивается у 10 тыс. пациентов [2].
Срединный трансстернальный доступ для хирургических вмешательств на органах средостения был предложен Мильтоном С. (1897), а широко он был внедрен в хирургическую практику Джулианом С. (1957) [3].
Учитывая особенности анатомического строения передней грудной стенки и оперативного доступа, гнойно-септические осложнения при этом наиболее часто проявляются нестабильностью остеосинтеза грудины, поверхностным инфильтрированием мягких тканей (SSI) и глубокой стернальной инфекцией (DSI) (остеомиелит грудины, гнойный передний медиастинит) [4; 5].
Стерномедиастинитом принято считать развитие глубокого инфекционного процесса области оперативного вмешательства при несостоятельности шва грудины после срединной стернотомии. Нередко в данной ситуации больные не получают должного объема хирургического лечения, и осложнение принимает затяжной и рецидивирующий характер, летальность при котором достигает 25% [6].
Значимыми факторами риска в развитии стерномедиастинита являются: ожирение, сахарный диабет, хронические обструктивные заболевания легких, остеопороз грудины, наличие хронических очагов инфекции, повторные трансстернальные вмешательства [1; 5].
Помимо гнойного воспаления в клетчатке переднего средостения при стерномедиастините отмечается остеомиелитическое поражение грудины, а в ряде случаев и ребер. Объем гнойно-некротического поражения грудины может быть различным: от локального краевого остеомиелита до тотального остеонекроза всей грудины. Нередко в гнойно-воспалительный процесс данной локализации вовлекаются хрящевая часть реберной дуги с развитием хондро-перихондрита и грудно-реберные сочленения с формированием гнойного остеоартрита [4; 7].
В настоящее время приято различать следующие стерномедиастиниты: возникающие в ближайший месяц послеоперационного периода (от 4 суток до 3 недель) и позднее (от 1 месяца до 1 года). Раннее осложнение стернотомии протекает наиболее тяжело, обычно сопровождаясь тотальным нагноением раны, широким диастазом краев грудины и обширным вовлечением в гнойный процесс клетчатки переднего средостения. Поздние стерномедиастиниты, протекающие более доброкачественно, клинически проявляются чаще всего, формированием гнойных лигатурных свищей в области послеоперационного рубца.
В диагностике стерномедиастини-та первостепенную роль играет мульти-спиральная компьютерная томография (МСКТ) с 3D-реконструкцией, позволяющая определить локализацию, распространенность, объем гнойного поражения мягких тканей и остеомиелитический процесс грудины и ребер. Однако, даже комплексное инструментальное обследование (УЗИ, фистулография, МСКТ и т.д.) не всегда дает возможность объективизировать реальную картину зоны поражения тканей гнойно-некротическим процессом. Поэтому только тщательная интраоперационная ревизия тканей помогает наиболее точно оценить весь объем инфекционного очага.
Наиболее существенным и важным моментом диагностики является, по нашему мнению, верификация бактериальных патогенов, вызывающих развитие стерномедиастинита, которые в 37,3% случаев представлены микроорганизмами MRSA и MRSE с высокой степенью антибиотикорезистентности. Выявление патогенной флоры, ее изменчивость и определение вирулентности, позволяет в большинстве случаев проводить адекватную целенаправленную антибиоти-котерапию.

В основе хирургического лечения стерномедиастинита лежит радикальная хирургическая обработка гнойно-некротического очага поражения мягких тканей грудной клетки и костных структур с полным иссечением всех участков нежизнеспособной подкожной и медиастинальной клетчатки, очагов остеомиелита грудины и ребер с участками хондрита. В обязательном порядке мы стараемся удалить все инфицированные проволочные швы грудины, т.к. именно они являются эпицентрами локализации бактериальных биопленок, представляющих собой сообщества микроорганизмов, вегетирующих в полисахаридном матриксе, влияющие на механизмы антибиоти-корезистентности. Формирование биопленки является ключевым фактором вирулентности широкого круга патогенных бактерий, которые вызывают как острые, так и хронические инфекции. Толерантность бактерий биопленки к антибактериальным средствам лежит в основе большинства малокурабельных рецидивирующих и хронических стер-номедиастинитов после стернотомий и операций на сердце.
Послеоперационное ведение раны (в I фазе течения раневого процесса) грудной клетки после радикальной хирургической обработки стерномедиастинита в большинстве случаев осуществляется открыто с применением асептических мазей на водорастворимой основе (лево-меколь, левосин и т.д.). После разрешения гнойно-воспалительного процесса (во II фазе течения раневого процесса) при возможности проводятся реостеосинтез грудины и кожная пластика раны местными тканями. При больших и сложных дефектах используют миопластику костного дефекта грудными мышцами.
В настоящее время нами накоплен определенный опыт в лечении гнойных осложнений в кардиохирургии, прежде всего такого жизнеугрожающего состояния, как стерномедиастинит, с помощью вакуум-ассистированных систем. Наложение вакуумной повязки производим интраоперационно под эндотрахеальным наркозом после радикальной хирургической обработки гнойно-некротического очага и тщательного гемостаза. Вакуум-ассистированная система позволяет не только осуществить адекватный контроль экссудации, но и обеспечить стабилизацию костного каркаса грудной клетки. Смена повязки осуществляется каждые 2–3 суток в первую неделю лечения с последующим увеличением экспозиции до 4–5 суток.
Для стимуляции роста грануляционной ткани в ране во II фазе течения раневого процесса нами в последние годы широко используется эпидермальный фактор роста в сочетании с сульфадиазином серебра (препарат «Эбермин»), который продемонстриовал наилучшие результаты в подавлении микробного раневого пейзажа, улучшающий трофику и регенерацию тканей, способствуя эпите-лизации, рубцеванию и восстановлению эластичности тканей. Осложнений и нежелательных явлений при проведении вакуумной терапии в сочетании с местным применением эпидермального фактора роста в комплексном лечении стерноме-диастинита мы не наблюдали.
Клиническое наблюдение
Больная Х., 60 лет, поступила в НМХЦ им. Н.И.Пирогова для оперативного лечения по поводу хронической ИБС, стенокардии 3 функционального класса. 26.11.2024 года пациентке выполнено: аутоартериальное шунтирование ПМЖА с использованием ЛВГА и аутовенозное шунтирование с ПМЖА и ВТК в условиях ИК, холодовой кровяной кардиоплегии. Операция сопровождалась техническим сложностями, длительность ее составила 5 часов. Послеоперационный период протекал тяжело, с развитием фибрилляции предсердий, инфаркта миокарда, сердечной недостаточности. На 7-е сутки послеоперационного периода у пациентки отмечен краевой некроз в области раны (Рис. 1), повышение температуры тела до 38,6 °С. В анализах крови – лейкоцитоз до 21 х 109/л и повышение уровня маркеров воспаления (прокальцитонин – 4 нг/мл). Компьютерная томография подтвердила наличие несостоятельности остеосинтеза грудины, ее остеомиелит и передний стерномеди-астинит (Рис. 2). Больная оперирована. Произведено иссечение некротизированных тканей кожи и подкожной-жировой клетчатки с вскрытием абсцесса (60 мл) в нижне-переднем средостении. При ревизии раны отмечен диастаз краев грудины в нижней трети, нагноение в области всех проволочных швов с распространением гноя в переднее средостение в пределах расхождения грудины (Рис. 3). Результат бактериального посева подтвердил наличие Enterococcus faecalis. В этой области края распила грудины остеомиелитически изменены на протяжении 2 мм от края. Произведено снятие проволочных швов, остеонекрэктомия, санация раны раствором пронтосана. Учитывая распространенность гнойного процесса и
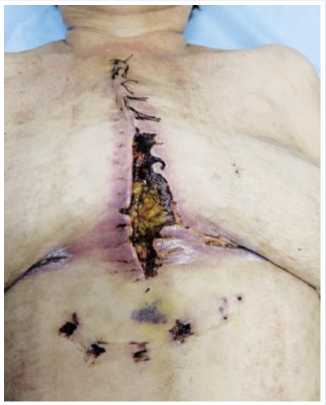
Рис. 1. Ранний послеоперационный стерноме-диастинит с расхождением кожной раны (7-е сутки после операции).
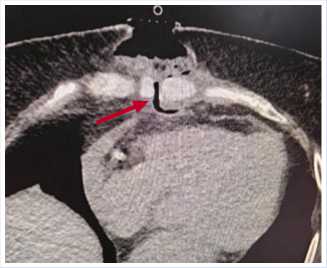
Рис. 2. КТ грудины: несостоятельность остеосинтеза, признаки остеомиелита.
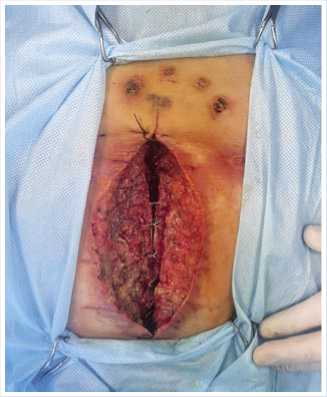
Рис. 3. Состояние раны после вскрытия гнойника (60 мл) в переднем средостении, радикальной хирургической обработки с сохранением проволочных швов (I фаза течения раневого процесса).

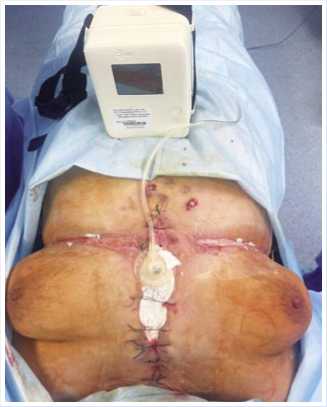
Рис. 4. Вакуумная система, наложенная на рану после хирургической обработки (постоянное отрицательное давление – 80 мм рт. ст.).
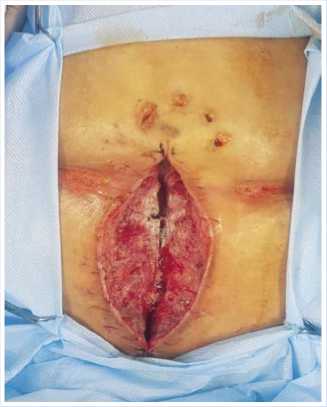
Рис. 6. Вид раны после снятия вакуумной системы на 6-е сутки.
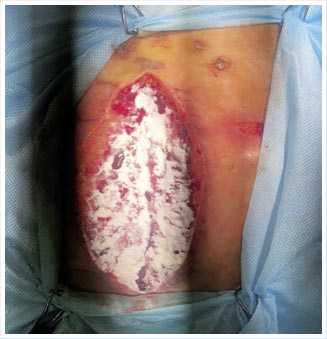
Рис. 8. Обработка гранулирующей стернальной раны мазью «Эбермин».
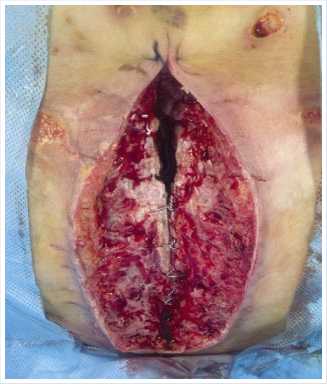
Рис. 5. Гранулирующая рана передне-нижнего средостения с диастазом краев грудины после снятия проволочных швов и выполнения краевой остеонекрэктомии (II фаза течения раневого процесса).

Рис. 7. Осложнение вакуум-терапии – аррозив-ное кровотечение под фиксированное пленочное покрытие.
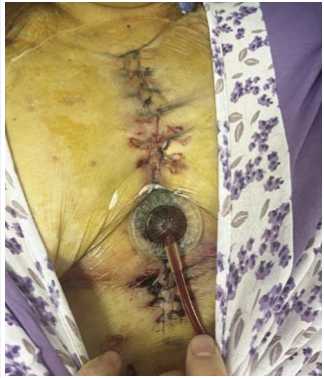
Рис. 9. Частичное ушивание стернальной раны с сохранением вакуумной повязки.
особенности течения стерномедиасти-нита с нестабильностью грудины, решено ведение раны осуществлять открыто с использованием вакуумной повязки (Рис. 4) с разрежением 70 мм рт. ст. Вакуумную терапию проводили в течение 12 суток. Выполнено четыре смены VAC-системы (Рис. 5, 6) с удалением раневого эксудата объемом до 300 мл/сут-ки. После третьей замены VAC-системы возникло осложнение – аррозивное кровотечение (Рис. 7), которое потребовало демонтажа VAC-системы и выполнения тщательного гемостаза. В дальнейшем
рана велась с применением эпидермального фактора роста и сульфадиазина серебра (Рис. 8). С появлением грануляций в ране и отрицательных бактериологических посевов, была выполнена ее вторичная хирургическая обработка с частичным ушиванием и сохранением вакуумной повязки (Рис. 9). После полного купирования гнойного процесса и хорошего стимулирующего эффекта препарата «Эбермин», операционная рана вновь подвергнута вторичной хирургической обработке с наложением адаптационного серкляжного шва на грудину мононитью №2, закрытием раневого дефекта вторичными швами на резинках (Рис. 10).
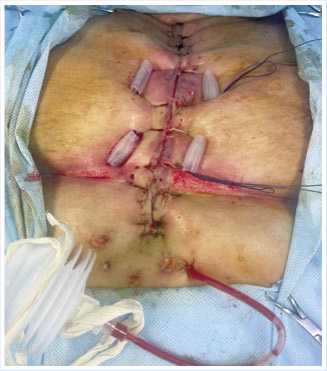
Рис. 10. Вторичная хирургическая обработка раны с демонтированием вакуумной повязки и наложением вторичных швов с серкляжным швом грудины.

Г
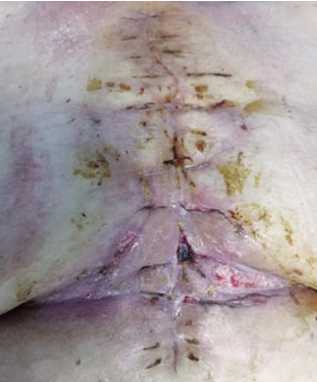
Рис. 11. Окончательный вид раны после снятия вторичных швов (18-е сутки лечения).
Послеоперационный период протекал без осложнений, заживление раны – первичным натяжением (Рис. 11). На 30-е сутки больная была выписана из стационара. На контрольной КТ грудной клетки отмечено полное сопоставление грудины, отсутствие признаков воспалительного процесса и скопления экссудата (Рис. 12).
Качество жизни пациентки при выписке, согласно общего опросника здоровья SF-36, составило 30 баллов, а индекс физической активности увеличился в 2,5 раза, что свидетельствует о правильности и эффективности выбранного метода лечения такого грозного осложнения, как гнойный стерномедиа-стинит после кардиохирургического оперативного вмешательства, путем применения вакуумной терапии в сочетании с эпидермальным фактором роста.
Следует отметить, что раны любого происхождения едины в своих биологических законах заживления, которые детерминированы генетически. В связи с этим, общие принципы лечения должны быть едины для ран любой этиологии, а лечебная тактика должна определяться фазой раневого процесса и его особенностями. Только дифференцированный подход и раннее направленное воздействие на раневой процесс на различных этапах лечебного алгоритма, с учетом индивидуальных особенностей ран и
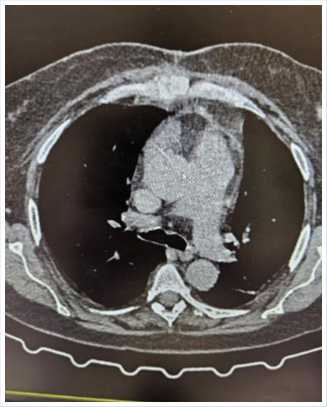
Рис. 12. Контрольное КТ грудины: консолидация, полное сопоставление.
их течения, позволяют добиться основной цели – подавления бактериальной флоры, купирования воспалительного процесса и избавления больного от раневого дефекта.
Заключение
Таким образом, применение вакум-терапии в сочетании с эпидермальным фактором роста у больных гнойным послеоперационным стерномедиастинитом позволяет значительно сократить сроки первой фазы течения раневого процесса, длительность подготовки пациентов к реконструктивным вмешательствам, снизить количество травматичных перевязок, ускорить рост грануляции и стимуляцию регенеративных процессов в ране, во второй фазе течения раневого процесса, с последующим наложением ранних вторичных швов. Внедрение вышеуказанной методики в широкую хирургическую практику с высокой долей вероятности может привести к снижению уровня летальности у этой тяжёлой категории пациентов. Вакум-терапия должна использоваться с высокой степенью осторожности у больных кардиохирургического профиля, когда есть возможность получения активного аррозивного кровотечения, в виду необходимости приёма антикоагулянтной терапии. Оптимальным методом для оценки эффективности проводимой методики является бакте- риологические исследования с забором посевов из раны при каждой перевязке, с помощью которых определяется биологическая обсемененность раны, этиология и вид возбудителя, чувствительность его к антибактериальным препаратам.
Список литературы Применение вакуум-терапии и эпидермального фактора роста в комплексном лечении стерномедиастинита
- Слесаренко С.С., Агапов В.В. Прелатов В.А. Медиастинит. - М., 2005. - 199 с.
- Оболенский В.Н., Никитин В.Г., Семенистый А.Ю. и др. Использование принципа локального отрицательного давления в лечении ран и раневой инфекции // Новые технологии и стандартизация в лечении осложнённых ран: Сб. ст. - М., 2011. - C.58-65.
- Павлюченко С.В., Жданов А.И., Попов К.В. Современные подходы к хирургическому лечению послеоперационного стерномедиастинита // Грудная и сердечно-сосудистая хирургия. - 2019. - №4. - C.299-308. EDN: WKGHOY
- Винокуров И.А., Иванов К.П., Тагабилев Д.Г. и др. Новая парадигма лечения стерномедиастинита // Хирургия. - 2023. - №12. - C.52-68.
- Вишневский А.А. Хирургия грудной стенки: Руководство. М., 2005. - 312 с.
- Стойко Ю.М., Левчук А.Л., Игнатьев А.И. Применение метода локального отрицательного давления в комплексном лечении пациентов с раневой инфекцией. - М., 2021. - 47 с. EDN: ELUUAU
- Lafci G, Yasar E, Cicer O, et al. A novel modified Robicsek technique for sternal closure: "Double-check", Asian Cardiovascular and Thoracic Annals 2013; 22(6): 758-760.


