Принципы организации и технологии развития службы безопасности лекарств и фармаконадзора в Самарской области
Автор: Зарубина Елена Григорьевна, Бакчеева Раиса Филипповна, Родимова Марина Васильевна, Девяткин Анатолий Анатольевич
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Клиническая медицина
Статья в выпуске: 3 (3), 2011 года.
Бесплатный доступ
Значительные успехи в различных областях медицины, достигнутые за последние годы, во многом обязаны внедрению в медицинскую практику новых высокоэффективных лекарственных средств. Вместе с тем, большую тревогу вызывают все чаще появляющиеся сообщения об осложнениях лекарственной терапии. Однако врач сегодня не может работать без лекарств. Внедрение в его практику новых лекарственных препаратов способно в значительной мере продлить жизнь пациентам и обеспечить качество их жизни.
Фармаконадзор, лекарственное средство, биологически активные добавки, безопасность лекарств
Короткий адрес: https://sciup.org/14343982
IDR: 14343982
Principles of organization and development techniques in security department of drug and pharmacological surveillance in Samara region
Significant progress in various fields of medicine, achieved in recent years, largely due to the introduction into medical practice new high-performance drugs. However, more alarming is increasingly appearing reports about complications of drug therapy. However, a doctor can not function without medication today. Practical application of new drugs can significantly prolong patients' lives and ensure the quality of their lives.
Текст научной статьи Принципы организации и технологии развития службы безопасности лекарств и фармаконадзора в Самарской области
Проблема безопасности лекарств в последнее время стала одной из актуальнейших проблем здравоохранения в мире. Это вызвано появлением множества лекарственных средств с высокой биологической активностью, возросшей сенсибилизацией людей к химическим и биологическим веществам, нерациональным применением лекарств, взаимодействием препаратов друг с другом и с биологически активными добавками, с использованием недоброкачественных препаратов. В результате у многих пациентов возникают тяжелые, подчас необратимые осложнения, возрастает число госпитализации и летальных исходов, вызванных лекарственной терапией.
Общеизвестно, что осложнения лекарственной терапии вышли на четвертое место среди причин смертности после сердечно-сосудистых заболеваний, травм и несчастных случаев, онкозаболеваний (Lazaran I. et al., 1998). В то же время процент госпитализации в связи с неблагоприятными побочными реакциями (НПР) составляет: Норвегия - 11,5 %, Франция – 13 %, Великобритания – 16 %. Кроме того, 15-20 % бюджета больниц расходуется на лечение больных с НПР и на контроль безопасности лекарственных средств (КБЛС) (Wite I. et al., 1999) .
Таких данных по России нет. Поэтому можно констатировать, что в России недостаточно ведется работа по выявлению, регистрации, научному анализу НПР, что сказывается на ограниченности КБЛС. В стране не налажена система сбора и обобщения информации по НПР и КБЛС, отсутствуют четкие рекомендации, а там, где они имеются, они не соблюдаются: использование лекарственных средств (ЛС) у беременных женщин, у детей, особенно младших возрастов. В геронтологии до сих пор не получило должной оценки явление полипрагмазии.
Научный международный и национальный опыт показывает, что такая ситуация приводит к существенному росту суммарного бремени общественных затрат как за счет чисто медицинских (повышения сроков госпитализации и нетрудоспособности), так и социальных (повышение процента инвалидности, снижение продолжительности жизни, повышение летальности и смертности) последствий от НПР и недостаточности контроля КБЛС. Все это привело к тому, что практически во всех развитых странах созданы и функционируют специальные службы по контролю безопасности лекарств (фармаконадзор).
Всемирная Организация Здравоохранения (ВОЗ) уделяет большое внимание этой чрезвычайно актуальной проблеме и проводит специальный проект «Создание и развитие фармаконадзора в странах СНГ», в том числе и в Российской Федерации. Российская Федерация в декабре 1997 года стала полноправным участником этой программы. Федеральный центр по изучению побочных действий лекарств Минздрава России начал активное сотрудничество с Центром ВОЗ, в базе данных которого имеется около 2 миллионов сообщений о неблагоприятных побочных действиях лекарств.
Условиями включения в международную Программу ВОЗ по мониторингу лекарств являются:
Наличие Национального Центра по контролю НПР, утвержденного МЗ РФ. Пути обмена информацией о нежелательных побочных действиях лекарств рассматриваются в схеме, изображенной на рис. 1.
Рис. 1. Пути обмена информацией о нежелательных побочных действиях лекарств
Рассмотренные выше статистические данные привели к необходимости создания pharmacovigilance (фармакобдительность, фармаконадзор) - системы контроля безопасности лекарств, которая включает в себя выявление, изучение, оценку и профилактику неблагоприятных побочных реакций.
Учитывая важность и масштаб проблемы лекарственных осложнений, во многих странах были приняты специальные законы о лекарственных средствах, которые, в частности, обязывают медицинских и фармацевтических работников, а также производителей лекарств сообщать в соответствующие государственные службы здравоохранения о выявленных и подозреваемых случаях НПР (Астахова А.В., Лепахин В.К., 2001). В 1998 г. в России был принят федеральный закон «О лекарственных средствах», статья 41. Субъекты обращения лекарственных средств обязаны сообщать... обо всех случаях побочных действий лекарственных средств и об особенностях взаимодействия лекарственных средств с другими лекарственны- ми средствами, которые не соответствуют сведениям о лекарственных средствах, содержащихся в инструкциях по их применению».
Структура контрольно-разрешительной системы нашей страны приведена на рис. 2.
Проблема лекарственной терапии осложняется еще тем, что сегодня очень важно определить, какими лекарствами надо пользоваться российскому врачу: инновационными препаратами или, как многие страны мира, воспроизведенными ЛС. Безусловно, наиболее приемлемо сочетанное применение оригинальных и дженериковых ЛС. Однако по словам члена-корреспондента РАМН, главного клинического фармаколога России Белоусова Ю.Б., на фармацевтическом рынке России сегодня реализуют свою продукцию 1500 дженериковых компаний, и в такой ситуации нельзя гарантировать качество ЛС и отсутствие их риска для больных, в то время как, например, на рынке США работают порядка 10 крупных производителей дженериков, но не возникает вопросов к качеству ЛС, так как крупная компания с большими продажами никогда не пойдет на то, чтобы сэкономить на качестве препарата и поставить под удар здоровье пациента, а, следовательно, свою репутацию.
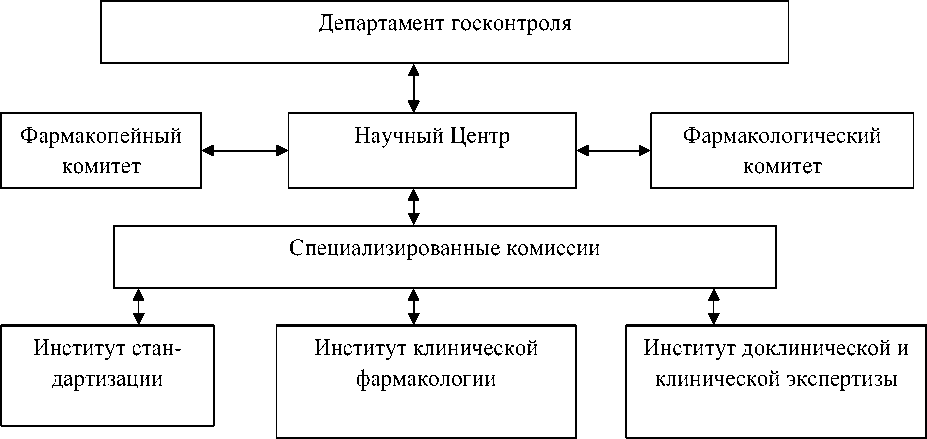
Рис. 2. Структура контрольно-разрешительной системы в РФ
Отечественный и зарубежный опыт, связанный с выявлением и изучением НПР, свидетельствует о том, что для повышения результативности в этой работе в стране с большой территорией и многомиллионным населением создание сети региональных центров является абсолютно необходимым. В настоящее время в России функционируют более 30 региональных центров по изучению неблагоприятных побочных действий лекарств. Самарский региональный центр начал работать с марта 2004 года на базе ООО «Информ-бюро». Основными задачами центра являются организация работы по выявлению и учету НПР на лекарственные препараты в регионе, анализ, систематизация, верификация сообщений о побочных реакциях, информирование медицинской общественности о побочных реакциях и о проблемах, связанных с лекарственными осложнениями. Несмотря на то, что изучение переносимости и выявление побочных реакций на новые препараты проводится на стадии доклинического и клинического изучения, истинное представление о переносимости препарата может быть по- лучено только в процессе их широкого применения на большом количестве больных. Особенности действия лекарственных препаратов у больных различных категорий (дети, беременные, лица старших возрастных групп, больные с поражением функций почек, печени), а также последствия взаимодействия лекарств выясняются, как правило, после регистрации лекарств и их многолетнего применения в реальной жизни. Поэтому необходим послереги-страционный мониторинг. Нежелательные побочные реакции могут возникать при приеме любых лекарственных препаратов и главная задача врача, провизора, фармацевта - раннее выявление и предупреждение этих реакций. При этом чем более наблюдательным и ответственным будет врач, тем меньше времени пройдет до открытия относительно редких негативных воздействий и принятия мер для их предупреждения, соответствующих дополнений в инструкции по применению лекарства, или вообще запрещения использования препарата в медицинской практике. Жизнь показала, что заставить врача сообщать о негативных эффектах лекарств не могут никакие законы и приказы. Здесь необходимы образование, убеждение, принципиальность, воспитание соответствующей культуры. Врач должен понимать свою ответственность не только перед конкретным больным, но и перед тысячами других пациентах, которые будут принимать препарат. Сообщая о побочных действиях лекарств, врач не должен бояться наказания за назначение препарата, ведь таково свойство всех лекарств - кроме терапевтического иметь побочные явления. Прежде всего, необходимо отметить, что врач не обязательно должен быть уверен в наличии причинно-следственной связи между приемом препарата и возникновением осложнения. Врач должен заполнить карту извещения о подозреваемой неблагоприятной реакции на лекарственное средство, разработанную и утвержденную Минздравом РФ. Сообщать следует в Центр:
-
1) обо всех подозрениях по новым лекарственным средствам (новыми считаются препараты в течение пяти лет после их регистрации);
-
2) о неожиданных реакциях на «старые» препараты;
-
3) о серьезных неблагоприятных эффектах на все препараты или при взаимодействии лекарственных средств;
-
4) о негативных влияниях на плод и новорожденных;
-
5) о неэффективности лекарственного препарата.
Напоминаем врачам и провизорам, что, согласно статье 41 Федерального закона «О лекарственных средствах», все медицинские работники обязаны сообщать о любых случаях побочных действий лекарств и об особенностях их взаимодействия, не соответствующих сведениям, содержащимся в инструкциях по применению, в региональный центр по контролю НПР в виде правильно заполненных карт извещений по адресу: 443 045 г. Самара, ул. Уссурийская 2а, «Самарский региональный центр по контролю побочных неблагоприятных действий лекарств» ООО «Информ-бюро».
Неблагоприятные побочные реакции - это вредные, нежелательные эффекты, которые возникают при использовании доз ЛС, рекомендованных для профилактики и лечения заболеваний (Белоусов Ю.Б., Леонова М.В., 2002). Механизмами развития неблагоприятных побочных реакций лекарственных средств являются: тератогенные эффекты, прямое токсическое действие препарата или его метаболита, аллергические реакции, канцерогенные эффекты, генетические нарушения.
Побочные реакции типа А («действие лекарства») связаны с токсичностью самого препарата или его метаболита, фармацевтическими, генетическими факторами, а также заболеваниями почек и печени, приводящими к изменениям фармакокинетики препарата и, как следствие этого, развитию нежелательных реакций. Они зависят от дозы ЛС, обычно предсказуемы, возникают довольно часто, большая часть побочных реакций выявляется до широкого применения препарата в клинической практике, большую часть побочных реакций можно избежать индивидуальным подбором доз. Для них характерна относительно низкая летальность.
Реакции типа В чаще всего являются реакциями аллергической природы, к этому типу относятся также некоторые генетически детерминированные реакции. Неблагоприятные побочные реакции типа В - это реакции гиперчувствительности, обычно связанные с иммунологическими или генетическими механизмами, они не зависят от дозы, непредсказуемы и возникают редко, обычно выявляются на стадии широкого применения, чаще серьезные, Для них характерна относительно высокая летальность.
Неблагоприятные побочные реакции типа С возникают при длительном использовании лекарственного вещества. Обычно они проявляются развитием толерантности, лекарственной зависимости, «эффектом отмены». Примеры побочных реакций типа С: «эффект отмены» - гипертензия после резкого прекращения приема «Празозина», тахикардия после отмены β-блокаторов; медленная нейролептическая дискинезия; пневмосклероз, вызванный «Бромокриптином», «Фенитоином», «Метотрексатом»; «обратная связь» при применении гормонов щитовидной железы, кортикостероидов; «ломка» при использовании опиоидов.
Реакции типа Д (отсроченные реакции) возникают через месяцы или годы после лечения. Неблагоприятные побочные реакции типа Д включают: канцерогенность, нарушение репродуктивной функции, тератогенность, мутагенные эффекты. Примерами побочных реакций типа Д являются синдром Крейцфильда - Якобса, проявляющийся годы спустя после инъекций экстракта гормона роста; аденокарцинома у дочерей женщин, принимавших «Ди-этилстильбэстрол» во время беременности; лимфоцитарная лейкемия при длительном использовании иммунодепрессантов.
К факторам, определяющим побочные реакции лекарственного вещества (зависящие от используемого вещества), относятся:
физико-химические и фармакокинетические характеристики:
-
а) эксципиенты (индифферентная составная часть лекарства);
-
б) биодоступность препарата;
доза, способ введения и длительность применения.
Факторами, определяющими побочные реакции лекарственного вещества (пациент и состояние здоровья), являются следующие: физиологические особенности (возраст, пол, беременность, недостаточность питания), патологические особенности (заболевания почек, печени, прочее), аллергический статус, генетическая предрасположенность.
К иным внешним факторам, определяющим побочные реакции лекарственного вещества, относятся: параллельное назначение иных лекарственных веществ (количество препарата, вид лекарства), загрязнение окружающей среды, употребление алкоголя, курение.
На возникновение НПР также оказывают влияние физиологические показатели, изменяющиеся с возрастом: концентрация альбуминов в плазме, объем мышечной массы, объем жидкости в организме, сердечный выброс, функция почек, активность энзимов в печени, двигательная активность ЖКТ.
Неблагоприятные побочные реакции могут быть ожидаемые и неожиданные, серьезные и несерьезные. Неожиданная неблагоприятная побочная реакция - это реакция, сведения о природе и тяжести которой отсутствуют в брошюре исследователя или инструкции по применению препарата и ее не ожидают, исходя из существующих знаний о свойствах препарата, т.е. речь идет о неизвестной реакции на препарат (Фармаконадзор, 2000).
Серьезные неблагоприятные побочные реакции составляют угрозу жизни, приводят к смерти, приводят к потере работоспособности, требуют удлинения срока или длительной госпитализации, вызывают возникновение опухоли и врожденные аномалии, могут быть следствием передозировки.
Несерьезные неблагоприятные побочные реакции определяются как любая из побочных реакций, которая не отвечает критериям серьезной побочной реакции. Различие между серьезными и тяжелыми неблагоприятными побочными реакциями состоит в том, что в случае серьезных НПР предполагается значительный вред или ущерб для больного вследствие развития состояний, предусмотренных определением «серьезной побочной реакции». А в случае тяжелых НПР предполагается степень выраженности побочных явлений.
НПР могут возникать также в результате различных вариантов фальсификации лекарств. К методам выявления и изучения НПР относятся: исследования на животных, клинические испытания, эпидемиологические методы (спонтанные сообщения, постмаркетинговые исследования, интенсивные стационарные исследования и др.). Тем не менее, наиболее доступным и распространенным методом являются спонтанные сообщения, поступающие от врачей ЛПУ, которые заполняют специально разработанную и утвержденную МЗ РФ карту-извещение.


