Прямая невротизация анального неосфинктера как способ улучшения его функциональной морфологии
Автор: Бацаленко Н.П., Решетов И.В.
Журнал: Хирургическая практика @spractice
Статья в выпуске: 1, 2019 года.
Бесплатный доступ
В настоящее время существует множество методик по устранению каловой инконтиненции. Используя материал мышц тазового дна, удается физически воссоздать неосфинктер, но его функциональные возможность не всегда соответствуют потребностям больного. Использование микрохирургической техники в реконструктивной хирургии привело к появлению новых методик, к которым относят невротизацию мышцы.
Неосфинктер, невротизация, функция, хирургия, практика
Короткий адрес: https://sciup.org/142221871
IDR: 142221871 | УДК: 159.9.07 | DOI: 10.17238/issn2223-2427.2019.1.38-44
Direct neurotization of anal neosphincter as a way to improve its functional morphology
Currently, there are many methods to eliminate fecal incontinence. Using the material of the pelvic floor muscles, it is possible to physically recreate the neosphincter, but its functionality does not always correspond to the needs of the patient. The use of microsurgical techniques in reconstructive surgery has led to the emergence of new techniques, which include neuroticization of muscles.
Текст научной статьи Прямая невротизация анального неосфинктера как способ улучшения его функциональной морфологии
Недержание кишечного содержимого – тяжелое заболевание, которое ведет к инвалидизации больного, исключая его из активной трудовой деятельности и общественной жизни, ставит в сложные взаимоотношения с окружающими, снижает уровень социальной активности [1,7,8]. У взрослого населения она может встречаться на фоне закрытия дефектов у пациентов, перенесших экстирпацию прямой кишки и удаление запирательного аппарата, у пациентов с травмами и ранениями прямой кишки. У детей причиной данного заболевания могут быть пороки аноректального развития [9]. Прямая невротизация мышцы впервые была описана Хейни-ке более века назад, который имплантировал центральный конец добавочного нерва спины в парализованную трапециевидную мышцу [4,5]. Стендлер и Эльсберг, проводя эксперименты на собаках, доказали, что имплантированные в денервированную мышцу нервы образуют соединения, которые приводят к мышечной реиннервации и восстановле-
-
a E-mail: morbus007@mail.ru
-
b E-mail: 2487784@mail.ru
нию двигательной активности через восемь недель [4,5,11]. В клинической практике невротизацию используют при реконструктивных операциях на плечевом сплетении и лице, а также для восстановления чувствительности при реконструкции молочной железы [3-6,10].
Для стимуляции посттравматической регенерации нервных стволов перспективным представляется применение нейрональных факторов роста (нейротрофинов) [12-14]
Обобщая изложенное выше, можно предположить, что выполнение прямой невротизации мышцы при проведении пластики запирательного аппарата, в том числе с использованием нейротрофинов, является перспективным направлением хирургии.
Настоящее экспериментальное исследование было проведено с целью оценки функциональной морфологии сформированного неосфинктера в зависимости от того, проводилась ли невротизация и использовались ли для этого нейротро-фины.
Материалы и методы
Настоящее исследование одобрено Локальным комитетом по этике ФГБАУ ВО Первого МГМУ им И.М. Сеченова (протокол № 10-18 от 05.12.2018).
Экспериментальные исследования проводились на 18 самцах крыс линии Wistar средним весом 350 г и возрастом 4-6 месяцев. Во время проведения эксперимента было выделено 3 группы животных:
-
1. Группа крыс, которым выполнялась пластика запирательного аппарата прямой кишки без прямой невротизации мышцы
-
2. Группа крыс, которым выполнялась пластика запирательного аппарата прямой кишки с прямой невротизацией мышцы
-
3. Группа крыс, которым выполнялась пластика запирательного аппарата прямой кишки с прямой невротизацией мышцы и созданием градиента нейротрофинов
Все оперативные вмешательства проводились под общим наркозом препаратом «Золетил-100» (0,1мл на 1 кг тела внутрибрюшинно). Профилактика инфекций проводилась с помощью препарата «Байтрил» (0,1 мл в течение 5 дней внутримышечно).
Первой группе живаотных выполнялась пластика запирательного аппарата прямой кишки без прямой невротизации мышцы.
Под общей анестезией препаратом Золетил-100 выполнен линейный разрез, длинной около 7 см, по срединной линии дорзальной поверхности крысы. С обеих сторон выделена длинная мышца, отводящая хвост. Контроль гемостаза. С целью профилактики циркуляторных нарушений мышцы с обеих сторон накрыты салфетками с тёплым физраствором.
Двумя окаймляющими разрезами выделен и полностью иссечен сфинктер прямой кишки с удалением её участка на расстоянии 1,5 см от уровня кожи. Прямая кишка низведена, подшита к окружающим тканям
Длинная мышца, отводящая хвост, с обеих сторон отсечена от места крепления к хвосту, взята на швы-держалки. Через сформированный с обеих сторон канал, по средствам тоннелёра, длинная мышца, отводящая хвост, низведена к прямой кишке. Концы длинной мышцы, отводящей хвост, фиксированы друг другу, подшиты к прямой кишке по типу окаймляющей манжеты. Сформирован неосфинктер. Послойный шов раны.
Второй группе животных выполнялась пластика запирательного аппарата прямой кишки с прямой невротизацией мышцы.
Под общей анестезией препаратом Золетил-100 выполнен линейный разрез, длинной около 7 см, по срединной линии дорзальной поверхности крысы. С обеих сторон выделена и денервирована длинная мышца, отводящая хвост. Контроль гемостаза. С целью профилактики циркуляторных нарушений мышцы с обеих сторон накрыты салфетками с тёплым физраствором.
Двумя окаймляющими разрезами выделен и полностью иссечен сфинктер прямой кишки с удалением её участка на расстоянии 1,5 см от уровня кожи. Прямая кишка низведена, подшита к окружающим тканям
Длинная мышца, отводящая хвост, с обеих сторон отсечена от места крепления к хвосту, взята на швы-держалки. Через сформированный с обеих сторон канал, по средствам тоннелёра, длинная мышца, отводящая хвост, низведена к прямой кишке. Концы длинной мышцы, отводящей хвост, фиксированы друг другу, подшиты к прямой кишке по типу окаймляющей манжеты. Сформирован неосфинктер.
Со стороны левой длинной мышцы, отводящей хвост, в проекции крыла подвздошной кости выделен седалищный нерв. Основываясь на анатомических ориентирах, а так же, на сокращении мышц тазового дна, выделена ветвь промежностного нерва. На расстоянии 1,5 см от седалищного нерва ветвь промежностного нерва отсечена. Выполнена прямая невротизация мышцы: культя ветви промежностного нерва разделена на фасцикулы, выполнено введение культи ветви промежностного нерва в толщу длинной мышцы, отводящей хвост на глубину 1\3, нерв фиксирован к мышце Викрилом 10\0. Неразделенная часть ветви промежностного нерва укрыта в виде манжеты основанием длинной мышцы, отводящей хвост. Послойный шов раны.
Третьей группе животных выполнялась пластика запирательного аппарата прямой кишки с прямой невротизацией мышцы и созданием градиента нейротрофинов
Под общей анестезией препаратом Золетил-100 выполнен линейный разрез, длинной около 7 см, по срединной линии дорзальной поверхности крысы. С обеих сторон выделена и денервирована длинная мышца, отводящая хвост. Контроль гемостаза. С целью профилактики циркуляторных нарушений мышцы с обеих сторон накрыты салфетками с тёплым физраствором.
Двумя окаймляющими разрезами выделен и полностью иссечен сфинктер прямой кишки с удалением её участка на расстоянии 1,5 см от уровня кожи. Прямая кишка низведена, подшита к окружающим тканям
Длинная мышца, отводящая хвост, с обеих сторон отсечена от места крепления к хвосту, взята на швы-держалки. Через сформированный с обеих сторон канал, по средствам тоннелёра, длинная мышца, отводящая хвост, низведена к прямой кишке. Концы длинной мышцы, отводящей хвост, фиксированы друг другу, подшиты к прямой кишке по типу окаймляющей манжеты. Сформирован неосфинктер.
Со стороны левой длинной мышцы, отводящей хвост, в проекции крыла подвздошной кости выделен седалищный нерв. Основываясь на анатомических ориентирах, а так же, на сокращении мышц тазового дна, выделена ветвь промежностного нерва. На расстоянии 1,5 см от седалищного нерва ветвь промежностного нерва отсечена. Выполнена прямая невротизация мышцы: культя ветви промежностного нерва разделена на фасцикулы, выполнено введение культи ветви промежностного нерва в толщу длинной мышцы, отводящей хвост на глубину 1\3, нерв фиксирован к мышце Викрилом 10\0. Неразделенная часть ветви промежностного нерва укрыта в виде манжеты основанием длинной мышцы, отводящей хвост.
Далее от места проведенной прямой невротизации мышцы, в направлении сформированного неосфинктера выполнено создание градиента нейротрофинов непосредственно в длинной мышце, отводящей хвост с увеличением концентрации нейротрофинов при удалении от места невротизации к сформированному неосфинктеру.
Для улучшения прямой невротизации мышцы применяли гелеобразный раствор нейротрофинов в плюронике, который в диапазоне температур до +25 °С имеет свойства жидкости, а выше свойства геля, что позволяет ему оставаться продолжительное время в тканях. Раствор готовили следующим образом: стерильную навеску плюроника F-127 (Thermo Fisher) растворяли в физ. растворе в концентрации 27% при +4 °С в течении суток. После чего вносили ней-ротрофины NGF, NT-3, EGF, BDNF, GDNF, SDF-1a, ILGF-II (Thermo Fisher) и перемешивали еще 2 часа при +4 °С.. Градиент нейротрофинов создали путем разбавления исходного раствора в 5 и 10 раз. Затем раствор отбирали в инсулиновые шприцы и замораживали при -20 ˚С на срок не более 3 недель. Шприцы с нейротрофинами размораживали при +4 °C непосредственно перед операциями, с целью избежать разрушения нейротрофинов. Во время операции растворы в трех концентрациях вводилась в мышцу по градиенту роста нерва с минимальной концентрацией у места иннервации.
Введение нейротрофинов осуществлено в трех концентрациях: малая, средняя, большая, в соответствующей последовательности в объеме не более 0,1 мл каждого типа. После создания градиента нейротрофинов выполнен послойный шов раны.
Животные содержались в стандартных условиях вивария с режимом день/ночь 12/12, со свободным доступом к воде и пище.
Через 90 дней после операции у животных был забран биоматериал для гистологического исследования: длинная мышца, отводящая хвост, с левой (на ней была выполнена невротизация и градиент нейротрофином во второй и третьей экспериментальных группах) и правой стороны, сформированный неосфинктер и фрагменты ветви промежностного нерва слева (у животных из второй и третьей экспериментальных групп).
Образцы тканей фиксировали в 10% нейтральном забу-ференном формалине в течение 24 часов и пропускали через стандартный протокол проводки для гистологического обследования. Препараты были залиты в парафиновые блоки.
Препараты окрасили гематоксилином-эозином. Для им-мунофлуоресцентного исследования образцы депарафини- ровали и проводили демаскировку антигена в Трис-ЭДТА буфере pH 10.0 (abcam), блокировали не специфическое связывание антител 5% раствором бычьего сывороточного альбумина (БСА) в фосфатном солевом буфере (ФБС) с добавлением 0.05% детергента Твин-20. Препараты окрашивали первичными моноклональными мышиными антителами к b3-тубулину (Thermo Fisher) и кроличьими поликлональными антителами к синаптотагмину (Sigma), отмывали в ФБС буфере и антиген детектировали при помощи конъюгированных вторичных козьих антител против мыши, меченными флуоресцентной меткой Alexa 488 (Thermo Fisher) и козьих антител против кролика меченными Alexa 594 (Thermo Fisher). Стекла отмывали, ядра прокрашивали DAPI (Thermo Fisher) и заключали под покровное стекло в 80% глицерин в ФБС.
Затем препараты были изучены и описаны двумя опытными патологоанатомами независимо друг от друга. Патологоанатомы не имели сведений о принадлежности гистологических препаратов к экспериментальным группам. Микроскопическое исследование препаратов проводили на универсальном микроскопе LEICA DM4000 B LED с камерой LEICA DFC7000 T, с использованием компьютера с программным обеспечением LAS V4.8 software (Leica Microsystems, Switzerland).
Морфометрическое исследование гистологических препаратов проводили на увеличении ×200 с помощью описанного выше микроскопа с программным обеспечением. Для получения статистически достоверных результатов каждый препарат фотографировали в 10 случайно отобранных участках (размер поля зрения 623 × 467 мкм). На каждом изображении сформированного неосфинктера измеряли толщину слизистой оболочки толстой кишки и толщину прилежащего эпидермиса, в мышцах измеряли суммарную площадь их пучков в процентах от площади поля зрения, а также – их минимальный и максимальный диаметры.
Статистический анализ данных исследований был проведен на GraphPad Prism версии 8.00 для Windows (GraphPad Software, Inc.). Межгрупповые различия были оценены однофакторным дисперсионным анализом с поправкой Тьюки (исследование толщин) и двухфакторным дисперсионным анализом с поправкой Сидака (исследование площади мышечной ткани). Результаты представлены в виде столбиковых графиков со средними значениями и SEM. Уровень статистической значимости был принят р < 0,05.
Результаты
У всех животных первой группы, которым проводилась пластика запирательного аппарата без прямой невротизации мышцы, в области сформированного неосфинктера, определялся стык между слизистой оболочкой толстой кишки и эпидермисом кожи (рис. 1а). В области стыка отмечалась эрозивные и язвенные дефекты, окруженные выраженной полиморфноклеточной (лимфоциты, макрофаги, нейтрофилы, плазмоциты) инфильтрацией подлежащей ткани. Эпителий слизистой толстой кишки был преимущественно регенераторного типа, с немногочисленными бокаловидными клетками. Эпидермис прилежащих к сформированному неосфинктеру кожных покровов был несколько утолщен, незрелый, местами отмечался акантоз.
Правые и левые мышцы были представлены тканью с тонкими фиброваскулярными прослойками (рис. 1 б, в). Их строение не отличалось между собой.
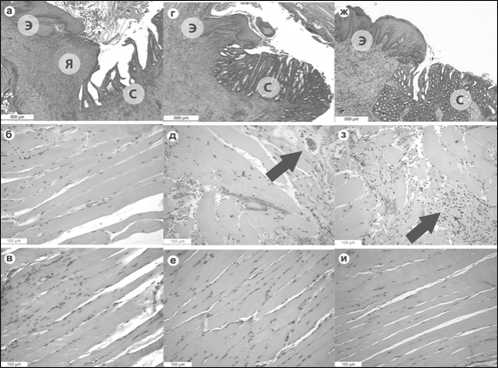
Рис.1. Гистологические препараты неосфинктера. Группа экспериментальных животных 1 (а-в), 2 (г-е) и 3 (ж-и): а, г, ж – фрагменты неосфинктера: в каждом из препаратов виден стык между слизистой оболочкой толстой кишки (С) и эпидермисом (Э), в группе 1 в этом месте определяется язвенный дефект (Я) (рис. а); окраска гематоксилином и эозином, ×50; б, д, з – левые мышцы, в, е, и – правые мышцы: в группах 2 и 3 диаметр мышечных волокон в составе левых мышц местами превышает 100 мкм, в отличие от правых, также видны нервные стволики (обозначены стрелками), окраска гематоксилином и эозином, ×200.
У всех экспериментальных животных второй группы, которым была проведена пластика запирательного аппарата прямой кишки с выполнением прямой невротизации мышцы без создания градиента нейротрофинов, признаки воспаления в области стыка эпидермиса и слизистой прямой кишки были несколько меньше, чем в первой группе экспериментальных животных, эрозивные и язвенные дефекты отсутствовали, а эпителий слизистой и эпидермис характеризовались несколько большей степенью зрелости (рис. 1г). Общая толщина слизистой оболочки прямой кишки, по сравнению с первой группой, была несколько больше.
Во второй группе экспериментальных животных были отмечены различия между правой и левой мышцами. Так, в левой длинной мышце, отводящей хвост, которая была не-вротизирована, встречались нервные стволики и гипертрофированные мышечные волокна (рис. 1 д, е).
У всех экспериментальных животных третьей группы, которым проводилась пластика запирательного аппарата с выполнением прямой невротизации мышцы и созданием градиента нейротрофинов, признаки воспаления в области стыка эпидермиса и слизистой прямой кишки практически отсутствовали, что значительно отличало их от живаотных остальных групп. Также как и во второй группе экспериментальных животных, у животных третьей группы эрозивные и язвенные дефекты в области стыка слизистой кишки и эпидермиса отсутствовали, а эпителиальная выстилка кожи и слизистой характеризовались наибольшей степенью зрелости (рис. 1ж). Общая толщина слизистой оболочки прямой кишки, по сравнению с остальными группами, была максимальной.
Различия между правой и левой мышцами у экспериментальных животных третьей группы были умеренно выраженными. Так, в левых мышцах часто встречались относительно крупные нервные стволики и гипертрофированные мышечные волокна (рис. 1 з, и), что было сходно со второй группой.
При реакции иммунофлуоресценции было доказано наличие клеток, содержащих b3-тубулин, — нервные стволики, вокруг которых выявлялась слабая экспрессия синаптотаг-мина (рис. 2).
В препаратах от животных третьей группы были выявлены относительно толстые нервные волокна в левых мышцах, и незначительное количество в правых мышцах. В то время как в правых мышцах первой и второй групп они не обнаруживались, что подтвердили данные статистического анализа (рис. 2г).
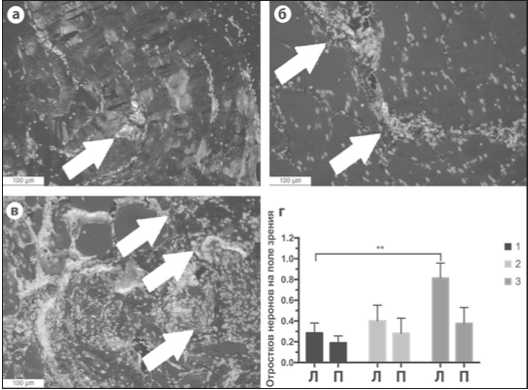
Рис.2. Фрагменты левых мышц, флюоресцентная микроскопия (×200). Препараты от животных группы 1 — (а), 2 — (б), 3 — (в). Зеленая флуоресценция — b3-тубулин, красная флуоресценция — синапто-тагмин, голубая флуоресценция — ядра клеток, желтая и оранжевая флуоресценция — неспецифическая и аутофлуоресценция. Стрелками обозначены b3-тубулин положительные нервные пучки. (г) количество отростков нейронов в поле зрения; двухфакторный дисперсионный анализ с поправкой Сидака, Л – левая мышца, П – правая мышца, графики отображают среднее значение ± SEM, ** - p <0.010
Толщины слизистых во всех группах экспериментальных животных достоверно отличались, причем максимальное среднее значение соответствовало третьей группе экспери-ментальныхживотных, минимальное-первойгруппе(рис.3а). Достоверные отличия были выявлены так же в толщинах эпидермиса между первой и третьей группами в сравнении со второй группой (рис. 3б). При исследовании различий в морфологии мышц было выявлено достоверное отличие между правой и левой мышцей во второй группе экспериментальных животных, при этом левая мышца первой группы экспериментальных животных достоверно была меньше левой мышцы второй группы. У экспериментальных животных третьей группы отличий между правой и левой мышцами практически не наблюдалось (рис. 3в). В левых и отчасти в правых мышцах часто встречались относительно крупные нервные стволики и гипертрофированные мышечные волокна.
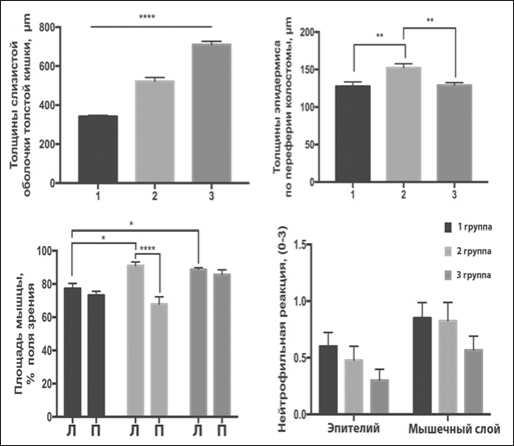
Рис.3. Морфометрический анализ состояния неосфинктера: (а) толщина слизитостой оболочки толстой кишки в области неосфинктера; (б) толщина эпидермиса в области неосфинктера; (в) площадь мышц неосфинкетра; (г) оценка интенсивности воспаления области неосфинктера. Л – левая мышца, П – правая мышца, графики отображают среднее значение ± SEM, * - p <0.05, ** - p <0.01, *** - p <0.001, **** - p <0.0001
Интенсивность воспалительной реакции была минимальной в третьей группе животных (рис. 3г), которым проводилась невротизация с использованием нейротрофинов.
Обсуждение полученных результатов
Выявленные морфологические изменения косвенно подтверждают эффективность применения невротизации для улучшения работы неосфинктера, особенно при дополнительном использовании нейротрофинов.
Выраженная воспалительная инфильтрация, эрозивные и язвенные дефекты, незрелость эпидермиса и слизистой прямой кишки у животных, которым была проведена пластика запирательного аппарата прямой кишки без прямой невротизации мышцы, свидетельствуют о постоянном раз- дражении этой области каловыми массами, вследствие отсутствия нормальной сократительной активности неосфинктера.
В то же время, у животных из второй группы, которым проводилась пластика запирательного аппарата прямой кишки с выполнением прямой невротизации мышцы без создания градиента нейротрофинов, признаки воспаления в области стыка эпидермиса и слизистой прямой кишки были меньше, чем в первой группе экспериментальных животных, эрозивные и язвенные дефекты отсутствовали, а эпителий слизистой оболочки и эпидермис характеризовались несколько большей степенью зрелости. Общая толщина слизистой оболочки прямой кишки, по сравнению с первой группой, была несколько больше. Также во второй группе экспериментальных животных были отмечены различия между правой и левой длинной мышцей, отводящей хвост. Так, в левой длинной мышце, отводящей хвост, которая подверглась невротизации, встречались нервные стволики и гипертрофированные мышечные волокна, в то время как в правой нет. Все это косвенно свидетельствует о хорошей функции неосфинктера.
У всех экспериментальных животных третьей группы, которым проводилась пластика запирательного аппарата с выполнением прямой невротизации мышцы и созданием градиента нейротрофинов, признаки воспаления в области стыка эпидермиса и слизистой прямой кишки практически отсутствовали, что значительно отличало их от остальных групп. Так же, как и во второй группе экспериментальных животных, у животных третьей экспериментальной группы эрозивные и язвенные дефекты в области стыка слизистой кишки и эпидермиса отсутствовали, а эпителиальная выстилка кожи и слизистой характеризовались наибольшей степенью зрелости. Общая толщина слизистой оболочки прямой кишки, по сравнению с остальными группами, была максимальной.
Различия между правой и левой мышцами у экспериментальных животных третьей группы были умеренно выраженными. Так, в левых мышцах часто встречались относительно крупные нервные стволики и гипертрофированные мышечные волокна. При реакции иммунофлуоресценции было доказано наличие клеток, содержащих b3-тубулин, – нервные стволики, вокруг которых выявлялась слабая экспрессия синаптотагмина.
Кроме того, от первой к третьей группе возрастала относительная толщина слизистой оболочки кишки, что, в сочетании с приведенными выше данными, указывает на ее полноценную регенерацию во второй и третьей группах. Эта тенденция обусловлена более физиологичным функционированием неосфинктера.
На основании полученных данных можно сказать, что предложенная методика пластики неосфинктера с невротизацией и созданием градиента нейротрофинов позволя- ет получить гистологическую картину, близкую к таковой нормально функционирующего сфинктера, и в перспективе может быть применена при лечении больных недержанием кишечного содержимого.
Список литературы Прямая невротизация анального неосфинктера как способ улучшения его функциональной морфологии
- Андреев А.В., Чеканов М.Н., Гатилов А.В. О функциональных результатах сфинктеросохраняющих резекций прямой кишки // Сибирский медицинский журнал. 2009. № 6. С. 41-45
- Байтингер В. Ф., Байтингер А. шов нерва конец-в-бок: стратегия "получения" аксонов из интактного нерва (часть III) // Вопросы реконструктивной и пластической хирургии. 2013. T. 16. № 2. C. 13-19
- Байтингер В. Ф., Силкина К. А., Байтингер А. В., Фёдоров Е. В. Total Breast Reconstruction: от неприятия до золотого стандарта // Вопросы реконструктивной и пластической хирургии 2014. T. 3. C. 50
- Говенько Ф., Монашенко Д., Лукин Д., Команцев В. Невротизация трех крупных нервов при тракционном повреждении плечевого сплетения // Вестник Российской военно-медицинской академии. 2012. № 4. C. 12-19
- Горшков Р. П., Нинель В., Норкин И., Делиникайтис С., Коршунова Г. Возможности тендомиопластики в реабилитации больных с грубыми повреждениями стволов плечевого сплетения // Саратовский научно-медицинский журнал. 2009. T. 5. №3
- Задоянный Л., Жданова В., Братусь Н. Клиника и лечение паралитического лагофтальма у больных с нейрохирургической патологией // Офтальмологический журнал. 2012. № 2. C. 63-67
- Иванов П.В., Киргизов И.В., Баранов К.Н., Шишкин И.А. Этапное лечение аноректальных пороков у детей // Медицинский вестник Северного Кавказа. 2010. № 3. С. 88-89
- Карпов О.Э., Максименков А.В., Степанюк И.В., Левчук А.Л., Назаров В.А., Стойко Ю.М. Лапароскопические и роботические технологии в лечении больных раком прямой кишки // Вестник Национального медико-хирургического Центра им. Н.И. Пирогова. 2016. Т. 11. № 2. С. 49-53
- Морозов Д.А., Окулов Е.А., Пименова Е.С. Российский консенсус по хирургическому лечению детей с аноректальными пороками. Первые шаги // Российский вестник детской хирургии, анестезиологии и реаниматологии. 2013. Т.3. №4. С. 8-13
- Ханнанова И.Г., Масгутов Р.Ф., Галлямов А.Р., Ризванов А.А., Богов А.А. Восстановление функции двуглавой мышцы плеча методом невротизации в сочетании с аутотрансплантацией клеток стромальной васкулярной фракции жировой ткани // Практическая медицина. Т. 4 (89). С. 197-199
- Konofaos P., Wallace R.D. Basic science of muscle neurotization: a review. Journal of reconstructive microsurgery, 2015, T. 31, no. 07, pp. 481-486
- Netta R. Blondheim, Yossef S. Levy, Tali Ben-Zur, Alex Burshtein, Tirza Cherlow, Inna Kan, Ran Barzilai, Merav Bahat-Stromza, Yael Barhum, Shlomo Bulvik, Eldad Melamed, And Daniel Offen. Human Mesenchymal Stem Cells Express Neural Genes, Suggesting a Neural Predisposition. Stem cells and development, 2006, 15, pp. 141-164
- Nnodim J.O. Testosterone mediates satellite cell activation in denervated rat levator ani muscle. The Anatomical Record: An Official Publication of the American Association of Anatomists, 2001, T. 263, no. 1, pp. 19-24
- Robert Sullivan, Travis Dailey, Kelsey Duncan, Naomi Abel and Cesario V. Borlongan. Peripheral Nerve Injury: Stem Cell Therapy and Peripheral Nerve Transfer. International Journal of Molecular Sciences, 2016, pp. 1-12


