Прямая невротизация анального неосфинктера как способ улучшения его функции
Автор: Бацаленко Н.П., Решетов И.В.
Журнал: Московский хирургический журнал @mossj
Статья в выпуске: 1 (65), 2019 года.
Бесплатный доступ
Недержание кишечного содержимого - тяжелое заболевание, которое ведет к инвалидизации больного, исключая его из активной трудовой деятельности и общественной жизни, ставит в сложные взаимоотношения с окружающими, снижает уровень социальной активности. У взрослого населения она может встречаться на фоне закрытия дефектов у пациентов, перенесших экстирпацию прямой кишки и удаление запирательного аппарата, у пациентов с травмами и ранениями прямой кишки. У детей причиной данного заболевания могут быть пороки аноректального развития. В настоящее время существует множество методик по устранению каловой инконтиненции.
Неосфинктер, невротизация, функция, хирургия, практика
Короткий адрес: https://sciup.org/142221719
IDR: 142221719 | УДК: 615.47.03 | DOI: 10.17238/issn2072-3180.2019.1.50-55
Direct neurotic anal neosphincter as a way to improve its function
Incontinence of intestinal contents is a serious disease that leads to disability of the patient, excluding him from active work and social life, puts him in a complex relationship with others, reduces the level of social activity. In the adult population, it can occur against the background of closure of defects in patients undergoing rectal extirpation and removal of the obturator apparatus, in patients with injuries and injuries of the rectum. In children, anorectal malformations can be the cause of this disease. Currently, there are many methods to eliminate fecal incontinence.
Текст научной статьи Прямая невротизация анального неосфинктера как способ улучшения его функции
Используя материал мышц тазового дна, удается физически воссоздать неосфинктер, но его функциональные возможность не всегда соответствуют потребностям больного. Использование микрохирургической техники в реконструктивной хирургии привело к появлению новых методик, к которым относят невротизацию мышцы [2,4]. Прямая невротизация мышцы впервые была описана Хейнике более века назад, который имплантировал центральный конец добавочного нерва спины в парализованную трапециевидную мышцу [4,5]. Стендлер и Эльсберг, проводя эксперименты на собаках, доказали, что имплантированные в денервированную мышцу нервы образуют соединения, которые приводят к мышечной реиннервации и восстановлению двигательной активности через восемь недель [4,5,11]. В клинической практике невротизацию используют при реконструктивных операциях на плечевом сплетении и лице, а также для вос-
становления чувствительности при реконструкции молочной железы [3-6, 10].
Для стимуляции посттравматической регенерации нервных стволов перспективным представляется применение нейрональных факторов роста (нейротрофинов) [12-14]
Обобщая изложенное выше, можно предположить, что выполнение прямой невротизации мышцы при проведении пластики запирательного аппарата, в том числе с использованием нейротрофинов, является перспективным направлением хирургии. Для проверки этой гипотезы было проведено данное экспериментальное исследование.
Материалы и методы
Настоящее исследование одобрено Локальным комитетом по этике ФГБАУ ВО Первого МГМУ им И.М. Сеченова (протокол № 10-18 от 05.12.2018).
Экспериментальные исследования проводились на 18 самцах крыс линии Wistar средним весом 350 г и возрастом 4-6 ме- сяцев. Во время проведения эксперимента было выделено четыре группы животных:
-
1. Группа крыс, которым выполнялась пластика запирательного аппарата прямой кишки без прямой невротизации мышцы.
-
2. Группа крыс, которым выполнялась пластика запирательного аппарата прямой кишки с прямой невротизацией мышцы.
-
3. Группа крыс, которым выполнялась пластика запирательного аппарата прямой кишки с прямой невротизацией мышцы и созданием градиента нейротрофинов.
-
4. Контрольная группа – здоровые животные.
Через 90 суток от момента выполненной операции проводилась оценка резульатов операции, в том числе с использованием разработанного и запатентованного сфинктерома-нометра.
Все оперативные вмешательства проводились под общим наркозом препаратом «Золетил-100» (0,1мл на 1 кг тела внутрибрюшинно). Профилактика инфекций проводилась с помощью препарата «Байтрил» (0,1 мл в течение 5 дней внутримышечно).
Первой группе живаотных выполнялась пластика запирательного аппарата прямой кишки без прямой невротизации мышцы.
Под общей анестезией препаратом Золетил-100 выполнен линейный разрез, длинной около 7 см, по срединной линии дорзальной поверхности крысы. С обеих сторон выделена длинная мышца, отводящая хвост. Контроль гемостаза. С целью профилактики циркуляторных нарушений мышцы с обеих сторон накрыты салфетками с тёплым физраствором.
Двумя окаймляющими разрезами выделен и полностью иссечен сфинктер прямой кишки с удалением её участка на расстоянии 1,5 см от уровня кожи. Прямая кишка низведена, подшита к окружающим тканям.
Длинная мышца, отводящая хвост, с обеих сторон отсечена от места крепления к хвосту, взята на швы-держалки. Через сформированный с обеих сторон канал, посредством тоннелёра, длинная мышца, отводящая хвост, низведена к прямой кишке. Концы длинной мышцы, отводящей хвост, фиксированы друг другу, подшиты к прямой кишке по типу окаймляющей манжеты. Сформирован неосфинктер. Послойный шов раны.
Второй группе животных выполнялась пластика запирательного аппарата прямой кишки с прямой невротизацией мышцы.
Под общей анестезией препаратом Золетил-100 выполнен линейный разрез, длинной около 7 см, по срединной линии дорзальной поверхности крысы. С обеих сторон выделена и денервирована длинная мышца, отводящая хвост. Контроль гемостаза. С целью профилактики циркуляторных нарушений мышцы с обеих сторон накрыты салфетками с тёплым физраствором.
Двумя окаймляющими разрезами выделен и полностью иссечен сфинктер прямой кишки с удалением её участка на расстоянии 1,5 см от уровня кожи. Прямая кишка низведена, подшита к окружающим тканям.
Длинная мышца, отводящая хвост, с обеих сторон отсечена от места крепления к хвосту, взята на швы-держалки. Через сформированный с обеих сторон канал, посредством тоннелёра, длинная мышца, отводящая хвост, низведена к прямой кишке. Концы длинной мышцы, отводящей хвост, фиксированы друг другу, подшиты к прямой кишке по типу окаймляющей манжеты. Сформирован неосфинктер.
Со стороны левой длинной мышцы, отводящей хвост, в проекции крыла подвздошной кости выделен седалищный нерв. Основываясь на анатомических ориентирах, а так же, на сокращении мышц тазового дна, выделена ветвь промежностного нерва. На расстоянии 1,5 см от седалищного нерва ветвь промежностного нерва отсечена. Выполнена прямая невротизация мышцы: культя ветви промежностного нерва разделена на фасцикулы, выполнено введение культи ветви промежностного нерва в толщу длинной мышцы, отводящей хвост на глубину 1/3, нерв фиксирован к мышце Викрилом 10/0. Неразделенная часть ветви промежностного нерва укрыта в виде манжеты основанием длинной мышцы, отводящей хвост. Послойный шов раны.
Третьей группе животных выполнялась пластика запирательного аппарата прямой кишки с прямой невротизацией мышцы и созданием градиента нейротрофинов
Под общей анестезией препаратом Золетил-100 выполнен линейный разрез, длинной около 7 см, по срединной линии дорзальной поверхности крысы. С обеих сторон выделена и денервирована длинная мышца, отводящая хвост. Контроль гемостаза. С целью профилактики циркуляторных нарушений мышцы с обеих сторон накрыты салфетками с тёплым физраствором.
Двумя окаймляющими разрезами выделен и полностью иссечен сфинктер прямой кишки с удалением её участка на расстоянии 1,5 см от уровня кожи. Прямая кишка низведена, подшита к окружающим тканям.
Длинная мышца, отводящая хвост, с обеих сторон отсечена от места крепления к хвосту, взята на швы-держалки. Через сформированный с обеих сторон канал, посредством тоннелёра, длинная мышца, отводящая хвост, низведена к прямой кишке. Концы длинной мышцы, отводящей хвост, фиксированы друг другу, подшиты к прямой кишке по типу окаймляющей манжеты. Сформирован неосфинктер.
Со стороны левой длинной мышцы, отводящей хвост, в проекции крыла подвздошной кости выделен седалищный нерв. Основываясь на анатомических ориентирах, а так же, на сокращении мышц тазового дна, выделена ветвь промежностного нерва. На расстоянии 1,5 см от седалищного нерва ветвь промежностного нерва отсечена. Выполнена прямая невротизация мышцы: культя ветви промежностного нерва разделена на фасцикулы, выполнено введение культи ветви промежностного нерва в толщу длинной мышцы, отводящей хвост на глубину 1/3, нерв фиксирован к мышце Викрилом 10/0. Неразделенная часть ветви промежностного нерва укрыта в виде манжеты основанием длинной мышцы, отводящей хвост.
Далее от места проведенной прямой невротизации мышцы, в направлении сформированного неосфинктера выполнено создание градиента нейротрофинов непосредственно в длинной мышце, отводящей хвост с увеличением концентрации нейротрофинов при удалении от места невротизации к сформированному неосфинктеру.
Для улучшения прямой невротизации мышцы применяли гелеобразный раствор нейротрофинов в плюронике, который в диапазоне температур до +25°С имеет свойства жидкости, а выше свойства геля, что позволяет ему оставаться продолжительное время в тканях. Раствор готовили следующим образом: стерильную навеску плюроника F-127 (Thermo Fisher) растворяли в физ. растворе в концентрации 27% при +4°С в течении суток. После чего вносили нейротро-фины NGF, NT-3, EGF, BDNF, GDNF, SDF-1a, ILGF-II (Thermo Fisher) и перемешивали еще 2 часа при +4°С. Градиент ней-ротрофинов создали путем разбавления исходного раствора в 5 и 10 раз. Затем раствор отбирали в инсулиновые шприцы и замораживали при -20°С на срок не более 3 недель. Шприцы с нейротрофинами размораживали при +4°C непосредственно перед операциями, с целью избежать разрушения нейротрофинов. Во время операции растворы в трех концентрациях вводилась в мышцу по градиенту роста нерва с минимальной концентрацией у места иннервации.
Введение нейротрофинов осуществлено в трех концентрациях: малая, средняя, большая, в соответствующей последовательности в объеме не более 0,1 мл каждого типа. После создания градиента нейротрофинов выполнен послойный шов раны.
Здоровые животные использовались в качестве контрольной группы.
Животные содержались в стандартных условиях вивария с режимом день/ночь 12/12, со свободным доступом к воде и пище.
Через 90 дней после проведения операции проводилось фотографирование области неосфинктера с последующим измерением его площади в спокойном состоянии и оценка функции неосфинктера. Для последнего нами был разработан и запанетован сфинктероманометр СФМББ2, способный оценивать импульсы, силу сжатия и частоту сокращений сформированного неосфинктера. В сформированный неосфинктер крысы, после предварительной подготовки вводился сдутый баллонный катетер для проведения сфин-ктероманометрии размером 8Fr, после чего он надувался до появления мышечного сопротивления. В статическом состоянии баллонного катетера оценивались сила сжатия, частота сокращений. В момент эвакуации баллонного катетера в динамике оценивались периоды напряжения и расслабления мышц сфинктера, сила сжатия, частота сокращения.
Статистический анализ был проведен с использование программы для ЭВМ GraphPad Prism версии 7.00 для MacOS (GraphPad Software, Inc.). Достоверные различия площади неосфинктера в исследуемых группах оценивали с помощью непараметрического теста Краскела-Уоллиса с поправкой Данна. Для оценки максимального напряжения сфинктера максимальные значения вокруг пика, характеризующего сжатие датчика, сравнивали однофакторным дисперсионным анализом с поправкой Тьюки. Значения считали статистически значимыми при p <0,05.
Результаты
Изучение макроскопической формы неосфинктера у крыс на 90 сутки после оперативного вмешательства показало статистически достоверные различия между тремя группами экспериментальных животных (Рисунок 1).
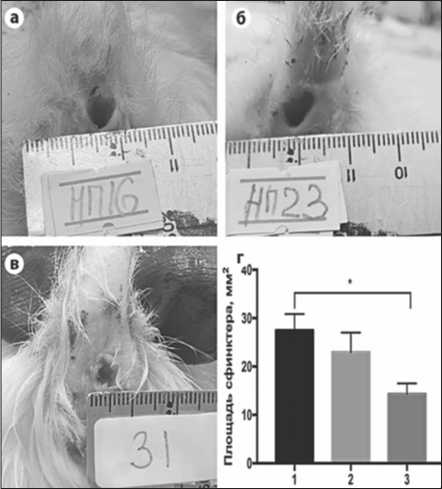
Рис.1. (а,б,в) Фотографии неосфинктера типовых представителей группы 1 (а), группы 2 (б) и группы 3 (в) на 90 сутки после операции.
(г) Площадь сфинктеров (среднее и SEM).
1 – операция без невротизации, группа 2 – операция с проведением невротизации, группа 3 – операция с проведением невротизации и созданием градиента нейротрофинов. * - p <0,05.
Так, в первой группе крыс, которым выполнялась пластика запирательного аппарата прямой кишки без прямой невротизации мышцы, отмечается увеличение площади неосфинктера, не сомкнутость ануса, его зияние, хроническое воспаление, каломазание и в 50% случаев неоформленность стула.
Во второй группе крыс, которым выполнялась пластика запирательного аппарата прямой кишки с прямой невротизацией мышцы, без создания градиента нейротрофинов, отмечается меньшая площадь сформированного неосфин- ктера, его сомкнутость. Стул был сформирован, каломазание наблюдалось только в 10% случаев.
Площадь неосфинктера, его сомкнутость у третьей группы крыс, которым выполнялась пластика запирательного аппарата прямой кишки с прямой невротизацией мышцы и созданием градиента нейротрофинов, значимо не отличалась от данного показателя в группе контроля. Зияния ануса и каломазания не наблюдалось. Полученный результат косвенно свидетельствует о функциональной активности мышечного аппарата неосфинктера и его возможности удерживать каловые массы.
В результате функционального исследования было показано, что в контрольной группе экспериментальных животных максимальное значение напряжения неосфинктера составило 0,066±0,005 В. В первой группе животных, которым выполнялась пластика запирательного аппарата прямой кишки без прямой невротизации мышцы, максимальное напряжение неосфинктера составило 0,020±0,010 В. Во второй группе животных, которым проводилась пластика запирательного аппарата прямой кишки с выполнением прямой невротизации мышцы без создания градиента нейротрофи-нов максимальное значения напряжения неосфинктера составило 0,026±0,006 В. В третьей группе экспериментальных животных, которым проводилась пластика запирательного аппарата прямой кишки с выполнением прямой невротизации мышцы с созданием градиента нейротрофинов, максимальное значение напряжения неосфинктера составило 0,063±0,0057 В. При этом контрольная и третья группа значимо не отличались (p=0,1747), чего нельзя сказать при сравнении контрольной группы с первой (p=0,0002) и второй (p=0,0006). Третья группа также достоверно отличалась от первой (p=0,0019) и второй (p=0,0076).
Основываясь на полученных данных динамической оценки эвакуации баллонного катетера, нами был установлен механизм дефекации у здоровых крыс и прооперерированных животных (Рисунок 2).
У здоровых животных контрольной группы в процессе дефекации отмечаются регулярные эпизоды периодического напряжения и расслабления мышц сфинктера прямой кишки с тенденцией к полному его расслаблению, что способствует эвакуации каловых масс.
У крыс третьей группы, которым проводилась пластика запирательного аппарата прямой кишки с выполнением прямой невротизации мышцы с созданием градиента ней-ротрофинов, наблюдалась абсолютно идентичная картина. Эвакуация баллонного катетера также сопровождалась регулярными эпизодами напряжения и расслабления мышц неосфинктера с тенденцией к полному расслаблению неосфинктера. Процесс эвакуации по времени не отличался от контрольной группы.
У крыс второй группы, которым проводилась пластика запирательного аппарата прямой кишки с выполнением пря- мой невротизации мышцы без создания градиента нейро-трофинов, эвакуация баллонного катетера тоже сопровождалась регулярными эпизодами напряжения и расслабления мышц с тенденцией к полному расслаблению. Достоверным отличием от третьей и контрольной групп экспериментальных животных являлось большая сила сжатия и менее длительные периоды расслабления неосфинктера, а также более длительный период полной эвакуации баллонного катетера.
У крыс первой группы, которым проводилась пластика запирательного аппарата прямой кишки без выполнения прямой невротизации мышцы, отмечалось появление диаметрально противоположного механизма эвакуации баллонного катетера. Короткий период расслабления неосфинктера сопровождался резким увеличением его тонуса, с тенденцией к нарастанию без периодов расслабления, вплоть до полной эвакуации баллонного катетера.
Полученный результат свидетельствует о том, что во второй и третьей группе экспериментальных животных восстановлена нормальная физиология акта дефекации. А у первой группы крыс действует компенсаторный механизм эвакуации каловых масс, диаметрально противоположный группе контроля, сопровождающийся нарастанием тонуса и отсутствием периодов расслабления.
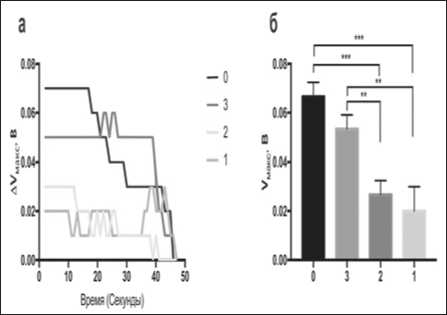
Рис.2. (а) Динамика расслабления сфинктера. (б) Максимальное сжатие сфинтера (среднее значение ± SD). Группа 0 – контрольная без проведения операции, группа 1 – операция без невротизации, группа 2 – операция с проведением невротизации, группа 3 – операция с проведением невротизации и созданием градиента ней-ротрофинов. * - p <0,05, ** - p <0,01, *** - p <0,001, **** - p <0,0001
Обсуждение полученных результатов
В ходе данного исследования были изучены результаты пластики запирательного аппарата прямой кишки у трех групп экспериментальных животных. У животных, которым была проведена операция с проведением невротизации и созданием градиента нейротрофинов, функциональное состояние неосфинктеров было наиболее близким к состоянию сфинктеров в группе контроля. В то же время, функциональные характеристики неосфинктеров в остальных группах были достоверно хуже.
Наихудший результат был получен в группе экспериментов, где проводилось создание неосфинктера без невротизации. В этом случае была выявлена несомкнутость сфинктера, зачастую его зияние, наличие хронического воспаления, неоформленность стула, нарушение нормального физиология акта дефекации. Это может быть обусловлено тем, что длинная мышца, отводящая хвост, применяемая для формирования неосфинктера, вероятнее всего воспринималась организмом не как часть запирательного аппарата прямой кишки, а как мышца с иной функцией. Для естественного «переобучения» мышцы требуется слишком длительный период времени, что в свою очередь привело к формированию компенсаторного механизма акта дефекации, несостоятельности сформированного неосфинктера, ограничение его замыкающей функции, формированию хронического воспаления.
У животных, которым была выполнена прямая невротизация неосфинктера ветвями промежностного нерва без создания градиента нейротрофинов, лишь в 10% случаев отмечалось зияние ануса, стул был оформлен, каломазания не наблюдалось. Сила сокращения неосфинктера была до-ставерно больше, чем у животных без проведения невротизации, но меньше, чем у животных из группы контроля. Также наблюдалась тенденция к восстановлению нормальной физиологии акта дефекации. Таким образом, у данных животных результат операции частично соответствует клиническим требованиям. Это может быть обусловлено тем, что длинная мышца, отводящая хвост, иннервируемая ветвью промежностного нерва, воспринимается организмом как часть запирательного аппарата прямой кишки.
Результаты нашего исследования позволяют утверждать, что пластика запирательного аппарата прямой кишки с выполнением прямой невротизации мышцы и созданием градиента нейротрофинов в перспективе может стать той методикой, которая может дать практически полное восстановление запирательной функции. Проведение же пластики запирательного аппарата без выполнения прямой невротизации мышцы, зачастую приводит к тому, что мышца, участвующая в формировании неосфинктера, будет восприниматься как чужеродная, что влечет за собой несостоятельность выполняемой операции и отрицательный ее результат.
Предложенная методика (пластика неосфинктера с невротизацией его и созданием градиента нейротрофинов) в перспективе может быть применена на людях.
Список литературы Прямая невротизация анального неосфинктера как способ улучшения его функции
- Андреев А.В., Чеканов М.Н., Гатилов А.В. О функциональных результатах сфинктеросохраняющих резекций прямой кишки // Сибирский медицинский журнал. 2009. № 6. С. 41-45.
- Байтингер В. Ф., Байтингер А. Шов нерва конец-в-бок: стратегия "получения" аксонов из интактного нерва (часть III) // Вопросы реконструктивной и пластической хирургии. 2013. T. 16. № 2. C. 13-19.
- Байтингер В. Ф., Силкина К. А., Байтингер А. В., Фёдоров Е. В. Total Breast Reconstruction: от неприятия до золотого стандарта // Вопросы реконструктивной и пластической хирургии 2014. T. 3. C. 50.
- Говенько Ф., Монашенко Д., Лукин Д., Команцев В. Невротизация трех крупных нервов при тракционном повреждении плечевого сплетения // Вестник Российской военно-медицинской академии. 2012. № 4. C. 12-19.
- Горшков Р. П., Нинель В., Норкин И., Делиникайтис С., Коршунова Г. Возможности тендомиопластики в реабилитации больных с грубыми повреждениями стволов плечевого сплетения // Саратовский научно-медицинский журнал. 2009. T. 5. №3.
- Задоянный Л., Жданова В., Братусь Н. Клиника и лечение паралитического лагофтальма у больных с нейрохирургической патологией // Офтальмологический журнал. 2012. № 2. C. 63-67.
- Иванов П.В., Киргизов И.В., Баранов К.Н., Шишкин И.А. Этапное лечение аноректальных пороков у детей // Медицинский вестник Северного Кавказа. 2010. № 3. С. 88-89.
- Карпов О.Э., Максименков А.В., Степанюк И.В., Левчук А.Л., Назаров В.А., Стойко Ю.М. Лапароскопические и роботические технологии в лечении больных раком прямой кишки // Вестник Национального медико-хирургического Центра им. Н.И. Пирогова. 2016. Т. 11. № 2. С. 49-53
- Морозов Д.А., Окулов Е.А., Пименова Е.С. Российский консенсус по хирургическому лечению детей с аноректальными пороками. Первые шаги // Российский вестник детской хирургии, анестезиологии и реаниматологии. 2013. Т.3. №4. С. 8-13.
- Ханнанова И.Г., Масгутов Р.Ф., Галлямов А.Р., Ризванов А.А., Богов А.А. Восстановление функции двуглавой мышцы плеча методом невротизации в сочетании с аутотрансплантацией клеток стромальной васкулярной фракции жировой ткани // Практическая медицина. Т. 4 (89). С. 197-199.
- Konofaos P., Wallace R.D. Basic science of muscle neurotization: a review. Journal of reconstructive microsurgery, 2015, T. 31, no. 07, pp. 481-486.
- Netta R. Blondheim, Yossef S. Levy, Tali Ben-Zur, Alex Burshtein, Tirza Cherlow, Inna Kan, Ran Barzilai, Merav Bahat-Stromza, Yael Barhum, Shlomo Bulvik, Eldad Melamed, And Daniel Offen. Human Mesenchymal Stem Cells express Neural Genes, Suggesting a Neural Predisposition. Stem cells and development, 2006, 15, pp. 141-164.
- Nnodim J.O. Testosterone mediates satellite cell activation in denervated rat levator ani muscle. The Anatomical Record: An Official Publication of the American Association of Anatomists, 2001, T. 263, no. 1, pp. 19-24.
- Robert Sullivan, Travis Dailey, Kelsey Duncan, Naomi Abel and Cesario V. Borlongan. Peripheral Nerve Injury: Stem Cell Therapy and Peripheral Nerve Transfer. International Journal of Molecular Sciences, 2016, pp. 1-12.


