Проблемы и перспективы совершенствования водоподготовки
Автор: Саканская-грицай Е.И.
Журнал: Технико-технологические проблемы сервиса @ttps
Рубрика: Организационно-экономические аспекты сервиса
Статья в выпуске: 3 (29), 2014 года.
Бесплатный доступ
Проведен анализ правовых документов по теме водоподготовки питьевой воды. Рассмотрены имеющиеся действующие бытовые установки очистки воды. Акцентировано внимание на опасности употребления искусственно созданной воды. Уточнены некоторые вопросы по традиционным способам очистки воды. Проведен обзор электрохимических установок, методов обработки водных растворов. Предложен способ совмещения реагентной и электрохимической очистки воды на этапе службы жилищно-коммунального хозяйства (ЖКХ).
Обеспечение населения питьевой водой как национальная безопасность, анализ бытовых установок по очистке воды, опасность деминерализованной и восстановленной воды, традиционные способы водоподготовки, электрохимические способы очистки воды, эффективность совмещения реагентных и электрохимических способов
Короткий адрес: https://sciup.org/148186185
IDR: 148186185 | УДК: 544.6.076
Problemy and prospects for improvement of water treatment
The analysis of legal documents on water treatment of drinking water. Reviewed existing domestic water purification. The attention on the dangers of drinking artificially created water. Clarified some questions on traditional methods of water purification. The review of electrochemical devices, methods of processing aqueous solutions. A method of combining reagent and electrochemical water treatment at the stage of service of housing and communal services (HCS).
Текст научной статьи Проблемы и перспективы совершенствования водоподготовки
PROBLEMY AND PROSPECTS FOR IMPROVEMENT OF WATER TREATMENT
E.I. Sakanskaja-Gritsay
St. Petersburg state University of Economics ( SPbSEU ), 191023, Saint-Petersburg, Sadovaya street , 21 .
The analysis of legal documents on water treatment of drinking water. Reviewed existing domestic water purification. The attention on the dangers of drinking artificially created water. Clarified some questions on traditional methods of water purification. The review of electrochemical devices, methods of processing aqueous solutions. A method of combining reagent and electrochemical water treatment at the stage of service of housing and communal services (HCS).
Keyords: Provision of potable water as a national security; analysis of household water treatment plants; the danger of demineralized and recovered water; traditional water treatment methods; electrochemical methods of water treatment; the effectiveness of the combination of the reagent and electrochemical methods.
-
I. Правовое обоснование актуальности темы разработки способа очистки питьевой воды
«Обеспечение населения России питьевой водой является для многих регионов страны одной из приоритетных проблем, решение которой необходимо для сохранения здоровья, улучшения условий деятельности и повышения уровня жизни населения». [1]
Реализация Стратегии национальной безопасности Российской Федерации до 2020 года призвана стать мобилизующим фактором улучшения качества жизни населения. [2]
В пункте 87 Указа Президента РФ говорится, что «состояние национальной безопасности в сфере экологии усугубляется сохранением значительного количества опасных производств, деятельность которых ведет к нару- шению экологического баланса, включая нарушение санитарно-эпидемиологических и (или) санитарно-гигиенических стандартов потребляемой населением страны питьевой воды…» Соответственно среди факторов, гарантирующих национальную безопасность страны в области здоровья, наиболее существенным социально значимым вопросом является обеспечение населения России питьевой водой. Это неоднократно отмечено в резолюциях и решениях Совета Безопасности РФ (1995 и 2001 гг.) и Президиума Госсовета РФ.
Министерством экономического развития Российской Федерации разработана и реализуется программа «Чистая вода», которая направлена на реформирование и модернизацию сектора водоснабжения и водоотведения.
Государственная программа "Чистая вода" представляет собой комплекс взаимно увязанных мероприятий, осуществляемых органами государственной власти и органами местного самоуправления, организациями промышленности, финансового сектора, научными организациями, реализация которых обеспечит поэтапное достижение цели: обеспечение граждан страны чистой водой. Среди задач программы – стимулирование производства инновационного отечественного оборудования, технологий и материалов, необходимых для создания и обеспечения функционирования систем водоснабжения и водоотведения в соответствии с современными стандартами.
Рассчитано, что до 2020 года доля населения страны, имеющего доступ к централизованному водоснабжению, увеличится на 40 процентов. Важно чтобы до потребителя доходила вода соответствующая стандарту Санитарных правил и норм СанПиН 2.1.4.559-96 «Питьевая вода. Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения. Контроль качества».
В свете этих документов актуальна разработка инновационных рентабельных и экономичных многоуровневых способов очистки питьевой воды на этапе службы жилищнокоммунального хозяйства (ЖКХ).
-
II. Анализ потребительского рынка
На сегодняшний день ответственность за качество потребляемой воды фактически переложена на самого потребителя, поскольку изношенные водопроводные сети, устаревшее оборудование станций очистки не гарантируют подачу качественной воды населению. Кроме того, множество производителей предлагают на выбор опять же потребителя и в зависимости от его возможностей, свои установки с различными технологиями доочистки воды от дешёвых до достаточно существенных цен, при этом гарантия безопасности употребления доочищен-ной воды остаётся под вопросом. Чаще всего в этих установках используют фильтры различной степени очистки на основе полипропилена, активированного угля, активированного углеродного волокна, ионообменных смол, КДФ (высокоочищенные Zn и Си) и т.д.
Фильтры с КДФ (рис.1), например, используют в установке доочистки питьевой воды, состоящей из 5 фильтров, предназначенных для глубокой очистки водопроводной воды от вредных примесей.
Фильтр №1 – механический полипропиленовый очищает воду от грязи, взвешенных частиц и нерастворимых примесей.
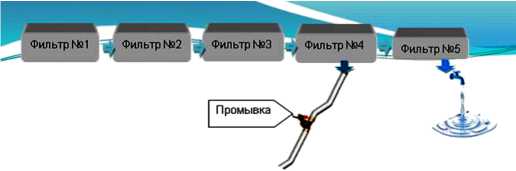
Рисунок 1 – Пятиступенчатый фильтр доочистки водопроводной воды
Фильтр №2 – прессованный активированный уголь (по технологии карбон-блок СТО) пористость 5 мкм, на данном уровне происходит адсорбция воды, удаляется неприятный запах и цвет, очищают воду от свободного хлора, тяжелых металлов и др. органических соединений.
Фильтр №3 – (ультрафильтрационная мембрана (УФ мембрана) на основе полимера) пористость 0,1-0,001мкм, удаляет органические загрязнители, железо, марганец, тяжелые металлы и другие растворенные примеси
Фильтр №4 – сорбционный фильтр с гранулами активированного угля и KDF, очищает от активного хлора, растворенного железа, тяжёлых металлов, происходит глубокая антибактериальная очистка, уничтожаются опасные бактерии и вирусы.
Фильтр №5 – сорбционный фильтр с гранулами активированного кокосового угля. Очищает воду от хлорорганических соединений, нефтепродуктов, тяжёлых металлов, улучшает вкусовые качества воды.
Используется также (рис.1) ручная промывка фильтров.
Некоторые производители предлагают широкий спектр фильтров от кувшинов до установок для очистки воды с использованием различных фильтров, а также метода обратного осмоса.
Так, например, одна из отечественных установок имеет систему фильтров и обратноосмотическую мембрану рулонного типа, пористость которой 0,0001 мкм. Размер ее поры сравним с размером молекулы воды, поэтому мембрана обратного осмоса пропускает только молекулы воды и меньше, например хлор. Также в установку входит минерализатор на основе природных и экологически чистых материалов.
Известна установка, разработанная сотрудниками кафедры биомедфизики УдГУ, которая сочетает в себе обратный осмос, электроактивацию и дозированную минерализацию. Здесь для очистки воды используется улучшенная 5-ти ступенчатая схема обратного осмоса. Активация (ионизация) воды проводится путем электрообработки в активационном реакторе. Режим активации можно выставлять на пульте
– (100%, 50%, 25%, 0% активации). Далее в обессоленную обратным осмосом и активированную воду в автоматическом капельном режиме добавляется жидкий минеральный комплекс (кальций, калий, магний, йод). Уровень насыщения воды солями выставляется потребителем нажатием кнопки на пульте управления.
Известны также фильтры для воды, разработанные в Северо-западном научном центре российской академии сельскохозяйственных наук, принцип действия которых основан на использовании электрохимических методов обработки питьевой воды. Эти фильтры очищают воду посредством окислительновосстановительных реакций, реализуемых последовательно в электрохимическом и каталитическом реакторах. Оба реактора выполнены в виде унифицированных, миниатюрных, проточных, высокопроизводительных устройств.
Конструктивно фильтры состоят из:
-
• высокопроизводительного проточного миниатюрного диафрагменного электрохимического реактора с оксидно-рутениевыми электродами и ультрафильтрационной диафрагмой из оксида циркония;
-
• вспомогательных реакторов (каталитического, флотационного, микропузырькового, электрокинетического);
-
• блока питания и индикации.
Требуется техническое обслуживание установки после получения каждых 400÷500 литров очищенной воды, для этого необходимо промыть электрохимический реактор установки кислотным раствором с целью удаления катодных отложений.
Специалисты отмечают, что «несмотря на эффективность очистки воды этими установками остаются актуальными вопросы экологии, т.к. в процессе электрохимической обработки воды синтезируются соединения озон, пероксидные соединения, атомарный кислород, диоксид хлора, свободные радикалы и др., которые могут быть даже более вредными по воздействию на организм, чем первоначально имеющиеся в воде с непредсказуемым эффектом» [7].
Что касается фильтров вообще. Доктор химических наук, профессор, директор Инcтитyтa коллоидной химии и химии воды, академик АН Украины В.В. Гончарук считает, что в фильтрах протекают естественные биологические процессы, накапливаются микроорганизмы, которые живут и выделяют токсины. В результате такие фильтры еще больше загрязняют воду. Дорогой хороший многоступенчатый фильтр быстро изнашивается за счёт большого содержания хлора в российской воде, и выдаёт некачественную воду [8].
-
III. Свойства деминерализованной и восстановленной воды
Обратный осмос и последующая минерализация воды всё шире применяется для приготовления питьевой воды и даже считается некоторыми специалистами безальтернативной. Однако в литературе все чаще поднимается полемика по поводу свойств искусственно минерализованной питьевой воды.
Так, в ноябре 2003 года в Риме (Европейский Центр Окружающей среды и Здоровья) собралась группа экспертов в области питания и медицины для работы над вопросами, касающимися состава питьевой воды и ее возможного вклада в общее поступление питательных веществ.
Изначальной целью данной встречи было внесение вклада в развитие Руководства по здоровому и экологически безопасному опреснению вод, введенного Восточным Средиземноморским Региональным Офисом ВОЗ и предназначенного для подготовки 4-го издания Руководства по качеству питьевой воды ВОЗ (РКПВ).
Всего было приглашено 18 экспертов из Канады, Чили, Республики Чехия, Германии, Ирландии, Италии, Молдовы, Сингапура, Швеции, Объединенного Королевства и США. Дополнительно были представлены доклады экспертов, которые не смогли приехать лично...
В частности, встал вопрос о последствиях длительного употребления воды, прошедшей деминерализацию: о пресной воде, прошедшей обработку в мембранной системе, а также о воссоздании их минерального состава [3].
Получение питьевой воды из сильносоленых вод типа морских и солоноватых посредством обессоливания широко практикуется в регионах, испытывающих ее острую нехватку. И если реминерализация морской воды обязательна: она агрессивна по отношению к распределительным системам, и выбора тут пока нет, то насколько оправдан обратный осмос для пресных вод?
Учёные считают, что искусственно обработанная деминерализованная вода, которую изначально получали методом дистилляции, а затем методом обратного осмоса, должна использоваться для промышленных, технических и лабораторных целей. На сегодняшний день доказано, что потребление воды, бедной минеральными веществами, оказывает негативное влияние на механизмы гомеостаза, обмен минеральных веществ и воды в организме.
Риск водной «интоксикации» (гипонатриемического шока) возрастает с уменьшением минерализации воды. Серьезные проблемы со здоровьем возникали у альпинистов, употреблявших пищу, приготовленную на талом льду. Такая вода не содержит анионов и катионов, необходимых человеку. У детей, которые употребляют напитки, приготовленные на дистиллированной или слабоминерализованной воде, возникали такие заболевания, как отек мозга, конвульсии и ацидоз [3].
Малое поступление или отсутствие поступления кальция и магния приводит к сердечно-сосудистым заболеваниям, усталости, слабости, мышечным судорогам
В процессе приготовления пищи на мягкой воде из продуктов (овощи, мясо, злаки) теряются важные элементы. Потери кальция и магния могут достигать 60 %, других микроэлементов – даже больше (медь-66 %, марганец-70 %, кобальт-86 %). Напротив, во время приготовления пищи на жесткой воде, потери минералов заметно ниже, а содержание кальция в готовом блюде может даже повыситься [3].
Вода с малой минерализацией нестабильна и как следствие проявляет высокую агрессивность по отношению к материалам, с которыми вступает в контакт. Эта вода легче растворяет металлы и некоторые органические компоненты труб, накопительных танков и емкостей, шлангов и фитингов, не будучи при этом способной образовывать комплексные соединения с токсичными металлами, снижая этим их негативное влияние. Обычно воду обогащают минеральными веществами, пропуская через известняк или другие карбонатсодержащие минералы. Вода при этом насыщается в основном кальцием, а дефицит магния и других микроэлементов, например, фтора и калия ничем не восполняется. А ведь питьевая вода является основным источником поступления в организм фтора, недостаточное содержание которого в воде (ниже 0,6 мг/л) может быть причиной кариеса зубов, а избыточное (более 1,5 мг/л) служит причиной эндемического флюороза (см.). [3].
Кроме того, количество вносимого кальция регулируется скорее техническими (снижение агрессивности воды), нежели гигиеническими соображениями. Возможно, ни один из способов искусственного обогащения воды минеральными веществами не является оптимальным, поскольку насыщения всеми важными минеральными веществами не происходит. Как правило, методики стабилизации минерального состава воды разрабатываются с целью снижения коррозионной активности деминерализованной воды [3].
Природные воды существенно различаются по своему составу вследствие геологического и географического происхождения, климатическими, гидрологическими условиями и региональными различиями в степени и характере хозяйственного освоения территории, а также обработки, которой они подверглись. В настоящее время с целью улучшения санитарно-бытовых свойств воды ее умягчают (при централизованном водоснабжении), добиваясь того, чтобы общая жесткость не превышала 7 мг-экв/л, т. е. 20°. Для местных водоисточников (колодцы) допускается жесткость воды не выше 14 мг-экв, т. е. 40°[5].
Минеральные воды используют в лечебных целях. Бальнеотерапия – метод лечения минеральными водами (при наружном и внутреннем их применении) – рассматривается как патогенетическое лечение различных заболеваний, направленное на различные звенья патологического процесса. Химический (растворы солей), газовый состав и ионизирующие излучение каждого вида минеральной определяют дифференцированные показания и противопоказания к ее применению [4].
Кроме того, существует большое различие между неорганическими и органическими минералами.
-
IV. Традиционные способы водоподготовки. Водоканал СПб.
На водоканале СПб внедряются новые способы очистки воды, но в некоторых случаях до потребителя по-прежнему доходит некачественная вода, в основном это связано с изношенными водопроводными сетями, и с устаревшим оборудованием и технологиями, которые заменяются постепенно.
Например, в 2010 году была усовершенствована система биомониторинга качества воды в реке Нева, водозабор невской воды контролируется речными раками, к панцирям которых прикреплены специальные датчики, которые фиксируют кардиоритм животных. Если в воде появятся токсичные вещества – сердцебиение раков резко изменится, и соответствующий сигнал поступит диспетчерам [9].
С 2007 года на водоканале Санкт-Петербурга действует двухступенчатая технология комплексного обеззараживания питьевой воды на водопроводных станциях, которая включает в себя использование гипохлорита натрия и ультрафиолетовую обработку воды».
Использование таких эффективных методов обеззараживания, как озонирование и ультрафиолет не исключает необходимости хлорирования воды на одном из этапов ее очистки. Дезинфицирующая активность ультрафиолета зависит от мутности воды, ее жесткости (образования отложений на поверхности лампы), осаждения органических загрязнений на поверхности лампы, а также колебаний в электрической сети, влияющих на изменение длины волны [10].
Технологический процесс водоподготовки на водоканале СПб включает, как правило, следующие основные этапы:
-
• аммонирование воды (используется сульфат аммония);
-
• обеззараживание воды (используется гипохлорит натрия);
-
• коагуляция загрязняющих веществ (используется сульфат алюминия);
-
• флокуляция (используется катионный флокулянт);
-
• фильтрация через песчаную загрузку на контактных осветлителях (одноступенчатая схема очистки);
-
• отстаивание и фильтрация через песчаную загрузку на скорых фильтрах (двухступенчатая схема очистки);
-
• обеззараживание УФ-излучением [9].
Аммонирование воды (используется дешевый реагент – сульфат аммония (NH4)2SO4 - его вводят в обрабатываемую воду за несколько секунд до хлора. С хлором он образует хлорамины, связывая свободный хлор, благодаря чему значительно сокращается образование хлорорганики, вредной для организма человека, сокращается расход хлора, уменьшается коррозия труб водопровода. В частности, содержание хлороформа снизилось с 90÷120 до 1÷5 мкг/дм3 Использование сульфата аммония, водные растворы которого имеют слабокислую реакцию, увеличивает содержание дихлораминов, усиливая эффективность обеззараживания обрабатываемой воды. Некоторое снижение значения рН обрабатываемой воды вследствие замены аммиачной воды сульфатом аммония улучшает процесс коагуляции воды сульфатом алюминия, создавая оптимальные по кислотности среды условия [12].
Гипохлорит натрия - NaOCl, неорганическое соединение, натриевая соль хлорноватистой кислоты. Применяется в жидком виде (товарная концентрация растворов – 10 ÷ 12%), возможно получение на месте применения электрохимическим способом.
-
• Эффективен против большинства болезнетворных микроорганизмов; грибки, вызывающие кандидоз, Candida albicans , погибают in vitro в течение 30 секунд при действии 5,0 ± 0,5%-го раствора NaOCl (при концентрации действующего вещества ниже 0,05 % они проявляют устойчивость только спустя 24 часа после воздействия на них ГПХН); более резистентные к действию гипохлорита натрия энтерококки. Так, например, патогенный Enterococcus faecalis погибает через 30 секунд после обработки 5,25% -ым раствором или че-
- рез 30 минут после обработки 0,5%-ым раствором; грамотрицательные анаэробные бактерии, такие как Porphyromonas gingivalis, Porphyromonas endodontalis и Prevotella intermedia, погибают в течение 15 секунд после обработки 5,0 ± 0,5%-м раствором NaOCl
-
• Относительно безопасен при хранении и использовании
-
• При получении на месте не требует транспортировки и хранения опасных химикатов.
-
• Неэффективен против цист (Giardia, Cryptosporidium)
-
• Теряет активность при длительном хранении,
-
• Потенциальная опасность выделения газообразного хлора при хранении
-
• Образует побочные продукты дизин-фекции, включая тригалометаны, в том числе бромоформ и броматы в присутствии бромидов
-
• При получении на месте требует либо немедленного использования, либо, для обеспечения возможности хранения, специальных мер по очистке исходной воды и соли от ионов тяжелых металлов.
При хранении растворов NaClO с концентрацией активного хлора более 450 мг/л и рН более 9 происходит накопление хлоратов 3NaClO = NaClO3 + 2NaCl
Гипохлорит натрия (ГПХН) – неустойчивое соединение, легко разлагающееся с выделением кислорода. Самопроизвольное разложение медленно происходит даже при комнатной температуре: например, за 40 суток наиболее устойчивая форма – пентагидрат ГПХН (NaOCl • 5H2O) теряет около 30 % активного хлора: 2 NaOCl ^ 2 NaCl + O2.
При нагревании ГПХН параллельно с его разложением происходит реакция диспропорционирования:
-
3 NaOCl ^ NaClO3 + 2NaCl.
Гипохлорит натрия образует в воде хлорноватистую кислоту и гипохлорит ион в соотношениях, определяемых рН раствора, а именно соотношение между ионом гипохлорита и хлорноватистой кислотой определяется протеканием реакций гидролиза гипохлорита натрия и диссоциации хлорноватистой катионы натрия и анионы хлорноватистой кислоты:
NaOCl ^ Na + + OCl — .
Так как хлорноватистая кислота (HOCl) является очень слабой, гипохлорит-ион в водной среде подвергается гидролизу: OCl — + Н2О ^ HOCl + ОН — водные растворы ГПХН неустойчивы и со временем разлагаются даже при обычной температуре, и что наиболее устойчивы растворы с сильнощелочной средой (pH > 11). В сильнощелочной среде (pH > 10), когда гидролиз гипохлорит-иона подавлен, разложение происходит следующим образом:
-
2 OCl - ^ 2 Cl " + O2 .
При температурах выше 35°C распад сопровождается реакцией диспропорционирования:
OCl- ^ ClO: + 2 Cl-.
В среде со значением рН от 5 до 10, когда концентрация хлорноватистой кислоты в растворе заметно выше, разложение протекает по следующей схеме:
HOCl + 2 ClO- ^ ClO : + 2 Cl- + H+ ;
HOCl + ClO- ^ O2 + 2 Cl- + H+ .
При дальнейшем уменьшении рН, когда в растворе уже нет ClO- ионов, разложение идет следующим путем:
-
3 HClO ^ ClO: + 2 Cl- + 3 H+;
-
2 HClO ^ O2 + 2 Cl- + 2 H+ .
Когда рН раствора ниже 3, разложение будет сопровождаться выделением молекулярного хлора:
-
4 HClO ^2 Cl2 + O2 + H2O
При рН выше 10 происходит кислородное разложение, при рН 5÷10 – кислородное и хлоратное, при рН 3÷5 – хлорное и хлоратное, при рН меньше 3 – хлорное разложение растворов гипохлорита натрия.
Таким образом, подкисляя раствор гипохлорита натрия соляной кислотой, можно получить хлор: NaOCl + 2HCl ^ NaCl + Cl 2 + H 2 O.
В отличие от хлора растворы ГПХН имеют щелочной характер и могут применяться для повышения уровня рН обрабатываемой воды. С изменением значения рН обрабатываемой воды меняются соотношения между хлорноватистой кислотой и ионами гипохлорита. Проведенные в Японии исследования показали, что при использовании гипохлорита натрия для дезинфекции воды необходимо учитывать концентрацию щелочи в гипохлорите и поддерживать ее ниже определенного уровня. С возрастанием рН хлорноватистая кислота распадается на ионы Н и ClO -. Так, например, при рН = 6 доля HClO составляет 97%, а доля ионов гипохлорита 3%. При рН = 7 доля HClO составляет 78%, а гипохлорита – 22%, при рН = 8 доля HClO - 24%, гипохлорита - 76%. Таким образом, при высоких значениях рН в воде HClO превращается в гипохлорит ион.
Значит, повышение значения рН раствора товарного гипохлорита натрия следует проводить для того, чтобы повысить устойчивость щелочного раствор гипохлорита натрия.
На границе взаимодействия обрабатываемой воды и рабочего раствора ГПХН образуется осадок гидрооксида магния и диоксида кремния, забивающий водные каналы. Поэтому концентрация щелочи в гипохлорите натрия должна быть такой, чтобы не вызывать образования этого осадка. Экспериментально установлено, что оптимальный диапазон рН воды при ее обработке гипохлоритом натрия находится в пределах от 7,2 до 7,4.
Помимо значения рН на дезинфицирующие свойства ГПНХ оказывают влияние температура и содержание свободного активного хлора в рабочем растворе [13]. Наивысшая бактерицидная активность гипохлорита натрия проявляется в нейтральной среде, когда концентрации HClO и гипохлорит-анионов ClO- в процессе гидролиза и диссоциации ГПХН приблизительно равны.
Процесс обеззараживания воды ультрафиолетом, заключающийся в облучении воды имеет следующие особенности:
-
• Не требует хранения и транспортировки химикатов
-
• Эффективен против цист (Giardia, Cryptosporidium)
-
• Требует больших затрат на оборудование и техническое обслуживание
-
• Требует высоких операционных (энергетических) затрат
-
• Дезинфицирующая активность зависит от мутности воды, ее жесткости (образования отложений на поверхности лампы), осаждения органических загрязнений на поверхности лампы, а также колебаний в электрической сети, влияющих на изменение длины волны
-
• Отсутствует возможность оперативного контроля эффективности обеззараживания воды
Общим недостатком известных решений в области очистки питьевой воды является возможность образования побочных продуктов.
-
V. Электрохимические методы обработки питьевой воды
Электрохимические методы очистки питьевой воды на сегодня признаются ведущими специалистами мира как наиболее перспективные. Эти методы, в первую очередь, позволяют упростить процесс приготовления химических растворов, сократить число и объем реагентов [10]. Здесь под действием электрического поля уничтожаются микроорганизмы, окисляются органические вещества, разрушаются различные токсичные соединения, удаляются в дренаж ионы тяжелых металлов, нитраты, нитриты. Но есть мнение, что фильтр неэффективен в отношении солей тяжелых металлов, жесткой воды, радиоактивных элементов. Недостатком является также то, что необходимо наличие источника электроэнергии и, вместе с тем, высокая стоимость фильтра, а также повышение кислотности воды, в результате чего воду в течение нескольких часов пить нельзя.
Однако использование электрического тока в процессе очистки воды многими специалистами считается наиболее перспективным. К настоящему времени имеются многочисленные патенты на электрохимические установки (технологии), среди которых заслуживают внимание следующие.
Устройство для электрохимической обработки воды (патент РФ RU2110483). Дата начала действия патента: 1997.03.24. Изобретение относится к устройству для электрохимической обработки воды, содержащему, по крайней мере, один проточный диафрагменный электролизер.
Устройство для электрохимической обработки воды или водных растворов (патент РФ № 2367616), начало действия патента: 30.11.2007. Изобретение относится к области электрохимической обработки воды и/или водных растворов солей с целью изменения их окислительных и восстановительных свойств.
Способ электрохимической очистки питьевой воды (патент Российской Федерации RU2043308). Дата начала действия патента: 28.11.1991. Способ получения электрохимически активированного дезинфицирующего раствора и установка для его осуществления (патент РФ № 2329197) начало действия патента: 29.09.2006 Способ получения электрохимически активированного дезинфицирующего раствора осуществляют электролизом исходного раствора в реакторе.
Устройство для обработки воды электрическими разрядами (патент РФ № 2372296), начало действия патента: 24.03.2008. Устройство включает реактор для обрабатываемой воды, содержащий искровой разрядник, по крайней мере, с одной парой электродов, контактирующих непосредственно с обрабатываемой водой.
-
VI. Объединие реагентной и химической очистки
Дальнейшее совершенствование технологии очистки питьевой воды возможно в сочетании традиционной реагентной очистки с электрохимической [6,15,16], что позволит устранить отрицательные качества обеих технологий и использовать их несомненные преимущества.
Электрореагентным методом можно корректировать физико-химические свойства обрабатываемой воды, они обладают высоким бактерицидным эффектом, значительно упрощают технологические схемы очистки. Во многих случаях электрохимичесреагентный метод исключает «вторичное» загрязнение воды анионными и катионными остатками, характерными для реагентных и электрохимических методов.
Полная схема очистки воды электрореа-гентным методом может быть обеспечена установкой, состоящей из двух последовательных технологических контуров [16], включающих электрохимический реактор, дозатор реагентов, отстойник-дозреватель, фильтр и стерилизатор. Оба контура одинаковы по структуре операций и аппаратурному оформлению и отличаются только используемыми реагентами и параметрами ведения процесса. Каждая стадия очистки состоит из следующих операций: 1 – смешение воды с реагентной смесью; 2 – электрокаталитическая обработка; 3 – отстаивание и фильтрование; 4 – стерилизация.
Первой операцией обработки воды является смешение воды с реагентной смесью. Введение дозированного количества реагентов в обрабатываемую воду производится с помощью струйного насоса-дозатора. В результате операции в воду поступают структурообразующие вещества, устанавливается необходимое значение водородного показателя (рН) воды и производится ингибирование микроорганизмов.
Электрообработка проводится в двухсекционном электрохимическом реакторе, где вода рециркулирует под действием осевого насоса. На стадии электрообработки вода подвергается действию постоянного и импульсного электрического тока. Обработка обеспечивает структурирование и выделение в осадок взвешенных веществ и примесей тяжелых металлов, окислительную деструкцию токсичных веществ, органических загрязнений, хлорпро-изводных, СПАВ, и микроорганизмов. Процесс электрообработки основан на реакциях электрокаталитического окисления, гидроксилирования и поликонденсации с сопутствуюшим синтезом нерастворимых комплексных солей, структурированных в крупнодисперсные коллоидные ассоциаты, пригодные для отделения отстаиванием и фильтрованием.
Осадки, выделяемые из воды при очистке и кондиции, соответствую классу токсичности лучше Класс5 (пригодны для отсыпки в грунт), а также пригодны для сброса в хозбытовую канализацию или для вывоза на свалки бытовых отходов.
Для доочистки водопроводной воды, которая уже прошла обработку (включая обез- зараживание) на водоканале может быть использована одноконтурная установка, разработанная в СПбГЭУ (рис.2), реализующая все перечисленные стадии электрореагентного процесса: последовательную дозированную подачу кислого РС-1 и щелочного РС-2 реагента, отстаивание и фильтрование воды.

Рисунок 2 – Опытная установка электрореагент-ной очистки воды
Низкие параметры напряжения (U = 9В) и импульса (300Гц) установки дают возможность создать довольно экономичный вариант получения питьевой воды с определёнными преимуществами. В качестве реагентов используются относительно безопасные для здоровья человека: РС1 ортофосфорная кислота (H3PO4) и термосульфат кальция (CaS04); РС2 гидроксид натрия (NaOH) и калия (КОН).
Так пищевую ортофосфорную кислоту применяют в производстве газированной воды и для получения солей, изготовления печенья, сухарей. Применение в качестве регулятора кислотности.
Возможность использования неблагородных и относительно дешевых металлов вместо металлов платиновой группы в качестве материалов для изготовления малоизнашиваю-щихся анодов исследуется.
Коррозионная стойкость металлических анодов при анодной поляризации объясняется образованием адсорбционных или фазовых окисных слоев на поверхности анода, приводящих к его пассивации. Такого рода аноды следует рассматривать как составные аноды, у которых основанием электрода является не титан, а неблагородный металл с активным покрытием из его окислов, образующихся в процессе анодной поляризации электрода[14].


