Процессы ассоциации и водородные связи в растворах органических кислот
Автор: Верстаков Е.С., Коробкова С.А.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Рубрика: Экспериментальные исследования
Статья в выпуске: 1 (29), 2011 года.
Бесплатный доступ
Исследована кинетика процессов ассоциации и образование водородных связей в растворах уксусной кислоты, анионы которой дают определенный вклад в электрохимические взаимодействия в биосистемах на молекулярном уровне. По полученным данным рассчитаны энтальпия ( ΔН ≠), свободная энергия (ΔF ≠) и энтропия (T·ΔS ≠) активации дипольной релаксации и вязкого течения, которые близки к энергетическим характеристикам водородной связи.
Короткий адрес: https://sciup.org/142148884
IDR: 142148884 | УДК: 53:661.73
Assosiation processes and h-bond of organic acids
It was investigated kinetics of association processes and formation of H-bond in solutions of an acetic acid, the anions of which give the certain contribution to electrochemical interactions to biosystems at a molecular level. The enthalpy (AH*), free energy (ΔF ≠) and entropy (T·ΔS ≠) of dipole relaxations activation and viscose flow which are close to power characteristics of H-bond were calculated due to the received data.
Текст научной статьи Процессы ассоциации и водородные связи в растворах органических кислот
Известно [9], что при физиологическом раздражении клеток передача сигнала является процессом, связанным с электрическими свойствами биологических объектов. При этом цитоплазма в состоянии покоя клеток всегда имеет отрицательный потенциал по отношению к межклеточной жидкости, а избыток положительных зарядов ионов калия внутри клеток компенсируется в основном органическими анионами, которые являются продуктами диссоциации органических кислот.
Проведенные многочисленные эксперименты и полученные данные объяснялись фазовой теорией биопотенциалов [4, 7]. В последнее время на смену фазовой пришла полиэлектролитная теория [3, 8], которая объясняет возникновение потенциала покоя и потенциала действия свойствами молекул, органических и неорганических ионов, а также их взаимодействием в полиэлектролитной среде.
Кроме того, предполагается участие в этих процессах многих других молекул и их групп (-COOH, -NH2, -NH, OH). Между этими группами возможны химические связи, в основном типа водородной, дающие возможность возникновения структур, способствующих денатурации белков.
ЦЕЛЬ РАБОТЫ
Исследовать кинетику взаимодействия молекул и анионов органических кислот с компонентами, имеющими обширную сетку водородных связей и высокую диэлектрическую проницаемость, а также ее возможный энергетический вклад в величину равновесного потенциала покоя клетки.
МЕТОДИКА ИССЛЕДОВАНИЯ
В качестве первого компонента нами был выбран формамид (HCONH2), растворы которого с неор- ганическими ионами исследованы [5], а его водные растворы во всем диапазоне концентраций не образуют ассоциатов [6], создавая лабильную сетку водородных связей. Кроме того, статическая диэлектрическая постоянная для формамида £S = 109,5.
Вторым компонентом выбрана уксусная кислота (СH3COOH), водные растворы которой содержат ассоциаты [11], а по отношению к воде она является слабым электролитом.
Волноводным методом определены действительная £'(0) и мнимая £"(a) части комплексной диэлектрической проницаемости (ДП) на частотах 3; 3,76; 9,4 и 14 ГГц, в температурном интервале 7—50 °С. Установки калиброваны по чистым жидкостям, параметры которых взяты из [1]. Ошибки измерений составили 2—2,5 % для £'(О) и 3—3,5 % для £"(ю). Следует отметить, что в данной работе представляла интерес только та часть общих диэлектри- ческих потерь, которая обусловлена поляризационными процессами. Ее расчет проводился по формуле:
£" = £"(a) - 2o/v (1), где ε (ω)— общая величина диэлектрических потерь, измеренная в диапазоне СВЧ, ε π — диэлектрические потери, обусловленные поляризационными процессами, 2dv — потери ионной проводимости, о—удельная электропроводность, измеренная на низких частотах (v = 1000 Гц).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Экспериментальные данные приведены в табл. 1. Cтатическая диэлектрическая проницаемость ( £S ) исследованных растворов в указанном интервале температур определена методом круговых диаграмм. На рис. 1 представлена одна из них.
ТАБЛИЦА 1
Время диэлектрической релаксации τ 0 , статическая диэлектрическая проницаемость ε s и параметр распределения α -растворов формамид — уксусная кислота
|
t °С |
Мольные доли уксусной кислоты |
|||||||||||
|
0 |
0,1 |
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
0,8 |
0,9 |
1,0 |
||
|
т 0 х 1012с |
7 |
59 |
64 |
68 |
71 |
74 |
73 |
71 |
67 |
62 |
56 |
- |
|
15 |
51 |
55 |
58 |
61 |
62 |
60 |
58 |
55 |
53 |
50 |
- |
|
|
25 |
39 |
42,5 |
46 |
49 |
51 |
50,5 |
49 |
47,5 |
46,5 |
45 |
44 |
|
|
35 |
31 |
34 |
37 |
40 |
42 |
41,5 |
41 |
40,5 |
40 |
40 |
39,5 |
|
|
50 |
28 |
29,5 |
31,5 |
33,5 |
34,5 |
34,5 |
34 |
34 |
34 |
34 |
33,5 |
|
|
ε s |
7 |
116,6 |
100 |
85 |
72 |
59 |
48 |
40 |
31 |
23 |
16 |
- |
|
15 |
113,5 |
97 |
82 |
69 |
56 |
45,5 |
57,5 |
29 |
21 |
14,5 |
- |
|
|
25 |
109,5 |
93 |
78,5 |
65 |
52 |
43 |
34 |
26 |
20 |
12 |
6,2 |
|
|
35 |
105,5 |
88 |
74,5 |
63 |
51 |
41,5 |
33 |
25,5 |
19,5 |
12 |
6,3 |
|
|
50 |
95 |
81 |
69 |
58 |
48 |
40 |
32 |
25 |
19 |
12 |
6,4 |
|
|
α |
7 |
- |
0,057 |
0,122 |
0,229 |
0,330 |
0,345 |
0,338 |
0,306 |
0,165 |
0,076 |
- |
|
15 |
- |
0,047 |
0,099 |
0,187 |
0,268 |
0,338 |
0,262 |
0,259 |
0,105 |
0,070 |
- |
|
|
25 |
- |
0,04 |
0,085 |
0,16 |
0,23 |
0,26 |
0,22 |
0,168 |
0,090 |
0,065 |
- |
|
|
35 |
- |
0,035 |
0,061 |
0,102 |
0,118 |
0,137 |
0,111 |
0,105 |
0,065 |
0,05 |
- |
|
|
50 |
- |
0,017 |
0,037 |
0,077 |
0,098 |
0,124 |
0,082 |
0,079 |
0,040 |
0,031 |
- |
|
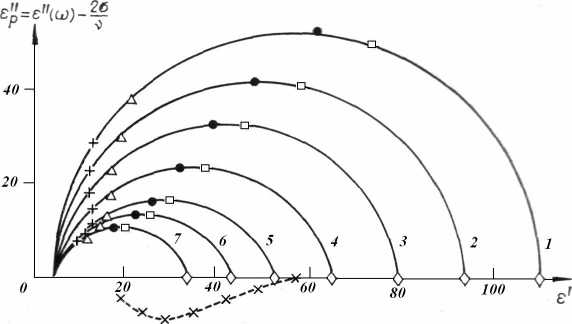
Рис. 1. Круговая диаграмма растворов формамид — уксусная кислота при 25 °С для мольных долей уксусной кислоты:
1 — 0; 2 — 0,1; 3 — 0,2; 4 — 0,3;
5 — 0,4; 6 — 0,5; 7 — 0,6. х — v = 14 ГГц;
А — v = 9,4 ГГц; • — v = 3,76 ГГц;
□ — v = 3 ГГц
Вид круговых диаграмм свидетельствует о том, что основная область дисперсии исследованной системы с достаточным приближением описывается уравнением Коула-Коула [10]. Полученные значения £s , наиболее вероятного времени дипольной релаксации т 0 , параметра распределения времен релаксации приведены в табл. 1.
При увеличении концентрации уксусной кислоты в формамиде наиболее вероятные времена релаксации т 0 проходят через максимум в области концентрации х2 » 0,4 ( х2 — мольная доля уксусной кислоты), что, по всей видимости, связано с образованием дополнительного числа водородных связей или с их упрочнением. Кроме того, наблюдаются отрицательные отклонения £s от аддитивности. Эти отклонения превышают возможную ошибку, которая неизбежна при графическом определении статической ДП.
Отклонения концентрационной зависимости статической ДП от аддитивности указывают на достаточ- но сильное межмолекулярное взаимодействие в растворах и дают основание предполагать существование ассоциатов. На рис. 2 представлена зависимость Аего = sa-sj от состава смесей формамид—уксусная кислота при 25 °С, где е^ = es1 го + es2 (1 - го), es1 и es2 — статическая ДП формамида и уксусной кислоты соответственно, го — объемные доли уксусной кислоты.
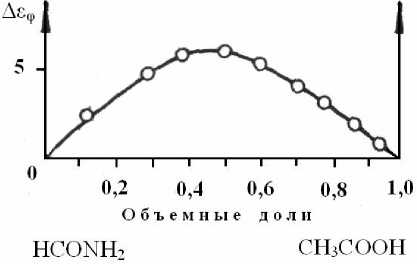
Рис. 2. Концентрационная зависимость отклонения статической диэлектрической проницаемости от аддитивности для смесей формамид — уксусная кислота при 25 °С
Отрицательные значения Аего и резкое уменьшение статической ДП с увеличением концентрации уксусной кислоты, по всей видимости, указывают на уменьшение количества ассоциатов в формамиде,
ТАБЛИЦА 2
разрыв в них водородных связей и установление новых. Приведенная зависимость Аего подтверждает наличие смешанных ассоциатов типа (НСОNН2)⋅ l , (CH3COOH)⋅ r , HCONH2 n ⋅(СН3СООН), CH3COOH m ⋅(HCONH2) с различными значениями l , r , n , m , образованных водородными связями, максимальное число которых приходится на концентрацию р « 0,5 ( х2 ≈ 0,4).
Что касается параметра распределения времен релаксации α, то увеличение его с уменьшением температуры указывает на большую размытость функции распределения времен релаксации при относительно низких температурах. В свою очередь, ширина спектра распределения времен свидетельствует о том, что эти процессы не сводятся только к переориентации отдельных молекул, но затрагивают также и соседние молекулы, то есть имеют место кооперативные эффекты с образованием и разрушением водородных связей.
Между процессами диэлектрической релаксации и вязкого течения существует определенная связь, которую можно выразить посредством уравнения теории абсолютных скоростей реакций [2]. Поэтому для сравнительного анализа энергетических характеристик дипольной релаксации и вязкого течения были измерены вязкость и плотность вышеуказанных растворов, а также рассчитаны молярные объемы смесей (табл. 2—4).
Вязкость в сПз (0,1 Па^с) растворов уксусной кислоты в формамиде
|
t °С х 2 |
7 |
15 |
25 |
35 |
50 |
||||
|
эксп. |
эксп. |
расч. |
эксп. |
расч. |
эксп. |
расч. |
эксп. |
Расч. |
|
|
0 |
5,750 |
4,375 |
3,300 |
2,685 |
2,040 |
||||
|
0,1 |
6,483 |
4,936 |
4,864 |
3,584 |
3,709 |
2,901 |
3,037 |
2,106 |
2,323 |
|
0,2 |
6,978 |
5,161 |
5,144 |
3,809 |
3,966 |
3,031 |
3,268 |
2,221 |
2,517 |
|
0,3 |
7,385 |
5,430 |
5,172 |
3,925 |
4,034 |
3,142 |
3,344 |
2,269 |
2,594 |
|
0,4 |
7,664 |
5,555 |
4,951 |
3,985 |
3,902 |
3,241 |
3,256 |
2,274 |
2,543 |
|
0,5 |
7,380 |
5,402 |
4,506 |
3,843 |
3,591 |
3,058 |
3,015 |
2,201 |
2,372 |
|
0,6 |
6,842 |
4,973 |
3,902 |
3,523 |
3,144 |
2,813 |
2,656 |
2,045 |
2,104 |
|
0,7 |
5,592 |
4,248 |
3,213 |
2,978 |
2,618 |
2,416 |
2,226 |
1,791 |
1,775 |
|
0,8 |
4,085 |
3,212 |
2,517 |
2,375 |
2,073 |
1,936 |
1,774 |
1,476 |
1,425 |
|
0,9 |
2,649 |
2,310 |
1,876 |
1,579 |
1,562 |
1,436 |
1,345 |
1,147 |
1,088 |
|
1,0 |
1,330 |
1,120 |
0,970 |
0,790 |
|||||
ТАБЛИЦА 3
Плотность растворов уксусной кислоты в формамиде, г/см3
|
х 2 t °С |
0 |
0,1 |
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
0,8 |
0,9 |
1,0 |
|
7 |
1,1450 |
1,1412 |
1,1344 |
1,1306 |
1,1237 |
1,1164 |
1,1102 |
1,0995 |
1,0888 |
1,0770 |
- |
|
15 |
1,1400 |
1,1373 |
1,1295 |
1,1228 |
1,1171 |
1,1074 |
1,1007 |
1,0921 |
1,0814 |
1,0708 |
1,0542 |
|
25 |
1,1320 |
1,1263 |
1,1225 |
1,1128 |
1,1071 |
1,1005 |
1,0918 |
1,0811 |
1,0704 |
1,0588 |
1,0443 |
|
35 |
1,1250 |
1,1193 |
1,1147 |
1,1100 |
1,1023 |
1,0966 |
1,0871 |
1,0754 |
1,0658 |
1,0492 |
1,0337 |
|
50 |
1,1100 |
1,1046 |
1,0962 |
1,0909 |
1,0885 |
1,0772 |
1,0708 |
1,0604 |
1,0491 |
1,0368 |
1,0175 |
ТАБЛИЦА 4
Молярный объем смесей при 25°
|
х 2 |
0 |
0,1 |
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
0,8 |
0,9 |
1,0 |
|
106 м3/моль |
39,753 |
41,259 |
42,813 |
44,393 |
45,986 |
47,595 |
49,110 |
50,068 |
53,068 |
54,976 |
57,190 |
Ошибки в измеренных значениях вязкости составляли ± 0,003 сПз, плотности ± 5-10 -4 г/см3.
Рассчитанные энергетические характеристики дипольной релаксации ( А Н * , a f * , т -a s ; ) и вязкого течения ( ан ; , А Ғ П , Т -А П представлены на рис. 3—5.
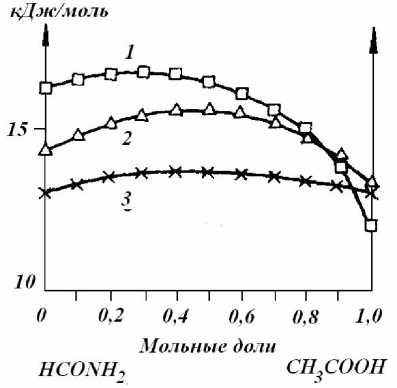
Рис. 3. Зависимости энтальпии и свободной энергии активации вязкого течения и дипольной релаксации от состава смесей: 1 — А Н ; , 2 — А Ғ П , 3 — A F*
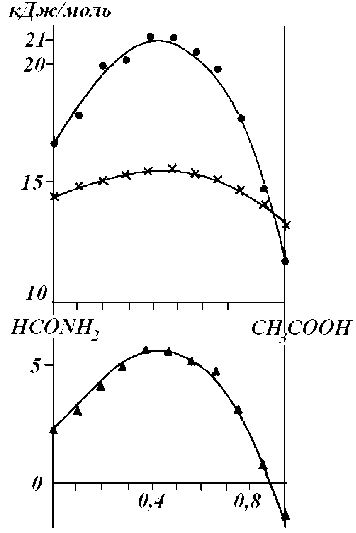
Рис. 4. Зависимость энтальпии, энтропии и свободной энергии активации вязкого течения от состава смесей: — АН* , х — AF* , ж — A S*
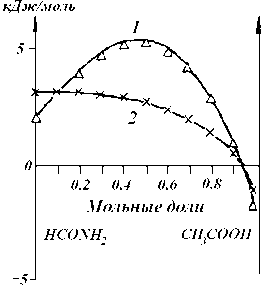
Рис. 5. Зависимость энтропии активации вязкого течения и дипольной релаксации от состава смесей:
1 — Т -as; , 2 — Т -a s
Как видно из рис. 3, А Н * значения лежат в пределах 12—16 кДж/моль, что подтверждает представление о данных смесях как о растворах с водородными связями. Характер изменения энтальпии активации вязкого течения а н* (рис. 4), ее величина в максимуме (^ 21 кДж/моль), а также характер изменения a f* и Т -as; указывают на образование водородных связей между компонентами. Соответственно достижение активированного состояния требует затраты энергии на образование дырки и на разрыв некоторого числа водородных связей, благодаря чему a s * > 0 при х2 < 0,9 ( х2 — мольная доля СН3СООН). Однако при х2 > 0,9, A S * < 0. По-видимому, это можно рассматривать как указание на сравнительно слабую степень упорядоченности начального состояния.
Так как скорость реакции всегда определяется величиной свободной энергии активации, примерное равенство и симбатное изменение a F * и af* , представленные на рис. 3, в пределах ошибки эксперимента можно рассматривать как свидетельство того, что процессы дипольной ориентации и вязкого течения для данных смесей, с энергетической точки зрения, имеют одинаковые или подобные активированные состояния. В связи с этим весьма характерны изменения энтропийных характеристик дипольной релаксации т - a S * и вязкого течения Т -as; , представленные на рис. 5.
При х2 < 0,9 т -a S * > 0 и Т -as; > 0, а смена знака в обоих случаях происходит при х2 ~ 0,9, что, по-видимому, определяется практическим отсутствием в растворах c х2 > 0,9 ассоциатов смешанного состава. В области х2 < 0,9 при активации эти ассоциаты имеют менее упорядоченную структуру по сравнению с исходной. По всей видимости, активированное состояние при диэлектрической релаксации достигается в них за счет разрыва и образования водородных связей с одновременным вращением вокруг оставшейся. Так как при х2 < 0,9 A S * > A S ; , то, вероятно, активированное состояние при вязком течении достигается в том случае, когда обеспечен критический свободный объем за счет перераспределения водородных связей и смещения молекул в ближайшем окружении.
Дополнительные сведения о характере межмолекулярных взаимодействий в исследованной системе получены из зависимости V i - V 0 от состава смесей, которая приведена на рис. 6, где V i — парциальный молярный объем, Vi 0 — молярный объем чистого компонента.
Относительн ы е парциальные молярные объемы компонентов V i - V 0 являются плавными функциями концентрации и не меняют знака во всей области составов (рис. 6). Максимум вязкости, хотя он и наблюдается при всех изученных температурах, не сингулярен (табл. 2), как не сингулярны и функции активации вязкого течения.
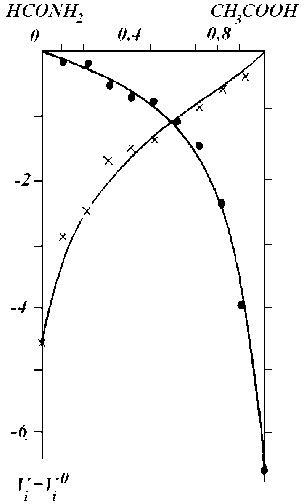
Рис. 6. Зависимость от состава смесей
ЗАКЛЮЧЕНИЕ
Таким образом, установлено, что в исследуемых растворах образуются смешанные ассоциаты типа (HCONH2)⋅ l , (HC3COOH)⋅ r , HCONH2 n ⋅(CH3COOH), CH3COOH m ⋅(HCONH2) c различными значениями l , r , n , m , образованными водородными связями.
Максимальная энергия и число H-связей приходится на концентрацию уксусной кислоты x2 ≈ 0,4 ( x2 — мольная доля).
Принимая во внимание, что константа диссоциации уксусной кислоты Kд = 1,754⋅10-5, ее анио- нов явно недостаточно для компенсации избытка положительных зарядов ионов калия в клетке.
По всей видимости, высокая диэлектрическая проницаемость (для формамида, для воды), наличие прочных водородных связей и образование смешанных ассоциатов будут являться факторами, которые ослабляют сольватную оболочку для неорганических ионов, определяющих величину равновесного потенциала покоя.


