Профилактическая рентгенэндоваскулярная артериальная эмболизация у пациентов с язвенными гастродуоденальными кровотечениями с высоким риском рецидива
Автор: Бедин В. В., Коржева И. Ю., Цуркан В. А., Бочарников Д. С., Соколов К. А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Сердечно-сосудистая хирургия
Статья в выпуске: 1 (83), 2023 года.
Бесплатный доступ
Введение. Язвенная болезнь является основной причиной кровотечения из верхних отделов желудочно-кишечного тракта (ЖКТ). Язвенные кровотечения (ЯЗ)остаются одним из лидирующих заболеваний в структуре экстренной медицинской помощи. Общая летальность при данной патологии достигает 40 % с учетом лапаротомий. Это доказывает необходимость дальнейшего поиска оптимальных методов лечения, одним из которых является профилактическая рентгенэндоваскулярная (РЭВ) эмболизация у пациентов с высоким риском рецидива кровотечения.Цель исследования. Оценить эффективность профилактической РЭВ у пациентов с высоким риском повторного желудочно-кишечного кровотечения (ЖКК).Материалы и методы. В исследование были включены 84 пациента с ЯЗ, имеющие высокий риск рецидива. Основную группу составили 40 пациентов, которым проводилась профилактическая РЭВ, группа контроля 44 пациента, которым РЭВ проводилась по 2-х рецидивов. Сравнивались количество рецидивов, лапаротомий и уровня летальности.Результаты. При сравнении в основной группе отмечается уменьшение среднего койко-дня 6,1 против 8,3 (p=0,017), доли рецидивов 7,5 % против 27,3 % (p=0,002), показатели летальности 1 пациент против 8 (p=0,002), необходимость в лапаротомии отсутствовала (p=0,028).Заключение. Проблема рецидива язвенного кровотечения, с последующими осложнениями вплоть до летального исхода, диктует необходимость правильной и своевременной стратификации высокого риска повторного кровотечения и определения наиболее верной тактики лечения, приводящей к уменьшению числа рецидивов, лапаротомий, смертности. Профилактическая РЭВ по результатам проведенного анализа полностью удовлетворяет эти требования.
Язвенные кровотечения, высокий риск рецидива, рентгенэндоваскулярная эмболизация
Короткий адрес: https://sciup.org/142237461
IDR: 142237461 | УДК: 006.617-089 | DOI: 10.17238/2072-3180-2023-1-50-56
Preventive X-ray endovascular arterial embolization in patients with ulcerative gastroduodenal bleeding with a high risk of recurrence
Introduction. Peptic ulcer is the main cause of bleeding from the upper gastrointestinal tract (GT). Ulcerative bleeding (UB) remains one of the leading diseases in the structure of emergency medical care. The total mortality in this pathology reaches 40% taking into account laparotomies. This the need for further search for optimal treatment methods. One of which is Preventive transcatheter arterial embolization(TAE) in patients with a high risk of recurrent bleeding.Study purpose. To evaluate the effectiveness of TAE in patients with a high risk of recurrent gastrointestinal bleeding (RGIB).Materials and methods. The study included 84 patients with UBa high risk of RGIB. The main group consisted of 40 patients who underwent preventive TAE, the control group consisted of 44 patients who underwent TAE after 2 relapses. The number of relapses, laparotomies and mortality rates were compared.Outcomes. When compared in the main group, there was a decrease in the average stay in hospitalof 6,1 versus 8,3 (p=0,017), the relapse rate of 7,5% versus 27,3% (p=0,002), mortality rates of 1 patient versus 8 (p=0,002), there was no need for laparotomy (p=0,028).Conclusion. The problem of recurrence of ulcerative bleeding, with subsequent complications up to death, dictates the need for correct and timely stratification of the high risk of recurrent bleeding and determining optimal treatment tactics, leading to a decrease in the number of relapses, laparotomies, mortality. Preventive TAE according to the results of the analysis fully satisfies these requirements.
Текст научной статьи Профилактическая рентгенэндоваскулярная артериальная эмболизация у пациентов с язвенными гастродуоденальными кровотечениями с высоким риском рецидива
Язвенная болезнь (ЯБ) желудка и двенадцатиперстной кишки (ДПК), осложненная кровотечением, остается одним из лидирующих заболеваний по причине госпитализаций как в России, так и в мире. Показатели заболеваемости 37–172 на 100000 человек [1–3]. В связи с развитием лекарственной терапии, а именно ингибиторов протоновой помпы (ИПП), проведением эффективной эррадикационной терапии H. Pylori, а также с развитием эндоскопии удалось снизить число заболеваемости по сравнению с прошлым десятилетием. Однако, отмечается рост числа желудочно-кишечных кровотечений (ЖКК). Общая летальность при данной патологии остается стабильно высокой и достигает 14 % по оценкам разных авторов без учета тех пациентов, которым потребовалось проведение лапаротомии. При наличии открытого оперативного вмешательства смертность при данном заболевании возрастает до 40 %, что может быть связано с изменением демографии населения, так как пожилые люди страдают большим числом сопутствующих заболеваний [1, 2].
Язвенная болезнь является причиной кровотечения из верхних отделов желудочно-кишечного тракта (ЖКТ) в 31–67 % случаях [1, 3, 4]. Язвенные ЖКК можно разделить на желудочные кровотечения и кровотечения из ДПК, причем последние происходят в 1,3–2,3 чаще. Из-за анатомических особенностей проведение эндоскопического гемостаза при кровотечении из двенадцатиперстной кишки может быть очень сложной задачей, особенно при локализации язвы на задней стенке луковицы двенадцатиперстной кишки. Кроме того, за задней стенкой ДПК располагается гастродуоденальная артерия и ее эрозия или эрозия ее ветвей приводит к массивному кровотечению с высоким риском рецидива. Все это связано с более высокой частотой хирургических вмешательств и смертностью у пациентов с дуоденальными кровотечениями, чем с желудочными [5].
Это доказывает, что важно не только знать современные рекомендации по лечению гастродуоденальных кровотечений, но и правильно оценить и вовремя выявить пациентов с высоким риском рецидива кровотечения, чтобы своевременно предпринять лечебные мероприятия направленные на снижение вероятности повторного кровотечения. Наиболее оптимальным методом выбора, по нашему мнению, является проведение профилактической рентгенэндоваскулярной эмболизации (РЭВ). Целью этой статьи является оценка данного метода и его влияния на снижение случаев повторного кровотечения, количества лапаротомий и уровня летальности.
Материалы и методы
Были проанализированы данные 84 пациентов, поступивших в стационар в период с января 2017 г. по июль 2022 г. в тяжелом и крайне тяжелом состоянии, с кровотечением из язв желудка и двенадцатиперстной кишки, у которых после проведенного первичного комбинированного гемостаза сохранялся высокий риск рецидива.
У больных с нестабильной гемодинамикой первым этапом проводились меры по стабилизации состояния. Части пациентам помимо устранения дефицита ОЦК, проводились гемотрансфузии эритроцитарной массы по ограничительной стратегии переливания крови (порог гемоглобина 70 г/л) [7, 8]. Так же некоторым пациентам проводилась коррекция системы гемостаза. При этом у пациентов, принимающих антагонисты витамина К, пороговым значением было МНО<2,5, так как было доказано, что эндоскопический гемостаз у таких больных может быть, успешно достигнут при МНО 2,5–1,5 по сравнению с пациентами без антикоагулянтов [9].
Кроме того, еще большее число пациентов принимают непрямые пероральные антикоагулянты (НОАК), которые повышают риск желудочно-кишечных кровотечений [9]. В связи с тем, что не существует клинических исследований, посвященных лечению НОАК у пациентов с язвенным кровотечением, терапия НОАК приостанавливалась.
Всем пациентам проводилась противоязвенная терапия ингибиторами протоновой помпы (ИПП) в высоких дозах по схеме (80 мг эзомепразола болюсно внутривенно и непрерывная инфузия 8 мг/ч в течение 72 ч.).
Каждый пациент был госпитализирован в отделение реанимации, с последующим проведением эндоскопического комбинированного гемостаза. В последующем по каждому пациенту проводилась стратификация риска рецидива кровотечения. Оценка производится на основании шкалы Forrest (Ia, Ib, IIa – высокий риск), эндоскопической картины язвы (локализация на задней стенке луковицы двенадцатиперстной кишки, размер язвы >2 см, размер кровоточащего сосуда >2 мм), шкалы Rockall (>5 баллов – высокий риск) [6]. Таким пациентам проводилась профилактическая РЭВ.
Критериями включения в данное исследование были пациенты с язвенными гастродуоденальными кровотечениями (опухолевый генез язвы исключался патоморфологическим исследованием) и имеющие высокий риск рецидива кровотечения.
Критериями исключения являлись:
-
1. Опухолевый генез язвенного кровотечения, пациенты с онкогематологией.
-
2. Пациенты с гемофилией.
-
3. Пациенты с iv стадией онкологического заболевания и прогрессированием онкопатологией
-
4. Пациенты поступившие в отделение реанимации в агональном состоянии.
Данное исследование проводилось с целью доказательства того, что профилактическая рентгенэндоваскулярная эмболизация, проводимая превентивно при наличие высокого риска повторного кровотечения после первичного комбинированного эндоскопического гемостаза, а не после 2-х неэффективных повторных эндоскопических гемостазов, улучает показатели лечения у данной группы пациентов.
Данное исследование проводилось частично ретроспективно, а также частично проспективно, учитывая стандартизированный протокол ведения пациентов с гастродуоденальными язвенными кровотечениями
Рассматриваемая выборка из 84 человек была разделена на 2 подгруппы. I группа (ретроспективная с января 2017 г. по декабрь 2019 г.) включала 44 пациента с высоким риском рецидива, где эндоваскулярная эмболизация проводилась после дважды неэффективного эндоскопического гемостаза. II группа (ретро- проспективная с января 2020 г. по июль
2022 г.) составила 40 пациента, которым проводилась профилактическая РЭВ.
При оценке однородности групп по полу, возрасту, локализации язвенного дефекта и диагнозу статистически значимых различий не было (табл. 1). Сравнивались показатели рецидива, койка-дня, проведения хирургического вмешательства, летальности. Для проведения статистического анализа использовалось программное обеспечение SPSS для Windows версии 23.0. Статистический анализ проведен при помощи тестов U-категории Манна-Уитни и Пирсоне.
Таблица 1
Сравнительная характеристика основной и контрольной групп
Table 1
Comparative characteristics of the main and control groups
|
Признак Sign |
Основная группа, Main group, n=44 |
Группа контроля, Control group, n=40 |
p |
|
Пол: муж/жен Gender: male / female |
13/31 |
12/28 |
0,16 |
|
Средний возраст, лет Average age, years |
71,2 (от 57 до 86 года, from 57 to 86 years old) |
68,5 (от 49 до 88 лет, from 49 to 88 years old) |
0,26 |
|
Диагноз: острая язва, хроническая язва Diagnosis: acute ulcer, chronic ulcer |
27/17 |
29/11 |
0,21 |
|
Локализация: желудок, ДПК Localization: stomach, duodenum |
16/28 |
15/25 |
0,77 |
Результаты
В группе I (n=44) средний койко-день составил до 8,3, рецидив кровотечения отмечен в 12 случаях (27,3 %), РЭВ проведена у 11 пациентов (25 %). Открытое хирургическое вмешательство проведено 5 больным (11,4 %), у 4 пациентов эндоскопический и рентгенэндоваскулярный гемостаз оказался неэффективен, у 1 пациента при первичном эндоскопическом исследовании не удалось достигнуть стойкого гемостаза. Общая летальность 8 человек (18 %), послеоперационная летальность 2 пациента (40 %).
В группе II средний койко-день 6,1, РЭВ проведена всем пациентам (100 %). Рецидив кровотечения отмечен в 3 случаях (7,5 %). Никому в данной группе не выполнялась лапаротомия. Общая летальность 1 пациент (2,5 %), послеоперационной летальности не было.
Всем пациентам проводился 2-х и 3-х компонентный эндоскопический гемостаз без осложнений.
Рентгенэндоваскулярная эмболизация проводилась по стандартной методике: гемостатической губкой – 8 (15,7 %), микросферами – 24 (47,0 %) и спиралями – 11 (21,6 %), комбинацией микросфер и спиралей – 8 (15,7 %). В обеих группах отмечены следующие осложнения: постэмболизационный синдром – 3 (5,9 %), ишемия слизистой желудка и ДПК – 1 (2,0 %).
При сравнении двух групп отметается уменьшение среднего койко-дня 6,1 против 8,3 (p=0,017), снижение доли рецидивов 7,5 % против 27,3 % (p=0,002), необходимость в лапаротомии в группе II отсутствовала (p=0,028). Значительно снизились показатели летальности: 1 пациент в группе I, по сравнению с 8 пациентами в группе 2 (p=0,002) (табл. 2), (рис. 1).
Обсуждение
Все пациенты, рассматриваемые в нашем исследовании, поступали в тяжелом и крайне тяжелом состоянии и госпитализировались в шоковую палату реанимационного отделения.
Таблица 2
Сравнение результатов
Table 2
Comparison of results
|
Показатель Sign |
Основная группа Main group |
Группа контроля Control group |
p |
|
Средний койкодень Hospital bed-day |
8,3 |
6,1 |
0,017 |
|
Число рецидивов Number of relapses |
12 |
3 |
0,002 |
|
Число Лапаротомий Number of laparotomies |
5 |
0 |
0,028 |
|
Летальность Lethality |
8 |
1 |
0,002 |
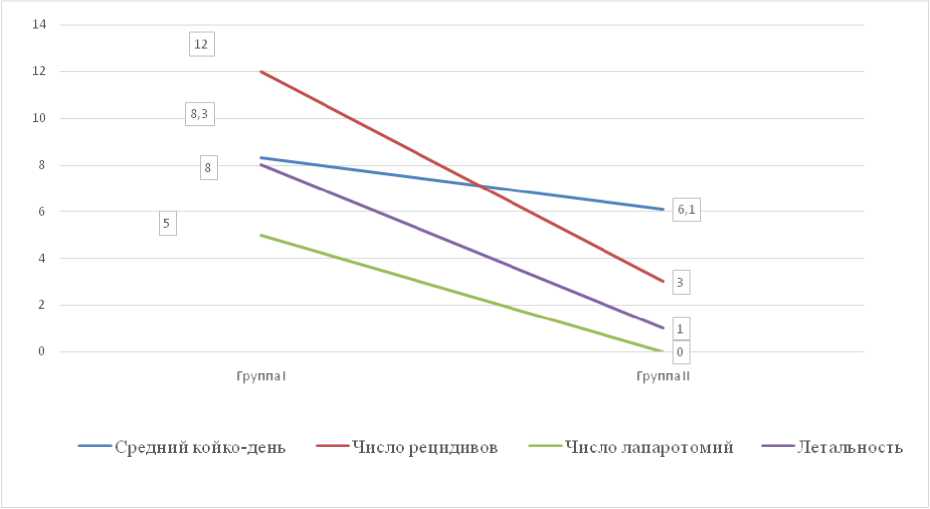
Рис. 1. Сравнение результатов Группы I и Группы II
Fig. 1. Comparison of Group I and Group II results
Эндоскопия является золотым стандартов в диагностике и лечении ЖКК. Последние рекомендации предлагают проводить эндоскопию в течение 24 часов после поступления [12]. Однако, по нашему мнению, следует дополнительно дифференцировать пациентов по тяжести их состояния и по выраженности клиники кровотечения. Эндоскопическое исследование в рассматриваемой группе пациентов проводилось в течение 2 часов или сразу после стабилизации у больных с нестабильной гемодинамикой. Первым шагом, осуществлялась классификация очагов кровотечения по шкале Forrest с целью принятия решения о необходимости проведения эндоскопического гемостаза и оценки риска повторного кровотечения. Поражения FIa, Ib, IIa (рис. 2, рис. 3) являются абсолютными показаниями к гемостазу и расцениваются как фактор высо- кого риска рецидива. Эндоскопический гемостаз проводился исключительно комбинацией различных методов: инъекции адреналина, аргоноплазменная коагуляция, клипирование (рис. 4, рис. 5). После проведения первичного эндоскопического гемостаза пациентам продолжалось проведение интенсивной терапии в условиях реанимации.
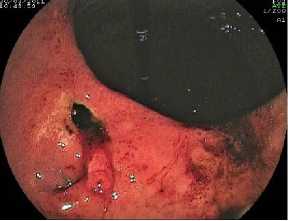
Рис. 2. Язва желудка FIIa
Fig. 2. Stomach ulcer FIIa
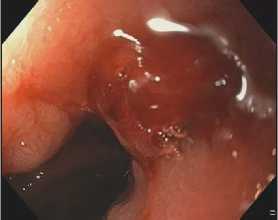
Рис. 3. Язва ДПК FIb
Fig. 3. Duodenal ulcer FIb
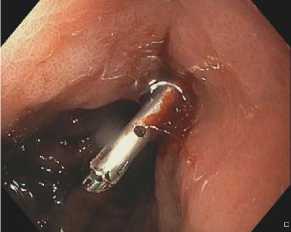
Рис. 4. Клипирование язвы ДПК
Fig. 4. Clipping of a duodenal ulcer
Последние клинические рекомендации по лечению пациентов с язвенными желудочно-кишечными кровотечениями рекомендуют ограничится первичным эндоскопическим гемостазом, провести стратификацию рисков повторного кровотечения с целью проведения контрольной эндоскопии в течение 24 часов для оценки гемостаза. В случае рецидива проводится повторный эндоскопический гемостаз, а при втором рецидиве выставляются показания к проведению РЭВ [15] (рис. 6, рис. 7).
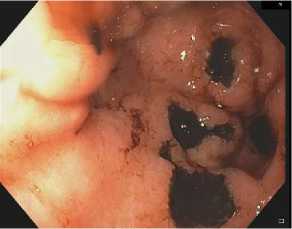
Рис. 5. Гемостаз АПК
Fig. 5. Hemostasis of the APK
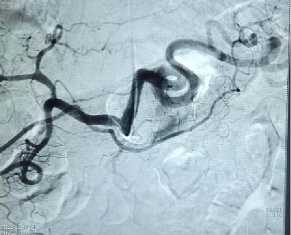
Рис. 6. РЭВ эмболизация правой желудочной артерии
Fig. 6. TEA of the right gastric artery
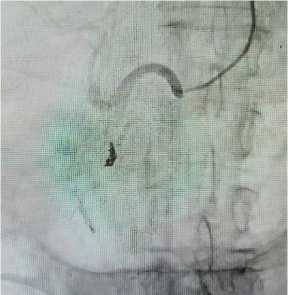
Рис. 7. Профилактическая РЭВ эмболизация ГДА по эндоскопической клипсе
Fig. 7. Preventive REV embolization of GDA by endoscopic clip
Неэффективность описанных методов – показание к проведению открытого хирургического вмешательства. При этом лапаротомия по-прежнему связана с высокими числом осложнений (≈50 %) и смертностью (от 18 % до 40 %).
В нашей клинике был предложен метод профилактической РЭВ (рис. 6) в группе пациентов с высоким риском рецидива, не дожидаясь повторного кровотечения. Показатели риска были несколько изменены и дополнены: шкала Forrest (Ia, Ib, IIa), эндоскопическая картина язвы (локализация на задней стенке луковицы ДПК, размер язвы ≥2 см, размер кровоточащего сосуда >2 мм), шка- ла Rockall (≥5 баллов – высокий риск), наличие тяжелых сопутствующих патологий.
Данный анализ показывает высокую эффективность концепции профилактической эмболизации. При изучении мировой литературы было найдено четыре похожих исследования. В первом из них пациенты с пептическими язвами высокого риска (от Forrest Ia до IIb) были разделены после эндоскопического гемостаза на подходящих для профилактической РЭВ или подлежащих консервативному лечению. К сожалению, это исследование было недостаточно мощным, поэтому они могли только показать, что профилактическая РЭВ может быть безопасно выполнено без обнаружения разницы в частоте рецидивов [1, 12]. Второе исследование, включающее пациентов с кровотечением из язв двенадцатиперстной кишки, показала, что концепция профилактической рентгенэндоваскулярной эмболизации при язвенных кровотечениях с высоким риском рецидива безопасна и эффективна, что приводит к низкой частоте операций и низкой смертности, связанной с кровотечением [1]. Еще в одном исследовании авторы смогли показать в следующем исследовании, что профилактическая РЭВ привело к снижению частоты повторного кровотечения (3,4 против 16,2 %; р = 0,005) и снтжению частоты хирургического вмешательства по сравнению со стандартным лечением [14]. Основными критериями для профилактических мер в этом исследовании были язвенная болезнь по классификации Forrest от Ia до IIb, оценка по шкале Rockal ≥5 и индивидуальный профиль высокого риска (возраст и сопутствующие заболевания). С другой стороны, авторы недавно опубликованного исследования сравнили профилактическую РЭВ после эндоскопического гемостаза со стандартным лечением. Авторы не смогли найти пользы от использования данного метода в этом исследовании.
Интересно, что повторное кровотечение было уменьшено только у пациентов с размером язвы ≥15 мм [15].
Все вышеописанное говорит о том, что проблема высокого числа рецидивов кровотечения и летальности беспокоит мировое сообщество экстренных хирургов. Ведутся поиски нахождения более верной тактики лечения, чем принятая в последних рекомендациях. Однако малое количество таких исследований не дает с уверенностью назвать концепцию профилактической эмболизации стандартом лечения у пациентов с высоким риском рецидива гастродуоденальных язвенных кровотечений. До сих пор нет четкой классификации и методов оценки рисков. Тем не менее, анализ методики, применяемой в нашей клинике, показывает качественное и количественное превосходство по сравнению с общепринятой тактикой.
Выводы
В настоящее время проблема рецидива язвенного кровотечения, с последующими осложнениями вплоть до летального исхода, остается достаточно актуальной. Данное исследование, а также другие, описанные выше, подтверждают необходимость правильной и своевременной стратификации высокого риска повторного кровотечения. Это позволяет подобрать наиболее верную тактику лечения таких пациентов, приводящую к уменьшению числа рецидивов, лапаротомий, к более ранней выписке из стационара, уменьшению смертности. Метод профилактической эндоваскулярной эмболизации на основании результатов проведенного анализа полностью удовлетворяет эти требования.
Список литературы Профилактическая рентгенэндоваскулярная артериальная эмболизация у пациентов с язвенными гастродуоденальными кровотечениями с высоким риском рецидива
- Mille M., Engelhardt T., Stier A. Bleeding Duodenal Ulcer: Strategies in High-Risk Ulcers. Visceral Medicine, 2021, №37(1), рр. 52-62. https://doi.org/10.1159/000513689
- Vanleerdam M., Vreeburg E., Rauws E. et al. . The American Journal of Gastroenterology, 2003, № 98(7), рр. 1494-1499. https://doi.org/10.1016/S0002-9270(03)00299-5
- Hearnshaw S.A., Logan R.F.A., Lowe D., Travis S.P.L., Murphy M.F., Palmer K.R. Acute upper gastrointestinal bleeding in the UK: Patient characteristics, diagnoses and outcomes in the 2007 UK audit. Gut, 2011, № 60(10), рр. 1327-1335. https://doi.org/10.1136/gut.2010.228437
- Theocharis G.J., Thomopoulos K.C., Sakellaropoulos G., Katsakoulis E., Nikolopoulou V. Changing Trends in the Epidemiology and Clinical Outcome of Acute Upper Gastrointestinal Bleeding in a Defined Geographical Area in Greece, 2008.
- Quan S., Frolkis A., Milne K. et al. Upper-gastrointestinal bleeding secondary to peptic ulcer disease: Incidence and outcomes. World Journal of Gastroenterology, 2014, № 20(46), рр. 17568-17577. https://doi.org/10.3748/wjg.v20.i46.17568
- Tarasconi A., Coccolini F., Biffl W.L. et al. Perforated and bleeding peptic ulcer: WSES guidelines. World Journal of Emergency Surgery, 2020, № 15(1). https://doi.org/10.1186/s13017-019-0283-9
- Jairath V., Kahan B.C., Gray A. et al. Restrictive versus liberal blood transfusion for acute upper gastrointestinal bleeding (TRIGGER): A pragmatic, open-label, cluster randomised feasibility trial. The Lancet, 2015, № 386(9989), рр. 137-144. https://doi.org/10.1016/S0140-6736(14)61999-1
- Villanueva C., Colomo A., Bosch A. et al. Transfusion Strategies for Acute Upper Gastrointestinal Bleeding. New England Journal of Medicine, 2013, № 368(1), рр. 11-21. https://doi.org/10.1056/nejmoa1211801
- Holster I.L., Valkhoff V.E., Kuipers E.J., Tjwa E.T.T.L. New oral anticoagulants increase risk for gastrointestinal bleeding: A systematic review and meta-analysis. Gastroenterology, 2013, № 145(1). https://doi.org/10.1053/j.gastro.2013.02.041
- Sreedharan A., Martin J., Leontiadis G.I. et al. Proton pump inhibitor treatment initiated prior to endoscopic diagnosis in upper gastrointestinal bleeding. Cochrane Database of Systematic Reviews, 2010, July; № 7. https://doi.org/10.1002/14651858.cd005415.pub3
- Laine L., McQuaid K.R. Endoscopic Therapy for Bleeding Ulcers: An Evidence-Based Approach Based on Meta-Analyses of Randomized Controlled Trials. Clinical Gastroenterology and Hepatology, 2009, № 7(1), рр. 33-47. https://doi.org/10.1016/j.cgh.2008.08.016
- Barkun A.N., Almadi M., Kuipers E.J. et al. Management of nonvariceal upper gastrointestinal bleeding: Guideline recommendations from the international consensus group. Annals of Internal Medicine, 2019, № 171(11), рр. 805-822. https://doi.org/10.7326/M19-1795
- Laursen S.B., Hansen J.M., Andersen P.E., Schaffalitzky De Muckadell O.B. Supplementary arteriel embolization an option in high-risk ulcer bleeding - A randomized study. Scandinavian Journal of Gastroenterology, 2014, № 49(1), рр. 75-83. https://doi.org/10.3109/00365521.2013.854829
- Kaminskis A., Ivanova P., Kratovska A., et al. Endoscopic hemostasis followed by preventive transarterial embolization in high-risk patients with bleeding peptic ulcer: 5-year experience. World Journal of Emergency Surgery, 2019, № 14(1). https://doi.org/10.1186/s13017-019-0264-z
- Lau J.Y.W., Pittayanon R., Wong K.T. et al. Prophylactic angiographic embolisation after endoscopic control of bleeding to high-risk peptic ulcers: A randomised controlled trial. Gut., 2018, № 25. https://doi.org/10.1136/gutjnl-2018-316074


