Профилактика несостоятельности кишечного шва в условиях экспериментального распространенного перитонита
Автор: Суковатых Б.С., Мосолова А.В., Затолокина М.А., Жуковский В.А., Анущенко Т.Ю.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.16, 2021 года.
Бесплатный доступ
Цель. Предупредить развитие несостоятельности кишечного шва в условиях экспериментального распространённого перитонита путем введения в брюшную полость иммобилизованной формы антисептика мирамистина, а также использования шовного материала, импрегнированного антисептиком. Материалы и методы. Эксперимент выполнен на 288 крысах-самцах линии Wistar разделенных на 3 группы по 96 особей в каждой. Моделирование перитонита осуществлялось путем введения в брюшную полость 10% каловой взвеси. Через 24 часа проводили лапаротомию, затем промывали брюшную полость стерильным 0,9% изотоническим раствором натрия хлорида и наносили на стенку толстой кишки рану длиной 1 см, которую в первой (контрольной) группе животных ушивали полигликолидной нитью без антибактериального покрытия, во второй группе - полигликолидной нитью, покрытой полимерным раствором, содержащим 10% мирамистина от массы полимера, а в третьей группе - полигликолидной нитью, покрытой полимерным раствором, содержащим 20% мирамистина от массы полимера. На заключительном этапе животным второй и третьей группах в брюшную полость вводили по 5 мл иммобилизованной формы мирамистина на основе натриевой соли карбоксиметилцеллюлозы. Из эксперимента животных выводили на 1, 3, 7 сутки после операции. Подсчитывали частоту несостоятельности швов и процент летальности животных в каждой группе. На гистологическое исследование брались участки толстой кишки в области наложенного шва. Результаты. Несостоятельность кишечного шва развилась у 48% животных в первой, у 32,3% во второй и у 18% в третьей группах, а летальные исходы зафиксированы соответственно у 79,2%, 50% и 37,2%. При гистологических исследованиях стенки толстой кишки у животных первой группы на всех сроках эксперимента сохранялась выраженная воспалительная реакция. Во второй группе к концу эксперимента отмечено снижение интенсивности воспаления. В третьей группе выявлено уменьшение зон некроза и нейтрофильно-лимфоцитарной инфильтрации к 3-м суткам до полного исчезновения к 7-м суткам эксперимента. Заключение. Введение в брюшную полость иммобилизованной формы мирамистина и наложение кишечного шва полигликолидной нитью покрытой полимерным раствором, содержащим 10 и 20% мирамистина от массы полимера, в условиях перитонита патогенетически обосновано и эффективно.
Моделирование распространенного перитонита, кишечный шов, мирамистин, иммобилизованная форма, полигликолидные хирургические нити, антимикробные свойства
Короткий адрес: https://sciup.org/140261824
IDR: 140261824 | DOI: 10.25881/20728255_2021_16_3_52
Prevention of intestinal seal insurance under experimental expanded peritonitis
Purpose. To prevent the development of intestinal suture incompetence in conditions of experimental widespread peritonitis by introducing an immobilized form of an antiseptic miramistin into the abdominal cavity, as well as using a suture material impregnated with an antiseptic. Materials and methods. The experiment was carried out on 288 male Wistar rats divided into 3 groups of 96 animals each. Modeling of peritonitis was carried out by introducing 10% fecal matter into the abdominal cavity. After 24 hours, a laparotomy was performed, then the abdominal cavity was washed with sterile saline and a 1 cm wound was applied to the colon wall, which in the first (control) group of animals was sutured with a polyglycolide thread without an antibacterial coating, in the second group-with a polyglycolide thread covered with a polymer solution, containing 10% miramistin by weight of the polymer, and in the third group - with a polyglycolide thread covered with a polymer solution containing 20% miramistin by weight of the polymer. At the final stage, the animals of the second and third groups were injected into the abdominal cavity with 5 ml of immobilized form of miramistin based on sodium salt of carboxymethylcellulose. The animals were taken out of the experiment on days 1, 3, 7 after the operation. The frequency of suture failure and the percentage of lethality of animals in each group were calculated. The sections of the large intestine in the area of the suture were taken for histological examination. Results. Intestinal suture failure developed in 48% of animals in the first group, in 32.3% in the second and 18% in the third group, and deaths were recorded in 79.2%, 50% and 37.2%, respectively. of the first group, a pronounced inflammatory reaction persisted at all periods of the experiment. In the second group, by the end of the experiment, a decrease in the intensity of inflammation was noted. In the third group, a decrease in the zones of necrosis and neutrophil-lymphocytic infiltration was revealed by the 3rd day until complete disappearance by the 7th day of the experiment. Conclusion. The introduction of an immobilized form of miramistin into the abdominal cavity and the imposition of an intestinal suture with a polyglycolide thread covered with a polymer solution containing 10% and 20% of miramistin by weight of the polymer is pathogenetically substantiated and effective under conditions of peritonitis.
Текст научной статьи Профилактика несостоятельности кишечного шва в условиях экспериментального распространенного перитонита
Одной из проблем абдоминальной хирургии является несостоятельность кишечного шва в условиях распространенного перитонита. Если в плановой абдоминальной хирургии несостоятельность кишечного шва колеблется в пределах 2–5%, то при разлитом перитоните она достигает 20–30% [1]. Причиной такого роста является воспаление стенки кишки, которая становится проницаемой для микроорганизмов, находящихся как в брюшной полости, так и в просвете кишечника [2].
Наложенные на патологически измененную стенку швы подвергаются воздействию микроорганизмов, что приводит к их несостоятельности [3].
Следовательно, для улучшения результатов лечения необходимо, во-первых, остановить прогрессирование перитонита, во-вторых, применять шовный материал с антимикробными свойствами. Одним из путей предупреждения прогрессирования перитонита является полноценная санация брюшной полости. Исследования последних лет показали, что водные растворы антисепти-

ков быстро (в течение 20–30 мин.) инактивируются перитонеальным экссудатом и для санации лучше применять их иммобилизованные формы, сохраняющие лечебный эффект в течение нескольких суток [4; 5].
Одним из самых эффективных отечественных препаратов, имеющих широкий спектр свойств является ми-рамистин. Он нашел широкое применение в различных областях медицины: хирургии, урологии, оториноларингологии, гинекологии и других. До настоящего времени данный антисептик в профилактике несостоятельности кишечного шва в условиях распространенного перитонита не применялся.
Цель исследования : предупредить развитие несостоятельности кишечного шва в условиях экспериментального распространённого перитонита путем введения в брюшную полость иммобилизованной формы антисептика мирамистина, а также использования шовного материала импрегнированного антисептиком.
Материалы и методы
Эксперимент выполнен на 288 крысах-самцах линии Wistar массой 250–300 г в условиях лаборатории «Экспериментальной хирургии и онкологии» НИИ экспериментальной медицины Курского государственного медицинского университета. Манипуляции с лабораторными животными осуществляли в соответствии с принципами биоэтики, правилами лабораторной практики (GLP) и международными рекомендациями по проведению медико-биологических исследований с использованием животных (1985).
Придание антимикробной активности рассасывающейся полигликолидной нити (производство фирмы Gunze) осуществляли путем нанесения полимерного покрытия в два слоя, в которое вводили антимикробный препарат. Для нанесения покрытия использовали растворы поли- ε -ка-пролактона (производство фирмы Purac) в 1,3-диоксолане, содержащие мирамистин, который также хорошо растворяется в данном растворителе. Для первого и второго покрытия использовали 2 и 10% растворы полимера. Мира-мистин вводили в оба покрытия в количестве 10 % или 20% от массы полимера. Дальнейшее повышение концентрации антисептика нарушает структуру шовного материала. Образцы шовного материала, участвующие в эксперименте, были предоставлены компанией ООО «Линтекс».
Моделирование перитонита осуществлялось по методике, разработанной в клинике, путем введения в брюшную полость животных 10% каловой взвеси [6]. Манипуляции на животных проводились под общим обезболиванием. В качестве средства для наркоза применялся эфир. Эвтаназию проводили путем передозировки наркотического средства.
Перед операцией готовили гелевую форму мирами-стина, по следующей методике: к 100 мл 0,01% раствора мирамистина при постоянном перемешивании добавляли 2 грамма натриевой соли карбоксиметилцеллюлозы (Na-КМЦ). Полученный гель с антимикробными свойствами стерилизовали методом автоклавирования [7].
Лабораторные животные были разделены на три группы по 96 особей в каждой. В первой (контрольной) группе животных через 24 часа после введения каловой взвеси в асептических условиях проводили лапаротомию и промывание брюшной полости стерильным 0,9% изотоническим раствором натрия хлорида. Затем на воспаленную стенку толстой кишки наносили раневой дефект длиной 1см, который ушивали с помощью полигликолидной нити без антимикробного покрытия (инертной). Животным второй и третьей групп производили аналогичные манипуляции, но раневой дефект толстой кишки во второй группе ушивали по-лигликолидной нитью, покрытой раствором полимера, содержащим 10% мирамистина от массы полимера, а в третьей группе — полигликолидной нитью, покрытой раствором полимера, содержащим 20% мирамистина от массы полимера. На заключительном этапе животным второй и третьей групп в брюшную полость вводили по 5 мл иммобилизованной формы мирамистина на основе натриевой соли карбоксиметилцеллюлозы. Из эксперимента животных выводили на 1, 3, 7 сутки после операции, путем передозировки средства для наркоза. Подсчитывали частоту несостоятельности швов и процент летальности животных в каждой группе. На гистологическое исследование брались участки толстой кишки в области наложенного шва, которые подвергались исследованию по общепринятой методике, с фиксацией препаратов в нейтральном формалине, заливкой в парафин, а также окраской срезов гематоксилин-эозином и по Ван-Гизону (пикро-фуксином). Статистическую обработку проводили с использованием пакета Microsoft Excel 2010. Достоверность отличий между показателями групп оценивали по критерию Манна-Уитни.
Результаты
Частота несостоятельности кишечных швов в экспериментальных группах представлена в таблице 1.
Представленные в таблице данные показывают положительное влияние антимикробного покрытия на раневой процесс в кишечной ране.Частота несостоятельности швов в третьей группе животных после ушивания полиглико-лидной нитью с полимерным покрытием, содержащим 20% мирамистина, на 1-е сутки была ниже на 23%, чем в
Табл. 1. Динамика несостоятельности кишечного шва экспериментальных животных
|
Сроки после операции |
Группы животных |
|||||
|
1 (n = 96) |
2 (n = 96) |
3 (n = 96) |
||||
|
Абс. число |
% |
Абс. число |
% |
Абс. число |
% |
|
|
1 сутки |
35 |
36,5 |
24 |
25* |
13 |
13,5* ** |
|
3 сутки |
7 |
7,3 |
5 |
5,2 |
3 |
3,3 |
|
7 сутки |
4 |
4,2 |
2 |
2,1 |
1 |
1,2 |
|
Итого |
46 |
48 |
31 |
32,3* |
17 |
18* ** |
Примечание: * — p ≤ 0,05 по сравнению с показателями первой группы;
** — p ≤ 0,05 по сравнению с показателями второй группы.
первой группе после ушивания дефекта инертной нитью и на 12,5% , чем во второй группе, где в качестве шовного материала использовалась нить с полимерным покрытием, содержащим 10% мирамистина. На третьи сутки несостоятельность шва в третьей группе животных была меньше на 4%, чем в первой, и на 1,9%, чем во второй, а на 7-е сутки, соответственно, на 3% и 0,9%. Еще более показательным является общее снижение несостоятельности кишечного шва на всех сроках эксперимента в третьей группе по сравнению с первой на 30% и со второй на 14,3%.
Динамика летальности в экспериментальных группах представлена в таблице 2.
Согласно полученным данным, наибольший процент летальности среди экспериментальных животных наблюдался в первой группе где в брюшную полость дополнительно не вводился антисептик. В этой группе на 1-е сутки эксперимента летальность животных была на 25% больше, чем во второй и на 35,5%, чем в третьей. На третье сутки эксперимента летальность во второй и третьей группах была на 3,1% меньше чем в первой, а на седьмые сутки, соответственно, на 1,05% и 4%. Общая летальность в первой группе выше на 29,2% чем во второй и на 41,7% чем в третьей.
При изучении микропрепаратов стенки толстой кишки на 1-е сутки эксперимента в первой группе после ушивания дефекта инертной (без антимикробного покрытия) поли-гликолидной нитью наблюдалась круглоклеточная инфильтрация всех слоев стенки кишки, а также, визуализировались
Табл. 2. Динамика летальности экспериментальных животных
|
Сроки после операции |
Группы животных |
|||||
|
1 (n = 96) |
2 (n = 96) |
3 (n = 96) |
||||
|
Абс. число |
% |
Абс. число |
% |
Абс. число |
% |
|
|
1 сутки |
60 |
62,5 |
36 |
37,5* |
26 |
27* ** |
|
3 сутки |
10 |
10,4 |
7 |
7,3 |
7 |
7,3 |
|
7 сутки |
6 |
6,25 |
5 |
5,2 |
3 |
3,2 |
|
Итого |
76 |
79,2 |
48 |
50* |
36 |
37,5* ** |
Примечание: * — p < 0,05 по сравнению с показателями первой группы;
локальные инфильтраты, основным составляющим компонентом которых являлись нейтрофилы и лимфоциты. В подслизистой оболочке, кроме клеток воспалительного ряда, визуализировалось большое количество тучных клеток овальной формы и крупных размеров, находившихся в стадии дегрануляции. В участках наложения кишечного шва инертным шовным материалом визуализировались остатки нити, локальные кровоизлияния, пропитывания тканей фибрином, участки некротического повреждения тканей, образующих стенку кишки (Рис. 1 А).
Во второй группе в срезах толстого отдела кишечника в области наложения шва определялись обширные зоны инфильтрации, встречались локальные участки с некротизированной тканью, на фоне отека всех оболочек стенки кишки. В зонах инфильтрации, клеточном компоненте преобладали сегменто- и палочкоядерные нейтрофилы, лимфоциты и моноциты (Рис. 1 Б).
В третьей группе животных на 1-е сутки в срезах толстой кишки наблюдалась тотальная инфильтрация всех слоев стенки кишки. В области подслизистой и мышечной оболочек, в непосредственной близости шва визуализировались участки локального скопления лимфоцитов и нейтрофилов. В собственной пластинке слизистой и подслизистой оболочках выражены признаки интерстициального отека. Эпителиоциты, выстилающие крипты, отечные, увеличены в размерах, бокаловидные клетки крупные, заполнены мукоидным секретом (Рис. 1 В). Следовательно, на первых сутках эксперимента во всех группах животных определялись воспалительные и некротические изменения стенки кишки, наиболее выраженные в первой группе.
На третьи сутки эксперимента в первой группе животных в сравнении с предыдущим сроком в толстой кишке не наблюдалось участков с пропитыванием фибрином и кровоизлияний, однако степень инфильтрации клетками воспалительного ряда продолжает оставаться высокой. В области наложения шва определялись локальные очаги инфильтрации, что свидетельствовало о выраженном воспалении стенки кишечника (Рис. 2 А). Во второй группе в срезах толстой кишки наблюдалась тенденция к уменьшению площади инфильтрации тканей стенки кишки в об-
** — p < 0,05 по сравнению с показателями второй группы.
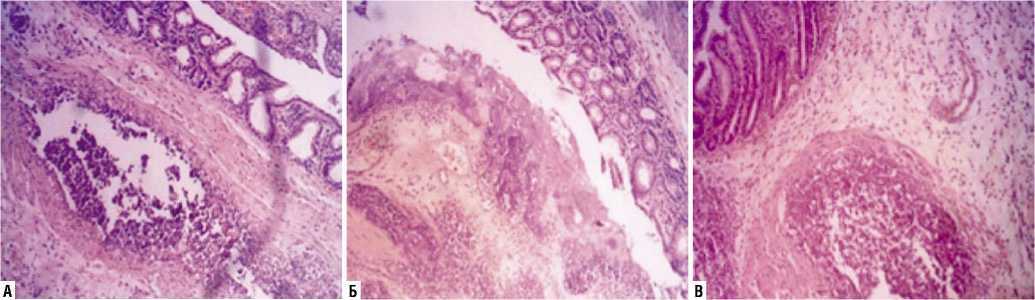
Рис. 1. Микрофотография среза отдела толстой кишки на 1-е сутки после ушивания дефекта: А — инертной полигликолидной нитью; Б — полиглико-лидной нитью с полимерным покрытием, содержащим 10% мирамистина; В — полигликолидной нитью, с полимерным покрытием, содержащим 20% мирамистина. Окрашено гематоксилином и эозином. Ув. х 200.
ласти шва. Некротизированные участки были единичные, признаки отека продолжали сохраняться. В некоторых срезах визуализировались остатки шовного материала. Плотность клеток во всех оболочках сохранялась высокая, в поле зрения преобладали лимфоциты, моноциты и клетки фибробластического дифферона (Рис. 2 Б). На третьи сутки эксперимента у животных из третьей труппы в срезах толстой кишки визуализировались участки с остатками шовного материала. При этом следует отметить, что в сравнении с первой группой эксперимента на данном сроке, площадь инфильтрата вокруг нитей шовного материала в несколько раз меньше. В клеточном компоненте преобладали лимфоциты и тучные клетки, находившиеся в стадии накопления гранул. В мышечной оболочке инфильтрации практически нет (Рис. 2 В).
На третьи сутки у животных второй и третьей групп отмечалось снижение воспалительных и некротических изменений в стенке кишки, наиболее выраженное в третьей группе. На 7-е сутки эксперимента в первой группе животных в слизистой и подслизистой оболочках сохранялся отек, инфильтрация и кровенаполнение кровеносных сосудов. Выраженность воспалительного процесса в стенке кишечника уменьшилась, но сохранялась высокой (Рис. 3 А).
Во второй группе в срезах стенки толстой кишки в области шва наблюдался интерстициальный отек, круглоклеточная инфильтрация не только слизистой и подслизистой оболочек, но и мышечной оболочки. Среди клеток воспалительного ряда преобладали нейтрофилы и лимфоциты. При этом в сравнении с предыдущей группой эксперимента, не выявлено локальных скоплений клеток воспалительного ряда, нет участков некроза.
В участках с визуализацией серозной оболочки сохранялся отек и увеличение размеров мезотелиоцитов и вертикальная ориентация их ядер по отношению к базальной мембране. Выраженность воспалительного процесса в стенке кишечника в этой группе животных к концу эксперимента умеренная (Рис. 3 Б).
На 7-е сутки эксперимента в третьей группе животных, где применялась иммобилизованная форма мирамистина совместно с нитью, содержащей в полимерном покрытии 20% мирамистина, в срезах толстой кишки, в сравнении с предыдущими сутками, клетки воспалительного ряда встречались в единичных случаях. Зон некроза и нейтро-
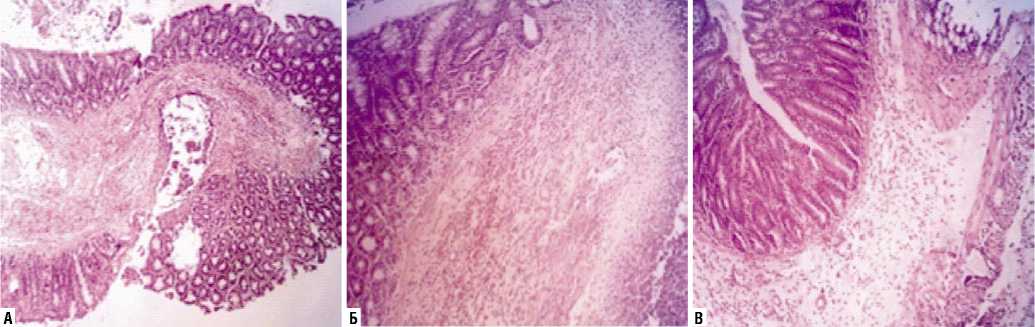
Рис. 2. Микрофотография среза отдела толстой кишки на третьи сутки после ушивания дефекта: А — инертной полигликолидной нитью; Б — полиглико-лидной нитью с полимерным покрытием, содержащим 10% мирамистина; В — полигликолидной нитью с полимерным покрытием, содержащим 20% мирамистина. Окрашено гематоксилином и эозином. Ув. х 200.
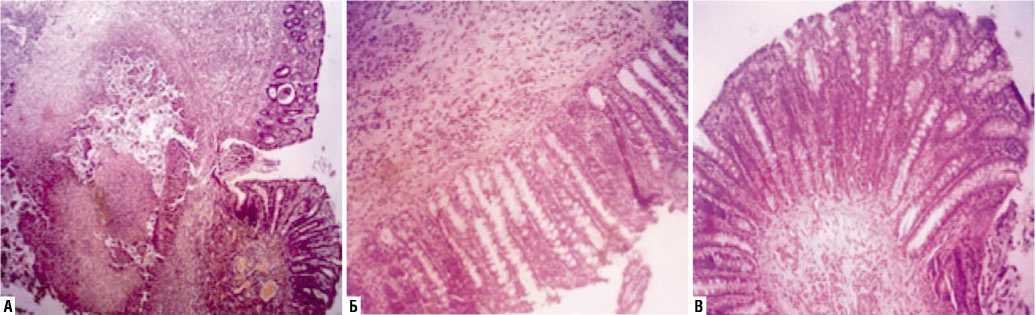
Рис. 3. Микрофотография среза отдела толстой кишки на 7-е сутки после ушивания дефекта: А — инертной полигликолидной нитью, Б — полиглико-лидной нитью с полимерным покрытием, содержащим 10% мирамистина, В — полигликолидной нитью с полимерным покрытием, содержащим 20% мирамистина. Окрашено гематоксилином и эозином. Ув. х 200.
фильно-лимфоцитарной инфильтрации не определялось. Круглоклеточная инфильтрация продолжала сохраняться в области мышечной и серозной оболочек. Кровеносные сосуды венозного русла умеренно расширены. Воспалительная реакция в кишечной стенке купировалась (Рис. 3 В).
Обсуждение
Отечественный антисептик мирамистин по химической структуре относится к четвертичным аммониевым соединениям и является поверхностно-активным веществом, которое разрушает наружную оболочку микробной клетки, приводя к ее гибели [8]. Он легко смешивается с карбоксиметилцеллюлозой, которая пролонгирует лечебное действие антисептика. Сообщений об отрицательном действии мирамистина на функцию жизненно важных органов не опубликовано.
Введение в брюшную полость иммобилизованной формы мирамистина на основе Na-КМЦ позволило снизить летальность экспериментальных животных к концу эксперимента на 29,2% во второй группе и на 41,7% в третьей, что свидетельствует об эффективности применения антисептика в составе геля при лечении перитонита. Применение шовного материала, импрегнированного антимикробным препаратом, позволило уменьшить частоту несостоятельности кишечного шва во второй группе животных на 15,7%, а в третьей — на 40% по сравнению с первой группой. Проведенные исследования показали, что шовный материал с покрытием, содержащим 20% мирамистина превосходит по свой эффективности покрытие, содержащее 10% антисептика.
Использование шовного материала с 20% содержанием антисептика позволяет значительно сократить сроки воспаления стенки толстой кишки в области наложения кишечного шва. Морфологическим обоснованием данного вывода служит хорошо выраженная динамика в сторону снижения признаков воспаления. Если на первых сутках наблюдалась множественная инфильтрация нейтрофилами и лимфоцитами всех слоев толстой кишки, то к концу эксперимента отмечено их снижение до обычного количества клеток воспалительного ряда в стенке кишки. Уменьшение в области кишечного шва зон некроза и нейтрофильно-лимфоцитарной инфильтрации к 3-м суткам до полного исчезновения к 7-м суткам эксперимента, так же свидетельствует о высокой эффективности предлагаемого шовного материала.
Результаты проведенного исследования показали преимущество применения иммобилизованной формы мирамистина в составе геля на основе Na-КМЦ в комплексе с антимикробным шовным материалом, содержащем в полимерном покрытии 20% препарата, в профилактике несостоятельности кишечных швов в условиях распространенного экспериментального перитонита.
Вывод
Использование иммобилизованной формы мирами-стина на основе натриевой соли карбоксиметилцеллюлозы в комплексе с полигликолидным шовным материалом с антимикробным покрытием, содержащим 10% мирамистина позволяет снизить процент несостоятельности кишечного шва на 15,7%, а с содержащим 20% антисептика — на 40% по сравнению с контрольной группой животных.
Соответствие нормам этики. Авторы подтверждают, что соблюдены права людей, принимавших участие в исследовании, включая получение информированного согласия в тех случаях, когда оно необходимо, и правила обращения с животными в случаях их использования в работе. Подробная информация содержится в Правилах для авторов.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Профилактика несостоятельности кишечного шва в условиях экспериментального распространенного перитонита
- Ермолов А.С., Воленко А.В., Горский В.А. Радикальное устранение источника перитонита - кардинальная проблема хирургического лечения перитонита // Анналы хирургии. - 2016. - №21(3). - С. 211-214.
- Алиев С.А., Алиев Э.С. Абдоминальный сепсис: состояние проблемы, интегральные системы оценки тяжести течения и критерии прогноза исхода // Вестник хирургии им. И.И. Грекова. - 2018. - №177(5). - С. 108-112.
- Плечева Д.В., Галимов О.В., Плечев В.В., Шикова Ю.В., Елова Е.В. Профилактика несостоятельности межкишечных анастомозов в плановой и ургентной хирургии // Вестник Национального медико-хирургического центра им. Н.И. Пирогова. - 2018. - №13(3). С. 47-49.
- Суковатых Б.С., Конопля А.И., Блинков Ю.А., Блинков Ю.Ю. Сравнительная эффективность водных и иммобилизированных форм гипохлорита натрия в лечении распространенного перитонита // Человек и его здоровье. - 2012. - №1. - С.118-124.
- McCagherty J, Yool DA, Paterson GK. Investigation of the in vitro antimicrobial activity of triclosan-coated suture material on bacteria commonly isolated from wounds in dogs. Am J Vet Res. 2020; 81(1): 84-90. DOI: 10.2460/ajvr.81.1.84 PMID: 31887087
- Патент РФ на изобретение №2338265. Блинков Ю.Ю., Липатов В.А., Суковатых Б.С., Ештокин С.А., Костин С.В., Беседин А. В., Окунев О.А., Ефременков А.М., Зайцев О.В., Ненахов А. А., Скориков Д. В., Стародубцева Е. В. Способ моделирования острого перитонита № 2007119763
- Патент РФ на изобретение № 2715922. Мосолова А.В., Суковатых Б.С., Затолокина М.А., Пашков В.М., Панкрушева Т.А., Чекмарёва М.С. Способ лечения распространенного перитонита № 2019124361.
- Данилова Т.А., Данилова Г.А., Аджиева А.А. Влияние мирамистина и фоспренила на микробные пленки // Бюллетень экспериментальной биологии и медицины. - 2017. - №163(4). - С. 435-439.


