Профилактика послеоперационных вентральных грыж и предикторы их образования
Автор: Федосеев А.В., Инютин А.С., Лебедев С.Н., Шкляр В.С.
Журнал: Хирургическая практика @spractice
Рубрика: Статьи
Статья в выпуске: 2 (42), 2020 года.
Бесплатный доступ
Вопрос прогнозирования и профилактики послеоперационных вентральных грыж является актуальным. Обследовано 450 больных для выявления и определения значимости факторов риска, а для оценки морфологии передней брюшной стенки 71 пациенту выполнена МРТ передней брюшной стенки. Выделены большие и малые предикторы грыжеобразования. МРТ позволила выявить дефекты апоневроза, не определяемые физикально, что является высоким риском формирования послеоперационных вентральных грыж. Основываясь на степени риска послеоперационных вентральных грыж, проведена их хирургическая профилактика. Пациентам группы низкого риска лапарорафию следует проводить шахматно-укрепляющим швом, при высоком риске - превентивное протезирование, а при его невозможности - лапарорафию с использованием нити из сетчатого полипропиленового имплантата по разработанной методике.
Лапаротомия, ушивание апоневроза, послеоперационная вентральная грыжа, превентивное протезирование, сетчатая нить, мрт передней брюшной стенки
Короткий адрес: https://sciup.org/142226489
IDR: 142226489 | УДК: 617.55-089.844 | DOI: 10.38181/2223-2427-2020-2-50-55
Prevention of postoperative ventral hernias and predictors of herniation
The issue of predicting and preventing postoperative ventral hernias is relevant. 450 patients were examined to identify and determine the significance of risk factors, and 71 patients underwent MRI of the anterior abdominal wall to assess the morphology of the anterior abdominal wall. Large and small predictors of herniation are identified. MRI revealed aponeurosis defects that are not physically determined, which is a high risk of postoperative ventral hernias. Based on the risk level of postoperative ventral hernias, their surgical prevention was performed. Patients at low risk should undergo laparorrhaphy with a staggered strengthening suture, at high risk - preventive using a mesh prosthesis, and if it is impossible - laparorrhaphy using a thread from a mesh polypropylene implant according to the developed technique.
Текст научной статьи Профилактика послеоперационных вентральных грыж и предикторы их образования
На сегодняшний день срединный лапаротомный доступ не уступает своих позиций, особенно в экстренной хирургии. Одним из осложнений операций, выполненных через указанный доступ, является послеоперационная вентральная грыжа (ПОВГ), частота которой варьируется от 2 до 33% [1,2,3,4]. ПОВГ является медицинской, социальной и экономической проблемой [3,5]. Риск возникновения послеоперационных вентральных грыж увеличивают такие факторы как ожирение, кахексия, женский пол, пожилой возраст, сахарный диабет, желтуха, аневризмы брюшной аорты, анемия, использование вазопрессорных препаратов, прием гормональных препаратов, курение, ХОБЛ, онкологические заболевания, доброкачественная гипертрофия предстательной железы, запоры и асцит [3,6,7,8]. Многие из факторов риска ПОВГ находятся вне контроля хирурга, в отличие от применяемой техники лапарорафии, значительно влияющей на появление подобного осложнения, о чем свидетельствует ряд рандомизированных исследований. [3,9,10]. В связи с этим, вопрос прогнозирования ПОВГ с выбором способа закрытия лапаротомной раны является актуальным [1,2,11,12]. Немаловажен и факт наличия возможных дефектов белой линии живота без клинических проявлений грыжи при отсутствии в анамнезе срединной лапаротомии, что нужно учитывать при выборе метода лапарорафии и требует проведения предоперационного инструментального обследования тканей передней брюшной стенки.
Цель исследования: выявление предикторов грыжеобра-зования у пациентов после выполнения срединной лапаротомии и улучшение результатов лечения данной категории больных путём уменьшения частоты эвентраций и ПОВГ.
Материалы и методы
Проведено обследование 450 больных, которым выполнялась срединная лапаротомия по поводу неотложной хирургической патологии. Проведен анализ порядка 45 потенциальных факторов риска формирования ПОВГ, среди которых вес, рост, индекс массы тела, наличие анатомо-функциональной недостаточности предней брюшной стенки, наличие признаков НДСТ с использованием критериев Смольновой Т.Ю.(2003), Т. Милковска-Дмитровой и А. Каркашева (1987), наличие в анамнезе тяжёлого физического труда, занятие силовыми видами спорта, показатели красной крови, уровень билирубина, креатинина, глюкозы крови, содержание белка в сыворотке сопутствующая патология, курение в анамнезе, основное заболевание, характер оперативного вмешательства и его длительность, наличие раневых инфекционных осложнений, наличие рубца в области оперативного доступа, способ закрытия лапаротом-ной раны, вид шовного материала, наличие перитонита, асцита, ношение бандажа в послеоперационном периоде. Через 1 год после операции пациенты обследованы на предмет наличия ПОВГ и дефектов апоневроза (физикально и по данным УЗИ).
Для оценки связи между конституциональными, возрастными факторами и морфологическим строением передней брюшной стенки проведено обследование 71 пациента, обратившегося для выполнения магнитно - резонансного исследования брюшной полости по поводу других, не связанных с патологией передней брюшной стенки, заболеваний. У лиц мужского пола распределение по возрасту составило: 11,7% -молодые; 35,3% - зрелые; 47% – пожилые. Женщины распределились следующим образом: 24% - молодые; 27,7% - зрелые; 42,6% - пожилые; 5,5% - лица старческого возраста. Определяли скрытые дефекты апоневроза, жировую инволюцию мышц, расширение пупочного кольца, диастаз прямых мышц.
На следующем этапе у пациентов высокого риска ПОВГ реализованы разработанные методы их хирургической профилактики: методику превентивного протезирования передней брюшной стенки (патент на изобретение № 2670684) и способ ушивания лапаротомной раны с применением сетчатой нити (патент на изобретение № 2714439).
Противопоказаниями к применению указанных методик являются: высокая вероятность релапаротомии (гнилостный перитонит, разлитой каловый перитонит, не устранённые внутрибрюшинные источники инфекции - инфильтраты, свищи, не устранённые источники кровотечения, требующие последующих ревизий); необходимость второго этапа; флегмона передней брюшной стенки; прорастание передней брюшной стенки опухолью, отказ пациента, а в случае превентивного протезирования и высокий анестезиологический риск, ввиду большей длительности реализации методики, в отличие от традиционной лапарорафии.
Выполнено 36 оперативных вмешательств у больных высокого риска ПОВГ: 20 (основная группа) – с применением превентивного эндопротезирования, заключающегося в имплантации сетчатого эндопротеза шириной 3 см. и длиной, соответствующей длине лапаротомии, в преперитонеальное пространство вдоль линии разреза срединного апоневроза и ушиванием последнего непрерывным швом с захватом сетчатого имплантата (12 больных) (Рис. 1).
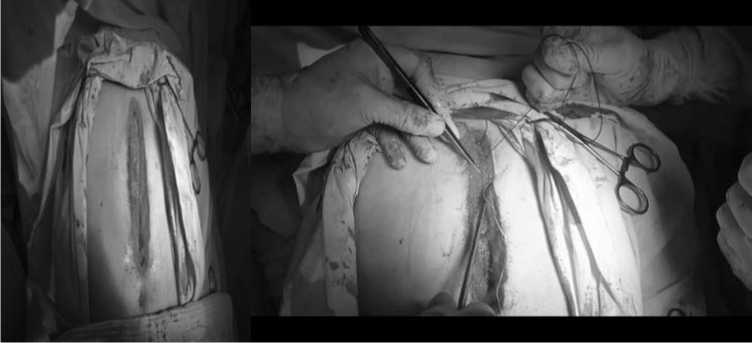
Рис. 1. Методика превентивного протезирования передней брюшной стенки. Слева - этап преперитонеального размещения сетчатого имплантата. Справа -последующее непрерывное ушивание белой линии живота.
В случае высокого анестезиологического риска (ASA >4 МНОАР-89 >5), технических трудностей при выполнении превентивного протезирования, в качестве альтернативы реализовывался способ ушивания лапаротомной раны с применением сетчатой нити (8 больных), ввиду меньшего времени и технической простоты исполнения методики. Способ основан на ушивании белой линии живота укрепляющими швами в местах наибольшего натяжения ее краев с последующим наложением непрерывного шва. В качестве материала для выполнения укрепляющих швов служит сетчатый эндопротез цилиндрической формы, получаемый путём растягивания за края полос сетчатого эндопротеза шириной 12 мм., длиной 15 см. на максимально возможную длину, фиксирующегося в открытом ушке режущей, изогнутой на 1/2 или 3/8 окружности, хирургической иглы с диаметром не менее 1мм. (Рис.2).
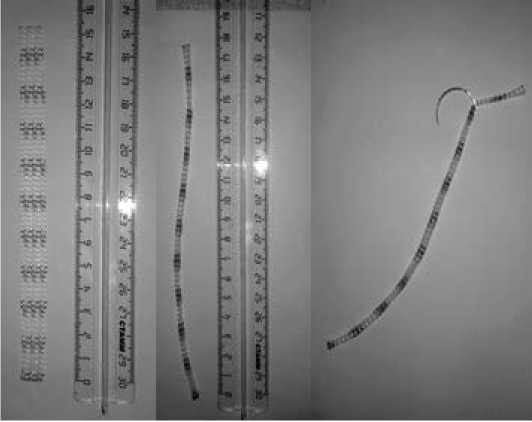
Рис. 2. Способ изготовления сетчатой нити.
Задачами сетчатой нити являются: создание основы для формирования прочного соединительнотканного рубца, повышение прочности шва апоневроза за счет обширного контакта используемой сетчатой нити с ушиваемыми тканями, снижение нагрузки на непрерывный шов.
Методика наложения шва заключается в том, что первый вкол иглы делается, отступив 1 см. от линии разреза белой линии живота снаружи внутрь, а выкол на противоположной вколу стороне белой линии живота в косом направлении на 1,5 см от края раны и в 1,5 см относительно уровня вко-ла, следующий вкол иглы выполняется на противоположной стороне белой линии живота на 1,5 см от края последней и на том же уровне, что и первый выкол иглы, а выкол производится на противоположной вколу стороне белой линии живота в косом направлении на 1 см от края раны на уровне первого вкола. Свободные концы сетчатых нитей завязываются на два узла, при этом лишние концы отрезаются в 2-3 мм. от второго узла и прошиваются проленовой нитью 2-0 (Рис. 3, 4).
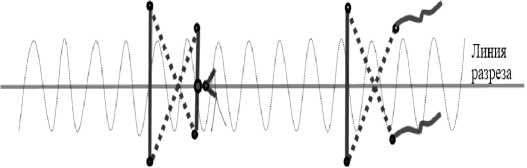
Рис. 3. Схема способа ушивания лапаротомной раны с применением сетчатой нити
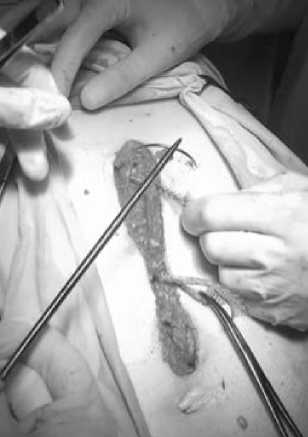
Рис. 4. Ушивание лапаротомной раны с применением сетчатой нити.
В группе сравнения у 16 больных с высоким риском гры-жеобразования лапарорафия проводилась по традиционной методике - отдельными узловыми швами.
Группы были сравнимы по типам и частоте применения той или иной разновидности срединной лапаротомии (tст= 0,73, p<0,05)., полу (tст=0,142; р=0,082), возрасту (tст -0,62 p<0,05), наличию сочетания нескольких факторов риска послеоперационного грыжеобразования. Показания к экстренному оперативному вмешательству через срединный доступ также значимых отличий не имели. Острая кишечная непроходимость в основной группе была диагностирована у восьми (40%) пациентов, в группе контроля – у пяти (31,2%), перфорация полого органа - у четырех (20%) пациентов основной группы и у трех (19%) - контрольной, воспалительно-деструктивные заболевания органов брюшной полости - у пяти (25%) и четырех (25 %) соответственно, желчекаменная болезнь, холедохолитиаз у трех (15%) пациентов основной группы и четырех (25%) контрольной.
В раннем и позднем послеоперационном периоде у пациентов основной и контрольной групп во время физикального и ультразвукового исследования оценивалась частота ране- вых осложнений, в том числе наличие эвентраций, послеопе-рационнных вентральных грыж.
При сравнении исследуемых групп применяли критерий Стьюдента (tСт). Для корреляционого анализа использовали линейную корреляцию Пирсона (r) и ранговую Спирмена (rСп). С целью проверки вероятности события использовали U-критерий Манна-Уитни. Достоверность результатов оценивали положительной при получении p<0,05.
Результаты. Частота формирования ПОВГ после срединных лапаротомий через 12-14 месяцев наблюдения составила 19% (85 случаев). С учетом силы корреляционной связи по методу Пирсона между фактом образования ПОВГ и значимыми факторами риска, были выделены «большие предикторы», сила связи которых составила 0,9 - 0,7 и «малые предикторы» - с силой связи от 0,7 до 0,5.
«Большими предикторами» являются возраст старше 60 лет, ожирение, верхнесрединный доступ, фибринозный, либо ограниченный гнойный перитонит, недифференцированная дисплазия соединительной ткани, возвращение к тяжёлому физическому труду.
«Малые предикторы»: возраст 44-59 лет, брахиморфный живот, повышенный уровень креатинина (110 мкмоль/л), повышенный уровень глюкозы крови (>7 ммоль/л), анемия IIIII ст., длительность операции более 120 мин.
Комбинация данных признаков даёт частоту грыжео-бразования в случае наличия двух «больших» предикторов в 65% (p<0,05), трёх «малых» - 75% (p<0,05), трёх «больших» -до 85% (p<0,05), в результате чего риск появления ПОВГ разделён на высокий (вероятность появления грыжи более 80%) и низкий (менее 80%).
При МРТ у 51 (41,4%) обследованных диагностировалась жировая инволюция мышц передней брюшной стенки, диастаз белой линии живота определялся у 31 (25,2%) больного, расширение пупочного кольца у 26 (21,1%) пациентов, а дефекты апоневроза белой линии, не определяемые при физикальном обследовании, в 15 (12,2%) случаях. Важен тот факт, что указанные изменения преобладали у лиц пожилого возраста, что объясняет сильную зависимость возраста старше 60 лет и риска грыжеобразования после срединной лапаротомии, а обнаружение дефектов апоневроза, являющимися по своей сути основой для формирования грыжи, не определяемыми при физикальном обследовании, указывает на «слабость» соединительнотканных структур, что следует отнести к высокому риску грыжеобразования.
В группе высокого риска грыжеобразования в 10 случаях превентивного эндопротезирования передней брюшной стенки (двое больных не обследовано по причине смерти) в течение 12 - 15 месяцев грыжевых выпячиваний, дефектов апоневроза выявлено не было. У пациентов, лапарорафия которым проводилась сетчатой нитью, грыжевых выпячиваний зафиксировано не было, но при УЗИ в одном случае диагностирован дефект апоневроза.
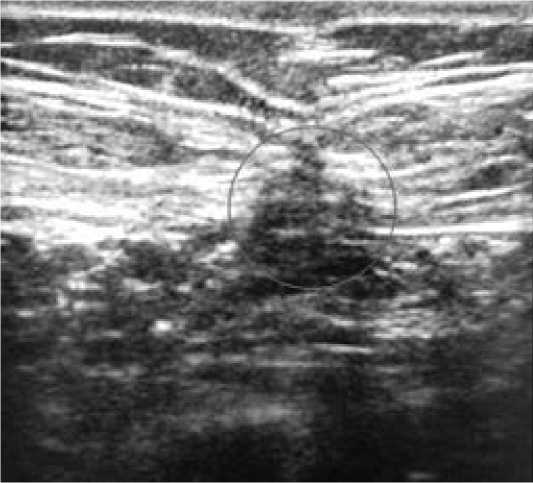
Рис. 5. Дефект рубца белой линии живота (УЗИ)
В контрольной группе грыжи зафиксированы у 8 (57%) из 14 человек (трое пациентов не обследованы по причине смерти). При превентивном протезировании серомы, потребовавшие дренирования под контролем ультразвука, диагностированы в трех случаях (1 типа по S. Morales-Conde 2012г.). У четырех пациентов серомы были клинически не значимыми (0 тип по S. Morales-Conde 2012г.) (Рис.5).
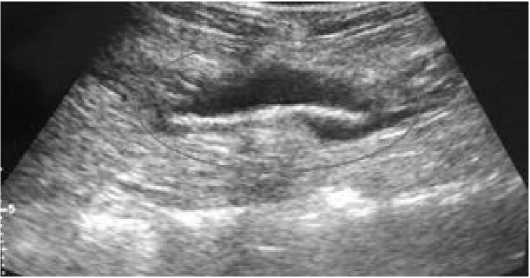
Рис. 6. Перипротезная серома (УЗИ)
У трех пациентов, первичное закрытие лапаротомной раны которым проводилось сетчатым швом и у трех с узловыми швами, выявлены клинически незначимые серомы (0 тип по S. Morales-Conde 2012г.). Нагноения послеоперационной раны, отторжения сетчатого имплантата зафиксировано не было. Частота формирования сером в основной группе была достоверно выше, чем в контрольной (p<0,05), но на результате лечения это не сказалось. Таким образом, оценка риска развития ПОВГ у пациентов перед лапаротомией позволяет провести хирургическую профилактику этого осложнения в случае высокой вероятности его появления.
Заключение
Для прогноза развития ПОВГ нужно учитывать несколько факторов их возникновения и в случае высокого риска применять превентивное протезирование, а при его невозможности - лапарорафию с использованием нити из сетчатого полипропиленового имплантата по разработанной методике.
МРТ позволяет выявить морфологические изменения передней брюшной стенки, что нужно учитывать при лапа-рорафии, применяя методики, способствующие формированию прочного рубца.
Список литературы Профилактика послеоперационных вентральных грыж и предикторы их образования
- Лебедев С.Н., Федосеев А.В., Инютин А.С., Муравьев С.Ю. Превентивное эндопротезирование при срединных лапаротомиях. Наука молодых (Eruditio Juvenium). 2018; 2(6):211-217.
- Федосеев А.В., Муравьев С.Ю., Бударев В.Н., Инютин А.С., Зацаринный В.В. Некоторые особенности белой линии живота, как предвестники послеоперационной грыжи. Российский медикобиологический вестник имени академика И.П. Павлова. 2016;1:109-115.
- J. Cornish1, R. L. Harries, D. Bosanquet, B. Rees, J. Ansell, N. Frewer, P. K. Dhruva Rao1, C. Parry, R. Ellis-Owen,S. M. Phillips, C. Morris, J. Horwood, M. L. Davies, M.M. Davies, R. Hargest, Z. Davies, J. Hilton, D. Harris,A. Ben-Sassi, R. Rajagopal, D. Hanratty, S. Islam, A. Watkins, N. Bashir, S. Jones, I. R. Russell,J. Torkington. Hughes Abdominal Repair Trial (HART) - Abdominal wall closure techniques to reduce the incidence of incisional hernias: study protocol for a randomized controlled trial Trials. 2016; 17:454 DOI: 10.1186/s13063-016-1573-0
- Skipworth JR, Khan Y, Motson RW, et al. Incisional hernia rates following laparoscopic colorectal resection. Int J Surg. 2010; 8(6):470-3.
- GH van Ramshorst, HH Eker, WC J Hop, J Jeekel, JF Lange. Impact of incisional hernia on health-related quality of life and body image: a prospective cohort study. Am J Surg. 2012; 204(2):144-50. DOI: 10.1016/j.amjsurg.2012.01.012
- Лаврешин П.М., Гобеджишвили В.К., Гобеджишвили В.В., Владимирова О.В., Юсупова Т.А. Прогнозирование развития первичных послеоперационных вентральных грыж. Современные проблемы науки и образования. 2015; 3. URL: http://www.science-education.ru/ru/article/view?id=18369 (дата обращения: 25.06.2020).
- Национальные клинические рекомендации по герниологии. Раздел "Послеоперационные вентральные грыжи" Российские клинические рекомендации по диагностике, лечению и профилактике венозных тромбоэмболических осложнений 2017 год. Краткое издание. М: Издательство Российского Общества Хирургов, Москва. 2017. 56 с.
- Горский В.А., Титков Б.Е., Агапов М.А., Азимов Р.Х., Сивков А.С., Глушков П.С. Профилактика образования грыж после лапароскопической холецистэктомии. Медицинский алфавит. 2018; 4(37): 33-33.
- Deerenberg EB, Harlaar JJ, Steyerberg EW, et al. Small bites versus large bites for closure of abdominal midline incisions (STITCH): a doubleblind, multicentre, randomised controlled trial. Lancet. 2015. Epub.
- DOI: 10.1016/S0140-6736(15)60459-7
- Rahbari NN, Knebel P, Kieser M, et al. Design and current status of CONTINT: continuous versus interrupted abdominal wall closure after emergency midline laparotomy - a randomized controlled multicenter trial. Trials. 2012;13:72.
- Кубышкин В.А., Галлямов Э.А., Агапов М.А., Какоткин В.В., Давлятов М.Р. Значение особенностей структуры и метаболизма внеклеточного матрикса в патогенезе грыж брюшной стенки. Обзор литературы. Хирургическая практика. 2020;(1):24-32.
- DOI: 10.38181/2223-2427-2020-1-24-32
- Amjad S., Zia A., Syed M. A., Salah G., Khalid A., Ahmed A., Rashad F., Abdulrahman A.A. Incisional Hernia Post Laparotomy-Incidence and Risk Factors. Journal of Surgery. 2018: 1(6): 19-22.
- DOI: 10.11648/j.js.20180601.14


