Прогностическая значимость оценки экспрессии иммуногистохимических маркеров и степени патоморфоза до и после лечения больных раком простаты высокого риска прогрессирования
Автор: Воронина Е.С., Фомкин Р.Н., Бучарская А.Б., Палатова Т.В., Попков В.М., Маслякова Г.Н.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Урология
Статья в выпуске: 2 т.15, 2019 года.
Бесплатный доступ
Цель: провести анализ экспрессии иммуногистохимических маркеров у пациентов с аденокарциномой простаты высокого риска прогрессирования до и после комбинированного и сочетанного лечения больных с уровнем простатического специфического антигена (ПСА) крови ниже дискриминационного. Материал и методы. Исследовали пациентов (n=80) с диагнозом «рак простаты высокого риска прогрессирования», с клинической стадией T3a, суммой баллов по шкале Глисона от 8 до 10, уровнем общего ПСА более 20 нг / мл. Пациентам 1-й группы (n=42) проведено только комбинированное хирургическое лечение в объеме ТУР и HIFU-аблации простаты; 2-й группе пациентов (n=38) дополнительно применена андрогенная депривация в адъювантном режиме. Результаты. ПСА крови, определяемый у пациентов после различных методов лечения, не всегда является объективным показателем его эффективности. Иммуногистохимические исследования ткани опухоли на пролиферативную активность опухолевых клеток, активацию в них апоптоза, а также оценки специфических онкомаркеров и генов супрессоров опухоли показали, что снижение экспрессии указанных маркеров у пациентов с показателями ПСА крови ниже дискриминационного наблюдается у всех больных независимо от вида лечения. Однако после лечения в 1-й группе пациентов, несмотря на достижение показателя ПСА уровня nadir, наблюдается снижение экспрессии маркера межклеточной адгезии Е-кадгерина, что свидетельствует о повышении риска метастазирования опухоли, а также увеличении экспрессии маркеров ингибитора апоптоза Всl-2 и андрогенов, что свидетельствует о возможности прогрессирования опухолевого роста. Заключение. Для более точной оценки лечебного патоморфоза у больных раком простаты высокого риска прогрессирования, которым проведена монотерапия методом HIFU-аблации, наряду с определением уровня ПСА крови, необходимо при контрольной биопсии простаты проведение иммуногистохимического исследования ткани опухоли для определения прогноза и риска развития рецидива.
Высокоинтенсивный сфокусированный ультразвук (hifu), иммуногистохимический анализ, патоморфоз, рак простаты
Короткий адрес: https://sciup.org/149135296
IDR: 149135296 | УДК: 616.65-002-006.6-085(045)
Prognostic significance of the assessment of the expression of immunohistochemical markers and the degree of pathomorphism before and after treatment of patients with prostate cancer at high risk of progression
Purpose: to analyze the expression of immunohistochemical markers in patients with prostate adenocarcinoma at high risk of progression before and after combined and combined treatment of patients with prostate specific antigen (PSA) level of blood below discriminatory. Material and methods. Examined patients (n = 80) with a diagnosis of “High-risk progression prostate cancer,” with clinical stage T3a, total score for Gleason scale from 8 to 10, the level of total PSA more than 20 ng / ml. Patients of the 1st group (n = 42) only combined surgical treatment in the scope of TUR and HIFU ablation the prostate; The 2nd group of patients (n = 38) additionally applied androgen deprivation in adjuvant mode. Results. Blood PSA, determined in patients after various methods of treatment is not always an objective indicator of its effectiveness. Immunohistochemical studies of tumor tissue for proliferative activity tumor cells, the activation of apoptosis in them, as well as the assessment of specific tumor markers and tumor suppressor genes showed that a decrease in the expression of these markers in patients with PSA values of blood lower than discriminatory observed in all patients independently on the type of treatment. However, after treatment in the 1st group of patients, despite the achievement PSA level of nadir, there is a decrease in the expression of an intercellular adhesion marker E-cadherin, which indicates an increased risk of tumor metastasis, as well as increased expression of markers of the apoptosis inhibitor Bcl-2 and androgens, which indicates about the possibility of progression of tumor growth. Conclusion For a more accurate assessment therapeutic pathomorphism in patients with prostate cancer at high risk of progression, which HIFU ablation monotherapy was carried out, along with the determination of blood PSA level, it is necessary during the control biopsy of the prostate immunohistochemical studies of tumor tissue to determine the prognosis and risk of relapse.
Текст научной статьи Прогностическая значимость оценки экспрессии иммуногистохимических маркеров и степени патоморфоза до и после лечения больных раком простаты высокого риска прогрессирования
-
1 Введение. Рак простаты (РП) является одной из наиболее актуальных проблем современной онкологии. По данным государственной медицинской статистики, распространенность РП в России неуклонно растет: с 478 случаев на 100 тыс. населения в 2006 г. до 1384 на 100 тыс. населения в 2016 г. [1]. На его долю приходится около 6% всех злокачественных новообразований. РП включает опухоли различной степени дифференцирования и агрессивности, что определяет прогноз заболевания. Тактика лечения определяется распространенностью опухолевого процесса и различными клиническими характеристиками заболевания, которые обусловливают риск прогрессирования онкологического процесса после радикального лечения [2, 3].
К радикальным методам лечения относят радикальную простатэктомию, лучевую терапию — дистанционную или брахитерапию, HIFU-аблацию простаты. Для оценки риска прогрессирования заболевания после проведенного радикального лечения существует несколько предикторных таблиц и номограмм. A. V. D»Amico и соавт. (1999) предложили характеристику риска прогрессирования заболевания в зависимости от основных клинических данных у больных РП после проведенной ЛТ [4]. Последующая валидация данной номограммы на подгруппах больных, перенесших хирургическое лечение, подтвердила ее прогностическую значимость [5].
Лечение больных группы высокого и очень высокого риска прогрессирования представляет определенную сложность [6, 7]. Группы высокого риска характеризуются более агрессивным течением заболевания и достоверно меньшими показателями безрецидивной, опухолеспецифической и общей выживаемости по сравнению с группами низкого и промежуточного риска. У такой категории пациентов риск развития биохимического рецидива, прогрессирования заболевания и смерти от РП значительно выше. Кроме того, в подгруппах высокого риска прогрессирования заболевания мультимодальная терапия с применением комбинации хирургического или лучевого методов и назначением гормональной терапии является основной терапевтической страте-
гией, поскольку приводит к достоверному улучшению показателей выживаемости больных [8].
В статье представлены результаты комбинированного и сочетанного лечения пациентов с высоким риском прогрессирования, которым выполнена комбинация трансуретральной резекции (ТУР) и высокоинтенсивной сфокусированной ультразвуковой аблации простаты (HIFU — High Intensity Focused Ultrasound) в сочетании и без сочетания с андрогенной депривацией.
Неоспоримым критерием оценки степени лечебного патоморфоза после воздействия на ткань простаты высокоинтенсивным сфокусированным ультразвуком является гистологический метод исследования. Известно, что морфологическими проявлениями патоморфоза служат повреждения паренхимы и стромы в виде дистрофии и некроза [9–11]. Однако нарушение метаболизма клеток может сочетаться с этими признаками и даже быть причиной указанных изменений, а не его проявлением. Поэтому для более объективной оценки лечебного патоморфоза в настоящее время используют иммуногистохимическое исследование. Иммуногистохимия является ценным дополнением к диагностике мельчайших очагов простатической карциномы и отличает ее от доброкачественных миметиков [12].
Цель: провести анализ экспрессии иммуногистохимических маркеров у пациентов с аденокарциномой простаты высокого риска прогрессирования до и после комбинированного и сочетанного лечения больных с уровнем простатического специфического антигена (ПСА) крови ниже дискриминационного.
Материал и методы. Исследование включало 80 пациентов в возрасте 73,5±1,2 года. У всех больных РП диагностирован при трансректальной биопсии, как минимум, из 12 точек. Выполнены магниторезонансная томография (МРТ) и остеосцинтиграфия для стадирования и исключения наличия метастазов в кости и лимфатических узлах. Критериями исключения являлись: ожидаемая продолжительность жизни менее пяти лет, высокий анестезиологический риск (American Society of Anesthesiologists class >3), Eastern Cooperative Oncology Group (ECOG) — статус (общее состояние) >2, наличие в настоящий момент или в анамнезе колоректального рака или воспалительных заболеваний прямой кишки, предшествующая ампутация прямой кишки, предшествующая брахитерапия, наличие ректальной фистулы в анамнезе.
Риск пациентов оценен согласно критериям D'Amico et al. (1999) и включал в себя дооперационный уровень общего ПСА, клиническую стадию и сумму баллов по шкале Глисона. К группе пациентов высокого риска были отнесены больные с клинической стадией T3a, суммой баллов по шкале Глисона от 8 до 10, уровнем общего ПСА более 20 нг/мл. Все пациенты были разделены на две группы, сопоставимые по исследуемым показателям. В 1-ю группу включены пациенты (n=42), которым проведено только комбинированное хирургическое лечение в объеме ТУР и HIFU-аблации простаты; во 2-ю группу — пациенты, которым применена сочетанная терапия в виде комбинированного хирургического лечения в объеме ТУР и HIFU-аблации простаты с назначением андрогенной депривации в адъювантом режиме (n=38).
В качестве андрогенной депривации применяли аналоги ЛГРГ в сочетании с периферическими блокаторами андрогеновых рецепторов. HIFU-аблация простаты проводилась на аппарате Ablatherm Integrated Imaging® (фирма-производитель EDAP TMS, Франция). Оценку и анализ лечебного патомор-фоза проводили через 2–18 месяцев после лечения. Для этого всем пациентам выполняли контрольную биопсию простаты, МРТ, ТРУЗИ, ЦДК, определяли уровень ПСА, однако в данной работе приводится только морфологическая оценка послеоперационных результатов лечения.
Иммуногистохимические исследования проводили с помощью стрептавидин-биотинового метода с использованием системы LSAB2 System, HRP (K0675) фирмы Dako, в качестве хромогена применяли диаминобензидин (Dako). Использовали следующие антитела: Monoclonal Mouse Anti-Human Androgen Receptor Clone AR 441, фирма Dako (разведение 1:50); Monoclonal Mouse Antibody-Human Vascular Endothelial Growth Factor (VEGF) CloneVG1, фирма Dako (разведение 1:50); Monoclonal Mouse Anti-Human Е-cadherin Clon NCH-38, фирма Dako (разведение 1:50); Monoclonal Mouse Anti-Human Ki-67 Antigen Clone MIB-1, фирма Dako (разведение 1:100); AMACR Rabbit Polyclonal Antibody RP 134 R, фирма Diagnoatic BioSystems (разведение 1:50); Monoclonal Mouse anti-Bcl-2 oncoprotein, фирма Dako (разведение 1:50); Monoclonal Mouse Anti-Human р53 Protein (клон D07, разведение 1:100), фирма Dako. Результаты экспрессии цитоплазматических и мембранных маркеров (AMACR, Вcl-2, Ecad, VEGF) оценивали полуколичественным методом по шкале от 0 до 3, с учетом выраженности реакции: 0 — отсутствие реакции, 1 — слабая реакция, 2 — умеренная реакция, 3 — выраженная реакция маркера. Результаты с ядерным антигеном (Andr и р53, Ki-67) оценивали по подсчету histochemical score (Hs): Hs =∑ P ( i ) * i , где i — интенсивность окрашивания, выраженная в баллах от 0 до 3; P ( i ) — процент окрашенных клеток.
Обработку данных осуществляли при помощи пакета программ статистической обработки результатов SSPS 13.0 for Windows. Тестирование полученных данных на нормальность распределения проводили тестом Колмогорова — Смирнова. При анализе результатов иммуногистохимической экспрессии для определения значимости различий между двумя зависимыми выборками (до и после лечения) использовали Т-критерий Вилкоксона. Значимость различия принималась при Т≤0,01.
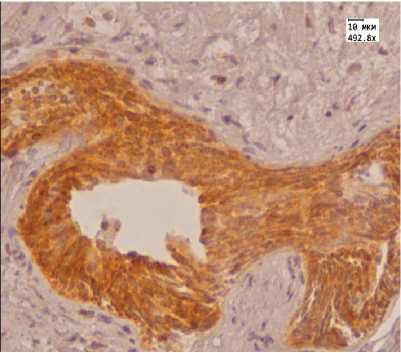
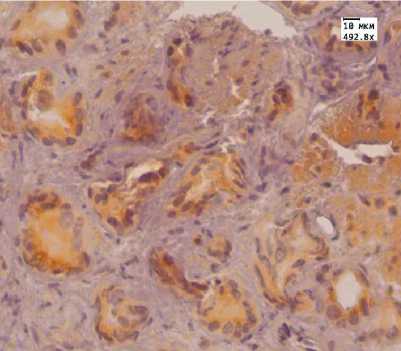
Результаты. При иммуногистохимическом исследовании с антителами к онкомаркеру альфа-ме-тилацил-КоА-рацемазе (AMACR) до лечения в обеих группах пациентов наблюдали выраженную и умеренную цитоплазматическую экспрессию данного маркера в виде мелких зерен коричневого цвета. Слабой и отрицательной экспрессии не было. После лечения у пациентов 1-й группы экспрессия данного маркера в простате у 27,5% пациентов оставалась на высоком уровне, у 47,5% она была слабой и отрицательной (рисунок: А, Б).
После лечения у пациентов 2-й группы экспрессия данного маркера снижалась: у 5% пациентов экспрессия оставалась на высоком уровне, у 57,5% пациентов была слабой. При статистическом анализе полученных данных с помощью Т-критерия Вил-коксона полученное эмпирическое значение T находилось в зоне значимости. Таким образом, различия в уровнях выборок существенные (таблица).
Для оценки пролиферативной активности, определения степени злокачественности аденокарциномы использовали маркер Ki-67. До лечения в обеих группах пациентов в аденокарциноме пролиферативная активность опухолевых клеток у 90% пациентов была умеренной и сильной. Слабая реакция была лишь у 2,5% пациентов, отрицательной реакции не было. Показатели гистосчета находились в пределах Hs= от 140 до 270 (медиана 180). После лечения у пациентов 1-й группы показатели гистосчета снижались: Hs= от 0 до 160 (медиана 45). Сильной реакции у пациентов не наблюдалось, у 75% пациентов экспрессия данного ядерного маркера была отрицательной и слабой. Сравнивая показатели групп до и после лечения по критерию Вилкоксона, установили, что полученное эмпирическое значение T находится в зоне значимости. После лечения у 67,5% пациентов 2-й группы преобладала слабая реакция: Hs= от 0 до 100 (медиана 30), у 25% реакция была отрицательной. Сравнивая показатели групп до и после лечения по критерию Вилкоксона, мы также получили существенные различия.
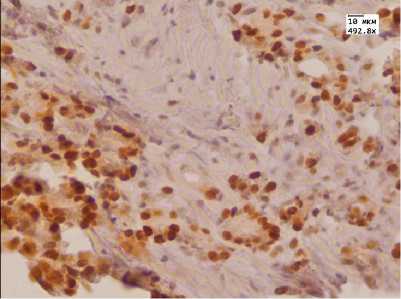
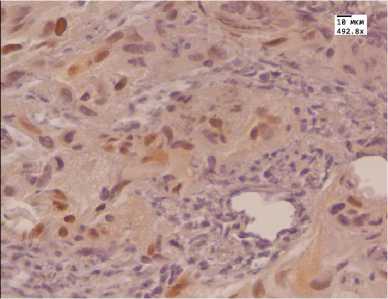
Ядерная экспрессия антител к рецепторам андрогенов на исходном этапе у 70% пациентов в обеих группах была выраженной (медиана Hs=190). У 30% пациентов отмечалась умеренная и слабая экспрессия данного маркера, показатели гистосчета у 68 % пациентов были выше 100 (медиана Hs=138). Количество рецепторов к андрогенам после лечения у пациентов 1-й группы оставалось на достаточно высоком уровне (медиана Hs=145). У 57,5% реакция была выраженной, у 25% пациентов умеренной. Критерий Вилкоксона не показал существенных различий между группами. После лечения у пациентов 2-й группы экспрессия маркера к рецепторам андрогенов заметно снижалась и у 82,5% пациентов была слабой и отрицательной (рисунок: В, Г). При статистическом анализе полученное эмпирическое значение T находится в зоне значимости, различия в уровнях выборок до и после лечения можно считать существенными.
При анализе экспрессии цитоплазматического и мембранного иммуногистохимического маркера Всl-2 до лечения в обеих группах мы получили следующие результаты: у 60% пациентов была выраженная экспрессия данного маркера, у 30% умеренная.
После лечения в 1-й группе у 77,5% пациентов экспрессия данного маркера была выраженной, у остальных пациентов умеренной. При статистической обработке данных групп мы не получили существенных различий между ними. После лечения у 50% пациентов 2-й группы экспрессия снижалась и становилась слабой, а у 12,5% она была от-
А
Б
В
Г
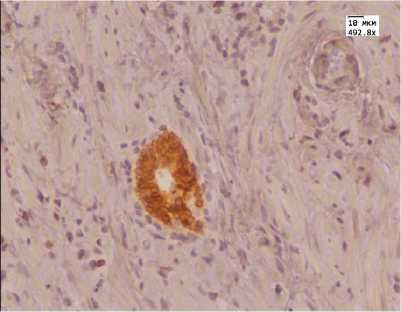
Д
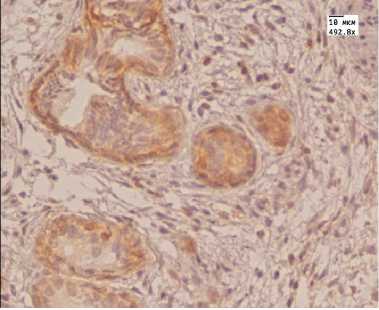
Е
Аденокарцинома простаты (Ув. 492,8): А — иммуногистохимическая реакция с антителом к AMACR до лечения HIFU-аблацией; Б — иммуногистохимическая реакция с антителом к AMACR после лечения HIFU-аблацией; В — иммуногистохимическая реакция с антителом Androgen до лечения МАБ; Г — иммуногистохимическая реакция с антителом Androgen после лечения МАБ; Д — иммуногистохимическая реакция с антителом к Bcl-2 до лечения МАБ; Е — иммуногистохимическая реакция с антителом к Bcl-2 после лечения МАБ
Экспрессия иммуногистохимических маркеров до и после лечения
|
Интенсивность экспрессии |
До лечения пациентов, % |
После лечения пациентов, % |
||
|
AMACR |
||||
|
1-я группа* |
2-я группа* |
1-я группа* |
2-я группа* |
|
|
+++ |
32,5 |
30 |
27,5 |
5 |
|
++ |
67,5 |
70 |
25 |
37,5 |
|
+ |
0 |
0 |
25 |
57,5 |
|
Отрицательная |
0 |
0 |
22,5 |
0 |
Окончание таблицы
Мембранная экспрессия антитела к Е-кадгерину до лечения у большинства пациентов (82,5%) обеих групп была выраженной и умеренной. После лечения у пациентов 1-й группы экспрессия данного маркера снижалась: лишь у 20% пациентов оставалась выра- женной, у 49% пациентов была отрицательной и слабой. При статистическом анализе Т-критерия полученное эмпирическое значение находится в зоне значимости, различия в уровнях выборок можно считать существенными. После лечения у пациентов 2-й группы экспрессия данного маркера снижалась незначительно, у 57,5% пациентов оставалась выраженной, у 17,5% умеренной, у 25% слабой и отрицательной. В результате сравнительного статистического анализа различия в уровнях выборок до и после лечения были несущественными.
При сравнительном изучении экспрессии антитела к васкулоэндотелиальному фактору роста (VEGF) у большинства пациентов экспрессия до лечения была умеренной и слабой (82%). После лечения у пациентов 1-й группы экспрессия VEGF немного снижалась, но по-прежнему преобладали пациенты с умеренной и слабой экспрессией (67,5%). После лечения у пациентов 2-й группы в 80% случаев экспрессия была слабой и умеренной. При обоих методах лечения различия в группах были статистически не значимы.
При анализе ядерной экспрессии маркера регуляции клеточного цикла р53 в группе пациентов до терапии показатели гистосчета у 79% пациентов показали выраженную реакцию, у 17,5% пациентов умеренную, у 12,5% слабую и отрицательную. После лечения у пациентов 1-й группы ядерная экспрессия данного маркера заметно снижалась, и лишь у 10% гистосчет показал выраженную реакцию, а у 75% пациентов реакция была отрицательной и слабой. При статистическом анализе теста Вилкоксона полученное эмпирическое значение T находилось в зоне значимости, различия в уровнях выборок до и после лечения можно считать существенными. После лечения у пациентов 2-й группы ядерная экспрессия данного маркера снижалась, и лишь у 5% гистосчет показал выраженную реакцию, а у 75% пациентов реакция с данным маркером была слабая или отрицательная. При статистическом сравнении этих групп полученное эмпирическое значение T находилось в зоне значимости, различия в уровнях выборок до и после лечения можно считать существенными.
Обсуждение. Уровень сывороточного ПСА является важнейшим признаком, позволяющим судить об эффективности лечения и о рецидивах опухоли [13]. В нашем исследовании у пациентов 1-й группы после лечения уровень ПСА крови снижался ниже дискриминационного уровня и в тканях простаты существенно снижалась экспрессия онкомаркера AMACR, маркера пролиферации Ki-67, маркера регуляции клеточного цикла р53, маркера клеточной адгезии Е-кадгерина. У пациентов 2-й группы после лечения уровень ПСА крови также снижался ниже дискриминационного уровня, и в простатической ткани существенно снижалась экспрессия онкомаркера AMACR, маркера пролиферации Ki-67, маркера регуляции клеточного цикла р53, маркера рецепторов к андрогенам и маркера апоптоза Вcl-2.
Таким образом, три иммуногистохимических маркера независимо от способа лечения аденокарциномы существенно снижаются при нормальных показателях ПСА. Значение онкомаркера AMACR и маркера пролиферации Ki-67 в диагностике и оценке лечебного патоморфоза признают и другие авторы [14–16]. Значение маркера регуляции клеточного цикла в оценке результатов лечения РП, по данным литературы, спорно [17, 18]. Однако в нашем исследовании у пациентов после лечения с уровнем ПСА ниже дискриминационного было существенное снижение экспрессии данного маркера в обеих группах. После лечения РП в обеих группах у пациентов снижалась и экспрессия Е-кадгерина, маркера межклеточной адгезии. Вероятно, это связано со специфическим воздействием высокоинтенсивного ультразвука на межклеточные адгезивные связи, так как в работах других авторов до лечения не выявлено корреляции уровня ПСА с экспрессией Е-кадгерина [19]. После проведенного лечения у пациентов 2-й группы в ядрах опухолевых клеток также существенно снижалась экспрессия антитела к рецепторам андрогенов, экспрессия Вcl-2, который повышает выживаемость опухолевых клеток и способствует опухолевой прогрессии, ингибируя апоптоз. VEGF (васкулоэндо-телиальный фактор роста) повышает способность эндотелиальных клеток к миграции, а опухолевых клеток к инвазии и метастазированию. В группах пациентов после лечения снижение экспрессии данного маркера были несущественными. Данные результаты совпадают с выводами других авторов, которые указывают, что экспрессия данного маркера не выявила статистически значимой прогнозирующей ценности при РП [20].
Заключение. Исследование показало, что ПСА крови, определяемое у пациентов с ацинарной аденокарциномой простаты после различных методов лечения, не всегда является объективным показателем его эффективности. Проведенное после лечения иммуногистохимическое исследование ткани опухоли на пролиферативную активность опухолевых клеток, активацию в них апоптоза, а также оценки специфических онкомаркеров и генов супрессоров опухоли показали, что снижение экспрессии всех указанных маркеров у пациентов с показателями ПСА крови ниже дискриминационного наблюдается у всех больных независимо от вида лечения. Однако после лечения в 1-й группе пациентов, несмотря на достижение показателя ПСА уровня nadir, наблюдается снижение экспрессии маркера межклеточной адгезии Е-кадгерина, что свидетельствует о повышении риска метастазирования опухоли, а также увеличении экспрессии маркеров ингибитора апоптоза Всl-2 и андрогенов, что свидетельствует о возможности прогрессирования опухолевого роста. Таким образом, для более точной и комплексной оценки лечебного патоморфоза у больных раком простаты высокого риска прогрессирования, которым проведена монотерапия методом HIFU-аблации, наряду с определением уровня ПСА крови, необходимо при контрольной биопсии простаты проведение иммуногистохимического исследования ткани опухоли для определения прогноза и риска развития рецидива.
Список литературы Прогностическая значимость оценки экспрессии иммуногистохимических маркеров и степени патоморфоза до и после лечения больных раком простаты высокого риска прогрессирования
- Русаков И. Г., Мишуткин С. В. Рак предстательной железы: тенденции и перспективы. Медицинский совет 2017; 14: 78-81
- Каприн А. Д., Троянов А. В., Иванов С. А., Карякин О. Б. Комплексное гормонохимиолучевое лечение больных неметастатическим раком предстательной железы группы высокого и очень высокого риска прогрессирования. Онкоурология 2017; 13 (1): 101-11
- Фомкин Р. Н., Глыбочко П. В., Попков В. М., Блюмберг Б. И. Лечение рака простаты у больных пожилого и старческого возраста высокоинтенсивным сфокусированным ультразвуком. Клиническая геронтология 2011; 17 (9-10): 27-33
- D'Amico AV, Whittington R, Malkowicz SB, et al. Pretreatment nomogram for prostate-specifc antigen recurrence after radical prostatectomy or external-beam radiation therapy for clinically localized prostate cancer. J Clin Oncol 1999; 17 (1): 168-72
- Heidenreich A, Bastian PJ, Bellmunt J, et al. Guidelines on Prostate Cancer. European Association of Urology, 2012
- Shao YH, Demissie K, Shih W, et al. Contemporary risk profle of prostate cancer in the United States. J Natl Cancer Inst 2009; 101 (18): 1280-3
- Фомкин Р. Н., Попков В. М., Блюмберг Б. И., Бромберг Б. Б. Эффективность высокоинтенсивной сфокусированной ультразвуковой абляции в лечении рака простаты высокой степени онкологического риска. Вестник Российской военно-медицинской академии 2013; 44 (4): 55-60
- Нюшко К. М., Алексеев Б. Я., Крашенинников А. А., Каприн А. Д. Хирургическое лечение больных раком предстательной железы с высоким риском прогрессирования. Онкоурология 2014; 10 (2): 38-45
- Бирманн К., Белтран А. Л. и др. Гистопатологические результаты после лечения рака предстательной железы использованием высокой интенсивности сфокусированного ультразвука (HIFU). Простата 2010; 11: 1196-200
- Фомкин Р. Н., Воронина Е. С., Попков В. М. и др. Патоморфоз рака предстательной железы при лечении высокоинтенсивным сфокусированным ультразвуком (HIFU). Онкоурология 2013; 1: 55-62
- Фомкин Р.Н., Воронина Е. С., Попков В. М., и др. Прогностическое значение молекулярно-биологических, морфологических и клинических маркеров в оценке эффективности лечения локализованного рака предстательной железы высокоинтенсивным сфокусированным ультразвуком. Экспериментальная и клиническая урология 2013; 4: 29-33
- Anand ODE, Satyanarayana RP, Kumar CK, Bhaskar RV. Diagnostic Utility of Immunohistochemical Markers in Prostate Cancer. Journal of Dental and Medical Sciences (IOSR-JDMS) 2017; 16 (3): 22-8
- Курзанов А. Н., Стрыгина Е. А., Медведев В. Л. Диагностические и прогностические маркеры рака предстательной железы. Современные проблемы науки и образования 2016; 2 URL: http://www.science- education.ru / ru / article / view? id=24439
- Paner GP, Luthringer DJ, Amin MB. Best practice in diagnostic immunohistochemistry: prostate carcinoma and its mimics in needle core biopsies. Arch Pathol Lab Med 2008; 132 (9): 1388-96. 10.1043 / 1543-2165 (2008)
- DOI: 10.1043/1543-2165(2008)
- Hameed O, Humphrey PA. Immunohistochemistry in diagnostic surgical pathology of the prostate. Semin Diagn Pathol 2005; 22 (1): 88-104
- Gobbo AD, Pellegrinelli A, Gaudioso G, et al. Analysis of NSCLC tumour heterogeneity, proliferative and 18F-FDG PET indices reveals Ki67 prognostic role in adenocarcinomas. Histopathology 2016; 68 (5): 746-51
- Saito H, Kitagawa K, Yoneda T, et al. Combination of p53-DC vaccine and rAd-p53 gene therapy induced CTLs cytotoxic against p53-deleted human prostate cancer cells in vitro. Cancer Gene Therapy 2017; 24: 289-96
- Gobbo AD, Ferrero S. Immunohistochemical Markers as Predictors of Histopathologic Response and Prognosis in Rectal Cancer Treated with Preoperative Adjuvant Therapy. Gastroenterology Research and Practice 2017; 2017: 2808235
- Hsu Y-S, Wang JS, Wu TT. E-Cadherin Expression in Prostate Adenocarcinomas in Chinese and Its Pathological Correlates. Urol Int 2004; 73: 36-40
- Liu Z-Q, Fang J-M, Xiao Y-Y, et al. Prognostic role of vascular endothelial growth factor in prostate cancer: a systematic review and meta-analysis. Int J Clin Exp Med 2015; 8 (2): 2289-98.


