Прогностическое значение показателей вариабельности сердечного ритма у больных хронической сердечной недостаточностью (трехлетнее наблюдение)
Автор: Кошелева Наталья Анатольевна
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Внутренние болезни
Статья в выпуске: 4 т.7, 2011 года.
Бесплатный доступ
Цель: оценить прогностическое значение показателей вариабельности сердечного ритма (ВСР) у больных с хронической сердечной недостаточностью (ХСН) в течение трех лет. Материал и методы. В исследование включены 110 пациентов, перенесших Q-инфаркт миокарда и имеющих симптомы ХСН. Средний возраст больных 55,2±6,5 года. Анализ ВСР выполнялся по результатам 5-минутных записей. Статистическая обработка полученных данных проводилась с использованием пакета программ Statistics 8.0. Результаты. В течение трех лет наблюдения у пациентов развилось 50 случаев сердечно-сосудистых осложнений: в 22 случаях было ухудшение ХСН, у 13 больных — повторный инфаркт миокарда, 15 пациентов умерли. Установлено, что при уровне низкочастотного спектра ВСР менее 5,2 In мс2 вероятность декомпенсации ХСН (р=0,048), летального исхода (р=0,02) выше, чем при большем значении этого показателя. Независимыми предикторами летального исхода у больных ХСН в течение трех лет являются фракция выброса левого желудочка, мочевая кислота, N-терминальный фрагмент мозгового натрийуретического пептида и низкочастотный компонент спектра ВСР Выводы. Разработанный алгоритм, оценивающий индивидуальный риск развития летального исхода у больного с ХСН в течение трех лет, позволит улучшить тактику ведения и прогноз у этой категории пациентов
Вариабельность сердечного ритма, хроническая сердечная недостаточность
Короткий адрес: https://sciup.org/14917421
IDR: 14917421
Текст научной статьи Прогностическое значение показателей вариабельности сердечного ритма у больных хронической сердечной недостаточностью (трехлетнее наблюдение)
Адрес: 410012, г. Саратов, ул. Большая Казачья, 112.
Тел.: 89172127708, (8452) 51-49-60.
дисфункции эндотелия, спазму коронарных артерий и снижению порога фибрилляции желудочков [4]. Одновременно с этим в последнее время растет интерес к неинвазивным методам оценки состояния автономной нервной системы, наибольшее распространение из которых получили методы оценки вариабельности сердечного ритма (ВСР) [5]. Анализ ВСР на коротких участках ЭКГ привлекает простотой и возможностью стандартизации условий определения. Существуют доказательства связи низкой ВСР на коротких участках ЭКГ с неблагоприятным прогнозом после инфаркта миокарда, в том числе и внезапной сердечной смертью (ВСС) [6]. Целью исследования стала оценка прогностического значения вариабельности сердечного ритма у больных хронической сердечной недостаточностью в течение трех лет наблюдения.
Методы. В открытое исследование были включены 110 пациентов (95 мужчин и 15 женщин) в возрасте от 46 до 70 лет (средний возраст 55,2±6,5 года), перенесших инфаркт миокарда с зубцом Q на ЭКГ, имеющие проявления ХСН, и 40 практически здоровых лиц (группа контроля). Из исследования исключались пациенты с нестабильной стенокардией и инфарктом миокарда в течение последних трех месяцев, выраженной печеночной и почечной недостаточностью, нарушениями ритма и проводимости. ВСР изучалась с использованием электрокардиографического аппаратно-программного комплекса «Волго-тех». Согласно протоколу исследования, в утренние часы после 5-минутного отдыха, в положении лежа, у больного производилась запись ЭКГ. Длительность регистрации ЭКГ составляла 5 минут. Методика регистрации и компьютерного анализа ВСР выполнялась в соответствии с принятыми международными стандартами [7].
Исследование вариабельности сердечного ритма осуществлялось во временной и спектральной (частотной) областях. Временные показатели включали: RR ср., мс — средняя длительность интервалов RR в течение 5 мин; RR max, мс — максимальная длительность интервалов NN в течение 5 мин; RR min, мс — минимальная длительность интервалов NN в течение 5 мин; SDNN, мс — стандартное отклонение средних значений интервалов NN; RMSSD, мс — квадратный корень из средней суммы квадратов разностей между соседними интервалами NN; pNN50, % — доля соседних интервалов NN, различающихся более чем на 50 мс. В спектральной области оценивали: TP, мс 2 — общую мощность всех интервалов RR (0,003–0,40 Гц); LF, мс 2 — мощность в диапазоне низких частот (0,04–0,15 Гц); HF, мс 2 — мощность в диапазоне высоких частот (0,15–0,40 Гц); LF / HF — отношение низкочастотной к высокочастотной составляющей спектра.
Кроме оценки функции вегетативной нервной системы (по результатам показателей ВСР), всем больным проводились общеклиническое обследование, включающее измерение АД, подсчет ЧСС, определение индекса массы тела (ИМТ), проба с дистанционной ходьбой в течение 6 мин [8]. Эхокардиография выполнялась на комплексе Acuson 128 XP / 10. Высокочувствительный С-реактивный белок (ВчСРБ) определяли с помощью реактивов фирмы Diasys (Германия). Уровень NТ-proBNP определяли иммуно- ферментным методом с помощью реактивов фирмы Biomedica (Словакия).
Все больные наблюдались в течение трех лет. За это время фиксировались следующие конечные точки: ухудшение ХСН, потребовавшее госпитализации, развитие нестабильной стенокардии и инфаркта миокарда, летальный исход, общее количество ССО.
Статистическая обработка полученных данных проводилась с использованием пакета программ Sta-tistica 8.0. Для сравнения средних величин, имеющих нормальное распределение, использовался t-тест, значения представлены в виде M±SD. В случаях, когда распределение существенно отличалось от нормального, анализу предшествовала логарифмическая трансформация данных. При непараметрическом распределении данных значения переменных представлялись в виде Ме [10%; 90%], сравнение средних величин проводили с помощью критерия Манна — Уитни. Для оценки взаимосвязи между отдельными показателями использовался корреляционный анализ Пирсона и Спирмена. Для определения влияния изучаемых параметров на развитие неблагоприятных исходов были построены кривые времени наступления неблагоприятных событий (Каплана — Мейера) с анализом достоверности различий про помощи теста Log-rank. Многофакторный анализ проводили с использованием логистической регрессии. Статистически значимыми считали различия при p<0,05.
Результаты . Больные с ХСН и лица группы контроля были сопоставимы по полу (86 и 85% мужчин было в каждой группе), по возрасту, уровню систолического и диастолического АД (табл. 1).
Таблица 1
Клинические параметры и показатели вариабельности сердечного ритма у больных ХСН и лиц контрольной группы, M±SD и Me [10%; 90%]
|
Клинический параметр |
Больные ХСН (n=110) |
Контроль (n=40) |
|
Пол (мужчины), абс. число, (%) |
95 (86%) |
34 (85%) |
|
Возраст, годы |
55,2 ± 6,5 |
52,2 ± 8,2 |
|
Систолическое АД, мм рт. ст. |
125,8 ± 18,1 |
123,4 ± 7,7 |
|
Диастолическое АД, мм рт. ст. |
76,3 ± 14,5 |
72,2 ± 8,4 |
|
ЧСС, уд. в мин |
65,7 ± 10,5** |
71,3 ± 7,3 |
|
Показатели ВСР |
||
|
RR ср., мс |
934,5 [750,6; 1118,0]** |
843,4 [788,0; 976,4] |
|
RR max, мс |
1142,5 [875,0; 1674,5]** |
980,0 [930,0; 1327,0] |
|
RR min, мс |
566,0 [233,0; 956,0] |
650,0 [244,4; 730,0] |
|
SDNN, мс |
51,0 [20,4; 146,0] |
50,2 [31,1; 147,8] |
|
RMSSD, мс |
54,5 [10,5; 240,0] |
44,84 [23,3; 136,4] |
|
pNN50, % |
4,0 [0,0; 32,5] |
6,0 [1,0; 26,0] |
|
TP, мс2 |
1044,5 [281,0; 2577,0]** |
1698,0 [660,0; 3925,0] |
|
LF, мс2 |
191,0 [53,0; 597,0]** |
536,0 [135,0; 1265,0] |
|
HF, мс2 |
139,5 [25,0; 537,0]** |
307,5 [88,0; 1063,0] |
|
LF/HF |
1,30 [0,40; 3,40]* |
1,77 [0,66; 4,21] |
|
Терапия |
||
|
Ингибиторы АПФ, (АРА II), % |
81 |
|
|
ß - блокаторы, % |
82 |
|
|
Ивабрадин, % |
36 |
Окончание табл. 1
|
Клинический параметр |
Больные ХСН (n=110) |
Контроль (n=40) |
|
Спиронолактон, % |
68 |
|
|
Диуретики, % |
18 |
|
|
Статины, % |
60 |
П р и м еч а н и е : * – различия достоверны с уровнем значимости p<0,01, ** – различия достоверны с уровнем значимости p<0,001.
ЧСС у пациентов с ХСН было ниже, чем у здоровых лиц, что можно объяснить приемом ß-блокаторов и ивабрадина. Наибольшие изменения ВСР у больных ХСН выявлены в спектральной области. Установлено снижение общей мощности интервалов RR, низкочастотной и высокочастотной составляющей спектра, их соотношения у больных ХСН по сравнению со здоровыми лицами.
Проведен корреляционный анализ показателей ВСР и исследуемых клинических параметров. Выявлена умеренная обратная взаимосвязь между LF спектра и возрастом (r=–0,35, р<0,001), ЧСС (r=– 0,30, р=0,02), NT-proBNP (r=–0,37, р<0,001), ВчСРБ (r=0,30, р=0,03), СДЛА (r=–0,30, р=0,004), приемом петлевых диуретиков (r=–0,37, р<0,001), умеренная положительная взаимосвязь между LF спектра и ФВ ЛЖ (r=0,31, р=0,002). Установлена умеренная обратная взаимосвязь между высокочастотным компонентом спектра и интенсивностью курения (r=–0,30, р=0,03). Курение, снижая парасимпатическую актив- ность, уменьшает вагусное действие в профилактике развития тахиаритмий.
В течение трех лет наблюдения обследованы 88 больных ХСН. Контакт с остальными больными ХСН был утерян. Определено, что у обследуемых пациентов с ХСН развилось 50 случаев ССО, в 22 случаях было ухудшение ХСН, у 13 больных — повторный инфаркт миокарда, 15 пациентов умерли. Учитывая, что распределение параметров ВСР существенно отличается от нормального, дальнейшему анализу предшествовала логарифмическая трансформация данных, позволившая применить методы параметрической статистики.
Показатели вариабельности сердечного ритма в зависимости от развития или отсутствия повторного инфаркта миокарда в течение трех лет у больных ХСН представлены в табл. 2.
Выявлено, что у больных ХСН с развившимся инфарктом миокарда (13 пациентов) в течение трех лет наблюдения ЧСС выше, а низкочастотный и высокочастотный компоненты спектра были ниже, чем у па-
Таблица 2
Показатели вариабельности сердечного ритма в зависимости от развития или отсутствия повторного инфаркта миокарда у больных ХСН, М±SD
|
Показатель ВСР |
Инфаркт миокарда (n=13) |
Без инфаркта миокарда (n= 5) |
р |
|
ЧСС, уд. в мин |
75,7±15,5 |
65,3±10,1 |
0,03 |
|
RR ср., ln мс |
6,70±0,21 |
6,83±0,16 |
0,08 |
|
SDNN, ln мс |
3,66±0,68 |
3,92 ± 0,72 |
0,44 |
|
RMSSD, ln мс |
3,77±1,20 |
3,85±1,09 |
0,86 |
|
pNN50, ln % |
1,06±0,54 |
1,87±0,95 |
0,24 |
|
TP, ln мс2 |
6,39±1,06 |
6,82±0,80 |
0,22 |
|
LF, ln мс2 |
4,15±1,3 |
5,23±0,95 |
0,01 |
|
HF, ln мс2 |
3,59±1,82 |
4,86±1,15 |
0,02 |
|
LF/HF |
1,22±0,30 |
1,11±0,22 |
0,29 |
Таблица 3
Показатели вариабельности сердечного ритма в зависимости от развития или отсутствия летального исхода у больных ХСН, М±SD
|
Показатель ВСР |
Летальный исход (n=15) |
Без летального исхода (n=73) |
р |
|
ЧСС, уд. в мин |
72,5±10,2 |
65,2±10,1 |
0,05 |
|
RR ср., ln мс |
6,74±0,18 |
6,83±0,16 |
0,13 |
|
SDNN, ln мс |
3,94±0,77 |
3,91±0,71 |
0,88 |
|
RMSSD, ln мс |
3,97±1,29 |
3,85±1,08 |
0,75 |
|
pNN50, ln% |
1,77±0,84 |
1,83±0,94 |
0,51 |
|
TP, ln мс2 |
6,44±0,85 |
6,83±0,82 |
0,18 |
|
LF, ln мс2 |
4,08±0,81 |
5,28±0,95 |
0,001 |
|
HF, ln мс2 |
3,67±1,39 |
4,88±1,17 |
0,01 |
|
LF/HF |
1,16±0,29 |
1,11±0,22 |
0,59 |
Таблица 4
Клинические параметры в зависимости от уровня низкочастотного компонента спектра ВСР у больных ХСН, М±SD
Определено, что у больных с летальным исходом (15 пациентов) в течение трех лет наблюдения ЧСС выше, а низкочастотный и высокочастотный компоненты спектра ниже, чем у выживших пациентов (73 больных) (табл. 3).
Учитывая, что низкочастотный компонент спектрального анализа в наибольшей степени отражает влияние симпатической нервной системы, обладает наибольшей прогностической значимостью, определили медиану для установления неблагоприятного значения этой переменной у обследуемых больных. Медиана LF спектра составила 5,2 ln мс 2 . В соответствии с этим показателем обследуемые разделены на 2 группы: I группа — низкочастотный компонент <5,2 ln мс 2 , II группа — низкочастотный компонент >5,2 ln мс 2 . Установлено, что больные I и II групп были сопоставимы по возрасту (p>0,05) (табл. 4).
Однако в I группе (LF<5,2 ln мс 2 ) ЧСС, NT-proBNP, ВчСРБ, СДЛА больше, а ФВ ЛЖ и СКФ меньше по сравнению с аналогичными показателями больных II группы (LF>5,2 ln мс 2 ) (p<0,05). Таким образом, LF<5,2 ln мс 2 является фактором, отражающим неблагоприятный прогноз у обследуемых больных.
Оценено прогностическое значение LF< или >5,2 ln мс 2 в развитии ССО у больных ХСН в течение трех лет наблюдения. В динамике обследовано в I группе (LF<5,2 ln мс 2 ) 33 пациента и во II группе (LF>5,2 ln мс 2 ) 55 больных. Определено, что в I группе в течение трех лет наблюдения декомпенсация СН развилась у 12 (36,4%) пациентов, а во II группе — у 10 (18,2%) больных.
Вероятность развития декомпенсации СН в течение трех лет при наличии LF<5,2 ln мс 2 выше, чем при LF>5,2 ln мс 2 (Log-rank, p=0,048) (рис. 1).
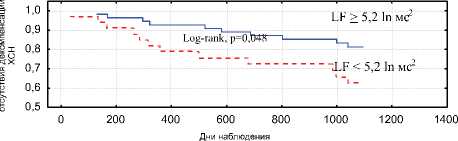
Рис.1. Кривые Каплана – Мейера кумулятивных вероятностей отсутствия декомпенсации ХСН в течение трех лет в зависимости от уровня LF спектра (Logrank, р=0,048)
Установлено, что в I группе в течение трех лет наблюдения летальный исход развился у 9 (27,3%) пациентов, а во II группе — у 6 (10,9%) больных. Вероятность развития летального исхода в течение трех лет при наличии LF<5,2 ln мс2 выше, чем при LF>5,2 ln мс2 (Log-rank, p=0,02) (рис. 2).
1,05
1,00
0,95
0,90
0,85
0,80
0,75
0,70
0,65
LF > 5,2 In мс2
Log-rank, р=0,02
,LF < 5,2 In мс2
0 200 400 600 800 1000 1200 1400
Дни наблюдения
Рис. 2. Кривые Каплана — Мейера кумулятивных вероятностей отсутствия летального исхода в течение трех лет в зависимости от уровня LF спектра (Log-rank, р=0,02)
Выявлено, что в I группе в течение трех лет наблюдения повторный инфаркт миокарда развился у 6 (18,2%) пациентов, а во II группе — у 7 (9,1%) больных. Значимых различий в течение трех лет наблюдения в развитие повторного инфаркта миокарда в изучаемых группах не было.
Таким образом, снижение низкочастотного компонента спектра менее 5,2 ln мс 2 можно рассматривать как показатель, влияющий на риск развития декомпенсации СН и летального исхода в течение последующих трех лет у больных ХСН.
Для выявления предикторов летального исхода заболевания использована логистическая регрессия. В регрессионный анализ включались классические факторы риска и низкочастотный компонент спектра ВСР. Независимыми предикторами летального исхода у больных ХСН в течение трех лет явились ФВ ЛЖ [ОР 1,217, ДИ 1,021–1,452; p=0,01], мочевая кислота [ОР 0,985, ДИ 0,971–1,000; p=0,03], NT — proBNP [ОР 0,987, ДИ 0,971–1,002; p=0,01] и низкочастотный компонент спектра ВСР [ОР 0,215, ДИ 0,012–5,072; p=0,10]. Чувствительность теста 96%, специфичность 80%. Площадь под ROC-кривой равна 0,972.
Используя уравнение логистической регрессии: P=ey / (1+ey), где (1 — Р) • 100% — вероятность развития события; е — основание натуральных логарифмов, равное 2,71; у = 4,464+0,211× ФВ ЛЖ – 0,021× мочевая кислота– 0,004× NT–proBNP– 1,254× ( LF <5,2=1 или >5,2=0), можно рассчитать индивидуальный риск развития летального исхода у больного с ХСН в течение трех лет наблюдения.
Обсуждение. Установлено, что у больных с ХСН, принимающих ß-блокаторы, сохраняется выраженное влияние симпатической нервной системы, проявляющееся в угнетении всех компонентов спектра RR интервалов, что совпадает с данным литературы о значении симпатоадреналовой активации в развитии ССО у этой категории больных [6].
Определено, что низкочастотный и высокочастотный компоненты спектра у больных с повторным инфарктом миокарда и летальным исходом ниже, а ЧСС выше, чем у пациентов в отсутствии этих осложнений.
На основании выявленной взаимосвязи между LF спектра и возрастом, NT-proBNP, ВчСРБ, ФВ ЛЖ, СДЛА, приемом петлевых диуретиков можно предполагать, что низкочастотная составляющая спектрального анализа — показатель, ассоциированный с нейрогормональной активностью и тяжестью состояния больного.
Разработанный алгоритм, оценивающий индивидуальный риск развития летального исхода у больного с ХСН в течение трех лет, позволит улучшить тактику ведения и прогноз у этой категории пациентов.
В последние годы предпринимаются попытки создания простых алгоритмов прогнозирования выживаемости при ХСН. В 2006 г. появилась Сиэттлская модель сердечной недостаточности (Seattle Heart Failure Model, SHFM), с помощью которой можно рассчитать вероятную продолжительность жизни отдельного пациента с ХСН. При расчете необходимо учитывать 28 различных параметров (из них 13 — клинические признаки, характеризующие состояние больного, 15 — варианты текущей терапии) [9]. Развитие представлений о ХСН, определение роли мозгового натрийуретического пептида (МНП) и NT-proB-NP в прогнозировании у этой категории пациентов привели к созданию в 2009 г. отечественной модели МНП — возрастной модели выживаемости (НЕВА-75) [10]. НЕВА-75 создана для пациентов старше 75 лет и учитывает возраст и уровень МНП. Алгоритм прогнозирования развития выживаемости в течение трех лет у больных ХСН, созданный нами, основан на современных характеристиках и охватывает большую группу больных ХСН в возрасте до 75 лет.
Выводы:
-
1. У больных с перенесенным Q-инфарктом миокарда и симптомами ХСН сохраняется выраженное влияние симпатической нервной системы, проявляющееся в угнетении всех компонентов спектра RR интервалов.
-
2. Низкочастотная составляющая спектрального анализа наиболее полно отражает выраженность нейрогормональной активности и тяжесть состояния больного.
-
3. Основными причинами смерти у больных с перенесенным Q-инфарктом миокарда и симптомами ХСН при годовой летальности 8% являются повторный инфаркт миокарда и внезапная сердечная смерть.
-
4. Определенный алгоритм, позволяющий рассчитать индивидуальный риск развития летального исхода у больного с ХСН в течение трех лет, даст возможность улучшить тактику ведения и прогноз у этой категории пациентов.
Список литературы Прогностическое значение показателей вариабельности сердечного ритма у больных хронической сердечной недостаточностью (трехлетнее наблюдение)
- ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure 2008: the Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2008 of the European Society of Cardiology.developed in collaboration with the Heart Failure Association of the ESC (HFA) and endorsed by the European Society of Intensive Care Medicine (ES1CM)/K. Dickstein, A. Cohen-Solal, G. Filippatos [et al.]//Eur. Heart J. 2008. Vol. 29 (19). P. 2388-2442.
- Plasma norepinephrine as a guide to prognosis in patients with chronic congestive heart failure/J.N. Cohn, ТВ. Levine, M.T. Olivari [et al.]//N. Engl. J. Med. 1994. Vol. 311 (13). P. 819-823.
- Frequency domain measures of heart period variability and mortality after myocardial infarction/J.T Bigger, J. L. Fleiss, R.C. Steinman [et al.]//Circulation. 1992. Vol.85. P. 164-171.
- Gillum R.F., Makuc D.M., Feldman J.J. Pulse rate, coronary heart disease, and death: the NHANES I Epidemilogical Follow-up Study//Amer. Heart J. 1991. Vol. 121. P. 172-177.
- MERIT-HF Study Group: Effects of metoprolol CR/XL in chronic heart failure: Metoprolol CR/XL Randomized International Trial in Congestive Heart Failure (MERIT-HF)//Lancet. 1999. Vol. 353 (9169). P. 2001-2007.
- Абрамкин Д. В., Явелов И. С, Грацианский Н.А. Неин-вазивные сердечно-сосудистые рефлекторные тесты и прогноз внезапной сердечной смерти после перенесенного инфаркта миокарда: какой метод предпочесть?//Кардиология. 2004. №10. С. 4-12.
- Task Force European Society of cardiology and the North American Society of pacing and Electrophysiology: Heart rate variability: standards of measurement, physiological interpretation, and clinical use//Eur. Heart. J. 1996. Vol. 17. P. 354-381.
- The 6-minute walk: a new measure of exercise capacity in patients with chronic heart failure/G.H. Guyatt, M. J. Sullivan, P. J. Thompson [et al.]//Can. Med. Assoc. J. 1985. Vol. 132 (8). P. 919-923.
- The Seattle Heart Failure Model: prediction of survival in heart failure/W. С Levy, D. Mozaffarian, D.T Linker [et al.]//Circulation. 2006. Vol. 113 (11). P. 1424-1433.
- Listing Criteria for Heart Transplantation: International Society for Heart and Lung Transplantation Guidelines for the Care of Cardiac Transplant Candidates -2006/M.R. Mehra, J. Kobashiqawa, R. Starling [et al.]//J. Heart and Lung Transplantat. 2006. Vol. 25 (19). P. 1024-1042.


