Прогнозирование осложнений при терапии COVID-19: использование биомаркеров и клинических показателей
Автор: Колотилина М.А., Мартишина Е.Е., Cухоруков Р.В., Тузов В.В., Винникова М.Д.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Обзоры литературы
Статья в выпуске: 1 т.21, 2026 года.
Бесплатный доступ
Обоснование. В условиях глобальной пандемии, вызванной SARS-CoV-2, важнейшим фактором в обеспечении благоприятных исходов лечения стало своевременное и точное выявление пациентов с высоким риском осложнений. Одной из перспективных методик, способствующих такому выявлению, является использование биомаркеров, которые позволяют прогнозировать осложнения и тяжесть течения COVID-19. Цель: оценка прогностической значимости различных биомаркеров у пациентов с COVID-19 и определение значимости разработки стандартизированных протоколов для мониторинга этих показателей в условиях пандемии. Материалы и методы. Для анализа были рассмотрены данные исследований, посвященных роли биомаркеров, таких как С-реактивный белок, D-димер, ферритин, лактатдегидрогеназа и тропонины, в прогнозировании осложнений у пациентов с COVID-19. Источники включали публикации в международных рецензируемых журналах, результаты клинических испытаний и мета-анализы, доступные в научных базах данных. Результаты. Повышенные уровни биомаркеров, таких как С-реактивный белок, D-димер, ферритин, лактатдегидрогеназа и тропонины, коррелируют с высоким риском острых осложнений, что делает их значимыми инструментами для мониторинга состояния пациентов. Внедрение унифицированных порогов для оценки тяжести состояния позволит снизить вариабельность данных и улучшить сопоставимость результатов между медицинскими учреждениями. Заключение. Данные подчеркивают значимость биомаркеров для мониторинга пациентов с COVID-19 и необходимость разработки стандартизированных протоколов для улучшения точности прогнозирования. Перспективы использования биомаркеров в адаптивных методах интенсивной терапии и реанимации являются важными направлениями для оптимизации исходов лечения и дальнейших исследований.
COVID-19, биомаркеры, клинические показатели, прогнозирование осложнений, SARS-CoV-2, стандартизация диагностики, смертность, интенсивная терапия, С-реактивный белок, D-димер
Короткий адрес: https://sciup.org/140314195
IDR: 140314195 | DOI: 10.25881/20728255_2026_21_1_146
Prediction of complications in COVID-19 therapy: use of biomarkers and clinical indicators
Rationale. With the pandemic caused by SARS-CoV-2, accurate identification of patients at high risk for complications has become a key factor in ensuring positive treatment outcomes. A promising technique to facilitate such identification is the use of biomarkers that can predict complications and severity of COVID-19 course. Objective. The purpose is to evaluate the prognostic significance of various biomarkers in individuals with COVID-19 and to determine the value of developing standardized protocols for monitoring these indicators under pandemic conditions. Methods. For the analysis, we reviewed studies on the role of biomarkers such as C-reactive protein, D-dimer, ferritin, lactate dehydrogenase and troponins in predicting complications in patients with COVID-19. Sources used were international peer-reviewed journal publications, clinical trial results, and meta-analyses available in scientific databases. Results. Elevated levels of biomarkers such as C-reactive protein, D-dimer, ferritin, lactate dehydrogenase and troponins correlate with a high risk of acute complications, making them useful tools for monitoring. The common thresholds for assessing severity of illness will reduce data variability and improve comparability of results between healthcare providers. Conclusion. The data highlights the importance of biomarkers for monitoring patients with COVID-19 and the need to develop standardized protocols to improve prognostic accuracy. Prospects for the use of biomarkers in adaptive critical care and resuscitation are important means to optimize patient outcomes and further research.
Текст научной статьи Прогнозирование осложнений при терапии COVID-19: использование биомаркеров и клинических показателей
Пандемия COVID-19, вызванная вирусом SARS-CoV-2, продолжает оказывать значительное влияние на систему здравоохранения во всем мире, приводя к росту числа госпитализаций и летальных исходов. По данным ВОЗ, на 2023 г. общее число подтвержденных случаев инфекции превысило 770 млн., а число смертей превысило 7 млн. [1]. В условиях высоких показателей заболеваемости и перегруженности медицинских учреждений, прогнозирование осложнений и своевременное выявление пациентов с высоким риском неблагоприятных исходов становятся ключевыми задачами для снижения смертности и улучшения качества медицинской помощи. COVID-19 может вызывать широкий спектр осложнений, включая острый респираторный дистресс-синдром (РДС), сепсис и поли-органную недостаточность, особенно у пациентов с сопутствующими хроническими заболеваниями, такими как сахарный диабет, артериальная гипертензия и ожирение [2]. В таких случаях использование стандартных клинических показателей в сочетании с биомаркерами, позволяет улучшить точность прогнозирования исходов.
Биомаркеры могут играть важную роль в оценке воспалительных реакций и системного ответа организма на инфекцию. В частности, такие показатели, как С-реактив-ный белок (СРБ), уровень ферритина, тропонина и лактатдегидрогеназы, широко используются для оценки степени

тяжести заболевания и прогноза [3]. Однако существует недостаток стандартизации в подходах к использованию биомаркеров в различных медицинских учреждениях и странах, что ограничивает возможность сопоставления результатов и их использования в международной практике.
Материалы и методы
Для проведения исследования был осуществлен систематический обзор и анализ доступных данных по использованию различных биомаркеров у пациентов с COVID-19. Основные источники информации включали базы данных MEDLINE, EMBASE и Cochrane, а также публикации в рецензируемых медицинских журналах с 2019 по 2024 гг. Поиск исследований осуществлялся с использованием ключевых слов и сочетаний, таких как «COVID-19», «биомаркеры», «SARS-CoV-2», «D-dimer», «Д-димер» , «С-реактивный белок» , «C-reactive protein», «ферритин», «ferritin», «lactate dehydrogenase», «лактатдегидрогенеза», «troponins» «тропонирн», «coagulopathy», «коагулопатия». Дополнительно применялись фильтры по датам и языкам публикаций (русский и английский).
Выбор исследований проводился по заранее определенным критериям: исследования должны были содержать данные о прогностической значимости биомаркеров, а также описывать клинические исходы, включая развитие острых осложнений и летальные случаи. Исследования, не соответствующие этим критериям, исключались. Также учитывались возраст, пол и наличие сопутствующих заболеваний у участников, таких как артериальная гипертензия, сахарный диабет и ожирение.
Основная часть
Наиболее изученным биомаркером является СРБ, который в условиях инфекции SARS-CoV-2 выступает индикатором системного воспалительного ответа [4]. Основной механизм его повышения связан с активацией системы врожденного иммунитета и продукции провос-палительных цитокинов, таких как интерлейкин-6 (ИЛ-6), интерлейкин-1 (ИЛ-1) и фактор некроза опухолей альфа (ФНО-α). В ответ на стимуляцию данными цитокинами, гепатоциты начинают активно синтезировать СРБ, который поступает в системный кровоток. В исследовании Ayad M Ali и соавт. изучались уровни тропонина, D-димера и СРБ у пациентов с COVID-19 [5]. Дизайн исследования включал два этапа: первый этап охватил 173 пациента с COVID-19 (91 мужчина и 82 женщины), из которых 143 пациента выжили (79 мужчин и 64 женщины), у 30 пациентов был летальный исход (12 мужчин и 18 женщин). Во втором этапе пациенты были разделены на две группы: семь семей, потерявших более одного члена (41 пациент; 23 мужчины и 18 женщин) с 15 зарегистрированными случаями смерти (7 мужчин и 8 женщин), и контрольная группа из 132 госпитализированных пациентов (69 мужчин и 63 женщины) с 15 случаями смерти (5 мужчин и 10 женщин). В ходе исследования были выявлены значительные различия в уровнях СРБ, D-димера и тропонина в первую неделю госпитализации между выжившими и погибшими пациентами (p<0,0001). Во вторую неделю госпитализации значительные различия сохранялись по всем исследованным параметрам. Уровни лейкоцитов в крови и СРБ у мужчин-выживших показали положительную корреляцию (r = 0,75, p<0,0001), у мужчин-погибших была выявлена положительная корреляция между количеством лейкоцитов и тропонином (r = 0,74, p = 0,007) (Рис. 1).
В группах семей, потерявших более одного члена, во вторую неделю была отмечена положительная корреляция тропонина с D-димером, CРБ и уровнем лейкоцитов (Рис. 2).
На основании результатов исследования авторами сделан вывод, что уровни тропонина, D-димера, CRP и лейкоцитов были значительно выше у умерших пациентов, чем у выживших, а также установлено, что высокие уровни тропонина и лейкоцитов имеют существенную корреляцию с семьями, потерявшими более одного члена, по сравнению с контрольной группой.
Провоспалительный цитокин ИЛ-6 участвует в патогенезе COVID-19 как один из медиаторов цитоки-нового шторма — состояния, при котором происходит неконтролируемая активация иммунной системы и
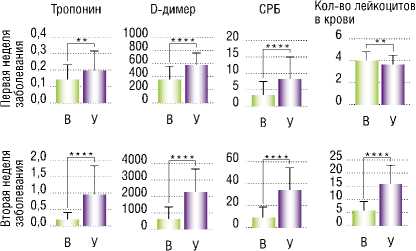
Рис. 1. Различия в параметрах между выжившими и умершими пациентами с COVID-19 на первой и второй неделе заболевания (NS, 0,1234; ** – р = 0,0021; ****– р < 0,0001) [5]. Примечание: В – выжившие, У – умершие.
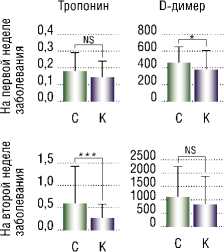
Рис. 2. Различия между семьями с >1 смертью и контрольной группой в некоторых значениях параметров на первой и второй неделе заболевания COVID-19. (NS = 0,1234; *р = 0,0332; **– р = 0,0021; *** – р = 0,0002; **** – р<0,0001) [5]. Примечание: С – семьи с одной смертью и более; К – контрольная группа; NS – статистически
СРБ Кол-во лейкоцитов в крови
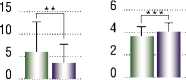
СК СК

СК СК
незначимо.

массовое выделение провоспалительных цитокинов [6]. SARS-CoV-2, связываясь с рецепторами ангиотен-зин-превращающего фермента-2 на клетках эпителия дыхательных путей и эндотелия сосудов, запускает каскад воспалительных реакций [7]. В ответ на повреждение и активацию клеток эпителия легких и макрофагов высвобождаются различные цитокины. В условиях гиперактивации иммунной системы ИЛ-6 способствует усиленной продукции других провоспалительных цитокинов, таких как ИЛ-1 и ФНО- α , что создает положительную обратную связь, поддерживающую воспалительный процесс. Под действием провоспалитель-ных цитокинов большое количество нейтрофилов и макрофагов устремляются в легочную ткань [8]. Данные клетки, высвобождая реактивные кислородные виды и протеолитические ферменты, вызывают повреждение альвеол и способствуют развитию гипоксии и нарушению газообмена. Действуя через свои рецепторы ИЛ-6, стимулирует активацию эндотелиальных клеток, что ведет к увеличению проницаемости сосудов и развитию эндотелиальной дисфункции. Данные процессы способствуют выходу плазмы и лейкоцитов в окружающие ткани, что является предрасполагающим фактором для формирования тромбов и микротромбообразования в легких и других органах. Исследование Eric A. Coomes и соавт. представляет собой систематический обзор и мета-анализ, направленный на оценку роли ИЛ-6 в патогенезе COVID-19 [9]. Исследование основано на анализе данных о дисрегуляции ИЛ-6 у пациентов с COVID-19 и оценивает его значимость как биомаркера для прогнозирования неблагоприятных исходов. Для анализа были использованы базы данных MEDLINE и EMBASE, а также другие литературные источники. Всего было отобрано 10 исследований (n = 1798), из которых 8 опубликованных статей и 2 препринта. Мета-анализ выявил, что концентрации ИЛ-6 в среднем в 2,9 раза выше у пациентов с осложненным течением COVID-19 по сравнению с пациентами с неосложненным течением (шесть исследований, n = 1302; 95% доверительный интервал (ДИ), 1,17-7,19). В анализе чувствительности, который включал сравнение пациентов, нуждающихся в лечении в отделении интенсивной терапии (ОИТ) и тех, кто не нуждался в ОИТ, результаты подтвердили увеличение ИЛ-6 в 3,24 раза (два исследования, n = 540; 95% ДИ, 2,54-4,14; p<0,001). Однако в группе с легкими случаями болезни (n = 561) статистически значимых различий не наблюдалось (p = 0,14). Авторы отмечают, что уровень ИЛ-6 является важным предиктором тяжелых осложнений, таких как острый респираторный дистресс-синдром (ОРДС) и летальный исход, и указывают на необходимость дополнительных исследований по изучению эффективности иммуномодуляторных терапий, таких как ингибиторы ИЛ-6, в лечении тяжелых форм COVID-19.
Ферритин выполняет не только функцию маркера воспаления, но и активного медиатора в развитии воспа- лительных реакций [10]. При COVID-19 вирус SARS-CoV-2 вызывает активацию врожденного иммунитета, в результате чего происходит высвобождение большого количества провоспалительных цитокинов, которые стимулируют продукцию ферритина. Уровень ферритина в крови значительно повышается, что указывает на активное вовлечение макрофагов и других клеток иммунной системы в воспалительный процесс, что может свидетельствовать о развитии цитокинового шторма [11]. Работа Moudhi Alroomi и соавт. посвящена оценке уровня сывороточного ферритина как предиктора тяжести и смертности у госпитализированных пациентов с COVID-19 [12]. В ретроспективное когортное исследование были включены 595 пациентов с подтвержденной инфекцией SARS-CoV-2 в возрасте от 18 лет и старше. Пациенты были разделены на две группы в зависимости от уровня ферритина: ≤1000 нг/мл и >1000 нг/мл. Основными результатами исследования стали установление связи между повышенными уровнями ферритина (>1000 нг/мл) и повышенной смертностью, а также более высоким риском развития тяжелых осложнений, таких как пневмония и ОРДС.
Проведенный авторам логистический регрессионный анализ показал, что ферритин >1000 нг/мл значительно увеличивает риск внутрибольничной смертности (95% ДИ = 0,21-0,62, p<0,001). Мужчины, пациенты с артериальной гипертензией и пневмонией также имели более высокий риск летального исхода (мужчины p = 0,003; артериальная гипертензия p <0,001; пневмония p<0,001). Кокс-пропорциональный регрессионный анализ и кривые выживаемости по Каплан-Мейеру подтвердили, что пациенты с высоким уровнем ферритина имели более высокую смертность (Рис. 3).
Кривая демонстрирует, что пациенты с более высоким уровнем ферритина имеют более низкую вероятность выживания, что подтверждает связь гиперферритинемии с повышенной смертностью у пациентов с COVID-19.
При COVID-19 наблюдается так называемая COVID-ассоциированная коагулопатия, которая характеризуется повышенным уровнем D-димера, фибриногена и возникновением синдрома диссеминированного внутрисосудистого свертывания (ДВС) [13]. Данный процесс является основой для развития тяжелых осложнений, таких септический шок и полиорганная недостаточность. Коагуляционный биомаркер D-димер, являясь продуктом деградации фибрина, отражает активацию коагуляционного каскада и повышен у большинства пациентов с COVID-19, особенно в тяжелых и критических случаях [14]. В патогенезе COVID-19 активация свертывающей системы происходит за счет выраженного эндотелиального повреждения и высвобождения провоспалительных цитокинов, что ведет к развитию ДВС-синдрома. Повышенные уровни D-димера указывают на наличие тромбообразования и последующего разрушения тромбов, что является маркером гиперкоагуляции у пациентов с COVID-19 [15]. В исследовании Yong Li и соавт. проводилась оценка уровня D-димера у
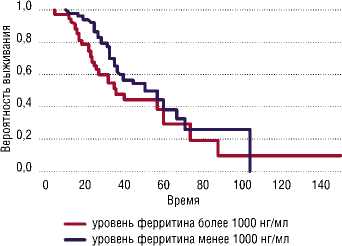
Рис. 3. График выживаемости Каплана-Майера по смертности, сгруппированный по рождаемости [12].
123456798 10
Дни после начала заболевания
3-я группа
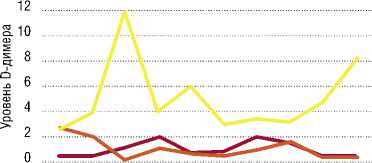
Рис. 4. Изменения Уровень D-димера в течение десяти последовательных суток Дни после начала заболевания [16].
279 пациентов с COVID-19, госпитализированных в три больницы провинции Хубэй, Китай [16]. Исследование анализирует динамику изменений уровня
D-димера на протяжении 10 суток после поступления. Пациенты были разделены на три группы: в первой группе степень тяжести заболевания была легкая или средняя и состояние пациентов постепенно улучшалось – 136 человек, во второй группе состояние пациентов оценивалось как среднетяжелое и тяжелое, но потом происходило улучшение – 23 человека, в третьей группе состояние пациентов оценивалось как крайне тяжелое, которое в дальнейшем привело к летальному исходу – 120 человек. В ходе исследования, было выявлено, повышенные уровни D-димера коррелируют с худшим прогнозом и высоким риском летального исхода, особенно в тяжелых случаях COVID-19 (Рис. 4).
На графике представлена динамика уровня D-димера у пациентов с COVID-19, разделенных на три группы в течение 10 суток после начала заболевания: в первой группе уровень D-димера остается стабильным и низким, что соответствует обычному течению заболевания. Во второй группе наблюдаются умеренные колебания уровня D-димера, но без значительных пиков, что отражает улучшение состояния. В третьей группе уровень D-димера резко повышается на 2–3 сутки и продолжает расти, что связано с ухудшением состояния и высоким риском летального исхода. Авторы работы пришли к заключению, что высокий уровень D-димера и его резкие колебания коррелируют с тяжелым течением COVID-19 и высоким риском летального исхода.
Исследование Jingrui Sui и соавт. было посвящено изучению связи между уровнем фибриногена и тяжестью COVID-19 [17]. В ретроспективное исследование были включены 119 пациентов с подтвержденным COVID-19, госпитализированных в Университет Алабамы с марта по июнь 2020 г. У 77,3% пациентов наблюдалось тяжелое течение заболевания, 59,5% потребовалась госпитализация в ОИТ. Уровень фибриногена был повышен у 67,2% пациентов и значительно коррелировал с маркерами воспаления, но не с уровнем тропонина. У пациентов с тяжелым течением болезни фибриноген был значительно выше (р = 0,001), а уровень 528 мг/дл использовался как оптимальный порог для прогнозирования тяжести заболевания с чувствительностью 66,7% и специфичностью 70,3% (р = 0,0006). Авторами был сделан вывод, что повышенный уровень фибриногена может служить маркером воспаления и тяжести COVID-19, а также определить необходимость госпитализации в ОИТ.
Для оценки степени повреждения легочной и сердечной ткани используются специфические биомаркеры, такие как лактатдегидрогеназа (ЛДГ) и тропонины [18]. Маркером клеточного повреждения служит ЛДГ, он высвобождается при разрушении клеток легочной ткани, что часто наблюдается у пациентов с COVID-19. Brandon Michael Henry и соавт. изучали связь между повышенным уровнем ЛДГ и тяжестью и смертностью от COVID-19 [19]. Авторы провели мета-анализ девяти исследований с участием 1532 пациентов с COVID-19. Повышенные уровни ЛДГ увеличивали вероятность развития тяжелой формы заболевания примерно в шесть раз (Отношение шансов (ОШ): 6,53, ДИ: 3,47-12,28) и вероятность смертности в 16 раз (ОШ: 16,64, ДИ: 7,07-39,13). Исследование подтверждает, что ЛДГ может служить важным биомаркером для прогнозирования тяжелых исходов при COVID-19.
Кардиальные биомаркеры, такие как тропонин I, используются для выявления поражения сердечной ткани [20]. Luis Garda de Guadiana-Romualdo и соавт. провели многоцентровое ретроспективное наблюдательное исследование BIOCOVID с целью определения распространенности и прогностической значимости повреждения миокарда у пациентов с COVID-19, используя уровни тропонина [21]. В исследование было включено 1280 пациентов с COVID-19, из которых 187 (14,6%) умерли во время госпитализации. Уровень тропонина измеряли в течение первых 24 часов после поступления. Повышенные уровни тропонина были определены в 26,9% случаев (344 пациента), а при использовании уровней тропонина, учитывающих половые различия — у 30% пациентов (384 пациента). Было установлено, что пациенты с повышенными уровнями тропонина имели значительно выше риск 30-дневной смертности (ОШ = 3,00, 95% ДИ), данный показатель оставался значимым независимо от типа используемого тропонина (T или I). Ассоциация была сильнее для тропонина I (ОШ = 3,69). В группе с тропонином T
42,9% пациентов имели повышенные уровни по половому порогу, тогда как для тропонина I этот показатель составил 21,9% (р<0,001). Также повышенные уровни тропонина были чаще обнаружены у женщин по сравнению с мужчинами при использовании уровней тропонина, учитывающих половые различия. Результаты подтверждают необходимость раннего измерения тропонина для оценки риска и стратификации пациентов с COVID-19, выявляя подгруппу пациентов с высоким риском неблагоприятных исходов и повреждением миокарда.
Обсуждение
Анализ представленных исследований демонстрирует, что биомаркеры, такие как СРБ, ферритин, D-димер, фибриноген, ЛДГ и тропонин играют значительную роль в оценке риска неблагоприятных исходов у пациентов с COVID-19. Основная закономерность заключается в том, что повышенные уровни данных маркеров связаны с высокой вероятностью развития тяжелых осложнений, таких как ОРДС, полиорганная недостаточность и ДВС-синдром и летальный исход. Включение пороговых значений, учитывающих половые различия, позволяет более точно предсказать тяжесть заболевания у пациентов мужского и женского пола, что подтверждает необходимость индивидуализированного подхода к оценке пациентов.
Результаты анализируемых работ показывают различия, обусловленные особенностями выборок и методов измерения. Во всех исследованиях подтверждается значимость тропонинов и D-димера в прогнозировании неблагоприятных исходов при COVID-19, однако наблюдаются вариации в уровнях и порогах, используемых для диагностики. Например, использование полово-специфических порогов показало более высокую точность в выявлении риска у женщин, что не всегда учитывалось в ранних исследованиях. Подобная ситуация подчеркивает необходимость стандартизации протоколов и методов диагностики, чтобы обеспечить сопоставимость результатов и оптимизацию лечения.
Заключение
Проведенный анализ данных из исследований, опубликованных с 2019 г., показывает, что различные биомаркеры, отражающие воспалительные, коагуляционные и органные процессы, имеют высокую прогностическую ценность при COVID-19. Важно учитывать комплексность патогенеза заболевания и использовать биомаркеры в совокупности для точной оценки риска осложнений. Стандартизация диагностических протоколов и унификация методов измерения необходимы для улучшения сопоставимости данных и повышения качества медицинской помощи. Дальнейшие исследования и разработка новых терапевтических стратегий на основе биомаркеров могут способствовать снижению летальности и улучшению исходов лечения.


